「遺伝学」の版間の差分
編集の要約なし |
m 明らかな誤変換を訂正 |
||
| (6人の利用者による、間の8版が非表示) | |||
| 1行目: | 1行目: | ||
{{脚注の不足|date=2024年5月}} |
|||
{{Expand English|date=2024年6月}} |
|||
{{Genetics sidebar}} |
{{Genetics sidebar}} |
||
'''遺伝学'''(いでんがく、 {{Lang-en-short|genetics}})は、生物の[[遺伝子]]、[[遺伝的変異]]、[[遺伝]]について研究する学問である<ref name="griffiths2000sect60">{{cite book | veditors = Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbart|title=An Introduction to Genetic Analysis |year=2000 |isbn=978-0-7167-3520-5 |edition=7th |publisher=W.H. Freeman |location=New York |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=iga.section.60 |chapter=Genetics and the Organism: Introduction}}</ref><ref name="Hartl_and_Jones">Hartl D, Jones E (2005)</ref><ref>{{Cite web|url=https://www.dictionary.com/browse/genetics|title=the definition of genetics|website=www.dictionary.com|language=en|access-date=25 October 2018}}</ref>。遺伝は生物の[[進化]]に不可欠であるため、遺伝学は[[生物学]]において重要な分野である。19世紀に[[モラヴィア]]地方の都市[[ブルノ]]で活動していた[[アウグスチノ会]]修道士、[[グレゴール・ヨハン・メンデル|グレゴール・メンデル]]は、遺伝学を科学的に研究した最初の人物である。メンデルは「形質遺伝」<!-- trait inheritance -->すなわち、[[形質]](生物の性質や特徴)が親から子孫へと時を超えて受け継がれる様式を研究した。そして、生物([[エンドウ]])が独立した「遺伝単位」<!-- discrete "units of inheritance" -->によって形質を継承することを観察した。この用語は今日でも使用されているが、遺伝子と呼ばれるものの定義としてはやや曖昧である。 |
|||
'''遺伝学'''(いでんがく、{{Lang-en-short|genetics}})は、[[生物]]の[[遺伝]]現象を研究する[[生物学]]の一分野である。遺伝とは[[世代]]を超えて[[形質]]が伝わっていくことであるが、[[遺伝子]]が生物の設計図的役割を果たすものであることが判明し、現在では生物学のあらゆる分野に深く関わるものとなっている。力学系などの数学諸分野との関わりについての研究も推進されている。 |
|||
[[形質]]遺伝や、遺伝子の[[分子遺伝学|分子遺伝]]のメカニズムは、21世紀の遺伝学の主要な原理であり続けているが、現代遺伝学は遺伝子の機能と挙動の研究へと拡大している。遺伝子の構造と機能・変異・分布は、[[細胞]]・生物(たとえば[[顕性]])・個体群という文脈の中で研究されている。遺伝学は、[[分子遺伝学]]、[[エピジェネティクス]]、[[集団遺伝学]]など、多くの研究領域へと発展した。この幅広い分野の研究対象となっている生物は、[[ドメイン (分類学)|生命のドメイン]]([[古細菌]]、[[細菌]]、[[真核生物]])にまたがる。 |
|||
== 概要 == |
|||
遺伝現象は、元来は世代を超えて生物の形質が伝えられることを指す。これは生物に見られる重要な特徴であり、例えば[[分類学]]や[[系統学]]もこれを基礎とするものである。この現象を扱う生物学の分野が遺伝学である。ただし、生物学の分野で[[実験]]が取り入れられた、という点ではこれは古いものである。これは[[品種改良]]などの形で現実世界でこれに近いことが行われてきたからでもあるだろう。その意味では、この分野はその初期から実用的側面が強く、それは[[育種学]]へと引き継がれる。 |
|||
遺伝的プロセス(過程)は、生物の環境や経験と結びついて、{{Ill2|個体発生|en|Ontogeny|label=発達|preserve=1}}や[[行動遺伝学|行動]]に影響を与える。これは、しばしば{{ill2|生まれつきか育ちか|en|Nature and nurture}}と呼ばれる。生細胞や生物の内外の環境が、遺伝子の転写を増減させる可能性がある。その典型例が、遺伝的に同一のトウモロコシの種子を2つ用意し、1つを温帯気候の場所に、もう1つを[[砂漠気候|乾燥気候]](十分な天然水や降雨がない)に植えることである。2本のトウモロコシの茎の平均の高さは、遺伝的に同等になるよう定まっているかもしれないが、乾燥気候のトウモロコシは、環境中の水や栄養分の不足のため、 温帯気候に植えた茎の半分ほどにしか成長しない。 |
|||
[[メンデル]]の得た法則はこの分野の進歩の基礎となったが、遺伝学の実質的な進歩はその法則の再発見からである。これによって[[遺伝子]]という概念が確立し、具体的に追求すべき対象が明らかにされた。しかも、それがその後すぐに[[染色体]]を介して[[細胞核]]に結びつけられることで、遺伝現象は単に世代を超えて何かを伝えるしくみではなく、生命の日常的活動をその基礎で支えるものと判明したことで、生物学の中心的な位置に出てくることになった。 |
|||
== 語源 == |
|||
[[ジェームズ・ワトソン|ワトソン]]と[[フランシス・クリック|クリック]]らによる[[DNA]]の[[二重らせん]]構造の発見後は、DNA上にある遺伝子の物質的な側面からの研究が発展し[[分子生物学]]とよばれる研究分野が開拓された。遺伝子の機能の解析は[[生物学]]のほとんどの分野と関係がある。特に[[フレデリック・グリフィス|グリフィス]]が発見した[[形質転換]]は生物の遺伝子を人為的に操作する方法へと道を開き、[[遺伝子工学]]へと発展した。 |
|||
遺伝学の英語、"{{en|genetics}}" は、[[古代ギリシア語]]の {{lang|grc|γενετικός}} (''{{lang|grc-Latn|genetikos}}'')「[[属格]] {{small|または}} 生成」に由来し、さらにこれは起源 (origin)を意味する {{lang|grc|γένεσις}} (''{{lang|grc-Latn|genesis}}'') に由来する<ref>{{cite web |url=https://www.perseus.tufts.edu/hopper/text?doc=Perseus%3Atext%3A1999.04.0057%3Aentry%3D%2321880&redirect=true |title=Genetikos (γενετ-ικός) |work=Henry George Liddell, Robert Scott, A Greek-English Lexicon |publisher=Perseus Digital Library, Tufts University |access-date=20 February 2012 |url-status=live |archive-url=http://webarchive.loc.gov/all/20100615000649/http://www.perseus.tufts.edu/hopper/text?doc=Perseus:text:1999.04.0057:entry=#1980&redirect=true |archive-date=15 June 2010}}</ref><ref>{{cite web |url=https://www.perseus.tufts.edu/hopper/text?doc=Perseus%3Atext%3A1999.04.0057%3Aentry%3D%2321873&redirect=true |title=Genesis (γένεσις) |work=Henry George Liddell, Robert Scott, A Greek-English Lexicon |publisher=Perseus Digital Library, Tufts University |access-date=20 February 2012 |url-status=live |archive-url=http://webarchive.loc.gov/all/20100615000649/http://www.perseus.tufts.edu/hopper/text?doc=Perseus:text:1999.04.0057:entry=#1980&redirect=true |archive-date=15 June 2010}}</ref><ref>{{cite dictionary |url=http://www.etymonline.com/index.php?search=Genetic&searchmode=none |title=Genetic |dictionary=Online Etymology Dictionary |access-date=20 February 2012 |url-status=live |archive-url=https://web.archive.org/web/20110823020616/http://www.etymonline.com/index.php?search=Genetic&searchmode=none |archive-date=23 August 2011}}</ref>。 |
|||
== 歴史 == |
|||
一方、個体群における遺伝子頻度の変化を、特に[[自然選択]]の視点から実験、観察、および数学的手法にもとづいて研究する分野は[[集団遺伝学]]と呼ばれる。 |
|||
{{Main|{{ill2|遺伝学の歴史|en|History of genetics}}}} |
|||
生物が、親から[[形質]](生物の性質や特徴)を受け継ぐという観察結果は、有史以前から、[[選抜育種]]による植物や動物の改良に利用されてきた<ref name="Publishing2009">{{cite book |title=Science: The Definitive Visual Guide |url=https://books.google.com/books?id=sFiJFuzRVFQC&pg=PA362 |year=2009 |publisher=Penguin |isbn=978-0-7566-6490-9 |page=362}}</ref><ref name="Poczai and Santiago-Blay 2022a">{{cite journal | authors = Poczai P, Santiago-Blay JA | title = Themes of Biological Inheritance in Early Nineteenth Century Sheep Breeding as Revealed by J. M. Ehrenfels | journal = Genes | volume = 13 | issue = 8 | page = 1311 | date = July 2022 | pmid = 35893050 | pmc = 9332421 | doi = 10.3390/genes13081311 | doi-access = free }}</ref>。この過程を理解しようとする現代遺伝学は、19世紀半ば、[[アウグスティヌス会|アウグスチノ会]]の修道士、[[グレゴール・ヨハン・メンデル|グレゴール・メンデル]]による研究に端を発する<ref name="Weiling">{{cite journal | authors = Weiling F | title = Historical study: Johann Gregor Mendel 1822-1884 | journal = American Journal of Medical Genetics | volume = 40 | issue = 1 | pages = 1–25; discussion 26 | date = July 1991 | pmid = 1887835 | doi = 10.1002/ajmg.1320400103 }}</ref>。 |
|||
さらに、遺伝基盤のもとに成立する生物進化について実験的、理論的研究が今後期待される。 |
|||
[[File:Festetics Imre-Oelenhainz.jpg|thumb|最初の{{Ill2|遺伝学者|en|Geneticist|redirect=1}}で、動物行動学者である [[:en:Imre_Festetics|Imre Festetics]] の肖像。彼の[[自然選択説|選択]]と[[進化]]に関する概念は、後に[[進化論#チャールズ・ダーウィンの進化論|チャールズ・ダーウィンの進化論]]で定式化された。]] |
|||
メンデル以前に、遺伝の文脈で「遺伝(genetic)」という用語を初めて使用した人物は、メンデルより前にケーゼグに住んでいた[[ハンガリー]]の貴族 [[:en:Imre Festetics|Imre Festetics]] であり、最初の遺伝学者としても知られている。彼は著書 ''The genetic laws of nature''(『自然の遺伝法則』、Die genetischen Gesetze der Natur、1819年)の中で、生物の遺伝に関するいくつかの法則を記述した<ref name="Poczai and Santiago-Blay 2021" />。彼の第二法則は、メンデルが発表した法則と同じである<ref name="Poczai and Szabó 2019">{{cite journal | authors = Szabó AT, Poczai P | title = The emergence of genetics from Festetics' sheep through Mendel's peas to Bateson's chickens | journal = Journal of Genetics | volume = 98 | issue = 2 | page = 63 | date = June 2019 | pmid = 31204695 | doi = 10.1007/s12041-019-1108-z | hdl-access = free | s2cid = 174803150 | hdl = 10138/324962 }}</ref>。第三法則で、変異の基本原則を提唱した(彼は[[ユーゴー・ド・フリース]]の先駆者ともいえる)<ref>{{cite journal | authors = Poczai P, Bell N, Hyvönen J | title = Imre Festetics and the Sheep Breeders' Society of Moravia: Mendel's Forgotten "Research Network" | journal = PLOS Biology | volume = 12 | issue = 1 | pages = e1001772 | date = January 2014 | pmid = 24465180 | pmc = 3897355 | doi = 10.1371/journal.pbio.1001772 | df = dmy-all | doi-access = free }}</ref>。Festetics は、動物、植物、人間の世代で観察される変化は、科学的な法則の結果であると主張した<ref name="Poczai 2022">{{cite book | author = Poczai P |title=Heredity Before Mendel: Festetics and the Question of Sheep's Wool in Central Europe |date=2022 |publisher=CRC Press |location=Boca Raton, Florida |isbn=978-1-032-02743-2 |page=113 |edition= |url=https://books.google.com/books?id=QJRwEAAAQBAJ&dq=info:maQOFGaQPfYJ:scholar.google.com&pg=PT6 |access-date=30 August 2022}}</ref>。彼は、生物はそれらの特徴を「獲得」するのではなく「継承」すると経験的に論じた。彼は、祖先の特徴が後に再び現れる可能性があり、生物が異なる特徴を持つ子孫を生み出す可能性を仮定することで、潜性形質や先天的変異<!-- recessive traits and inherent variation -->を認識した<ref name="Poczai et al. 2022">{{cite journal | authors = Poczai P, Santiago-Blay JA, Sekerák J, Bariska I, Szabó AT | title = Mimush Sheep and the Spectre of Inbreeding: Historical Background for Festetics's Organic and Genetic Laws Four Decades Before Mendel's Experiments in Peas | journal = Journal of the History of Biology | volume = 55 | issue = 3 | pages = 495–536 | date = October 2022 | pmid = 35670984 | pmc = 9668798 | doi = 10.1007/s10739-022-09678-5 | s2cid = 249433049 }}</ref>。これらの観察は、メンデルの{{Ill2|粒子遺伝|en|Particulate inheritance|label=粒子遺伝説}}(particulate inheritance)の重要な前触れとなり、遺伝を神話的な存在から科学的な学問へと移行させ、20世紀の遺伝学に基本的な理論的基盤を導いた<ref name="Poczai and Santiago-Blay 2021">{{cite journal | authors = Poczai P, Santiago-Blay JA | title = Principles and biological concepts of heredity before Mendel | journal = Biology Direct | volume = 16 | issue = 1 | pages = 19 | date = October 2021 | pmid = 34674746 | pmc = 8532317 | doi = 10.1186/s13062-021-00308-4 | doi-access = free }} [[File:CC-BY icon.svg|50px]] Text was copied from this source, which is available under a [https://creativecommons.org/licenses/by/4.0/ Creative Commons Attribution 4.0 International License] {{Webarchive|url=https://web.archive.org/web/20171016050101/https://creativecommons.org/licenses/by/4.0/ |date=16 October 2017 }}.</ref><ref name="Poczai and Santiago-Blay 2022b">{{cite journal | authors = Poczai P, Santiago-Blay JA | title = Chip Off the Old Block: Generation, Development, and Ancestral Concepts of Heredity | journal = Frontiers in Genetics | volume = 13 | pages = 814436 | date = 2022 | pmid = 35356423 | pmc = 8959437 | doi = 10.3389/fgene.2022.814436 | doi-access = free }}</ref>。[[File:Blending Inheritance.svg|thumb|{{Ill2|融合遺伝|en|Blending inheritance}}は、あらゆる特性を平均化する。技術者[[フリーミング・ジェンキン|フレミング・ジェンキン]]が指摘したように、これは[[自然選択説|自然選択]]による進化が不可能なことを意味する。]] |
|||
このように、遺伝学は遺伝子という生物の基本的な要素につながっているため、現在ではあらゆる分野に結びついている。 |
|||
メンデルの研究に先立つ、別の遺伝理論もあった。19世紀に広く支持されていた{{Ill2|融合遺伝|en|Blending inheritance|label=融合遺伝説}}(blending inheritance)は、[[チャールズ・ダーウィン]]の著書『[[種の起源]]』(1859年)でも示唆されていた理論である<ref name="Hamilton2011">{{cite book | author = Hamilton H |title=Population Genetics |url=https://books.google.com/books?id=ng85sd1UR7EC&pg=PT26 |year=2011 |publisher=Georgetown University |isbn=978-1-4443-6245-9 |page=26}}</ref>。メンデルの研究は、交配後に形質が明らかに融合しない例を示し、形質は連続的な混ざり合いではなく、異なる遺伝子の組み合わせによって生み出されることを示した。現在は、子孫における形質の融合は、{{Ill2|量的遺伝学|en|Quantitative genetics|label=量的効果}}を持つ複数の遺伝子の作用によって説明されている。当時、一定の支持を集めていたもう一つの理論に、[[ラマルキズム|獲得形質の遺伝説]]がある。これは、子孫が両親によって強化された形質を遺伝するという考え方である。この理論([[ジャン=バティスト・ラマルク]]に関連)は、現在では誤りであることが分かっていて、個体の経験は子孫に受け継がれる遺伝子に影響を及ぼすことはない<ref>Lamarck, J-B (2008). In [[:en:Encyclopædia Britannica|Encyclopædia Britannica]]. Retrieved from [http://www.search.eb.com/eb/article-273180 Encyclopædia Britannica Online] {{Webarchive|url=https://web.archive.org/web/20200414173437/http://www.search.eb.com/eb/article-273180 |date=14 April 2020 }} on 16 March 2008.</ref>。その他の理論としては、ダーウィンの[[パンゲネシス|パンゲネシス説]](獲得的と遺伝的の両側面を持つ)や、[[フランシス・ゴルトン]]によるパンゲネシス説の再定式化(粒子的と遺伝的の両側面を持つ)などがある<ref>[[:en:Peter J. Bowler|Peter J. Bowler]], ''The Mendelian Revolution: The Emergency of Hereditarian Concepts in Modern Science and Society'' (Baltimore: Johns Hopkins University Press, 1989): chapters 2 & 3.</ref>。 |
|||
== 遺伝学の歴史 == |
|||
=== 前史 === |
|||
遺伝現象は古くから知られていたが、その理論付けは困難であった。古くは[[ヒポクラテス]]がこれについて言及し、生物体の各部分が何らかの物質を作り、これが子孫に伝わって子を親の形に似せる、という、遺伝物質を想定したような表現をしている。[[アリストテレス]]はこの点についてははっきりとした表現をしていない。彼は[[優性]]を現象的には知っていたが、説明を持ち合わせなかった。彼は多くの生物が異種間の[[雑種]]として生まれたと考えていた<ref>中沢(1985)、p.15-17</ref>。 |
|||
=== メンデル遺伝学 === |
|||
他方、[[農業]]部門では[[雌雄異株]]の植物([[イチジク]]など)を通じて[[人工授粉]]の手法が古くから成立し、17世紀頃にはこれが交配に当たるとの認識が成り立った。植物で交雑実験を行ったのはドイツの[[ヨーゼフ・ゴットリープ・ケールロイター|ヨーゼフ・ケールロイター]]とされる。彼は18世紀半ばに様々な交配実験を行い、雑種は中間の形質を示すこと、ただし片方に似ることもあること、両者の縁が遠い場合には不稔の雑種ができること、また時に両者より強い雑種を生じること([[雑種強勢]])などを認めた。それ以降19世紀までこれに追随する交配実験が行われた。1830年には[[オランダ王立芸術科学アカデミー|オランダの科学アカデミー]]が交雑によって新変種を作る研究の懸賞論文を出している<ref>中沢(1985)、p.22-25</ref>。 |
|||
[[File:Sexlinked inheritance white.jpg|thumb|[[トーマス・ハント・モーガン|モーガン]]は、[[ショウジョウバエ]] ({{Snamei|[[:en:Drosophila|Drosophila]]}}) の白色目を引き起こす変異の[[伴性遺伝]]を観察し、遺伝子は染色体上に存在するという仮説を立てた]] |
|||
{{main|{{ill2|メンデル遺伝学|en|Mendelian inheritance|preserve=1}}}} |
|||
このような中で、遺伝する形質([[表現型]])は交雑とともに混じりあっていくと考えられていた。これは、雑種がその両親の中間的な性質を示すことが多いことに基づく。しかし、たとえば[[トーマス・アンドルー・ナイト|トーマス・ナイト]]は純系の株同士の交配では片親の形質だけが子に現れることを報告している。ちなみに、彼が行ったエンドウの実験が、後のメンデルの実験の基礎となっている。他に、1824年にジョン・ゴスはやはりエンドウについて、一代目で見られなかった形質が二代目に出現することも見ている。[[カール・ゲルトナー]]は上記懸賞論文に応募して賞を得た。彼は想定された遺伝物質をエレメントと名付け、これはメンデルも採用したところである。[[チャールズ・ダーウィン]]も交配実験に取り組み、一代目が片親の形質を示すこと、二代目には両方の形質が現れることなどを見ている。ただし二代目の分離比が一定になる、というような観点を持たず、やはり体で作られる物質が子の体の各部に配分される、というような説にまとまっている<ref>中沢(1985)、p.27</ref>。 |
|||
現代遺伝学は、植物における遺伝の性質に関するメンデルの研究から始まった。1865年に[[ブルノ]]の自然研究協会<!-- Naturforschender Verein (Society for Research in Nature) -->に提出された論文「''Versuche über Pflanzenhybriden''」({{Ill2|植物雑種の実験|en|Experiments on Plant Hybridization}})で、メンデルは[[エンドウ]]植物の特定の形質の遺伝様式を追跡し、数学的に説明した。この遺伝様式は、ごく一部の形質でのみ観察されたものであったが、メンデルの研究は、遺伝は粒子的であり獲得された(後天的な)ものではなく、しかも多くの形質の遺伝様式は、単純な規則と比率によって説明できることを示唆していた<ref name="mendel">{{cite web |title=Mendel's Paper in English |url=http://www.mendelweb.org/Mendel.html |author=Blumberg RB |url-status=live |archive-url=https://web.archive.org/web/20160113051202/http://www.mendelweb.org/Mendel.html |archive-date=13 January 2016 |access-date=2009-09-28}}</ref>。 |
|||
=== メンデルとその再発見以前 === |
|||
[[グレゴール・ヨハン・メンデル|メンデル]]は[[エンドウマメ]]の形態に注目して1856年から交配実験を行い、その結果を分析し、それが三つの法則にまとめられると考えた。彼は1865年にブルノ自然研究会で口頭発表し、翌年には会誌に論文を発表した。彼によると、形態の遺伝は一対の遺伝[[粒子]]を仮定することで説明できる。それは親の体内では変化を被ることなく子に受け継がれる。また各個体は両親からこれを1個ずつ受け取り、子をなす際には自分の作る配偶子にこれを1個ずつ分配する。詳しくは[[メンデルの法則]]を参照。 |
|||
メンデルの業績の重要性は、彼の死後、1900年に[[ユーゴー・ド・フリース]]をはじめとする科学者が、彼の研究を再発見して広く理解されるようになった。メンデルの研究を支持していた[[ウィリアム・ベイトソン]]は、1905年に「''genetics''(遺伝学)」という言葉を考案した<ref>genetics, ''n.'', [[:en:Oxford English Dictionary|Oxford English Dictionary]], 3rd ed.</ref><ref>{{cite web |url=http://www.jic.ac.uk/corporate/about/bateson.htm |title=Letter from William Bateson to Alan Sedgwick in 1905 |publisher=The John Innes Centre |access-date=15 March 2008 |author=Bateson W |url-status=dead |archive-url=https://web.archive.org/web/20071013020831/http://www.jic.ac.uk/corporate/about/bateson.htm |archive-date=13 October 2007}} The letter was to an Adam Sedgwick, a zoologist and "Reader in Animal Morphology" at [[:en:Trinity College, Cambridge|Trinity College, Cambridge]]</ref>。形容詞「''genetic''(遺伝的)」は、「origin(起源)」を意味するギリシャ語の γένεσις (''genesis'')に由来し、名詞よりも古く、1860年に初めて生物学的な意味で使用された<ref>genetic, ''adj.'', Oxford English Dictionary, 3rd ed.</ref>。ベイトソンは指導者として努めるとともに、ケンブリッジ大学ニューナム・カレッジの他の科学者たち、特に[[エディス・レベッカ・ソーンダース|ベッキー・ソーンダース]]<!-- Becky Saunders -->、[[:en:Nora_Barlow|Nora Darwin Barlow]]、[[:en:Muriel_Onslow|Muriel Wheldale Onslow]] の研究からも大いに助けを受けた<ref>{{cite journal | authors = Richmond ML | title = Opportunities for women in early genetics | journal = Nature Reviews. Genetics | volume = 8 | issue = 11 | pages = 897–902 | date = November 2007 | pmid = 17893692 | doi = 10.1038/nrg2200 | url = http://www.nature.com/reviews/genetics | url-status = live | s2cid = 21992183 | df = dmy-all | archive-url = https://web.archive.org/web/20080516070928/http://www.nature.com/reviews/genetics/ | archive-date = 16 May 2008 }}</ref>。ベイトソンは、1906年に[[ロンドン]]で開催された第3回国際植物増殖者会議<!-- Third International Conference on Plant Hybridization -->の就任演説で、遺伝の研究を説明する用語として「''genetics''(遺伝学)」を普及させた<ref name="bateson_genetics">{{cite conference |author=Bateson W |title=The Progress of Genetic Research |editor=Wilks, W |book-title=Report of the Third 1906 International Conference on Genetics: Hybridization (the cross-breeding of genera or species), the cross-breeding of varieties, and general plant breeding|publisher=Royal Horticultural Society |location=London |year=1907}} :Initially titled the "International Conference on Hybridisation and Plant Breeding", the title was changed as a result of Bateson's speech. See: {{Cite book|author=Cock AG, Forsdyke DR |year=2008|title=Treasure your exceptions: the science and life of William Bateson|url=https://archive.org/details/treasureyourexce00cock |url-access=limited |publisher=Springer|isbn=978-0-387-75687-5|page=[https://archive.org/details/treasureyourexce00cock/page/n265 248]}}</ref>。 |
|||
彼の発表、および論文がある程度の範囲の専門家の耳に入っていたのは間違いないが、大きな評価を得ることはできず、1900年に再発見されるまで反響はなかった。他方でそれまでと同様に様々な交配実験が行われ、時にはその報告にメンデルの論文が引用された例もある。むしろ、この間に細胞や[[染色体]]に関する知見が正確化した点が大きいかもしれない。たとえば植物において花粉と卵子が受精することが判明し、また[[減数分裂]]の存在が予想されるようになっている。 |
|||
メンデルの研究が再発見された後、科学者たちは細胞内のどの分子が遺伝に関与しているのか特定しようとした。1900年、[[:en:Nettie_Stevens|Nettie Stevens]] は[[ミールワーム]]<!-- mealworm -->の研究を始めた<ref name="net">{{cite web |title=Nettie Stevens: A Discoverer of Sex Chromosomes |url=https://www.nature.com/scitable/topicpage/nettie-stevens-a-discoverer-of-sex-chromosomes-6580266/ |website=Scitable |publisher=Nature Education |access-date=8 June 2020}}</ref>。それから11年間にわたる研究で、メスは [[X染色体]]のみを持ち、オスは X染色体と [[Y染色体]]の両方を持ち合わせていることを発見した<ref name="net" />。彼女は、性別は染色体因子であり、オスによって決定されるという結論に達した<ref name="net" />。1911年、[[トーマス・ハント・モーガン]]は、[[キイロショウジョウバエ|ショウジョウバエ]]の{{Ill2|白 (変異)|en|White (mutation)|label=白色眼}}の伴性変異<!-- sex-linked white eye mutation -->の観察に基づいて、遺伝子は[[染色体]]上にあると主張した<ref>{{cite journal |doi=10.1093/icb/23.4.855 |title=Thomas Hunt Morgan – The Geneticist |year=1983 | authors = Moore JA |journal=Integrative and Comparative Biology |volume=23 |pages=855–865 |issue=4|doi-access= }}</ref>。1913年、モーガンの教え子である[[アルフレッド・ヘンリー・スターティヴァント|アルフレッド・スターティヴァント]]は、[[遺伝的連鎖]]という現象を利用して、遺伝子が染色体上に直線状に配置していることを説明した<ref>{{cite journal | authors=Sturtevant AH |year=1913 |title=The linear arrangement of six sex-linked factors in Drosophila, as shown by their mode of association |journal=Journal of Experimental Biology |volume=14 |issue=1 |pages=43–59 |url=http://www.esp.org/foundations/genetics/classical/holdings/s/ahs-13.pdf |doi=10.1002/jez.1400140104 |bibcode=1913JEZ....14...43S |url-status=live |archive-url=https://web.archive.org/web/20080227183131/http://www.esp.org/foundations/genetics/classical/holdings/s/ahs-13.pdf |archive-date=27 February 2008 |citeseerx=10.1.1.37.9595 |s2cid=82583173}}</ref>。 |
|||
この時期、上記の流れとは別に、生物の多様性に注目した研究として[[フランシス・ゴルトン]]による[[生物統計学]]も創始されている。これは現代では非科学的な[[優生学]]を含んだものであったが、「継承されるもの」としての遺伝の性質を説明したメンデルの研究では捉えきれなかった、「集団内の連続的な多様性」を説明する遺伝の性質を捉えたものであった。<ref>http://www.iwanami.co.jp/.PDFS/00/9/0050550.pdf 鎌谷直之(2007) 遺伝統計学入門</ref>これらの研究は、対象の過程を研究する中で統計学の発展と生物現象への統計解析の導入を促し、集団遺伝学が誕生する土壌となったと言える。 |
|||
=== |
=== 分子遺伝学 === |
||
{{Main|{{ill2|分子遺伝学|en|Molecular genetics|preserve=1}}}} |
|||
1900年に3人の研究者([[ユーゴー・ド・フリース]]、[[カール・エーリヒ・コレンス]]、[[エーリヒ・フォン・チェルマク]])がそれぞれ独自にメンデルの法則を再発見した。ちなみに、同年、[[ウィリアム・ベイトソン]]はたまたまメンデルの論文を入手して、その重要性に驚いて広く説いて回った。とりわけ、ベイトソンと[[カール・ピアソン]]の間では激しい論争が繰り広げられた。 |
|||
[[File:DNA Overview2.png|thumb|upright=0.6|[[デオキシリボ核酸|DNA]]は生物の[[遺伝]]における分子的基盤である。DNAの各鎖はそれぞれ[[ヌクレオチド]]の鎖で、中央で互いに合致し、ねじれた[[梯子]]の横木のように見える。]] |
|||
このようにして遺伝子の論が広く知られると、1902年には[[ウォルター・S・サットン]]が[[染色体]]の観察から遺伝の[[染色体説]]を提唱した。染色体上に遺伝子があるとすると[[独立の法則]]が危うくなる(実際、ベイトソンや後述のモーガンがそれぞれスイートピーやショウジョウバエでこの法則が成立しないケースがあることを発見している<ref>後にこれは同じ染色体上にそれらの遺伝子が一緒に乗っていたためと判明。<br>([[#吉川・西沢1969|吉川・西沢(1969)p.134「独立の法則」]])</ref>)が、これを埋めたのが[[遺伝的連鎖|連鎖]]と[[組み換え]]の発見である。[[トーマス・ハント・モーガン|モーガン]]らは、[[ショウジョウバエ]]を材料として突然変異を調べ、目が白いものを筆頭にいくつもの突然変異を見つけ、そのうちのいくつかは[[伴性遺伝]]をすることから、雌雄によって本数が違うX染色体上にこれがあるはずだが、突然変異の数だけX染色体があるわけではない(雌2本、雄1本)のでこれらの突然変異が何か一定の関係をもってX染色体に乗っていることが推察され、そこで染色体上の遺伝子が「乗り換える」という仮説を立て、'''2本の相同染色体が互いにその一部を交換する'''と仮定して分析をしたところ、'''各々の遺伝子は染色体上の一定の位置に規則正しく配列されている'''という結論に達した(これ以外に突然変異の起こる率が染色体の長さに比例することや、染色体の[[染色体不分離|不分離]]現象からもこうしたことが確認された)。こうしたことを基に染色体説が証明され、ショウジョウバエなどでどこに何の遺伝子が乗っているかを調べる染色体地図(リンゲージ地図)という物が作成された<ref>[[#吉川・西沢1969|吉川・西沢(1969)p.134「独立の法則」]]</ref>。 |
|||
遺伝子が染色体上に存在することは分かっていたが、染色体は[[タンパク質]]とDNAの両方で構成されているため、2つのうちどちらが遺伝に関与しているか科学者たちは知らなかった。1928年、[[フレデリック・グリフィス]]は、死んだ細菌が別の生きている細菌に[[遺伝物質]]を伝達し、その細菌を[[形質転換]]させる[[グリフィスの実験|現象を発見した]]。それから16年後の1944年、[[アベリー-マクロード-マッカーティの実験|アベリー - マクロード - マッカーティの実験]]により、形質転換の原因分子がDNAであることが特定された<ref name="Avery_et_al">{{cite journal | authors = Avery OT, Macleod CM, McCarty M | title = STUDIES ON THE CHEMICAL NATURE OF THE SUBSTANCE INDUCING TRANSFORMATION OF PNEUMOCOCCAL TYPES : INDUCTION OF TRANSFORMATION BY A DESOXYRIBONUCLEIC ACID FRACTION ISOLATED FROM PNEUMOCOCCUS TYPE III | journal = The Journal of Experimental Medicine | volume = 79 | issue = 2 | pages = 137–158 | date = February 1944 | pmid = 19871359 | pmc = 2135445 | doi = 10.1084/jem.79.2.137 }} Reprint: {{cite journal | authors = Avery OT, MacLeod CM, McCarty M | title = Studies on the chemical nature of the substance inducing transformation of pneumococcal types. Inductions of transformation by a desoxyribonucleic acid fraction isolated from pneumococcus type III | journal = The Journal of Experimental Medicine | volume = 149 | issue = 2 | pages = 297–326 | date = February 1979 | pmid = 33226 | pmc = 2184805 | doi = 10.1084/jem.149.2.297 }}</ref>。真核生物における[[遺伝情報]]の保管場所としての[[細胞核|核]]の役割は、1943年に [[:en:Joachim Hämmerling|Hämmerling]] が単細胞藻類である[[カサノリ属]]({{Snamei|[[:en:Acetabularia|Acetabularia]]}})の研究で確立していた<ref>{{cite book |title=Cell and Molecular Biology | author = Khanna P |publisher=I.K. International Pvt Ltd |date=2008 |page=221 |isbn=978-81-89866-59-4 }}</ref>。1952年に[[ハーシーとチェイスの実験|ハーシーとチェイスが行った実験]]により、細菌に感染する[[ウイルス]]の遺伝物質はタンパク質ではなくDNAであることが確認され、DNAが遺伝を担う分子であるというさらなる証拠が示された<ref>{{cite journal | authors = Hershey AD, Chase M | title = Independent functions of viral protein and nucleic acid in growth of bacteriophage | journal = The Journal of General Physiology | volume = 36 | issue = 1 | pages = 39–56 | date = May 1952 | pmid = 12981234 | pmc = 2147348 | doi = 10.1085/jgp.36.1.39 }}</ref>。 |
|||
さらに1933年のペインターによる双翅類の唾腺染色体(普通の染色体に比べて長さも幅も100倍以上ある)の遺伝子のあると思われる部分にアセトカーミンで染めた場合濃い帯の縞模様が出てくるが、これが熟練するとどこの部位かも分かるほど太さや間隔に規則性が見られ、染色体異常の個体の場合も異常が明瞭に観察できると報告し、モーガンの弟子のブリッジェスはこの研究を進めショウジョウバエの「唾腺染色体地図」という物を作成し、ショウジョウバエの研究に前述のリンゲージ地図と共に重要な役割をしたが、この「遺伝子は染色体上に一定の順序で並んでいる」というのはその後人間を含む高等生物からカビ・バクテリア・ファージといった微生物まで成立すると分かった<ref>[[#吉川・西沢1969|吉川・西沢(1969)p.134「独立の法則」・p.149「唾腺染色体」]]</ref>。 |
|||
1953年、[[ジェームズ・ワトソン]]と[[フランシス・クリック]]は、[[ロザリンド・フランクリン]]と[[モーリス・ウィルキンス]]によるDNAがらせん構造であることを示す[[X線結晶構造解析]]の結果を基に、DNAの構造を決定した<ref>{{cite book |title=The Eighth Day of Creation: Makers of the Revolution in Biology | author = Judson H |author-link=Horace Freeland Judson |year=1979 |publisher=Cold Spring Harbor Laboratory Press |isbn=978-0-87969-477-7 |pages=51–169}}</ref><ref name="watsoncrick_1953a">{{cite journal | authors = Watson JD, Crick FH | title = Molecular structure of nucleic acids; a structure for deoxyribose nucleic acid | journal = Nature | volume = 171 | issue = 4356 | pages = 737–738 | date = April 1953 | pmid = 13054692 | doi = 10.1038/171737a0 | url = http://www.nature.com/nature/dna50/watsoncrick.pdf | url-status = live | s2cid = 4253007 | df = dmy-all | bibcode = 1953Natur.171..737W | archive-url = https://web.archive.org/web/20070204110320/http://www.nature.com/nature/dna50/watsoncrick.pdf | archive-date = 4 February 2007 }}</ref>。彼らの[[二重らせん]]モデルは 2本のDNA鎖で構成されており、一方の鎖上に結合したヌクレオチドは、他方の鎖上の相補的なヌクレオチドと合致し、ねじれた[[梯子]]の横木のような形を形成していた<ref name="watsoncrick_1953b">{{cite journal | authors = Watson JD, Crick FH | title = Genetical implications of the structure of deoxyribonucleic acid | journal = Nature | volume = 171 | issue = 4361 | pages = 964–967 | date = May 1953 | pmid = 13063483 | doi = 10.1038/171964b0 | url = http://www.nature.com/nature/dna50/watsoncrick2.pdf | url-status = live | s2cid = 4256010 | df = dmy-all | bibcode = 1953Natur.171..964W | archive-url = https://web.archive.org/web/20030621051153/http://www.nature.com/nature/dna50/watsoncrick2.pdf | archive-date = 21 June 2003 }}</ref>。この構造により、遺伝情報はそれぞれのDNA鎖上のヌクレオチド配列に存在することが明らかになった。また、この構造は簡単な[[DNA複製|複製方法]]も示唆していた。すなわち、DNAの2本鎖を分離すると、新しい[[相補性 (分子生物学)|相補]]鎖は古い鎖の配列に基づいて再構築される。この特徴により、新しいDNAの1本鎖は元のDNA鎖の親から作られるという、半保存的な性質がDNAにもたらされた<ref>{{cite journal | authors = Stratmann SA, van Oijen AM | title = DNA replication at the single-molecule level | journal = Chemical Society Reviews | volume = 43 | issue = 4 | pages = 1201–1220 | date = February 2014 | pmid = 24395040 | doi = 10.1039/c3cs60391a | url = https://pure.rug.nl/ws/files/14412201/2014ChemSocRevStratmann.pdf | url-status = live | s2cid = 205856075 | archive-url = https://web.archive.org/web/20170706055534/https://pure.rug.nl/ws/files/14412201/2014ChemSocRevStratmann.pdf | archive-date = 2017-07-06 }}</ref>。 |
|||
また、この時代と平行して、集団遺伝学の成立、[[ハーマン・J・マラー]]のX線によるショウジョウバエの人工突然変異の誘発、[[テロメア]]の発見、[[自然選択説]]と遺伝学の統合を図る[[ネオダーウィニズム]]の誕生、[[バーバラ・マクリントック]]によるトウモロコシにおける[[トランスポゾン]]の発見も起こっている。 |
|||
DNAの構造は遺伝の仕組みを示唆していたが、DNAが細胞の働きにどのように影響するかは、まだ分かっていなかった。その後の数年間、科学者たちは、DNAがどのように[[タンパク質生合成|タンパク質の生成プロセス]]を制御するかを理解しようと努めた<ref name="Betz2010">{{cite book | author = Frederick B |title=Managing Science: Methodology and Organization of Research |url=https://books.google.com/books?id=1ARRexcXgAgC&pg=PA76 |year=2010 |publisher=Springer |isbn=978-1-4419-7488-4 |page=76}}</ref>。そして、細胞はDNAを鋳型として、DNAと非常によく似たヌクレオチドを持つ分子である[[メッセンジャーRNA]](伝令RNAともいう)を生成することが明らかになった。メッセンジャーRNAのヌクレオチド配列は、タンパク質の[[アミノ酸]]配列を作るために使われる。このヌクレオチド配列とアミノ酸配列との変換は、[[遺伝暗号]](genetic code)と呼ばれている<ref name="Rice2009">{{cite book | author = Rice SA |title=Encyclopedia of Evolution |url=https://books.google.com/books?id=YRcAVvmE6eMC&pg=PA134 |year=2009 |publisher=Infobase Publishing |isbn=978-1-4381-1005-9 |page=134}}</ref>。 |
|||
==== 分子生物学の黎明期〜DNAの立体構造決定==== |
|||
これ以降、[[セントラルドグマ]]の時代までの研究は大きく2つの流れがある。一つは遺伝子の物質的な基礎の研究であり、もうひとつは遺伝子の形質発現のしくみの解明である。 |
|||
遺伝に関する分子的理解が深まるにつれて研究は爆発的に増加した<ref name="Sarkar1998">{{cite book | author = Sarkar S |title=Genetics and Reductionism |url=https://books.google.com/books?id=7lzpDHFw-40C&pg=PA140 |year=1998 |publisher=Cambridge University Press |isbn=978-0-521-63713-8 |page=140}}</ref>。1973年、[[太田朋子]]は、[[分子進化の中立説]]を拡張した[[分子進化のほぼ中立説]]という著名な理論を展開した。この理論で太田は、遺伝的[[進化]]が起こる速度に、自然選択と環境が重要な役割を果たすことを強調した<ref>{{cite journal | authors = Ohta T | title = Slightly deleterious mutant substitutions in evolution | journal = Nature | volume = 246 | issue = 5428 | pages = 96–98 | date = November 1973 | pmid = 4585855 | doi = 10.1038/246096a0 | s2cid = 4226804 | bibcode = 1973Natur.246...96O }}</ref>。重要な発見の一つに、1977年に[[フレデリック・サンガー]]が開発した[[DNAシークエンシング#酵素法|連鎖停止DNA配列決定法]](chain-termination DNA sequencing)がある。この技術により、科学者はDNA分子のヌクレオチド配列を読み取ることができるようになった<ref name="sanger_et_al">{{cite journal | authors = Sanger F, Nicklen S, Coulson AR | title = DNA sequencing with chain-terminating inhibitors | journal = Proceedings of the National Academy of Sciences of the United States of America | volume = 74 | issue = 12 | pages = 5463–5467 | date = December 1977 | pmid = 271968 | pmc = 431765 | doi = 10.1073/pnas.74.12.5463 | doi-access = free | bibcode = 1977PNAS...74.5463S }}</ref>。1983年には、[[キャリー・マリス|キャリー・バンクス・マリス]]が[[ポリメラーゼ連鎖反応|ポリメラーゼ連鎖反応法]](PCR)を開発し、混合物からDNAの特定部分を迅速に分離し増幅する方法がもたらされた<ref name="saiki_et_al">{{cite journal | authors = Saiki RK, Scharf S, Faloona F, Mullis KB, Horn GT, Erlich HA, Arnheim N | title = Enzymatic amplification of beta-globin genomic sequences and restriction site analysis for diagnosis of sickle cell anemia | journal = Science | volume = 230 | issue = 4732 | pages = 1350–1354 | date = December 1985 | pmid = 2999980 | doi = 10.1126/science.2999980 | bibcode = 1985Sci...230.1350S }}</ref>。2003年、[[ヒトゲノム・プロジェクト]]、[[アメリカ合衆国エネルギー省|米国エネルギー省]]、[[アメリカ国立衛生研究所|米国国立衛生研究所]](NIH)、民間企業[[セレラ|セレラ・コーポレーション]]による並行した取り組みによって、[[ヒトゲノム]]の配列が決定された<ref name="human_genome_project" /><ref>{{Cite journal|title=The sequence of the human genome|journal=Science|volume=291}}</ref>。 |
|||
===== 遺伝子の本体の追求 ===== |
|||
染色体は [[デオキシリボ核酸|DNA]] や[[タンパク質]]から構成されており、当時、遺伝子の正体はタンパク質であると考えられていた。しかしまず、1944年の[[肺炎双球菌]]の[[形質転換]]の研究や、1952年の[[ハーシーとチェイスの実験|ハーシーらの実験]]により DNA が遺伝子の本体であることが明らかにされた。その立体構造については、1953年に[[ジェームズ・ワトソン|ワトソン]]と[[フランシス・クリック|クリック]]が[[二重螺旋構造]]を提唱し、認められた。 |
|||
== 遺伝の特徴 == |
|||
[[フェニルケトン尿症]]などの研究から、遺伝子の発現が[[酵素]]の合成に関わるものであるとの予測はあった。[[ジョージ・ウェルズ・ビードル|ビードル]]と[[エドワード・ローリー・タータム|タータム]]は[[アカパンカビ]]を用いて[[栄養要求株]]の研究を行い、遺伝子は特定の酵素の合成に与るもので、形質は酵素の働きの結果であるとする[[一遺伝子一酵素説]]を1941年に発表した。 |
|||
=== 離散的遺伝とメンデルの法則 === |
|||
{{Main|{{ill2|メンデル遺伝学|en|Mendelian inheritance|preserve=1}}}} |
|||
DNAの立体構造決定以後、DNAが細胞にどのように作用するかという点が研究されていった。[[mRNA]]、[[tRNA]]、[[コドン]]の発見、機能解明から[[遺伝子発現]]の基礎的な仕組みが現在では分かっている。 |
|||
[[File:Punnett square mendel flowers.svg|right|thumb|紫 (B) と白 (b) の花をつける[[ヘテロ接合型]]のエンドウの交配を描いた{{Ill2|パネットの方形|en|Punnett square|preserve=1}}]] |
|||
技術的な発展としては、1977年に発表された[[サンガー法]]が改良された[[DNAシークエンシング]]や、80年代に発展した[[PCR法]]が標準的な手法となっている。 |
|||
最も基本的なレベルでは、生物の遺伝は、[[遺伝子]](gene)と呼ばれる離散的遺伝単位<!-- discrete heritable units -->を親から子へと受け継ぐことによって行われる<ref name="griffiths2000sect199">{{cite book | veditors = Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbart|title=An Introduction to Genetic Analysis |year=2000 |isbn=978-0-7167-3520-5 |edition=7th |publisher=W.H. Freeman |location=New York |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=iga.section.199 |chapter=Patterns of Inheritance: Introduction}}</ref>。この特徴は、[[エンドウ]]の遺伝形質の分離を研究したグレゴール・メンデルによって初めて観察された。たとえば、1本のエンドウの花の色は紫か白のどちらかであり、中間色はないことを示した。遺伝形質(表現型)を制御する同じ遺伝子の個々の型を[[アレル]](allele)と呼ぶ<ref name="mendel" /><ref name="griffiths2000sect200">{{cite book | veditors = Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbart|title=An Introduction to Genetic Analysis |year=2000 |isbn=978-0-7167-3520-5 |edition=7th |publisher=W.H. Freeman |location=New York |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=iga.section.200 |chapter=Mendel's experiments}}</ref>。 |
|||
そして、2003年には[[ヒトゲノム]]が解読完了しており、今後はゲノムレベル、細胞レベルでの遺伝子の役割や、多様性が注目されていくだろうと言われている。 |
|||
[[二倍体]]種<!-- diploid species -->であるエンドウの場合、各個体は両親から1つずつ遺伝子を受け継ぎ、遺伝子の複製を2つ持っている<ref name="griffiths2000sect484" />。ヒトを含む多くの生物種がこの遺伝様式である。ある遺伝子の2つのアレルが同一の二倍体生物は、その[[遺伝子座]]において[[ホモ接合型]](homozygous)と呼ばれ、一方、ある遺伝子の2つのアレルが異なる二倍体生物は[[ヘテロ接合型]](heterozygous)と呼ばれる。ある生物において、アレルの種類を[[遺伝子型]](genotype)といい、その生物の観察可能な形質を[[表現型]](phenotype)という。ある遺伝子がヘテロ接合型である場合、多くの場合、一方のアレルは生物の表現型を支配する性質を持つため[[顕性]](dominant){{Efn|かつての訳語は「優性」であったが、後述の潜性(劣性)とともに、優劣という価値観を含む語感により誤った理解をされることが多いことから、[[日本遺伝学会]]により2017年に用語が改定された<ref name="gsj">{{Cite report|和書|url=https://gsj3.org/wordpress_v2/wp-content/themes/gsj3/assets/docs/pdf/revisionterm_20170911.pdf|title=遺伝学用語改訂について|date=2017-09-11 |author=日本遺伝学会|pages=1–3|accessdate=2024-08-09}}</ref>。}}と呼ばれ、もう一方のアレルは性質が後退して観察されないため[[潜性]](recessive){{Efn|かつての訳語は「劣性」であったが、前述の顕性(優性)とともに、優劣という価値観を含む語感により誤った理解をされることが多いことから、[[日本遺伝学会]]により2017年に用語が改定された<ref name="gsj"/>。}}と呼ばれる。アレルの中には、[[完全優性|完全顕性]](complete dominance)ではなく、中間的な表現型を発現する[[不完全優性|不完全顕性]](incomplete dominance)を示したり、両方のアレルが同時に発現する[[共優性|共顕性]](codominance)を示すものもある<ref name="griffiths2000sect630">{{cite book | veditors = Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbart|title=An Introduction to Genetic Analysis |year=2000 |isbn=978-0-7167-3520-5 |edition=7th |publisher=W.H. Freeman |location=New York |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=iga.section.630 |chapter=Interactions between the alleles of one gene}}</ref>。 |
|||
==他分野との関連== |
|||
===発生学=== |
|||
一組の生物が[[有性生殖]]する場合、その子孫はどちらの両親からも2つのアレルのうちの1つを無作為に受け継ぐ。このような離散的遺伝とアレルの分離の観察は、総称して「メンデルの第一法則(Mendel's first law)」または「[[分離の法則]](Law of Segregation)」として知られている。しかし、ある遺伝子が他の遺伝子よりも顕性になる確率は、顕性、潜性、ホモ接合、ヘテロ接合によって変わる可能性がある。たとえば、メンデルは、ヘテロ接合体の生物を交配した場合、顕性形質が現れる確率は3:1であることを発見した。実際の遺伝学者は、理論的確率、経験的確率、積の法則、和の法則などを用いて確率を研究し、推定している<ref>{{Cite web |title=Probabilities in genetics (article) |url=https://www.khanacademy.org/science/ap-biology/heredity/mendelian-genetics-ap/a/probabilities-in-genetics |access-date=2022-09-28 |website=Khan Academy}}</ref>。 |
|||
[[発生学]]は『蛙の子がカエルになる』のはなぜかを解き明かすという点で、遺伝学と裏表の関係にある。ただし対象が組織であったためにその発達は早かった。[[実験発生学]]は[[胚発生]]の仕組みとして[[誘導]]を発見したが、その原因要素の解明の段階で深い混迷に沈んだ。これに手が着くようになったのは1990年代以降で、胚発生の段階で部域特異的に発現する遺伝子やそれによって合成される[[タンパク質]]群の機能を研究するような方法で進み始めた。そこでは[[遺伝子工学]]の方法が積極的に活用され、[[発生遺伝学]]といわれる分野を形成している。 |
|||
=== 表記法と図 === |
|||
[[File:Pedigree-chart-example.svg|thumb|left|upright=1.1|遺伝系図 (genetic pedigree charts) は、形質の遺伝様式を追跡するのに役立つ。]] |
|||
遺伝学者は、遺伝について図や記号で説明する。遺伝子は1文字または数文字で表される。上付きの「+」記号は、遺伝子の通常の[[野生型|非変異アレル]]を示すことが多い<ref>{{cite web|url=http://faculty.users.cnu.edu/rcheney/Genetic%20Notation.htm|title=Genetic Notation| author = Cheney RW |publisher=Christopher Newport University|access-date=18 March 2008|archive-url=https://web.archive.org/web/20080103021518/http://faculty.users.cnu.edu/rcheney/Genetic%20Notation.htm|archive-date=3 January 2008}}</ref>。 |
|||
受精と交配の実験(特にメンデルの法則について議論する場合)では、親をP世代、子をF1世代(雑種第一代)と呼ぶ。F1の子が互いに交配すると、その子孫はF2世代(雑種第二代)と呼ばれる。交配の結果を予測する際、一般的に使用される図表に{{Ill2|パネットの方形|en|Punnett square|preserve=1|label=パネット方形図}}がある<ref name="Müller-Wille-Parolini_2020">{{cite book |chapter=Punnett squares and hybrid crosses: how Mendelians learned their trade by the book | author = Müller-Wille S, Parolini G |publisher=[[:en:British Society for the History of Science|British Society for the History of Science]] / [[:en:Cambridge University Press|Cambridge University Press]] |date=2020-12-09 |series=BJHS Themes |volume=5 |title=Learning by the Book: Manuals and Handbooks in the History of Science |pages=149–165 |doi=10.1017/bjt.2020.12 |s2cid=229344415 |url=https://www.cambridge.org/core/journals/bjhs-themes/article/punnett-squares-and-hybrid-crosses-how-mendelians-learned-their-trade-by-the-book/18A1CE37A6EE536CC1CE1D4FF6FF3174 |access-date=2021-03-29 |url-status=live |archive-url=https://web.archive.org/web/20210329111650/https://www.cambridge.org/core/journals/bjhs-themes/article/punnett-squares-and-hybrid-crosses-how-mendelians-learned-their-trade-by-the-book/18A1CE37A6EE536CC1CE1D4FF6FF3174 |archive-date=2021-03-29}}</ref>。 |
|||
遺伝学者は、ヒトの[[遺伝性疾患]]を研究する際に、{{Ill2|系図 (遺伝学)|en|Pedigree chart|preserve=1|label=系図}}を用いて形質の遺伝を表現することがよくある<ref name="griffiths2000sect229">{{cite book | veditors = Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbart|title=An Introduction to Genetic Analysis |year=2000 |isbn=978-0-7167-3520-5 |edition=7th |publisher=W.H. Freeman |location=New York |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=iga.section.229 |chapter=Human Genetics}}</ref>。これらの図は、系図における形質の遺伝を表している。 |
|||
=== 複数遺伝子の相互作用 === |
|||
[[File:Galton-height-regress.png|thumb|right|ヒトの身長は、複雑な遺伝的要因と関連する形質である。[[フランシス・ゴルトン]]のデータは、親の平均身長と子供の身長の関係を示している (1889年)。]] |
|||
生物は数千もの遺伝子を持っており、有性生殖を行う生物では、これらの遺伝子は通常は互いに独立して組み合わされる。つまり、黄や緑のエンドウの種子(豆)の色に関するアレルの遺伝は、白や紫の花に関するアレルの遺伝とは無関係である。この現象は「メンデルの第二法則(Mendel's second law)」または「[[独立の法則]](Law of Independent Assortment)」として知られており、異なる遺伝子のアレルが両親の間でシャッフルされ、異なる組み合わせを持つ子孫が生まれることを意味する。異なる遺伝子が相互作用し、同じ形質に影響を与えることはよくある。たとえば、ブルーアイドメアリー({{Snamei|[[:en:Omphalodes verna|Omphalodes verna]]}})には、花の色(青または紫)を決定するアレルを持つ遺伝子が存在する。しかし、花が少しでも色づくか、それとも白いかは、別の遺伝子が制御する。この白いアレルを2つ持つ個体は、最初の遺伝子が青または紫のアレルを持つかどうかに関わらず、白い花を咲かせる。このような遺伝子間の相互作用は[[エピスタシス]](epistasis)と呼ばれ、二番目の遺伝子は最初の遺伝子よりも上位<!-- epistatic -->である<ref name="griffiths2000sect644">{{cite book | veditors = Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbart|title=An Introduction to Genetic Analysis |year=2000 |isbn=978-0-7167-3520-5 |edition=7th |publisher=W.H. Freeman |location=New York |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=iga.section.644 |chapter=Gene interaction and modified dihybrid ratios}}</ref>。 |
|||
多くの形質は、離散的な特徴(たとえば、紫や白の花の色)ではなく、連続的な特徴(たとえば、ヒトの身長や[[ヒトの肌の色|肌の色]])である。これらの{{Ill2|複雑な形質|en|Complex traits}}は、多くの遺伝子によって作り出される<ref>{{cite journal | authors = Mayeux R | title = Mapping the new frontier: complex genetic disorders | journal = The Journal of Clinical Investigation | volume = 115 | issue = 6 | pages = 1404–1407 | date = June 2005 | pmid = 15931374 | pmc = 1137013 | doi = 10.1172/JCI25421 }}</ref>。これらの遺伝子の影響は、生物が経験した環境によって(程度の差はあるが)媒介される。生物の特定の遺伝子が複雑な形質にどの程度寄与するかを[[遺伝率]](heritability)という<ref name="griffiths2000sect4009">{{cite book | veditors = Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbart|title=An Introduction to Genetic Analysis |year=2000 |isbn=978-0-7167-3520-5 |edition=7th |publisher=W. H. Freeman |location=New York |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=iga.section.4009 |chapter=Quantifying heritability}}</ref>。ある形質の遺伝率の大きさは相対的なものであり、より変動の大きい環境であれば、その形質の総変動に対する環境影響はより大きくなる。たとえば、ヒトの身長は複雑な原因を持つ形質である。米国における遺伝率は89%である。しかし、栄養状態や[[医療]]の普及にばらつきがあるナイジェリアでは、身長に対する遺伝率は62%にすぎない<ref>{{cite journal | authors = Luke A, Guo X, Adeyemo AA, Wilks R, Forrester T, Lowe W, Comuzzie AG, Martin LJ, Zhu X, Rotimi CN, Cooper RS | title = Heritability of obesity-related traits among Nigerians, Jamaicans and US black people | journal = International Journal of Obesity and Related Metabolic Disorders | volume = 25 | issue = 7 | pages = 1034–1041 | date = July 2001 | pmid = 11443503 | doi = 10.1038/sj.ijo.0801650 | doi-access = free }}</ref>。 |
|||
== 遺伝の分子的基盤 == |
|||
=== DNAと染色体 === |
|||
{{Main|DNA|{{ill2|染色体|en|Chromosome|preserve=1}}}} |
|||
[[File:DNA chemical structure.svg|thumb|right|DNAの[[分子構造]]。塩基は鎖間の[[水素結合]] (中央の点線) の配置によって対合する。]] |
|||
遺伝子の[[分子]]的基盤は[[デオキシリボ核酸]](DNA)である。DNAは[[デオキシリボース]](糖)、[[リン酸基]]、[[核酸塩基|塩基]]から構成されている。塩基は、[[アデニン]](A)、[[シトシン]](C)、[[グアニン]](G)、[[チミン]](T)の4種類がある。リン酸基は糖と[[ホスホジエステル結合|結合]]し、長い糖-リン酸骨格を形成する。2本の骨格鎖の間では塩基が互いに特異的に対合し(TとA、CとG)、梯子の横木のような形を作る。塩基、リン酸、糖が結合して[[ヌクレオチド]]を作り、それらが連結して長いDNA鎖が形成される<ref>{{Cite web | author = Urry L, Cain M, Wasserman S, Minorsky P, Reece J, Campbell N |title=Campbell Biology |url=https://plus.pearson.com/courses/gregg91165/products/GTP1DPWIL20/pages/ac865b14db19976dfd6054de245cd8d8e65000756?locale=&key=2790626781132109428282022&iesCode=5VEW6xrTXI |access-date=2022-09-28 |website=plus.pearson.com}}</ref>。[[遺伝情報]]はこれらのヌクレオチド配列中に存在し、遺伝子はDNA鎖に沿った配列の区間として存在する<ref name="Pearson_2006">{{cite journal | authors = Pearson H | title = Genetics: what is a gene? | journal = Nature | volume = 441 | issue = 7092 | pages = 398–401 | date = May 2006 | pmid = 16724031 | doi = 10.1038/441398a | s2cid = 4420674 | doi-access = free | bibcode = 2006Natur.441..398P }}</ref>。これらの鎖は二重らせん構造に巻かれ、さらに[[ヒストン]]という構造的な支持体となるタンパク質に巻き付く。ヒストンを芯に巻きついたDNAは[[染色体]](chromosome)と呼ばれる<ref>{{Cite web |title=Histone |url=https://www.genome.gov/genetics-glossary/histone |access-date=2022-09-28 |website=Genome.gov |language=en}}</ref>。[[ウイルス]]は、DNAの代わりに[[リボ核酸|RNA]]という類似分子を遺伝子として使用することがある<ref>{{cite book |title=Microbiology | author=Prescott LM, Harley JP, Klein DA |year=1996 |publisher=Wm. C. Brown |edition=3rd |isbn=0-697-21865-1 |url=https://archive.org/details/microbiology0000pres/page/342/mode/2up |page=343}}</ref>。 |
|||
DNAは通常、[[二重らせん]]状に巻かれた2本鎖分子として存在する。DNAを構成する各ヌクレオチドは、対向鎖上の対応するヌクレオチドと優先的に結合対を形成し、A は T と、C は G と[[水素結合]]を作る。したがって、2本の鎖からなる構造によって、各鎖は対向鎖と重複する形で、すべての必要な情報を保持している。DNAのこの構造は遺伝の物理的基盤となる。[[DNA複製]]では、まず2本鎖を分離し、各鎖を新しい対向鎖の鋳型として用いることにより遺伝情報を複製する<ref name="griffiths2000sect1523">{{cite book | veditors = Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbart|title=An Introduction to Genetic Analysis |year=2000 |isbn=978-0-7167-3520-5 |edition=7th |publisher=W.H. Freeman |location=New York |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=iga.section.1523 |chapter=Mechanism of DNA Replication}}</ref>。 |
|||
[[File:Human karyotype with bands and sub-bands.png|thumb|ヒトの[[カリオグラム]]模式図。22対の[[相同染色体]]と、女性 (XX) と男性 (XY) の両方の[[性染色体]] (右下)、および{{Ill2|ヒトミトコンドリアの遺伝学|en|Human mitochondrial genetics|label=ミトコンドリアゲノム}} (左下) を示す。{{further|{{ill2|核型|en|Karyotype|preserve=1}}}}]] |
|||
遺伝子は、DNA塩基配列の長い鎖に沿って直線的に配置している。[[細菌]]の場合、各細胞は通常1つの環状[[遺伝担体]]<!-- genophore -->を持っているが、[[真核生物]](植物や動物など)の場合、DNAは複数の線状染色体に配置されている。これらのDNA鎖は、非常に長い場合が多く、たとえばヒトの場合、最大の染色体の長さは約2億4,700万[[塩基対]]に達する<ref>{{cite journal | authors = Gregory SG, Barlow KF, McLay KE, Kaul R, Swarbreck D, Dunham A, Scott CE, Howe KL, Woodfine K, Spencer CC, Jones MC, Gillson C, Searle S, Zhou Y, Kokocinski F, McDonald L, Evans R, Phillips K, Atkinson A, Cooper R, Jones C, Hall RE, Andrews TD, Lloyd C, Ainscough R, Almeida JP, Ambrose KD, Anderson F, Andrew RW, Ashwell RI, Aubin K, Babbage AK, Bagguley CL, Bailey J, Beasley H, Bethel G, Bird CP, Bray-Allen S, Brown JY, Brown AJ, Buckley D, Burton J, Bye J, Carder C, Chapman JC, Clark SY, Clarke G, Clee C, Cobley V, Collier RE, Corby N, Coville GJ, Davies J, Deadman R, Dunn M, Earthrowl M, Ellington AG, Errington H, Frankish A, Frankland J, French L, Garner P, Garnett J, Gay L, Ghori MR, Gibson R, Gilby LM, Gillett W, Glithero RJ, Grafham DV, Griffiths C, Griffiths-Jones S, Grocock R, Hammond S, Harrison ES, Hart E, Haugen E, Heath PD, Holmes S, Holt K, Howden PJ, Hunt AR, Hunt SE, Hunter G, Isherwood J, James R, Johnson C, Johnson D, Joy A, Kay M, Kershaw JK, Kibukawa M, Kimberley AM, King A, Knights AJ, Lad H, Laird G, Lawlor S, Leongamornlert DA, Lloyd DM, Loveland J, Lovell J, Lush MJ, Lyne R, Martin S, Mashreghi-Mohammadi M, Matthews L, Matthews NS, McLaren S, Milne S, Mistry S, Moore MJ, Nickerson T, O'Dell CN, Oliver K, Palmeiri A, Palmer SA, Parker A, Patel D, Pearce AV, Peck AI, Pelan S, Phelps K, Phillimore BJ, Plumb R, Rajan J, Raymond C, Rouse G, Saenphimmachak C, Sehra HK, Sheridan E, Shownkeen R, Sims S, Skuce CD, Smith M, Steward C, Subramanian S, Sycamore N, Tracey A, Tromans A, Van Helmond Z, Wall M, Wallis JM, White S, Whitehead SL, Wilkinson JE, Willey DL, Williams H, Wilming L, Wray PW, Wu Z, Coulson A, Vaudin M, Sulston JE, Durbin R, Hubbard T, Wooster R, Dunham I, Carter NP, McVean G, Ross MT, Harrow J, Olson MV, Beck S, Rogers J, Bentley DR, Banerjee R, Bryant SP, Burford DC, Burrill WD, Clegg SM, Dhami P, Dovey O, Faulkner LM, Gribble SM, Langford CF, Pandian RD, Porter KM, Prigmore E | title = The DNA sequence and biological annotation of human chromosome 1 | journal = Nature | volume = 441 | issue = 7091 | pages = 315–321 | date = May 2006 | pmid = 16710414 | doi = 10.1038/nature04727 | doi-access = free | bibcode = 2006Natur.441..315G }}</ref>。染色体のDNAは、組織化し、緻密化し、接近を制御するための構造タンパク質と関連しており、[[クロマチン]]と呼ばれる構造を形成している。真核生物の場合、クロマチンは通常、[[ヒストン]]タンパク質の芯に巻きついたDNAセグメントである[[ヌクレオソーム]]から構成される<ref>{{Citation|title=Chromosomal DNA and Its Packaging in the Chromatin Fiber|last=Alberts|first=Bruce|last2=Johnson|first2=Alexander|last3=Lewis|first3=Julian|last4=Raff|first4=Martin|last5=Roberts|first5=Keith|last6=Walter|first6=Peter|date=2002|url=https://www.ncbi.nlm.nih.gov/books/NBK26834/|publisher=Garland Science|language=en|access-date=2024-07-25}}</ref>。生物の遺伝物質の完全な一式(通常はすべての染色体のDNA配列の組み合わせ)は[[ゲノム]](genome)と呼ばれる。 |
|||
DNAは[[細胞核]]内にもっとも多く存在するが、{{Ill2|ルース・セイガー|en|Ruth Sager}}は核の外に存在する非染色体遺伝子の発見に貢献した<ref name="ruth">{{cite web |title=Ruth Sager |url=https://www.britannica.com/biography/Ruth-Sager |website=Encyclopaedia Britannica |access-date=8 June 2020}}</ref>。植物の場合、これらは[[葉緑体]]によく見られ、他の生物では[[ミトコンドリア]]に存在する<ref name="ruth" />。これらの非染色体遺伝子は、有性生殖を行うどちらのパートナーからも受け継がれることがあり、世代を超えて複製され、活性状態を維持し、さまざまな遺伝形質<!-- hereditary characteristics -->の制御を果たす<ref name="ruth" />。 |
|||
[[半数体]]生物<!-- haploid organisms-->は各染色体の複製を1つしか持たないが、ほとんどの動物と多くの植物は[[二倍体]]生物で、各染色体を2つずつ持つため、すべての遺伝子が2つずつ存在する。遺伝子の2つのアレルは、2本の[[相同染色体]]の同じ[[遺伝子座]]に位置し、各アレルは異なる親から受け継がれる<ref name="griffiths2000sect484">{{cite book | veditors = Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbart|title=An Introduction to Genetic Analysis |year=2000 |isbn=978-0-7167-3520-5 |edition=7th |publisher=W.H. Freeman |location=New York |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=iga.section.484 |chapter=Mendelian genetics in eukaryotic life cycles}}</ref>。 |
|||
多くの生物種は、いわゆる[[性染色体]]を持っており、それぞれの生物の性別を決定している<ref name="griffiths2000sect222">{{cite book | veditors = Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbart|title=An Introduction to Genetic Analysis |year=2000 |isbn=978-0-7167-3520-5 |edition=7th |publisher=W.H. Freeman |location=New York |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=iga.section.222 |chapter=Sex chromosomes and sex-linked inheritance}}</ref>。ヒトや多くの動物の場合、[[Y染色体]]には特に男性的な特徴の発達を促す遺伝子が含まれている。進化の過程で、Y染色体はその内容の大半と遺伝子の大半を失ったのに対し、[[X染色体]]は他の染色体と似て、多くの遺伝子を含んでいる。それでも、{{Ill2|メアリー・フランシス・ライオン|en|Mary Frances Lyon}}は、X染色体が生殖の際に不活性化され、子孫に2倍の遺伝子が受け継がれるのを防ぐことを発見した<ref name="lyon">{{cite journal | authors = Rastan S | title = Mary F. Lyon (1925-2014) | journal = Nature | volume = 518 | issue = 7537 | pages = 36 | date = February 2015 | pmid = 25652989 | doi = 10.1038/518036a | publisher = Springer Nature Limited | s2cid = 4405984 | bibcode = 2015Natur.518...36R | doi-access = free }}</ref>。ライオンの発見は、{{Ill2|X染色体連鎖遺伝病|en|X-linked genetic disease|label=X連鎖性疾患}}の発見へとつながった<ref name="lyon" />。 |
|||
=== 生殖 === |
|||
{{Main|{{ill2|無性生殖|en|Asexual reproduction|preserve=1}}|有性生殖}} |
|||
[[File:Zellsubstanz-Kern-Kerntheilung.jpg|thumb|left|[[ヴァルター・フレミング]]による真核生物の細胞分裂の図。染色体は複製され、[[染色体凝縮|凝縮]]し、編制される。そして細胞が分裂すると、染色体複製が娘細胞に分離する。 (1882年)]] |
|||
細胞が分裂する際、ゲノム全体が複製され、それぞれの[[娘細胞]]はゲノムを1複製ずつ受け継ぐ。この過程は[[有糸分裂]]と呼ばれ、最も単純な生殖の形態であるとともに、[[無性生殖]]の基礎でもある。また、無性生殖は[[多細胞生物]]でも起こり、片方の親からゲノムを受け継いだ子孫が生まれる。親と遺伝的に同一の子孫は{{Ill2|クローニング|en|Cloning|label=クローン|preserve=1}}と呼ばれる<ref>{{cite web |url=https://www.merriam-webster.com/dictionary/clone |title= clone|author=<!--Not stated--> |date= |website=Merriam-Webster Dictionary |publisher= |access-date=13 November 2023 |quote=}}</ref>。 |
|||
[[真核生物]]では、有性生殖によって、2つの異なる両親から受け継いだ遺伝物質が混合した子孫を生み出すことが多い。有性生殖の過程では、ゲノムの複製が1つだけ存在する形態([[半数体]])と2つ存在する形態([[二倍体]])を交互に繰り返す<ref name="griffiths2000sect484" />。半数体細胞が融合し、遺伝物質が組み合わさると、染色体が対になった二倍体細胞が生まれる。二倍体生物は、DNAを複製することなく分裂することで半数体を形成し、それぞれの染色体対のうちの片方を無作為に受け継ぐ娘細胞を生成する。ほとんどの動物と多くの植物は、その生涯の大半を二倍体として過ごし、半数体の形態になるのは[[精子]]や[[卵子]]などの単細胞[[配偶子]]に限られる<ref>{{Cite web |title=Haploid |url=https://www.genome.gov/genetics-glossary/haploid |access-date=2024-02-10 |website=www.genome.gov |language=en}}</ref>。 |
|||
[[細菌]]の場合、半数体・二倍体による有性生殖を行わないが、新しい遺伝情報を獲得する方法は数多くある。一部の細菌は{{Ill2|細菌接合|en|Bacterial conjugation|label=接合}}し、小さな環状DNA断片を別の細菌に移すことができる<ref name="griffiths2000sect1304">{{cite book | veditors = Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbart|title=An Introduction to Genetic Analysis |year=2000 |isbn=978-0-7167-3520-5 |edition=7th |publisher=W.H. Freeman |location=New York |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=iga.section.1304 |chapter=Bacterial conjugation}}</ref>。また、細菌は環境中に存在する裸のDNA断片を取り込み、自身のゲノムに組み込むこともある。この現象は[[形質転換]](transformation)として知られている<ref name="griffiths2000sect1343">{{cite book | veditors = Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbart|title=An Introduction to Genetic Analysis |year=2000 |isbn=978-0-7167-3520-5 |edition=7th |publisher=W.H. Freeman |location=New York |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=iga.section.1343 |chapter=Bacterial transformation}}</ref>。これらの過程によって、[[遺伝子の水平伝播]]が起こり、遺伝情報の断片が本来は無関係な生物間で伝達される。[[遺伝的形質転換|自然形質転換]]は多くの細菌種で起こり、ある細胞から別の細胞(通常は同じ種)にDNAが伝達される[[有性生殖|性的プロセス]]と見なされている<ref name="Bernstein2018">{{cite journal | authors = Bernstein H, Bernstein C, Michod RE | title = Sex in microbial pathogens | journal = Infection, Genetics and Evolution | volume = 57 | pages = 8–25 | date = January 2018 | pmid = 29111273 | doi = 10.1016/j.meegid.2017.10.024 | doi-access = free | bibcode = 2018InfGE..57....8B }}</ref>。形質転換には多くの細菌性[[遺伝子産物]]の働きが必要で、その主な適応機能は、受容細胞における{{Ill2|DNA損傷 (自然発生)|en|DNA damage (naturally occurring)|label=DNA損傷}}の[[DNA修復|修復]]であると考えられる<ref name="Bernstein2018" />。 |
|||
=== 組換えと遺伝的連鎖 === |
|||
{{Main|{{ill2|乗換え (生物学)|en|Chromosomal crossover|preserve=1}}|{{ill2|遺伝的連鎖|en|Genetic linkage|preserve=1}}}} |
|||
[[File:Morgan crossover 2 cropped.png|thumb|right|[[トーマス・ハント・モーガン]]による、染色体間の二重交差の模式図 (1916年)]] |
|||
染色体が二倍体であることによって、異なる染色体上の遺伝子が[[独立の法則|独立して選別]]されたり、半数体配偶子が形成される[[有性生殖]]の際に相同対から分離されたりすることが可能になる。このようにして、交配対<!-- mating pair -->の子孫に新たな遺伝子の組み合わせが生まれる可能性がある。理論的には、同じ染色体上の遺伝子は組換えを起こさない。しかし、[[染色体交差]]という細胞内過程を通じた組換えが起こる。染色体交差は、染色体間でDNA断片を交換し、染色体間で遺伝子アレルを効果的にシャッフルする<ref name="griffiths2000sect929">{{cite book | veditors = Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbar |title=An Introduction to Genetic Analysis |year=2000 |isbn=978-0-7167-3520-5 |edition=7th |publisher=W. H. Freeman |location=New York |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=iga.section.929 |chapter=Nature of crossing-over}}</ref>。この染色体交差は通常、[[減数分裂]]という半数体細胞を生成する一連の[[細胞分裂]]中に起こる。{{Ill2|減数分裂の起源と機能|en|Origin and function of meiosis|label=減数分裂組換え}}は、特に[[微生物]]の[[真核生物]]において、DNA損傷を修復する適応機能を持つと考えられる<ref name="Bernstein2018" />。 |
|||
染色体交差の細胞学的実証は、1931年、{{Ill2|ハリエット・クレイトン|en|Harriet Creighton}} と[[バーバラ・マクリントック]]によって初めて行われた。彼らのトウモロコシに関する研究と実験は、対になった染色体上の遺伝子が実際に相同染色体間で入れ替わるという遺伝学の仮説を、細胞学に証明した<ref>{{cite journal | authors = Creighton HB, McClintock B | title = A Correlation of Cytological and Genetical Crossing-Over in Zea Mays | journal = Proceedings of the National Academy of Sciences of the United States of America | volume = 17 | issue = 8 | pages = 492–497 | date = August 1931 | pmid = 16587654 | pmc = 1076098 | doi = 10.1073/pnas.17.8.492 | doi-access = free | bibcode = 1931PNAS...17..492C }}</ref>。 |
|||
染色体上の特定の位置間で染色体交差が起こる確率は、その2点間の距離と関係がある。任意の長距離にわたって交差が起こる確率は十分に高いため、それらの遺伝子どうしの遺伝には事実上の相関はない<ref name="Staub1994">{{cite book | author = Staub JE |title=Crossover: Concepts and Applications in Genetics, Evolution, and Breeding |url=https://books.google.com/books?id=R43qWg5A-GsC&pg=PA55 |year=1994 |publisher=University of Wisconsin Press |isbn=978-0-299-13564-5 |page=55}}</ref>。しかし、遺伝子が互いに近接すると交差が起こる確率は低くなるため、それらの遺伝子は[[遺伝的連鎖]]を示し、2つの遺伝子のアレルが一緒に遺伝する傾向がある。一連の遺伝子間の連鎖量を組み合わせて線状[[遺伝的連鎖|連鎖地図]]を作成し、染色体上に沿った遺伝子の配置を大まかに示すことができる<ref name="griffiths2000sect899">{{cite book | veditors = Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbar |title=An Introduction to Genetic Analysis |year=2000 |isbn=978-0-7167-3520-5 |edition=7th |publisher=W. H. Freeman |location=New York |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=iga.section.899 |chapter=Linkage maps}}</ref>。 |
|||
== 遺伝子発現 == |
|||
=== 遺伝暗号 === |
|||
{{Main|遺伝暗号}} |
|||
[[File:Genetic code.svg|thumb|left|upright=1.3|DNAの[[遺伝暗号]]は、三連符を用いてタンパク質を指定し、[[メッセンジャーRNA]]を介してタンパク質へ伝達される]] |
|||
遺伝子は、細胞内のほとんどの機能を担う[[タンパク質]]分子の生成を通じて、その機能的な効果を[[遺伝子発現|発現]]する。タンパク質は、[[アミノ酸]]の配列からなる1本または複数の[[ポリペプチド鎖]]で構成される。遺伝子のDNA配列が、特異的な[[アミノ酸配列]]を生成するために使われる。この過程は、遺伝子のDNA配列と一致する配列を持つ[[リボ核酸|RNA]]分子の生成 -[[転写 (生物学)|転写]](transcription)と呼ばれる- から始まる。 |
|||
この[[メッセンジャーRNA]]分子は、次に、[[翻訳 (生物学)|翻訳]](translation)と呼ばれる過程を通じて対応するアミノ酸配列を生成する役割を果たす。DNA配列内の3個のヌクレオチドのセット[[コドン]](codon)と呼ばれ、タンパク質を作り出す20種類のアミノ酸のいずれか1つ、またはアミノ酸配列の[[終止コドン|終端の指示]]に対応する。この対応関係を[[遺伝暗号]](genetic code)と呼ぶ<ref>{{cite book |title=Biochemistry | author=Berg JM, Tymoczko JL, Stryer L, Clarke ND |edition=5th |year=2002 |publisher=W.H. Freeman and Company |location=New York |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=stryer.section.685 |chapter=I. 5. DNA, RNA, and the Flow of Genetic Information: Amino Acids Are Encoded by Groups of Three Bases Starting from a Fixed Point |url-status=live |archive-url=https://web.archive.org/web/20060411095303/http://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=stryer.section.685 |archive-date=11 April 2006}}</ref>。情報の流れは一方向であり、情報はDNAのヌクレオチド配列からタンパク質のアミノ酸配列へと転送されるが、その逆、つまりタンパク質からDNA配列へ戻ることはない。[[フランシス・クリック]]は、この現象を[[セントラルドグマ|分子生物学におけるセントラル・ドグマ]]と呼んだ<ref name="crick1970">{{cite journal | authors = Crick F | title = Central dogma of molecular biology | journal = Nature | volume = 227 | issue = 5258 | pages = 561–563 | date = August 1970 | pmid = 4913914 | doi = 10.1038/227561a0 | url = http://www.nature.com/nature/focus/crick/pdf/crick227.pdf | url-status = live | s2cid = 4164029 | df = dmy-all | bibcode = 1970Natur.227..561C | archive-url = https://web.archive.org/web/20060215024341/http://www.nature.com/nature/focus/crick/pdf/crick227.pdf | archive-date = 15 February 2006 }}</ref>。 |
|||
アミノ酸の特異的配列により、そのタンパク質に固有の[[三次構造|三次元構造]]が形成され、その三次元構造はタンパク質の機能と関連している<ref>{{Cite web|author=Alberts ''et al.''|date=2002|url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=mboc4.section.388 |title=I.3. Proteins: The Shape and Structure of Proteins|archiveurl=https://web.archive.org/web/20230101101721/https://www.ncbi.nlm.nih.gov/books/NBK26830/ |archivedate=2023-01-01 |accessdate=2024-08-09}}</ref><ref>{{Cite web|author=Alberts ''et al.'' |date=2002|url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=mboc4.section.452 I.3. |title=Proteins: Protein Function|archiveurl=https://web.archive.org/web/20060425162405/http://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=mboc4.section.452 |archivedate=2006-04-25 |accessdate=2024-08-09}}</ref>。タンパク質には、[[コラーゲン]]のように繊維を形成する単純な構造を持つ分子もある。また、タンパク質の中には、他のタンパク質や単純な分子と結合して、その分子の[[化学反応]]を促進する[[酵素]]として働くものもある(酵素タンパク質それ自体は変化しない)。タンパク質の構造は動的であり、[[ヘモグロビン]]というタンパク質は、哺乳類の血液内で[[酸素]]分子の捕捉、輸送、放出を促進するときに、わずかに異なる形状をとる{{cn|date=October 2022}}。 |
|||
DNA中の[[一塩基多型|1つのヌクレオチドの異なり]]が、タンパク質のアミノ酸配列を変化させることがある。タンパク質の構造はアミノ酸配列によって決定されるため、一部の変化がタンパク質の構造を不安定にしたり、他のタンパク質や分子との相互作用に影響を与える表面構造を変化させることで、タンパク質の特性を劇的に変える可能性もある。たとえば、[[鎌状赤血球貧血]]は、ヘモグロビンの βグロビン部分の[[コーディング領域]]内の1塩基の違いによって起こるヒトの遺伝病であり、1つのアミノ酸の変化がヘモグロビンの物理的特性の変化を引き起こす<ref>{{cite web |title=How Does Sickle Cell Cause Disease? |url=http://sickle.bwh.harvard.edu/scd_background.html |date=11 April 2002 |access-date=23 July 2007 |publisher=Brigham and Women's Hospital: Information Center for Sickle Cell and Thalassemic Disorders |url-status=live |archive-url=https://web.archive.org/web/20100923165921/http://sickle.bwh.harvard.edu/scd_background.html |archive-date=23 September 2010}}</ref>。鎌状赤血球型のヘモグロビンは互いに付着し、積み重なって繊維を形成し、そのタンパク質を輸送する[[赤血球]]の形を歪める。この鎌状の細胞は[[血管]]内を円滑に流れなくなり、詰まったり劣化する傾向があり、この病気に関連する医学的問題を引き起こす{{cn|date=October 2022}}。 |
|||
DNA配列の一部には、RNAへ転写されても、タンパク質に翻訳されないものもある。このようなRNA分子は[[ノンコーディングRNA]]と呼ばれる。ときには、これらの生成物が、重要な細胞機能に関する構造体を形成することもある(例:[[リボソームRNA]]や[[トランスファーRNA]])。RNAは、他のRNA分子(例:[[microRNA]])との[[ハイブリダイゼーション]]相互作用を通じて、調節作用を発揮することもある{{cn|date=October 2022}}。 |
|||
=== 生まれつきか育ちか === |
|||
{{Main|{{ill2|生まれつきか育ちか|en|Nature and nurture}}}} |
|||
[[File:Niobe050905-Siamese Cat.jpeg|thumb|upright|[[シャム (ネコ)|シャム猫]]は、温度に敏感な色素生成変異を持っている。]] |
|||
遺伝子は生物が機能するために必要なすべての情報を含んでいるが、最終的に生物が示す表現型を決定する上で、環境も重要な役割を果たしている。「{{ill2|生まれつきか育ちか|en|Nature and nurture}}」<!-- nature and nurture -->という成句は、この相補的な関係を指している。ある生物の[[表現型]]は、遺伝子と環境との相互作用によって決定される。興味深い例として、[[シャム (ネコ)|シャム猫]]の毛色がある。この場合、猫の体温が環境としての役割を果たす。猫の遺伝子は黒毛を[[遺伝暗号|コード]]しているため、猫の毛を生成する細胞は、黒毛を生やす細胞内タンパク質を生成する。しかし、この黒毛を生成するタンパク質は温度に敏感(すなわち、{{Ill2|温度感受性変異体|en|Temperature-sensitive mutant|label=温度感受性変異}}が起こる)であり、高温環境では{{Ill2|変性|en|Denaturation (biochemistry)|label=変性|preserve=1}}して、猫の体温が高い部位では黒毛の色素を生成できない。しかし、低温環境下では、タンパク質の構造は安定しており、通常どおり黒毛の色素を生成する。このタンパク質は、足、耳、尾、顔など、皮膚の温度が低い部位で機能するため、この猫は四肢に黒毛が生える<ref>{{cite journal | authors = Imes DL, Geary LA, Grahn RA, Lyons LA | title = Albinism in the domestic cat (Felis catus) is associated with a tyrosinase (TYR) mutation | journal = Animal Genetics | volume = 37 | issue = 2 | pages = 175–178 | date = April 2006 | pmid = 16573534 | pmc = 1464423 | doi = 10.1111/j.1365-2052.2005.01409.x }}</ref>。 |
|||
ヒトの遺伝病である[[フェニルケトン尿症]]は、環境が大きく影響している。フェニルケトン尿症を引き起こす変異は、[[フェニルアラニン]]というアミノ酸を分解する体の機能を妨げ、中間分子の毒性蓄積を引き起こし、その結果、進行性の知的障害や発作などの重篤な症状を引き起こす。しかし、フェニルケトン尿症の変異を持つ人でも、このアミノ酸を完全に避ける厳格な食事療法に従えば、健康で正常な状態を維持できる<ref>{{cite web |url=https://www.nlm.nih.gov/medlineplus/phenylketonuria.html |title=MedlinePlus: Phenylketonuria |access-date=15 March 2008 |publisher=NIH: National Library of Medicine |url-status=live |archive-url=https://web.archive.org/web/20080725183720/http://www.nlm.nih.gov/medlineplus/phenylketonuria.html |archive-date=25 July 2008}}</ref>。 |
|||
遺伝子と環境(「生まれつきか育ちか」)が表現型に及ぼす影響を判断する一般的な方法として、{{Ill2|双生児研究|en|Twin study|label=一卵性双生児や二卵性双生児}}、あるいは[[多胎児]]の兄弟姉妹の調査がある<ref>For example, {{cite book |title=Nature via Nurture: Genes, Experience and What Makes Us Human | author=Ridley M |publisher=Fourth Estate |year=2003|isbn= 978-1-84115-745-0 |page=73}}</ref>。一卵性双生児は同じ[[受精卵]]から生まれたため、遺伝的には同じである。一方、二卵性双生児は、遺伝的には普通の兄弟姉妹と同じくらい異なりがある。一卵性双生児の組と二卵性双生児の組で、ある疾患の発症頻度を比較することで、科学者はその疾患が遺伝的要因によるものか、出生後の環境要因によるものかを判断することができる。有名な例として、{{Ill2|ジェナイン家の四つ子|en|Genain quadruplets}}として知られる[[多胎児|一卵性四つ子]]が全員、[[統合失調症]]と診断された研究がある<ref name="Genain">{{Cite journal |title=The Genain Quadruplets: A Case Study and Theoretical Analysis of Heredity and Environment in Schizophrenia |journal=Behavioral Science |volume=9 |issue=4 | authors = Rosenthal D |year=1964 |page=371 |doi=10.1002/bs.3830090407 }}</ref>。 |
|||
=== 遺伝子調節 === |
|||
{{Main|[[遺伝子発現の調節]]<!--Regulation of gene expression-->}} |
|||
ある生物のゲノムには何千もの遺伝子が存在しているが、そのすべてが常に活動しているわけではない。ある遺伝子がメッセンジャーRNAへ転写されたときに発現し、タンパク質が細胞に必要とされる場合のみ合成されるように、遺伝子の発現を調節する多くの細胞機構<!-- cellular methods -->が存在する。[[転写因子]]は、DNAに結合し、遺伝子の転写を促進または抑制する制御タンパク質である<ref>{{cite journal | authors = Brivanlou AH, Darnell JE | title = Signal transduction and the control of gene expression | journal = Science | volume = 295 | issue = 5556 | pages = 813–818 | date = February 2002 | pmid = 11823631 | doi = 10.1126/science.1066355 | s2cid = 14954195 | citeseerx = 10.1.1.485.6042 | bibcode = 2002Sci...295..813B }}</ref>。たとえば、[[大腸菌]]({{Snamei|Escherichia coli}})のゲノムには、[[トリプトファン]]というアミノ酸の合成に必要な一連の遺伝子が存在する。しかし、トリプトファンがすでに細胞内に存在している場合は、トリプトファン合成のためのこれらの遺伝子は必要でなくなる。トリプトファンの存在は、遺伝子の活性に直接影響を与える。トリプトファン分子は、転写因子である{{Ill2|トリプトファンリプレッサー|en|Tryptophan repressor}}に結合し、[[リプレッサー]]の構造を変えて遺伝子に結合させる。トリプトファンリプレッサーは、遺伝子の転写と発現を抑制し、トリプトファン合成プロセスに[[負のフィードバック]]制御をもたらす<ref>Alberts et al. (2002), [https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=mboc4.section.1269#1270 II.3. Control of Gene Expression – The Tryptophan Repressor is a Simple Switch That Turns Genes On and Off in Bacteria] {{webarchive|url=https://web.archive.org/web/20070629040218/http://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=mboc4.section.1269 |date=29 June 2007 }}</ref>。[[File:Zinc finger DNA complex.png|thumb|upright|left|転写因子 (青) はDNA (燈) に結合して、関連する遺伝子の転写を抑制する]] |
|||
遺伝子発現の違いは特に[[多細胞生物]]において顕著になる。多細胞生物では、すべての細胞が同じゲノムを持っているにも関わらず、異なる遺伝子セットの[[遺伝子発現|発現]]により、細胞毎の構造や挙動は大きく異なる。多細胞生物のすべての細胞は単一の細胞に由来するが、外界や{{Ill2|細胞シグナル伝達|en|Cell signaling|label=細胞間シグナル|preserve=1}}に応じてさまざまな[[細胞#多細胞性|細胞型]]へ[[細胞分化|分化]]し、徐々に異なる遺伝子発現様式を確立して、さまざまな挙動を生み出す。多細胞生物の構造の{{Ill2|個体発生|en|Ontogeny|label=発達|preserve=1}}に関与する遺伝子は一つではないため、これらの様式は多くの細胞間の複雑な相互作用から生じる{{cn|date=October 2022}}。 |
|||
[[真核生物]]では、遺伝子の転写に影響を与える[[クロマチン]]の構造的特徴が存在し、多くの場合、DNAやクロマチンの修飾という形で娘細胞に安定的に受け継がれる<ref>{{cite journal | authors = Jaenisch R, Bird A | title = Epigenetic regulation of gene expression: how the genome integrates intrinsic and environmental signals | journal = Nature Genetics | volume = 33 | issue = Suppl | pages = 245–254 | date = March 2003 | pmid = 12610534 | doi = 10.1038/ng1089 | s2cid = 17270515 }}</ref>。これらの特徴はDNA配列の「上位」に存在し、細胞のある世代から次の世代へと遺伝情報を継承するため、「[[エピジェネティクス]]」(epigenetics、後成的とも)と呼ばれる。エピジェネティックな特徴によって、同じ培地内で培養された異なる細胞型は、非常に異なる特性を保持することができる。エピジェネティックな特徴は、発達過程において一般的に動的であるが、{{Ill2|パラミューテーション|en|Paramutation|label=パラミューテーション(パラ変異)}}現象のように世代を超えて継承され、遺伝の基盤であるDNAの一般的な法則に対するまれな例外として存在するものもある<ref>{{cite journal | authors = Chandler VL | title = Paramutation: from maize to mice | journal = Cell | volume = 128 | issue = 4 | pages = 641–645 | date = February 2007 | pmid = 17320501 | doi = 10.1016/j.cell.2007.02.007 | s2cid = 6928707 | doi-access = free }}</ref>。{{clear}} |
|||
== 遺伝子変化 == |
|||
=== 変異 === |
|||
{{Main|{{ill2|変異|en|Mutation|preserve=1}}}} |
|||
[[File:Gene-duplication.png|thumb|upright|遺伝子重複により冗長性がもたらされ、多様化を可能にする。つまり、1つの遺伝子が変異して本来の機能を失っても、生物体に害を及ぼすことはない。]] |
|||
[[DNA複製]]の過程において、第2鎖の合成時に誤りが発生することがある。このような誤りは{{ill2|変異|en|Mutation|preserve=1}}(mutation)と呼ばれ、特に遺伝子のタンパク質コード配列内で発生した場合、生物体の表現型に影響を与える可能性がある。[[DNAポリメラーゼ]]の「[[校正 (生物学)|校正]]」機能により通常、誤り率は非常に低く、1000万-1億塩基あたり1つの割合である<ref name="griffiths2000sect2706">{{cite book | veditors = Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbart|title=An Introduction to Genetic Analysis |year=2000 |isbn=978-0-7167-3520-5 |edition=7th |publisher=W.H. Freeman |location=New York |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=iga.section.2706 |chapter=Spontaneous mutations}}</ref><ref name="Kunkel">{{cite journal | authors = Freisinger E, Grollman AP, Miller H, Kisker C | title = Lesion (in)tolerance reveals insights into DNA replication fidelity | journal = The EMBO Journal | volume = 23 | issue = 7 | pages = 1494–1505 | date = April 2004 | pmid = 15057282 | pmc = 391067 | doi = 10.1038/sj.emboj.7600158 }}</ref>。DNAの変化率を高めるプロセスは{{Ill2|変異原|en|Mutagen|label=変異誘発|preserve=1}}<!-- mutagenic -->として知られる。変異誘発性化学物質<!-- mutagenic chemicals -->は、しばしば塩基対形成の構造に干渉して、DNA複製誤りを促進する。一方、[[紫外線]]はDNA構造に損傷を与えることで変異を誘発する<ref name="griffiths2000sect2727">{{cite book | veditors = Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbart|title=An Introduction to Genetic Analysis |year=2000 |isbn=978-0-7167-3520-5 |edition=7th |publisher=W. H. Freeman |location=New York |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=iga.section.2727 |chapter=Induced mutations}}</ref>。DNAへの化学的損傷は自然にも発生し、細胞はミスマッチや切断を修復するために[[DNA修復]]機構を使用する。ただし、修復は常に元の配列を復元するわけではない。DNA損傷の特に重要な原因として、{{Ill2|細胞呼吸|en|Cellular respiration|label=細胞内好気性呼吸|preserve=1}}によって生じる[[活性酸素種]]があり<ref name="pmid23378590">{{cite journal | authors = Cadet J, Wagner JR | title = DNA base damage by reactive oxygen species, oxidizing agents, and UV radiation | journal = Cold Spring Harbor Perspectives in Biology | volume = 5 | issue = 2 | page = a012559 | date = February 2013 | pmid = 23378590 | pmc = 3552502 | doi = 10.1101/cshperspect.a012559 }}</ref>、これが変異を引き起こす可能性がある<ref name="pmid22750987">{{cite journal | authors = Jena NR | title = DNA damage by reactive species: Mechanisms, mutation and repair | journal = Journal of Biosciences | volume = 37 | issue = 3 | pages = 503–517 | date = July 2012 | pmid = 22750987 | doi = 10.1007/s12038-012-9218-2 | s2cid = 14837181 }}</ref>。 |
|||
[[染色体交差]]を利用してDNAを交換し、遺伝子を組換える生物では、減数分裂時の整列誤りも変異の原因となる。交差の誤りは、特に、類似した配列が相同染色体<!-- partner chromosomes --> の誤った整列を引き起こした場合に起こりやすく、これによりゲノムの一部の領域が変異しやすくなる。これらの誤りは、DNA配列の大幅な構造変化や([[遺伝子重複|重複]]、{{Ill2|染色体逆位|en|Chromosomal inversion|label=逆位}}、領域全体の[[欠失]])、異なる染色体間で配列全体が偶然入れ替わる[[染色体転座]]を引き起こす可能性がある<ref name="griffiths2000sect2844">{{cite book | veditors = Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbart|title=An Introduction to Genetic Analysis |year=2000 |isbn=978-0-7167-3520-5 |edition=7th |publisher=W.H. Freeman |location=New York |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=iga.section.2844 |chapter=Chromosome Mutation I: Changes in Chromosome Structure: Introduction}}</ref>。[[File:Mutations.svg|thumb|RNA配列の変異を示す概略図。図1. 4つのコドンで構成された正常なRNA配列。図2. [[ミスセンス変異]] ([[点変異]]、[[サイレント変異|非サイレント変異]]でもある)。図3と4. いずれも[[フレームシフト変異]]を示す。図3では、2番目のコドンの2番目の塩基対が欠失している。また、図4では、2番目のコドンの3番目の塩基対位置に挿入がある。図5. コドン全体が複製された{{Ill2|三塩基反復配列伸長|en|Trinucleotide repeat expansion}}。]] |
|||
=== 自然選択と進化 === |
|||
{{Main|[[進化]]<!-- Evolution -->}} |
|||
{{further|{{ill2|自然選択|en|Natural selection|preserve=1}}}} |
|||
変異は生物の[[遺伝子型]]を変え、ときには異なる[[表現型]]を生み出す原因となる。ほとんどの変異は、生物の表現型、健康、遺伝的[[適応度]]にほとんど影響を与えない<ref>{{cite book | author = Schaechter M |title=Encyclopedia of Microbiology |url=https://books.google.com/books?id=rLhdW5YzuO4C&pg=RA1-PA551 |year=2009 |publisher=Academic Press |isbn=978-0-12-373944-5 |page=551}}</ref>。実際に影響をもたらす変異は通常有害であるが、ときには有益なこともある<ref name="CalverLymbery2009">{{cite book | author = Calver M, Lymbery A, McComb J, Bamford M |title=Environmental Biology |url=https://books.google.com/books?id=HemnRxzdiFQC&pg=PA118 |year=2009 |publisher=Cambridge University Press |isbn=978-0-521-67982-4 |page=118}}</ref>。ショウジョウバエ({{Snamei|Drosophila melanogaster}})の研究によると、ある遺伝子によって生成されるタンパク質が変異した場合、その変異の約70%は有害であり、残りは中立的またはわずかに有益であることが示唆された<ref>{{cite journal | authors = Sawyer SA, Parsch J, Zhang Z, Hartl DL | title = Prevalence of positive selection among nearly neutral amino acid replacements in Drosophila | journal = Proceedings of the National Academy of Sciences of the United States of America | volume = 104 | issue = 16 | pages = 6504–6510 | date = April 2007 | pmid = 17409186 | pmc = 1871816 | doi = 10.1073/pnas.0701572104 | doi-access = free | bibcode = 2007PNAS..104.6504S }}</ref>。 |
|||
[[File:Eukaryote tree.svg|thumb|left|複数の{{Ill2|オルソロガス遺伝子|en|Orthologous gene}}の比較により構築された[[真核生物]]の[[進化系統樹]]]] |
|||
[[集団遺伝学]]は、集団内の遺伝的差異の分布と、その分布が時間とともにどのように変化するかを研究する学問である<ref name="griffiths2000sect3842">{{cite book | veditors = Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbart|title=An Introduction to Genetic Analysis |year=2000 |isbn=978-0-7167-3520-5 |edition=7th |publisher=W.H. Freeman |location=New York |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=iga.section.3842 |chapter=Variation and its modulation}}</ref>。集団内の{{Ill2|アレル頻度|en|Allele frequency}}の変化は、主に[[自然選択説|自然選択]](あるアレルが生物にとって選択的または繁殖上の優位性をもたらすこと<ref name="griffiths2000sect3886">{{cite book | veditors = Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbart|title=An Introduction to Genetic Analysis |year=2000 |isbn=978-0-7167-3520-5 |edition=7th |publisher=W. H. Freeman |location=New York |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=iga.section.3886 |chapter=Selection}}</ref>)、[[変異]]、[[遺伝的浮動]]、[[ヒッチハイク効果|遺伝的ヒッチハイク]]<ref>{{cite journal | authors = Gillespie JH | title = Is the population size of a species relevant to its evolution? | journal = Evolution; International Journal of Organic Evolution | volume = 55 | issue = 11 | pages = 2161–2169 | date = November 2001 | pmid = 11794777 | doi = 10.1111/j.0014-3820.2001.tb00732.x | s2cid = 221735887 | doi-access = free }}</ref>、[[人為選択]]、[[遺伝子流動|流動]]などの要因によって影響を受ける<ref name="griffiths2000sect3906">{{cite book | veditors = Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbart|title=An Introduction to Genetic Analysis |year=2000 |isbn=978-0-7167-3520-5 |edition=7th |publisher=W.H. Freeman |location=New York |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=iga.section.3906 |chapter=Random events}}</ref>。 |
|||
世代を重ねるごとに生物のゲノムは大きく変化し、進化につながる。[[適応 (生物学)|適応]](adaptation)と呼ばれる過程では、有益な変異に対する選択によって、その種はその環境下でより生き残れる形へと進化する可能性がある<ref name="Darwin">{{cite book | author = Darwin C |author-link=Charles Darwin |year=1859 |title=On the Origin of Species |place=London |publisher=John Murray |edition= |page=1 |url=http://darwin-online.org.uk/content/frameset?itemID=F373&viewtype=text&pageseq=16 |isbn=978-0-8014-1319-3 |url-status=live |archive-url=http://archive.wikiwix.com/cache/20061212020054/http://darwin-online.org.uk/content/frameset?itemID=F373&viewtype=text&pageseq=16 |archive-date=12 December 2006 }}<br />Earlier related ideas were acknowledged in {{cite book | author = Darwin C |author-link=Charles Darwin |year=1861 |title=On the Origin of Species |place=London |publisher=John Murray |edition=3rd |page=xiii |url=http://darwin-online.org.uk/content/frameset?itemID=F381&viewtype=text&pageseq=20 |no-pp=true |isbn=978-0-8014-1319-3 |url-status=live |archive-url=http://archive.wikiwix.com/cache/20110223145332/http://darwin-online.org.uk/content/frameset?itemID=F381&viewtype=text&pageseq=20 |archive-date=23 February 2011 }}</ref>。新種は[[種分化]](speciation)と呼ばれる過程を経て形成されるが、その多くは地理的な隔離によって個体群間の遺伝子交換が妨げられることが原因である<ref name="Gavrilets">{{cite journal | authors = Gavrilets S | title = Perspective: models of speciation: what have we learned in 40 years? | journal = Evolution; International Journal of Organic Evolution | volume = 57 | issue = 10 | pages = 2197–2215 | date = October 2003 | pmid = 14628909 | doi = 10.1554/02-727 | s2cid = 198158082 }}</ref>。 |
|||
異なる生物種でゲノム間の{{Ill2|配列相同性|en|Sequence homology|label=相同性}}を比較することで、これらの種の進化距離と[[分子時計|分岐時期]]を推定することができる。一般的に、表現形質<!-- phenotypic characteristics -->の比較よりも遺伝的比較<!-- genetic comparisons -->の方が、生物種間の関連を特徴付ける上でより正確な方法であるとされている。生物種間の進化距離は、[[進化系統樹]]を作成するために利用することができる。これらの系統樹は、時間の経過に伴う種の[[共通祖先]]と分岐を表すが、無関係な種間での遺伝物質の移動([[遺伝子の水平伝播]]といい、細菌で最も一般的)は示さない<ref>{{cite journal | authors = Wolf YI, Rogozin IB, Grishin NV, Koonin EV | title = Genome trees and the tree of life | journal = Trends in Genetics | volume = 18 | issue = 9 | pages = 472–479 | date = September 2002 | pmid = 12175808 | doi = 10.1016/S0168-9525(02)02744-0 }}</ref>。 |
|||
== 研究と技術 == |
|||
=== モデル生物 === |
|||
[[File:Drosophila melanogaster - side (aka).jpg|thumb|right|[[キイロショウジョウバエ|ショウジョウバエ]]({{Snamei|Drosophila melanogaster}})は、遺伝学研究で広く使用されている[[モデル生物]]である]] |
|||
遺伝学者はもともと、幅広い生物の遺伝を研究していたが、研究対象となった生物種は徐々に絞られていった。その理由のひとつは、特定の生物についてすでに重要な研究が行われている場合、新たな研究者はその生物を研究対象に選ぶ可能性が高く、最終的には少数の[[モデル生物]]がほとんどの遺伝学研究の基礎となったことである。モデル生物遺伝学<!-- model organism genetics -->における一般的な研究テーマには、[[遺伝子発現の調節|遺伝子調節]]や[[形態形成|発生]]、[[悪性腫瘍|がん]]における遺伝子の関与などがある。生物の選定には利便性が考慮され(たとえば、世代交代までの期間が短く、[[遺伝子工学|遺伝子の操作]]が容易など)、一部の生物は遺伝学研究で人気のツールとなった。広く使用されているモデル生物には、腸内細菌の[[大腸菌]]({{Snamei|Escherichia coli}})、植物の[[シロイヌナズナ]]({{Snamei|Arabidopsis thaliana}})、[[パン酵母]]({{Snamei|Saccharomyces cerevisiae}})、線形動物の[[カエノラブディティス・エレガンス]]({{Snamei|Caenorhabditis elegans}})、[[キイロショウジョウバエ|ショウジョウバエ]]({{Snamei|Drosophila melanogaster}})、[[ゼブラフィッシュ]]({{Snamei|Danio rerio}})、[[ハツカネズミ]]({{Snamei|Mus musculus}})などがある<ref>{{cite web |url=http://www.loci.wisc.edu/outreach/text/model.html |title=The Use of Model Organisms in Instruction |access-date=15 March 2008 |publisher=University of Wisconsin: Wisconsin Outreach Research Modules |url-status=dead |archive-url=https://web.archive.org/web/20080313023531/http://www.loci.wisc.edu/outreach/text/model.html |archive-date=13 March 2008}}</ref>。 |
|||
=== 医学 === |
|||
[[File:Biochemistry, genetics and molecular biology.svg|alt=|thumb|[[生化学]]、遺伝学、[[分子生物学]]の概略的な関係]] |
|||
[[遺伝医学]]は、遺伝的変異がヒトの健康と疾患にどのように関係しているかを解明しようとする学問である<ref>{{cite web |url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=gnd |title=NCBI: Genes and Disease |publisher=NIH: National Center for Biotechnology Information |access-date=15 March 2008 |url-status=dead |archive-url=https://web.archive.org/web/20070220074727/http://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=gnd&ref=sidebar |archive-date=20 February 2007}}</ref>。ある疾患に関与している可能性のある未知の遺伝子を探す場合、研究者は一般的に、遺伝的連鎖図や{{Ill2|系図 (遺伝学)|en|Pedigree chart|preserve=1|label=遺伝系図}}を使用して、その疾患に関連するゲノムの位置を見つける。集団レベルでは、ゲノム上の疾患に関連する位置を見つけるために{{Ill2|メンデル無作為化|en|Mendelian randomization}}が行われる。この方法は、単一遺伝子では明確に定義できない{{Ill2|量的形質遺伝子座|en|Quantitative trait locus|label=多遺伝子形質|preserve=1}}<!-- multigenic traits -->に特に有用である<ref>{{cite journal | authors = Smith GD, Ebrahim S | title = 'Mendelian randomization': can genetic epidemiology contribute to understanding environmental determinants of disease? | journal = International Journal of Epidemiology | volume = 32 | issue = 1 | pages = 1–22 | date = February 2003 | pmid = 12689998 | doi = 10.1093/ije/dyg070 | doi-access = | author-link1 = George Davey Smith }}</ref>。候補となる遺伝子が見つかると、モデル生物において対応する(または[[相同|相同性]]のある)遺伝子について、さらなる研究が行われることが多い。遺伝性疾患の研究に加え、遺伝子型判定法の普及により、[[薬理遺伝学]]という分野が生まれた。これは、遺伝子型が薬剤応答性にどのような影響を与えるかを研究する分野である<ref>{{cite web|url=http://www.nigms.nih.gov/Initiatives/PGRN/Background/FactSheet.htm |title=Pharmacogenetics Fact Sheet |access-date=15 March 2008 |publisher=NIH: National Institute of General Medical Sciences |url-status=dead |archive-url=https://web.archive.org/web/20080512012316/http://www.nigms.nih.gov/Initiatives/PGRN/Background/FactSheet.htm |archive-date=12 May 2008}}</ref>。 |
|||
がんは[[遺伝性疾患]]であり、[[悪性腫瘍|がん]]を発症する遺伝的傾向には個人差がある。がん発症は、体内におけるいくつかの事象が組み合わさっている。体内の[[細胞分裂|細胞が分裂]]する際に、細胞内に変異が生じる場合がある。これらの変異が子孫に遺伝することはないが、細胞の挙動に影響を与え、細胞の増殖や分裂をより活発にさせる原因となることがある。こうした過程を防ぐための生物学的なメカニズムがあり、不適切に分裂している細胞に[[細胞シグナル伝達|シグナル]]が送られ、[[細胞死]]を引き起こす。しかし、細胞がシグナルを無視するような別の変異が発生することがある。体内で自然選択のプロセスが起こり、やがて細胞内に変異が蓄積して細胞自身の増殖を促進し、体内のさまざまな組織に浸潤して増殖する{{Ill2|腫瘍の不均一性|en|Tumour heterogeneity|label=癌性腫瘍}}を形成する。通常、細胞は[[成長因子]]と呼ばれるシグナルに反応してのみ分裂し、周囲の細胞と接触したり、増殖抑制シグナルに反応したりすると[[接触阻害|増殖を停止する]]。その後、細胞は通常、限られた回数しか分裂せず、[[上皮細胞|上皮]]内にとどまり、他の臓器に移動できないまま死んでゆく。がん細胞になるには、細胞はいくつかの遺伝子(3-7個)に変異を蓄積する必要がある。がん細胞は成長因子がなくても分裂し、増殖抑制シグナルを無視する可能性がある。また、がん細胞は不死であり、隣接する細胞と接触しても際限なく増殖し続けることができる。上皮から脱出し、最終的には[[原発性腫瘍|原発巣]]から脱出することもある。脱出した細胞は血管の内皮を横断し、血流にのって運ばれ、新たな臓器に定着し、致命的な[[転移 (医学)|転移]]を形成する。ごく一部のがんは遺伝的素因を示すが、大部分は腫瘍を形成する細胞分裂を繰り返す1つまたは少数の細胞に生じ・蓄積する一連の遺伝子変異によって引き起こされ、これらの変異は子孫に遺伝しない({{Ill2|体細胞変異|en|Somatic mutation}}を参照)。最もよく見られる変異は、[[がん抑制遺伝子|がん抑制因子]]である[[P53遺伝子|p53タンパク質]]の機能喪失、またはp53経路における機能喪失、[[Rasタンパク質]]または他の[[がん遺伝子]]の活性化変異である<ref>{{cite journal | authors = Frank SA | title = Genetic predisposition to cancer - insights from population genetics | journal = Nature Reviews. Genetics | volume = 5 | issue = 10 | pages = 764–772 | date = October 2004 | pmid = 15510167 | doi = 10.1038/nrg1450 | s2cid = 6049662 }}</ref><ref>{{cite book | author=Strachan T, Read AP |title=Human Molecular Genetics 2 |url=https://archive.org/details/humanmolecularge0002stra |url-access=registration |year=1999 |publisher=John Wiley & Sons Inc. |edition=second}} [https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=hmg.chapter.2342 Chapter 18: Cancer Genetics] {{webarchive|url=https://web.archive.org/web/20050926163641/http://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=hmg.chapter.2342 |date=26 September 2005 }}</ref>。 |
|||
=== 研究方法 === |
|||
[[File:Ecoli colonies.png|thumb|right|upright=0.8|細胞クローン技術によって作られた[[大腸菌]]の[[群体|コロニー]]。同様の方法は、{{Ill2|分子クローニング|en|Molecular cloning}}でもしばしば用いられる。]] |
|||
DNAは実験室で操作することができる。[[制限酵素]]は、DNAを特異的配列で切断し、予測可能なDNA断片を生成する酵素として一般的に使用されている<ref>Lodish et al. (2000), [https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=mcb.section.1582 Chapter 7: 7.1. DNA Cloning with Plasmid Vectors] {{webarchive|url=https://web.archive.org/web/20090527183555/http://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=mcb.section.1582 |date=27 May 2009 }}</ref>。DNA断片は、その長さに応じて分離する[[ゲル電気泳動|ゲル電気泳動法]]によって可視化できる<ref>{{Cite web |title=Gel electrophoresis (article) |url=https://www.khanacademy.org/science/ap-biology/gene-expression-and-regulation/biotechnology/a/gel-electrophoresis |access-date=2024-02-21 |website=Khan Academy |language=en}}</ref>。 |
|||
DNA断片を結合するために[[DNAリガーゼ]]と呼ばれる酵素が使用される。この方法により、研究者はさまざまな供給源から得たDNA断片を結合させて、[[組換えDNA]]を作成することができる。[[遺伝子組換え生物]]の研究では、組換えDNAとともに[[プラスミド]](数個の遺伝子を持つ短い環状DNA分子)がよく使われる。{{Ill2|分子クローニング|en|Molecular cloning}}と呼ばれる手法では、DNA断片を組み込んだプラスミドを細菌に挿入し寒天培地上で培養することで、DNA断片を増幅することが可能である。なお、クローニングはこのような分子遺伝学的な手法だけでなく、クローン生物を作成するためのさまざまな手段を指すこともある<ref>{{cite journal | authors = Keefer CL | title = Artificial cloning of domestic animals | journal = Proceedings of the National Academy of Sciences of the United States of America | volume = 112 | issue = 29 | pages = 8874–8878 | date = July 2015 | pmid = 26195770 | pmc = 4517265 | doi = 10.1073/pnas.1501718112 | bibcode = 2015PNAS..112.8874K | doi-access = free }}</ref>。 |
|||
[[ポリメラーゼ連鎖反応]](PCR)と呼ばれる手順を用いてDNAを増幅することもできる<ref>Lodish et al. (2000), [https://www.ncbi.nlm.nih.gov/books/bv.fcgi?highlight=PCR&rid=mcb.section.1718 Chapter 7: 7.7. Polymerase Chain Reaction: An Alternative to Cloning]</ref>。PCR法は、短い特異的なDNA配列を用いて標的のDNA領域を分離し、指数関数的に増幅することができる技術である。PCR法は、ごく微量のDNAからでも増幅できるため、特定のDNA配列の存在を検出する際にもよく用いられる<ref name="Chang_2017">{{cite journal |last1=Chang |first1=Dingran |last2=Tram |first2=Kha |last3=Li |first3=Ben |last4=Feng |first4=Qian |last5=Shen |first5=Zhifa |last6=Lee |first6=Christine H. |last7=Salena |first7=Bruno J. |last8=Li |first8=Yingfu |date=2017-06-08 |title=Detection of DNA Amplicons of Polymerase Chain Reaction Using Litmus Test |journal=Scientific Reports |volume=7 |issue=3110 |page=3110 |doi=10.1038/s41598-017-03009-z |pmid=28596600 |pmc=5465217 |bibcode=2017NatSR...7.3110C }}</ref><ref name="Garibyan_2013">{{cite journal |last1=Garibyan |first1=Lilit |last2=Nidhi |date=March 2013 |title=Polymerase Chain Reaction |url=https://www.jidonline.org/article/S0022-202X(15)36139-X/fulltext |journal=Journal of Investigative Dermatology |volume=133 |issue=3 |pages=1–4 |doi=10.1038/jid.2013.1 |pmid=23399825 |access-date=2024-02-27|pmc=4102308 }}</ref>。 |
|||
=== DNA配列決定とゲノミクス === |
|||
{{Main|{{ill2|DNAシークエンシング|en|DNA sequencing|preserve=1}}}} |
|||
[[DNA配列決定]](DNAシークエンシングともいう)は、遺伝学の研究のために開発された最も基本的な技術の一つであり、研究者はこれによってDNA断片中のヌクレオチド配列を決定することができるようになった。1977年に[[フレデリック・サンガー]]が率いた研究チームによって開発された{{Ill2|サンガー法|en|Sanger sequencing|label=連鎖停止配列決定法}}(chain-termination sequencing)は、現在もDNA断片の配列決定に日常的に使用されている。この技術により、多くのヒト疾患に関連する分子配列の研究が可能となった<ref>{{cite book | author=Brown TA |title=Genomes 2 |edition=2nd |year=2002 |isbn=978-1-85996-228-2 |chapter-url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=genomes.section.6452 |chapter=Section 2, Chapter 6: 6.1. The Methodology for DNA Sequencing |publisher=Bios |location=Oxford}}</ref>。 |
|||
配列決定の費用が下がったことで、研究者は[[配列アセンブリング|ゲノムアセンブリ]](genome assembly)と呼ばれる手法を用いて、多くの生物の[[ゲノムプロジェクト|ゲノム配列を決定]]した。これは、コンピュータを使用して、さまざまなDNA断片の配列をつなぎ合わせる技術である<ref>{{Cite web|author=Brown |date=2002|url=https://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=genomes.section.6481 |title=Section 2, Chapter 6: 6.2. Assembly of a Contiguous DNA Sequence|accessdate=2024-08-09 |archiveurl=https://web.archive.org/web/20070208115742/http://www.ncbi.nlm.nih.gov/books/bv.fcgi?rid=genomes.section.6481 |archivedate=2007-02-08 }}</ref>。これらの技術は、2003年に完了した[[ヒトゲノムプロジェクト|ヒトゲノム・プロジェクト]]において[[ヒトゲノム]]の配列決定に使用された<ref name="human_genome_project">{{cite web |url=http://www.ornl.gov/sci/techresources/Human_Genome/home.shtml |title=Human Genome Project Information |access-date=15 March 2008 |publisher=Human Genome Project |url-status=dead |archive-url=https://web.archive.org/web/20080315062131/http://www.ornl.gov/sci/techresources/Human_Genome/home.shtml |archive-date=15 March 2008}}</ref>。新しい[[DNAシークエンシング#自動化|ハイスループット配列決定]]技術により、DNA配列決定の費用が劇的に低下し、多くの研究者はヒトゲノムの再配列決定の費用を1,000ドルまで引き下げたいと考えている<ref>{{cite journal | authors = Service RF | title = Gene sequencing. The race for the $1000 genome | journal = Science | volume = 311 | issue = 5767 | pages = 1544–1546 | date = March 2006 | pmid = 16543431 | doi = 10.1126/science.311.5767.1544 | s2cid = 23411598 }}</ref>。次世代配列決定法({{Ill2|超並列シークエンシング|en|Massive parallel sequencing|label=}})は、配列決定の低コスト化に対する需要の高まりにより誕生した。 |
|||
これらの配列決定技術により、同時に何百万もの塩基配列を生成することが可能となった<ref name="hall2007">{{cite journal | authors = Hall N | title = Advanced sequencing technologies and their wider impact in microbiology | journal = The Journal of Experimental Biology | volume = 210 | issue = Pt 9 | pages = 1518–1525 | date = May 2007 | pmid = 17449817 | doi = 10.1242/jeb.001370 | doi-access = free }}</ref><ref name="church2006">{{cite journal | authors = Church GM | title = Genomes for all | journal = Scientific American | volume = 294 | issue = 1 | pages = 46–54 | date = January 2006 | pmid = 16468433 | doi = 10.1038/scientificamerican0106-46 | s2cid = 28769137 | bibcode = 2006SciAm.294a..46C | author-link1 = George M. Church }}{{subscription required}}</ref>。大量の配列データを利用して、生物のゲノム全体にわたるパターンを検索・分析するコンピュータツールを使用する[[ゲノミクス]]という研究分野も生まれた。ゲノミクスは、大量の{{Ill2|生物学データ|en|Biological data}}を分析するために計算手法を使用する[[バイオインフォマティクス]]の亜分野とも考えられる。これらの研究分野に共通する課題は、被験者データや{{Ill2|個人情報|en|Personal data|label=個人を特定しうる情報|preserve=1}}の管理と共有方法である{{cn|date=October 2022}}。 |
|||
== 社会と文化 == |
|||
{{See also|{{ill2|小説における遺伝学|en|Genetics in fiction}}}} |
|||
2015年3月19日、主要な生物学者グループが、遺伝可能な形でヒトゲノムを編集する手法、特に[[CRISPR]]と[[ジンクフィンガー]]の臨床使用を世界的に禁止するよう求めた<ref name="NYT-20150319">{{cite news | author = Wade N |title=Scientists Seek Ban on Method of Editing the Human Genome |url=https://www.nytimes.com/2015/03/20/science/biologists-call-for-halt-to-gene-editing-technique-in-humans.html |date=19 March 2015 |work=[[:en:The New York Times|The New York Times]] |access-date=20 March 2015 |url-status=live |archive-url=https://web.archive.org/web/20150319230002/http://www.nytimes.com/2015/03/20/science/biologists-call-for-halt-to-gene-editing-technique-in-humans.html |archive-date=19 March 2015}}</ref><ref name="NYT-20150303-AP">{{cite news | author = Pollack A |title=A Powerful New Way to Edit DNA |url=https://www.nytimes.com/2014/03/04/health/a-powerful-new-way-to-edit-dna.html |date=3 March 2015 |work=[[:en:The New York Times|The New York Times]] |access-date=20 March 2015 |url-status=live |archive-url=https://web.archive.org/web/20150326051509/http://www.nytimes.com/2014/03/04/health/a-powerful-new-way-to-edit-dna.html |archive-date=26 March 2015}}</ref><ref name="SCI-20150319">{{cite journal | authors = Baltimore D, Berg P, Botchan M, Carroll D, Charo RA, Church G, Corn JE, Daley GQ, Doudna JA, Fenner M, Greely HT, Jinek M, Martin GS, Penhoet E, Puck J, Sternberg SH, Weissman JS, Yamamoto KR | title = Biotechnology. A prudent path forward for genomic engineering and germline gene modification | journal = Science | volume = 348 | issue = 6230 | pages = 36–38 | date = April 2015 | pmid = 25791083 | pmc = 4394183 | doi = 10.1126/science.aab1028 | df = dmy-all | bibcode = 2015Sci...348...36B }}</ref><ref name="NAT-20150312">{{cite journal | authors = Lanphier E, Urnov F, Haecker SE, Werner M, Smolenski J | title = Don't edit the human germ line | journal = Nature | volume = 519 | issue = 7544 | pages = 410–411 | date = March 2015 | pmid = 25810189 | doi = 10.1038/519410a | df = dmy-all | doi-access = free | bibcode = 2015Natur.519..410L }}</ref>。2015年4月、中国の研究者が、CRISPRを使用して生育不能な[[胚|ヒト胚]]のDNAを編集する{{Ill2|基礎研究|en|Basic research|preserve=1}}の結果を報告した<ref name="NYT-20150423">{{cite news | author = Kolata G |title=Chinese Scientists Edit Genes of Human Embryos, Raising Concerns |url=https://www.nytimes.com/2015/04/24/health/chinese-scientists-edit-genes-of-human-embryos-raising-concerns.html |date=23 April 2015 |work=[[:en:The New York Times|The New York Times]] |access-date=24 April 2015 |url-status=live |archive-url=https://web.archive.org/web/20150424050616/http://www.nytimes.com/2015/04/24/health/chinese-scientists-edit-genes-of-human-embryos-raising-concerns.html |archive-date=24 April 2015}}</ref><ref name="PC-20150418">{{cite journal | authors = Liang P, Xu Y, Zhang X, Ding C, Huang R, Zhang Z, Lv J, Xie X, Chen Y, Li Y, Sun Y, Bai Y, Songyang Z, Ma W, Zhou C, Huang J | title = CRISPR/Cas9-mediated gene editing in human tripronuclear zygotes | journal = Protein & Cell | volume = 6 | issue = 5 | pages = 363–372 | date = May 2015 | pmid = 25894090 | pmc = 4417674 | doi = 10.1007/s13238-015-0153-5 }}</ref>。 |
|||
== 脚注 == |
== 脚注 == |
||
{{脚注ヘルプ}} |
{{脚注ヘルプ}} |
||
=== 注釈 === |
|||
{{Reflist}} |
|||
{{notelist}} |
|||
=== 出典 === |
|||
{{Reflist|2}} |
|||
== |
== 推薦文献 == |
||
{{See also|{{ill2|生物学の文献#遺伝学|en|Bibliography of biology#Genetics}}}} |
|||
*{{Cite book|和書 |
|||
|author = [[中沢信午]] |
|||
|title = 遺伝学の誕生 : メンデルを生んだ知的風土 |
|||
|year = 1985 |
|||
|publisher = [[中央公論社]] |
|||
|series = [[中公新書]] |
|||
|isbn = 4-12-100761-1 |
|||
|pages = |
|||
}} |
|||
* {{Cite book|和書 |
|||
| author = 吉川秀男・西沢一俊(編集責任者・代表) |
|||
| year =1969 |
|||
| title = 原色現代科学大事典 7-生命 |
|||
| publisher = 株式会社学習研究社 |
|||
| ref =吉川・西沢1969 |
|||
}} |
|||
== 関連項目 == |
|||
{{Commonscat|Genetics}} |
|||
{{Wiktionary}} |
|||
{{Wikiversity}} |
|||
*[[数理生物学]] |
|||
*[[発生遺伝学]] |
|||
*[[モデル生物]] |
|||
*[[日本遺伝学会]] |
|||
日本語: |
|||
== 外部リンク == |
|||
*{{Cite web|和書 |
|||
|author = |
|||
|date = |
|||
|url = http://wwwsoc.nii.ac.jp/gsj3/ |
|||
|title = 日本遺伝学会 |
|||
|publisher = |
|||
|accessdate = 2010-12-18 |
|||
}} |
|||
* {{cite book | 和書 | author = Daniel L. Hartl | translator=中村千春, 岡田清孝 | title=エッセンシャル遺伝学・ゲノム科学(原著第7版) | year=2021 | publisher=化学同人 | isbn=978-4759820485 | ref=none}} |
|||
*{{Cite web|和書 |
|||
* {{Cite book|和書 |title=細胞の分子生物学 第6版 |year=2017 |publisher=ニュートンプレス |isbn=978-4315520620 |author=Alberts, Johnson, Lewis, Raff, Roberts, Walter |translator=中村桂子, 松原謙一 監訳}} |
|||
|author = |
|||
* {{Cite book|和書 |title=分子細胞生物学 第9版 |date=2023/7/31 |year=2023 |publisher=東京化学同人 |isbn=978-4807920518 |author=H. Lodish ほか |translator=田利明, 須藤和夫, 山本啓一}} |
|||
|date = |
|||
|url = http://www.nig.ac.jp/ |
|||
|title = 国立遺伝学研究所 - National Institute of Genetics |
|||
|publisher = |
|||
|accessdate = 2012-12-13 |
|||
}} |
|||
*{{Cite web|和書 |
|||
|author = |
|||
|date = |
|||
|url = http://www.nig.ac.jp/museum/history/history.html |
|||
|title = 遺伝学電子博物館 - 国立遺伝学研究所 |
|||
|publisher = |
|||
|accessdate = 2012-12-13 |
|||
}} |
|||
英語: |
|||
*{{Cite web|和書 |
|||
|author = |
|||
{{refbegin}} |
|||
|date = |
|||
* {{cite book | author = Alberts B, Bray D, Hopkin K, Johnson A, Lewis J, Raff M, Roberts K, Walter P |title=Essential Cell Biology, 4th Edition|url=https://books.google.com/books?id=Cg4WAgAAQBAJ&pg=PP1|year=2013|publisher=Garland Science|isbn=978-1-317-80627-1 |ref=none}} |
|||
|url = http://genetics.ibio.jp/terms/bin/view/ |
|||
* {{cite book | veditors = Griffiths AJ, Miller JH, Suzuki DT, Lewontin RC, Gelbart|title=An Introduction to Genetic Analysis |year=2000 |isbn=978-0-7167-3520-5 |edition=7th |publisher=W. H. Freeman |location=New York |url=https://archive.org/details/introductiontoge0000unse_v1d3 |ref=none}} |
|||
|title = 日本遺伝学会 遺伝学用語集編纂プロジェクト |
|||
* {{cite book | author=Hartl D, Jones E |title=Genetics: Analysis of Genes and Genomes |edition=6th |publisher=Jones & Bartlett |year=2005 |isbn=978-0-7637-1511-3 |url=https://archive.org/details/genetics00dani |ref=none}} |
|||
|publisher = 日本遺伝学会 遺伝学用語編集委員会 |
|||
* {{cite book | author = King RC, Mulligan PK, Stansfield WD |title=A Dictionary of Genetics |edition=8th |year=2013 |isbn=978-0-19-976644-4 |publisher=Oxford University Press |location=New York |ref=none}} |
|||
|accessdate = 2012-12-13 |
|||
* {{cite book | author=Lodish H, Berk A, Zipursky LS, Matsudaira P, Baltimore D, Darnell J |title=Molecular Cell Biology |edition=4th |year=2000 |isbn=978-0-7167-3136-8 |publisher=Scientific American Books |location=New York |url=https://archive.org/details/molecularcellbio00lodi |ref=none}} |
|||
}} |
|||
{{refend}} |
|||
*{{Cite web|和書 |
|||
|author = |
|||
== 関連項目 == |
|||
|date = |
|||
{{div col|colwidth=20em}} |
|||
|url = http://sciterm.nii.ac.jp/cgi-bin/reference.cgi |
|||
* {{ill2|細菌ゲノム|en|Bacterial genome}} - 細菌のゲノム研究に関する話題 |
|||
|title = オンライン学術用語集 |
|||
* {{ill2|動物遺伝資源の凍結保存|en|Cryoconservation of animal genetic resources}} - 家畜の遺伝子を保護・保存するための、域外保全戦略 |
|||
|publisher = 国立情報学研究所 |
|||
* [[優生学]] - ヒトの遺伝的素質の改善を目指す取り組み |
|||
|accessdate = 2012-12-13 |
|||
* [[発生学]] - 配偶子、胚および胎児の成長を研究する生物学の一分野 |
|||
}} |
|||
* [[遺伝子疾患]] - ゲノムの異常によって引き起こされる健康上の問題 |
|||
* [[遺伝的多様性]] - ある生物種の遺伝子構成に含まれる遺伝的特性の総数 |
|||
* [[遺伝子工学]] - 技術を用いて生物の遺伝子を改変・操作すること |
|||
* {{ill2|ヒトの遺伝子強化|en|Human genetic enhancement}} - 遺伝子改変によるヒトの能力強化 |
|||
* {{ill2|細胞生物学および分子生物学の用語集|en|Glossary of genetics (M−Z)}} - 細胞生物学、分子生物学、分子遺伝学、生化学、微生物学などの研究で用いられる用語や概念のまとめ |
|||
* {{ill2|遺伝学関連記事の索引|en|Index of genetics articles}} |
|||
* [[遺伝医学]] - 遺伝性疾患の診断と管理を行う医学の一分野 |
|||
* {{ill2|核酸法|en|Nucleic acid methods}} - DNAやRNAのような核酸を研究するための技術 |
|||
* {{ill2|神経エピジェネティクス|en|Neuroepigenetics}} - 遺伝子のエピジェネティックな変化が神経系に及ぼす影響を研究する学問 |
|||
* {{ill2|遺伝学のあらまし|en|Outline of genetics}} - 遺伝学に関連する記事の一覧 (英語) |
|||
* {{ill2|遺伝学の歴史年表|en|Timeline of the history of genetics}} - 1850年代~ゲノム時代までの遺伝学の出来事 |
|||
* {{ill2|植物遺伝資源|en|Plant genetic resources}} - 人為的および自然選択の結果として主に農作物に生じた遺伝的変異 |
|||
{{div col end}} |
|||
== 外部リンク == |
|||
* [https://www.nig.ac.jp/museum/ 遺伝学電子博物館] - [[国立遺伝学研究所]] |
|||
{{Genetics |expanded}} |
{{Genetics |expanded}} |
||
{{Chromosome genetics}} |
{{Chromosome genetics}} |
||
{{Branches of biology}} |
|||
{{生物学}} |
|||
{{Biosci-stub}} |
|||
{{Normdaten}} |
{{Normdaten}} |
||
{{デフォルトソート:いてんかく}} |
{{デフォルトソート:いてんかく}} |
||
[[Category:遺伝学|*]] |
[[Category:遺伝学|*]] |
||
2024年8月16日 (金) 15:33時点における版
| 遺伝学 |
|---|
 |
遺伝学(いでんがく、 英: genetics)は、生物の遺伝子、遺伝的変異、遺伝について研究する学問である[1][2][3]。遺伝は生物の進化に不可欠であるため、遺伝学は生物学において重要な分野である。19世紀にモラヴィア地方の都市ブルノで活動していたアウグスチノ会修道士、グレゴール・メンデルは、遺伝学を科学的に研究した最初の人物である。メンデルは「形質遺伝」すなわち、形質(生物の性質や特徴)が親から子孫へと時を超えて受け継がれる様式を研究した。そして、生物(エンドウ)が独立した「遺伝単位」によって形質を継承することを観察した。この用語は今日でも使用されているが、遺伝子と呼ばれるものの定義としてはやや曖昧である。
形質遺伝や、遺伝子の分子遺伝のメカニズムは、21世紀の遺伝学の主要な原理であり続けているが、現代遺伝学は遺伝子の機能と挙動の研究へと拡大している。遺伝子の構造と機能・変異・分布は、細胞・生物(たとえば顕性)・個体群という文脈の中で研究されている。遺伝学は、分子遺伝学、エピジェネティクス、集団遺伝学など、多くの研究領域へと発展した。この幅広い分野の研究対象となっている生物は、生命のドメイン(古細菌、細菌、真核生物)にまたがる。
遺伝的プロセス(過程)は、生物の環境や経験と結びついて、発達や行動に影響を与える。これは、しばしば生まれつきか育ちかと呼ばれる。生細胞や生物の内外の環境が、遺伝子の転写を増減させる可能性がある。その典型例が、遺伝的に同一のトウモロコシの種子を2つ用意し、1つを温帯気候の場所に、もう1つを乾燥気候(十分な天然水や降雨がない)に植えることである。2本のトウモロコシの茎の平均の高さは、遺伝的に同等になるよう定まっているかもしれないが、乾燥気候のトウモロコシは、環境中の水や栄養分の不足のため、 温帯気候に植えた茎の半分ほどにしか成長しない。
語源
遺伝学の英語、"genetics" は、古代ギリシア語の γενετικός (genetikos)「属格 または 生成」に由来し、さらにこれは起源 (origin)を意味する γένεσις (genesis) に由来する[4][5][6]。
歴史
生物が、親から形質(生物の性質や特徴)を受け継ぐという観察結果は、有史以前から、選抜育種による植物や動物の改良に利用されてきた[7][8]。この過程を理解しようとする現代遺伝学は、19世紀半ば、アウグスチノ会の修道士、グレゴール・メンデルによる研究に端を発する[9]。

メンデル以前に、遺伝の文脈で「遺伝(genetic)」という用語を初めて使用した人物は、メンデルより前にケーゼグに住んでいたハンガリーの貴族 Imre Festetics であり、最初の遺伝学者としても知られている。彼は著書 The genetic laws of nature(『自然の遺伝法則』、Die genetischen Gesetze der Natur、1819年)の中で、生物の遺伝に関するいくつかの法則を記述した[10]。彼の第二法則は、メンデルが発表した法則と同じである[11]。第三法則で、変異の基本原則を提唱した(彼はユーゴー・ド・フリースの先駆者ともいえる)[12]。Festetics は、動物、植物、人間の世代で観察される変化は、科学的な法則の結果であると主張した[13]。彼は、生物はそれらの特徴を「獲得」するのではなく「継承」すると経験的に論じた。彼は、祖先の特徴が後に再び現れる可能性があり、生物が異なる特徴を持つ子孫を生み出す可能性を仮定することで、潜性形質や先天的変異を認識した[14]。これらの観察は、メンデルの粒子遺伝説(particulate inheritance)の重要な前触れとなり、遺伝を神話的な存在から科学的な学問へと移行させ、20世紀の遺伝学に基本的な理論的基盤を導いた[10][15]。

メンデルの研究に先立つ、別の遺伝理論もあった。19世紀に広く支持されていた融合遺伝説(blending inheritance)は、チャールズ・ダーウィンの著書『種の起源』(1859年)でも示唆されていた理論である[16]。メンデルの研究は、交配後に形質が明らかに融合しない例を示し、形質は連続的な混ざり合いではなく、異なる遺伝子の組み合わせによって生み出されることを示した。現在は、子孫における形質の融合は、量的効果を持つ複数の遺伝子の作用によって説明されている。当時、一定の支持を集めていたもう一つの理論に、獲得形質の遺伝説がある。これは、子孫が両親によって強化された形質を遺伝するという考え方である。この理論(ジャン=バティスト・ラマルクに関連)は、現在では誤りであることが分かっていて、個体の経験は子孫に受け継がれる遺伝子に影響を及ぼすことはない[17]。その他の理論としては、ダーウィンのパンゲネシス説(獲得的と遺伝的の両側面を持つ)や、フランシス・ゴルトンによるパンゲネシス説の再定式化(粒子的と遺伝的の両側面を持つ)などがある[18]。
メンデル遺伝学

現代遺伝学は、植物における遺伝の性質に関するメンデルの研究から始まった。1865年にブルノの自然研究協会に提出された論文「Versuche über Pflanzenhybriden」(植物雑種の実験)で、メンデルはエンドウ植物の特定の形質の遺伝様式を追跡し、数学的に説明した。この遺伝様式は、ごく一部の形質でのみ観察されたものであったが、メンデルの研究は、遺伝は粒子的であり獲得された(後天的な)ものではなく、しかも多くの形質の遺伝様式は、単純な規則と比率によって説明できることを示唆していた[19]。
メンデルの業績の重要性は、彼の死後、1900年にユーゴー・ド・フリースをはじめとする科学者が、彼の研究を再発見して広く理解されるようになった。メンデルの研究を支持していたウィリアム・ベイトソンは、1905年に「genetics(遺伝学)」という言葉を考案した[20][21]。形容詞「genetic(遺伝的)」は、「origin(起源)」を意味するギリシャ語の γένεσις (genesis)に由来し、名詞よりも古く、1860年に初めて生物学的な意味で使用された[22]。ベイトソンは指導者として努めるとともに、ケンブリッジ大学ニューナム・カレッジの他の科学者たち、特にベッキー・ソーンダース、Nora Darwin Barlow、Muriel Wheldale Onslow の研究からも大いに助けを受けた[23]。ベイトソンは、1906年にロンドンで開催された第3回国際植物増殖者会議の就任演説で、遺伝の研究を説明する用語として「genetics(遺伝学)」を普及させた[24]。
メンデルの研究が再発見された後、科学者たちは細胞内のどの分子が遺伝に関与しているのか特定しようとした。1900年、Nettie Stevens はミールワームの研究を始めた[25]。それから11年間にわたる研究で、メスは X染色体のみを持ち、オスは X染色体と Y染色体の両方を持ち合わせていることを発見した[25]。彼女は、性別は染色体因子であり、オスによって決定されるという結論に達した[25]。1911年、トーマス・ハント・モーガンは、ショウジョウバエの白色眼の伴性変異の観察に基づいて、遺伝子は染色体上にあると主張した[26]。1913年、モーガンの教え子であるアルフレッド・スターティヴァントは、遺伝的連鎖という現象を利用して、遺伝子が染色体上に直線状に配置していることを説明した[27]。
分子遺伝学
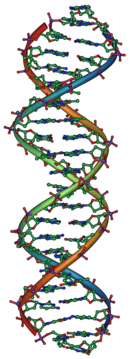
遺伝子が染色体上に存在することは分かっていたが、染色体はタンパク質とDNAの両方で構成されているため、2つのうちどちらが遺伝に関与しているか科学者たちは知らなかった。1928年、フレデリック・グリフィスは、死んだ細菌が別の生きている細菌に遺伝物質を伝達し、その細菌を形質転換させる現象を発見した。それから16年後の1944年、アベリー - マクロード - マッカーティの実験により、形質転換の原因分子がDNAであることが特定された[28]。真核生物における遺伝情報の保管場所としての核の役割は、1943年に Hämmerling が単細胞藻類であるカサノリ属(Acetabularia)の研究で確立していた[29]。1952年にハーシーとチェイスが行った実験により、細菌に感染するウイルスの遺伝物質はタンパク質ではなくDNAであることが確認され、DNAが遺伝を担う分子であるというさらなる証拠が示された[30]。
1953年、ジェームズ・ワトソンとフランシス・クリックは、ロザリンド・フランクリンとモーリス・ウィルキンスによるDNAがらせん構造であることを示すX線結晶構造解析の結果を基に、DNAの構造を決定した[31][32]。彼らの二重らせんモデルは 2本のDNA鎖で構成されており、一方の鎖上に結合したヌクレオチドは、他方の鎖上の相補的なヌクレオチドと合致し、ねじれた梯子の横木のような形を形成していた[33]。この構造により、遺伝情報はそれぞれのDNA鎖上のヌクレオチド配列に存在することが明らかになった。また、この構造は簡単な複製方法も示唆していた。すなわち、DNAの2本鎖を分離すると、新しい相補鎖は古い鎖の配列に基づいて再構築される。この特徴により、新しいDNAの1本鎖は元のDNA鎖の親から作られるという、半保存的な性質がDNAにもたらされた[34]。
DNAの構造は遺伝の仕組みを示唆していたが、DNAが細胞の働きにどのように影響するかは、まだ分かっていなかった。その後の数年間、科学者たちは、DNAがどのようにタンパク質の生成プロセスを制御するかを理解しようと努めた[35]。そして、細胞はDNAを鋳型として、DNAと非常によく似たヌクレオチドを持つ分子であるメッセンジャーRNA(伝令RNAともいう)を生成することが明らかになった。メッセンジャーRNAのヌクレオチド配列は、タンパク質のアミノ酸配列を作るために使われる。このヌクレオチド配列とアミノ酸配列との変換は、遺伝暗号(genetic code)と呼ばれている[36]。
遺伝に関する分子的理解が深まるにつれて研究は爆発的に増加した[37]。1973年、太田朋子は、分子進化の中立説を拡張した分子進化のほぼ中立説という著名な理論を展開した。この理論で太田は、遺伝的進化が起こる速度に、自然選択と環境が重要な役割を果たすことを強調した[38]。重要な発見の一つに、1977年にフレデリック・サンガーが開発した連鎖停止DNA配列決定法(chain-termination DNA sequencing)がある。この技術により、科学者はDNA分子のヌクレオチド配列を読み取ることができるようになった[39]。1983年には、キャリー・バンクス・マリスがポリメラーゼ連鎖反応法(PCR)を開発し、混合物からDNAの特定部分を迅速に分離し増幅する方法がもたらされた[40]。2003年、ヒトゲノム・プロジェクト、米国エネルギー省、米国国立衛生研究所(NIH)、民間企業セレラ・コーポレーションによる並行した取り組みによって、ヒトゲノムの配列が決定された[41][42]。
遺伝の特徴
離散的遺伝とメンデルの法則
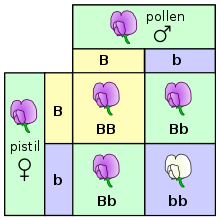
最も基本的なレベルでは、生物の遺伝は、遺伝子(gene)と呼ばれる離散的遺伝単位を親から子へと受け継ぐことによって行われる[43]。この特徴は、エンドウの遺伝形質の分離を研究したグレゴール・メンデルによって初めて観察された。たとえば、1本のエンドウの花の色は紫か白のどちらかであり、中間色はないことを示した。遺伝形質(表現型)を制御する同じ遺伝子の個々の型をアレル(allele)と呼ぶ[19][44]。
二倍体種であるエンドウの場合、各個体は両親から1つずつ遺伝子を受け継ぎ、遺伝子の複製を2つ持っている[45]。ヒトを含む多くの生物種がこの遺伝様式である。ある遺伝子の2つのアレルが同一の二倍体生物は、その遺伝子座においてホモ接合型(homozygous)と呼ばれ、一方、ある遺伝子の2つのアレルが異なる二倍体生物はヘテロ接合型(heterozygous)と呼ばれる。ある生物において、アレルの種類を遺伝子型(genotype)といい、その生物の観察可能な形質を表現型(phenotype)という。ある遺伝子がヘテロ接合型である場合、多くの場合、一方のアレルは生物の表現型を支配する性質を持つため顕性(dominant)[注釈 1]と呼ばれ、もう一方のアレルは性質が後退して観察されないため潜性(recessive)[注釈 2]と呼ばれる。アレルの中には、完全顕性(complete dominance)ではなく、中間的な表現型を発現する不完全顕性(incomplete dominance)を示したり、両方のアレルが同時に発現する共顕性(codominance)を示すものもある[47]。
一組の生物が有性生殖する場合、その子孫はどちらの両親からも2つのアレルのうちの1つを無作為に受け継ぐ。このような離散的遺伝とアレルの分離の観察は、総称して「メンデルの第一法則(Mendel's first law)」または「分離の法則(Law of Segregation)」として知られている。しかし、ある遺伝子が他の遺伝子よりも顕性になる確率は、顕性、潜性、ホモ接合、ヘテロ接合によって変わる可能性がある。たとえば、メンデルは、ヘテロ接合体の生物を交配した場合、顕性形質が現れる確率は3:1であることを発見した。実際の遺伝学者は、理論的確率、経験的確率、積の法則、和の法則などを用いて確率を研究し、推定している[48]。
表記法と図

遺伝学者は、遺伝について図や記号で説明する。遺伝子は1文字または数文字で表される。上付きの「+」記号は、遺伝子の通常の非変異アレルを示すことが多い[49]。
受精と交配の実験(特にメンデルの法則について議論する場合)では、親をP世代、子をF1世代(雑種第一代)と呼ぶ。F1の子が互いに交配すると、その子孫はF2世代(雑種第二代)と呼ばれる。交配の結果を予測する際、一般的に使用される図表にパネット方形図がある[50]。
遺伝学者は、ヒトの遺伝性疾患を研究する際に、系図を用いて形質の遺伝を表現することがよくある[51]。これらの図は、系図における形質の遺伝を表している。
複数遺伝子の相互作用

生物は数千もの遺伝子を持っており、有性生殖を行う生物では、これらの遺伝子は通常は互いに独立して組み合わされる。つまり、黄や緑のエンドウの種子(豆)の色に関するアレルの遺伝は、白や紫の花に関するアレルの遺伝とは無関係である。この現象は「メンデルの第二法則(Mendel's second law)」または「独立の法則(Law of Independent Assortment)」として知られており、異なる遺伝子のアレルが両親の間でシャッフルされ、異なる組み合わせを持つ子孫が生まれることを意味する。異なる遺伝子が相互作用し、同じ形質に影響を与えることはよくある。たとえば、ブルーアイドメアリー(Omphalodes verna)には、花の色(青または紫)を決定するアレルを持つ遺伝子が存在する。しかし、花が少しでも色づくか、それとも白いかは、別の遺伝子が制御する。この白いアレルを2つ持つ個体は、最初の遺伝子が青または紫のアレルを持つかどうかに関わらず、白い花を咲かせる。このような遺伝子間の相互作用はエピスタシス(epistasis)と呼ばれ、二番目の遺伝子は最初の遺伝子よりも上位である[52]。
多くの形質は、離散的な特徴(たとえば、紫や白の花の色)ではなく、連続的な特徴(たとえば、ヒトの身長や肌の色)である。これらの複雑な形質は、多くの遺伝子によって作り出される[53]。これらの遺伝子の影響は、生物が経験した環境によって(程度の差はあるが)媒介される。生物の特定の遺伝子が複雑な形質にどの程度寄与するかを遺伝率(heritability)という[54]。ある形質の遺伝率の大きさは相対的なものであり、より変動の大きい環境であれば、その形質の総変動に対する環境影響はより大きくなる。たとえば、ヒトの身長は複雑な原因を持つ形質である。米国における遺伝率は89%である。しかし、栄養状態や医療の普及にばらつきがあるナイジェリアでは、身長に対する遺伝率は62%にすぎない[55]。
遺伝の分子的基盤
DNAと染色体

遺伝子の分子的基盤はデオキシリボ核酸(DNA)である。DNAはデオキシリボース(糖)、リン酸基、塩基から構成されている。塩基は、アデニン(A)、シトシン(C)、グアニン(G)、チミン(T)の4種類がある。リン酸基は糖と結合し、長い糖-リン酸骨格を形成する。2本の骨格鎖の間では塩基が互いに特異的に対合し(TとA、CとG)、梯子の横木のような形を作る。塩基、リン酸、糖が結合してヌクレオチドを作り、それらが連結して長いDNA鎖が形成される[56]。遺伝情報はこれらのヌクレオチド配列中に存在し、遺伝子はDNA鎖に沿った配列の区間として存在する[57]。これらの鎖は二重らせん構造に巻かれ、さらにヒストンという構造的な支持体となるタンパク質に巻き付く。ヒストンを芯に巻きついたDNAは染色体(chromosome)と呼ばれる[58]。ウイルスは、DNAの代わりにRNAという類似分子を遺伝子として使用することがある[59]。
DNAは通常、二重らせん状に巻かれた2本鎖分子として存在する。DNAを構成する各ヌクレオチドは、対向鎖上の対応するヌクレオチドと優先的に結合対を形成し、A は T と、C は G と水素結合を作る。したがって、2本の鎖からなる構造によって、各鎖は対向鎖と重複する形で、すべての必要な情報を保持している。DNAのこの構造は遺伝の物理的基盤となる。DNA複製では、まず2本鎖を分離し、各鎖を新しい対向鎖の鋳型として用いることにより遺伝情報を複製する[60]。

遺伝子は、DNA塩基配列の長い鎖に沿って直線的に配置している。細菌の場合、各細胞は通常1つの環状遺伝担体を持っているが、真核生物(植物や動物など)の場合、DNAは複数の線状染色体に配置されている。これらのDNA鎖は、非常に長い場合が多く、たとえばヒトの場合、最大の染色体の長さは約2億4,700万塩基対に達する[61]。染色体のDNAは、組織化し、緻密化し、接近を制御するための構造タンパク質と関連しており、クロマチンと呼ばれる構造を形成している。真核生物の場合、クロマチンは通常、ヒストンタンパク質の芯に巻きついたDNAセグメントであるヌクレオソームから構成される[62]。生物の遺伝物質の完全な一式(通常はすべての染色体のDNA配列の組み合わせ)はゲノム(genome)と呼ばれる。
DNAは細胞核内にもっとも多く存在するが、ルース・セイガーは核の外に存在する非染色体遺伝子の発見に貢献した[63]。植物の場合、これらは葉緑体によく見られ、他の生物ではミトコンドリアに存在する[63]。これらの非染色体遺伝子は、有性生殖を行うどちらのパートナーからも受け継がれることがあり、世代を超えて複製され、活性状態を維持し、さまざまな遺伝形質の制御を果たす[63]。
半数体生物は各染色体の複製を1つしか持たないが、ほとんどの動物と多くの植物は二倍体生物で、各染色体を2つずつ持つため、すべての遺伝子が2つずつ存在する。遺伝子の2つのアレルは、2本の相同染色体の同じ遺伝子座に位置し、各アレルは異なる親から受け継がれる[45]。
多くの生物種は、いわゆる性染色体を持っており、それぞれの生物の性別を決定している[64]。ヒトや多くの動物の場合、Y染色体には特に男性的な特徴の発達を促す遺伝子が含まれている。進化の過程で、Y染色体はその内容の大半と遺伝子の大半を失ったのに対し、X染色体は他の染色体と似て、多くの遺伝子を含んでいる。それでも、メアリー・フランシス・ライオンは、X染色体が生殖の際に不活性化され、子孫に2倍の遺伝子が受け継がれるのを防ぐことを発見した[65]。ライオンの発見は、X連鎖性疾患の発見へとつながった[65]。
生殖

細胞が分裂する際、ゲノム全体が複製され、それぞれの娘細胞はゲノムを1複製ずつ受け継ぐ。この過程は有糸分裂と呼ばれ、最も単純な生殖の形態であるとともに、無性生殖の基礎でもある。また、無性生殖は多細胞生物でも起こり、片方の親からゲノムを受け継いだ子孫が生まれる。親と遺伝的に同一の子孫はクローンと呼ばれる[66]。
真核生物では、有性生殖によって、2つの異なる両親から受け継いだ遺伝物質が混合した子孫を生み出すことが多い。有性生殖の過程では、ゲノムの複製が1つだけ存在する形態(半数体)と2つ存在する形態(二倍体)を交互に繰り返す[45]。半数体細胞が融合し、遺伝物質が組み合わさると、染色体が対になった二倍体細胞が生まれる。二倍体生物は、DNAを複製することなく分裂することで半数体を形成し、それぞれの染色体対のうちの片方を無作為に受け継ぐ娘細胞を生成する。ほとんどの動物と多くの植物は、その生涯の大半を二倍体として過ごし、半数体の形態になるのは精子や卵子などの単細胞配偶子に限られる[67]。
細菌の場合、半数体・二倍体による有性生殖を行わないが、新しい遺伝情報を獲得する方法は数多くある。一部の細菌は接合し、小さな環状DNA断片を別の細菌に移すことができる[68]。また、細菌は環境中に存在する裸のDNA断片を取り込み、自身のゲノムに組み込むこともある。この現象は形質転換(transformation)として知られている[69]。これらの過程によって、遺伝子の水平伝播が起こり、遺伝情報の断片が本来は無関係な生物間で伝達される。自然形質転換は多くの細菌種で起こり、ある細胞から別の細胞(通常は同じ種)にDNAが伝達される性的プロセスと見なされている[70]。形質転換には多くの細菌性遺伝子産物の働きが必要で、その主な適応機能は、受容細胞におけるDNA損傷の修復であると考えられる[70]。
組換えと遺伝的連鎖

染色体が二倍体であることによって、異なる染色体上の遺伝子が独立して選別されたり、半数体配偶子が形成される有性生殖の際に相同対から分離されたりすることが可能になる。このようにして、交配対の子孫に新たな遺伝子の組み合わせが生まれる可能性がある。理論的には、同じ染色体上の遺伝子は組換えを起こさない。しかし、染色体交差という細胞内過程を通じた組換えが起こる。染色体交差は、染色体間でDNA断片を交換し、染色体間で遺伝子アレルを効果的にシャッフルする[71]。この染色体交差は通常、減数分裂という半数体細胞を生成する一連の細胞分裂中に起こる。減数分裂組換えは、特に微生物の真核生物において、DNA損傷を修復する適応機能を持つと考えられる[70]。
染色体交差の細胞学的実証は、1931年、ハリエット・クレイトン とバーバラ・マクリントックによって初めて行われた。彼らのトウモロコシに関する研究と実験は、対になった染色体上の遺伝子が実際に相同染色体間で入れ替わるという遺伝学の仮説を、細胞学に証明した[72]。
染色体上の特定の位置間で染色体交差が起こる確率は、その2点間の距離と関係がある。任意の長距離にわたって交差が起こる確率は十分に高いため、それらの遺伝子どうしの遺伝には事実上の相関はない[73]。しかし、遺伝子が互いに近接すると交差が起こる確率は低くなるため、それらの遺伝子は遺伝的連鎖を示し、2つの遺伝子のアレルが一緒に遺伝する傾向がある。一連の遺伝子間の連鎖量を組み合わせて線状連鎖地図を作成し、染色体上に沿った遺伝子の配置を大まかに示すことができる[74]。
遺伝子発現
遺伝暗号
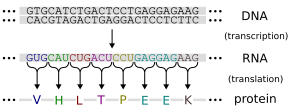
遺伝子は、細胞内のほとんどの機能を担うタンパク質分子の生成を通じて、その機能的な効果を発現する。タンパク質は、アミノ酸の配列からなる1本または複数のポリペプチド鎖で構成される。遺伝子のDNA配列が、特異的なアミノ酸配列を生成するために使われる。この過程は、遺伝子のDNA配列と一致する配列を持つRNA分子の生成 -転写(transcription)と呼ばれる- から始まる。
このメッセンジャーRNA分子は、次に、翻訳(translation)と呼ばれる過程を通じて対応するアミノ酸配列を生成する役割を果たす。DNA配列内の3個のヌクレオチドのセットコドン(codon)と呼ばれ、タンパク質を作り出す20種類のアミノ酸のいずれか1つ、またはアミノ酸配列の終端の指示に対応する。この対応関係を遺伝暗号(genetic code)と呼ぶ[75]。情報の流れは一方向であり、情報はDNAのヌクレオチド配列からタンパク質のアミノ酸配列へと転送されるが、その逆、つまりタンパク質からDNA配列へ戻ることはない。フランシス・クリックは、この現象を分子生物学におけるセントラル・ドグマと呼んだ[76]。
アミノ酸の特異的配列により、そのタンパク質に固有の三次元構造が形成され、その三次元構造はタンパク質の機能と関連している[77][78]。タンパク質には、コラーゲンのように繊維を形成する単純な構造を持つ分子もある。また、タンパク質の中には、他のタンパク質や単純な分子と結合して、その分子の化学反応を促進する酵素として働くものもある(酵素タンパク質それ自体は変化しない)。タンパク質の構造は動的であり、ヘモグロビンというタンパク質は、哺乳類の血液内で酸素分子の捕捉、輸送、放出を促進するときに、わずかに異なる形状をとる[要出典]。
DNA中の1つのヌクレオチドの異なりが、タンパク質のアミノ酸配列を変化させることがある。タンパク質の構造はアミノ酸配列によって決定されるため、一部の変化がタンパク質の構造を不安定にしたり、他のタンパク質や分子との相互作用に影響を与える表面構造を変化させることで、タンパク質の特性を劇的に変える可能性もある。たとえば、鎌状赤血球貧血は、ヘモグロビンの βグロビン部分のコーディング領域内の1塩基の違いによって起こるヒトの遺伝病であり、1つのアミノ酸の変化がヘモグロビンの物理的特性の変化を引き起こす[79]。鎌状赤血球型のヘモグロビンは互いに付着し、積み重なって繊維を形成し、そのタンパク質を輸送する赤血球の形を歪める。この鎌状の細胞は血管内を円滑に流れなくなり、詰まったり劣化する傾向があり、この病気に関連する医学的問題を引き起こす[要出典]。
DNA配列の一部には、RNAへ転写されても、タンパク質に翻訳されないものもある。このようなRNA分子はノンコーディングRNAと呼ばれる。ときには、これらの生成物が、重要な細胞機能に関する構造体を形成することもある(例:リボソームRNAやトランスファーRNA)。RNAは、他のRNA分子(例:microRNA)とのハイブリダイゼーション相互作用を通じて、調節作用を発揮することもある[要出典]。
生まれつきか育ちか

遺伝子は生物が機能するために必要なすべての情報を含んでいるが、最終的に生物が示す表現型を決定する上で、環境も重要な役割を果たしている。「生まれつきか育ちか」という成句は、この相補的な関係を指している。ある生物の表現型は、遺伝子と環境との相互作用によって決定される。興味深い例として、シャム猫の毛色がある。この場合、猫の体温が環境としての役割を果たす。猫の遺伝子は黒毛をコードしているため、猫の毛を生成する細胞は、黒毛を生やす細胞内タンパク質を生成する。しかし、この黒毛を生成するタンパク質は温度に敏感(すなわち、温度感受性変異が起こる)であり、高温環境では変性して、猫の体温が高い部位では黒毛の色素を生成できない。しかし、低温環境下では、タンパク質の構造は安定しており、通常どおり黒毛の色素を生成する。このタンパク質は、足、耳、尾、顔など、皮膚の温度が低い部位で機能するため、この猫は四肢に黒毛が生える[80]。
ヒトの遺伝病であるフェニルケトン尿症は、環境が大きく影響している。フェニルケトン尿症を引き起こす変異は、フェニルアラニンというアミノ酸を分解する体の機能を妨げ、中間分子の毒性蓄積を引き起こし、その結果、進行性の知的障害や発作などの重篤な症状を引き起こす。しかし、フェニルケトン尿症の変異を持つ人でも、このアミノ酸を完全に避ける厳格な食事療法に従えば、健康で正常な状態を維持できる[81]。
遺伝子と環境(「生まれつきか育ちか」)が表現型に及ぼす影響を判断する一般的な方法として、一卵性双生児や二卵性双生児、あるいは多胎児の兄弟姉妹の調査がある[82]。一卵性双生児は同じ受精卵から生まれたため、遺伝的には同じである。一方、二卵性双生児は、遺伝的には普通の兄弟姉妹と同じくらい異なりがある。一卵性双生児の組と二卵性双生児の組で、ある疾患の発症頻度を比較することで、科学者はその疾患が遺伝的要因によるものか、出生後の環境要因によるものかを判断することができる。有名な例として、ジェナイン家の四つ子として知られる一卵性四つ子が全員、統合失調症と診断された研究がある[83]。
遺伝子調節
ある生物のゲノムには何千もの遺伝子が存在しているが、そのすべてが常に活動しているわけではない。ある遺伝子がメッセンジャーRNAへ転写されたときに発現し、タンパク質が細胞に必要とされる場合のみ合成されるように、遺伝子の発現を調節する多くの細胞機構が存在する。転写因子は、DNAに結合し、遺伝子の転写を促進または抑制する制御タンパク質である[84]。たとえば、大腸菌(Escherichia coli)のゲノムには、トリプトファンというアミノ酸の合成に必要な一連の遺伝子が存在する。しかし、トリプトファンがすでに細胞内に存在している場合は、トリプトファン合成のためのこれらの遺伝子は必要でなくなる。トリプトファンの存在は、遺伝子の活性に直接影響を与える。トリプトファン分子は、転写因子であるトリプトファンリプレッサーに結合し、リプレッサーの構造を変えて遺伝子に結合させる。トリプトファンリプレッサーは、遺伝子の転写と発現を抑制し、トリプトファン合成プロセスに負のフィードバック制御をもたらす[85]。
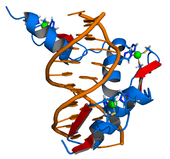
遺伝子発現の違いは特に多細胞生物において顕著になる。多細胞生物では、すべての細胞が同じゲノムを持っているにも関わらず、異なる遺伝子セットの発現により、細胞毎の構造や挙動は大きく異なる。多細胞生物のすべての細胞は単一の細胞に由来するが、外界や細胞間シグナルに応じてさまざまな細胞型へ分化し、徐々に異なる遺伝子発現様式を確立して、さまざまな挙動を生み出す。多細胞生物の構造の発達に関与する遺伝子は一つではないため、これらの様式は多くの細胞間の複雑な相互作用から生じる[要出典]。
真核生物では、遺伝子の転写に影響を与えるクロマチンの構造的特徴が存在し、多くの場合、DNAやクロマチンの修飾という形で娘細胞に安定的に受け継がれる[86]。これらの特徴はDNA配列の「上位」に存在し、細胞のある世代から次の世代へと遺伝情報を継承するため、「エピジェネティクス」(epigenetics、後成的とも)と呼ばれる。エピジェネティックな特徴によって、同じ培地内で培養された異なる細胞型は、非常に異なる特性を保持することができる。エピジェネティックな特徴は、発達過程において一般的に動的であるが、パラミューテーション(パラ変異)現象のように世代を超えて継承され、遺伝の基盤であるDNAの一般的な法則に対するまれな例外として存在するものもある[87]。
遺伝子変化
変異

DNA複製の過程において、第2鎖の合成時に誤りが発生することがある。このような誤りは変異(mutation)と呼ばれ、特に遺伝子のタンパク質コード配列内で発生した場合、生物体の表現型に影響を与える可能性がある。DNAポリメラーゼの「校正」機能により通常、誤り率は非常に低く、1000万-1億塩基あたり1つの割合である[88][89]。DNAの変化率を高めるプロセスは変異誘発として知られる。変異誘発性化学物質は、しばしば塩基対形成の構造に干渉して、DNA複製誤りを促進する。一方、紫外線はDNA構造に損傷を与えることで変異を誘発する[90]。DNAへの化学的損傷は自然にも発生し、細胞はミスマッチや切断を修復するためにDNA修復機構を使用する。ただし、修復は常に元の配列を復元するわけではない。DNA損傷の特に重要な原因として、細胞内好気性呼吸によって生じる活性酸素種があり[91]、これが変異を引き起こす可能性がある[92]。
染色体交差を利用してDNAを交換し、遺伝子を組換える生物では、減数分裂時の整列誤りも変異の原因となる。交差の誤りは、特に、類似した配列が相同染色体 の誤った整列を引き起こした場合に起こりやすく、これによりゲノムの一部の領域が変異しやすくなる。これらの誤りは、DNA配列の大幅な構造変化や(重複、逆位、領域全体の欠失)、異なる染色体間で配列全体が偶然入れ替わる染色体転座を引き起こす可能性がある[93]。

自然選択と進化
変異は生物の遺伝子型を変え、ときには異なる表現型を生み出す原因となる。ほとんどの変異は、生物の表現型、健康、遺伝的適応度にほとんど影響を与えない[94]。実際に影響をもたらす変異は通常有害であるが、ときには有益なこともある[95]。ショウジョウバエ(Drosophila melanogaster)の研究によると、ある遺伝子によって生成されるタンパク質が変異した場合、その変異の約70%は有害であり、残りは中立的またはわずかに有益であることが示唆された[96]。

集団遺伝学は、集団内の遺伝的差異の分布と、その分布が時間とともにどのように変化するかを研究する学問である[97]。集団内のアレル頻度の変化は、主に自然選択(あるアレルが生物にとって選択的または繁殖上の優位性をもたらすこと[98])、変異、遺伝的浮動、遺伝的ヒッチハイク[99]、人為選択、流動などの要因によって影響を受ける[100]。
世代を重ねるごとに生物のゲノムは大きく変化し、進化につながる。適応(adaptation)と呼ばれる過程では、有益な変異に対する選択によって、その種はその環境下でより生き残れる形へと進化する可能性がある[101]。新種は種分化(speciation)と呼ばれる過程を経て形成されるが、その多くは地理的な隔離によって個体群間の遺伝子交換が妨げられることが原因である[102]。
異なる生物種でゲノム間の相同性を比較することで、これらの種の進化距離と分岐時期を推定することができる。一般的に、表現形質の比較よりも遺伝的比較の方が、生物種間の関連を特徴付ける上でより正確な方法であるとされている。生物種間の進化距離は、進化系統樹を作成するために利用することができる。これらの系統樹は、時間の経過に伴う種の共通祖先と分岐を表すが、無関係な種間での遺伝物質の移動(遺伝子の水平伝播といい、細菌で最も一般的)は示さない[103]。
研究と技術
モデル生物

遺伝学者はもともと、幅広い生物の遺伝を研究していたが、研究対象となった生物種は徐々に絞られていった。その理由のひとつは、特定の生物についてすでに重要な研究が行われている場合、新たな研究者はその生物を研究対象に選ぶ可能性が高く、最終的には少数のモデル生物がほとんどの遺伝学研究の基礎となったことである。モデル生物遺伝学における一般的な研究テーマには、遺伝子調節や発生、がんにおける遺伝子の関与などがある。生物の選定には利便性が考慮され(たとえば、世代交代までの期間が短く、遺伝子の操作が容易など)、一部の生物は遺伝学研究で人気のツールとなった。広く使用されているモデル生物には、腸内細菌の大腸菌(Escherichia coli)、植物のシロイヌナズナ(Arabidopsis thaliana)、パン酵母(Saccharomyces cerevisiae)、線形動物のカエノラブディティス・エレガンス(Caenorhabditis elegans)、ショウジョウバエ(Drosophila melanogaster)、ゼブラフィッシュ(Danio rerio)、ハツカネズミ(Mus musculus)などがある[104]。
医学

遺伝医学は、遺伝的変異がヒトの健康と疾患にどのように関係しているかを解明しようとする学問である[105]。ある疾患に関与している可能性のある未知の遺伝子を探す場合、研究者は一般的に、遺伝的連鎖図や遺伝系図を使用して、その疾患に関連するゲノムの位置を見つける。集団レベルでは、ゲノム上の疾患に関連する位置を見つけるためにメンデル無作為化が行われる。この方法は、単一遺伝子では明確に定義できない多遺伝子形質に特に有用である[106]。候補となる遺伝子が見つかると、モデル生物において対応する(または相同性のある)遺伝子について、さらなる研究が行われることが多い。遺伝性疾患の研究に加え、遺伝子型判定法の普及により、薬理遺伝学という分野が生まれた。これは、遺伝子型が薬剤応答性にどのような影響を与えるかを研究する分野である[107]。
がんは遺伝性疾患であり、がんを発症する遺伝的傾向には個人差がある。がん発症は、体内におけるいくつかの事象が組み合わさっている。体内の細胞が分裂する際に、細胞内に変異が生じる場合がある。これらの変異が子孫に遺伝することはないが、細胞の挙動に影響を与え、細胞の増殖や分裂をより活発にさせる原因となることがある。こうした過程を防ぐための生物学的なメカニズムがあり、不適切に分裂している細胞にシグナルが送られ、細胞死を引き起こす。しかし、細胞がシグナルを無視するような別の変異が発生することがある。体内で自然選択のプロセスが起こり、やがて細胞内に変異が蓄積して細胞自身の増殖を促進し、体内のさまざまな組織に浸潤して増殖する癌性腫瘍を形成する。通常、細胞は成長因子と呼ばれるシグナルに反応してのみ分裂し、周囲の細胞と接触したり、増殖抑制シグナルに反応したりすると増殖を停止する。その後、細胞は通常、限られた回数しか分裂せず、上皮内にとどまり、他の臓器に移動できないまま死んでゆく。がん細胞になるには、細胞はいくつかの遺伝子(3-7個)に変異を蓄積する必要がある。がん細胞は成長因子がなくても分裂し、増殖抑制シグナルを無視する可能性がある。また、がん細胞は不死であり、隣接する細胞と接触しても際限なく増殖し続けることができる。上皮から脱出し、最終的には原発巣から脱出することもある。脱出した細胞は血管の内皮を横断し、血流にのって運ばれ、新たな臓器に定着し、致命的な転移を形成する。ごく一部のがんは遺伝的素因を示すが、大部分は腫瘍を形成する細胞分裂を繰り返す1つまたは少数の細胞に生じ・蓄積する一連の遺伝子変異によって引き起こされ、これらの変異は子孫に遺伝しない(体細胞変異を参照)。最もよく見られる変異は、がん抑制因子であるp53タンパク質の機能喪失、またはp53経路における機能喪失、Rasタンパク質または他のがん遺伝子の活性化変異である[108][109]。
研究方法
DNAは実験室で操作することができる。制限酵素は、DNAを特異的配列で切断し、予測可能なDNA断片を生成する酵素として一般的に使用されている[110]。DNA断片は、その長さに応じて分離するゲル電気泳動法によって可視化できる[111]。
DNA断片を結合するためにDNAリガーゼと呼ばれる酵素が使用される。この方法により、研究者はさまざまな供給源から得たDNA断片を結合させて、組換えDNAを作成することができる。遺伝子組換え生物の研究では、組換えDNAとともにプラスミド(数個の遺伝子を持つ短い環状DNA分子)がよく使われる。分子クローニングと呼ばれる手法では、DNA断片を組み込んだプラスミドを細菌に挿入し寒天培地上で培養することで、DNA断片を増幅することが可能である。なお、クローニングはこのような分子遺伝学的な手法だけでなく、クローン生物を作成するためのさまざまな手段を指すこともある[112]。
ポリメラーゼ連鎖反応(PCR)と呼ばれる手順を用いてDNAを増幅することもできる[113]。PCR法は、短い特異的なDNA配列を用いて標的のDNA領域を分離し、指数関数的に増幅することができる技術である。PCR法は、ごく微量のDNAからでも増幅できるため、特定のDNA配列の存在を検出する際にもよく用いられる[114][115]。
DNA配列決定とゲノミクス
DNA配列決定(DNAシークエンシングともいう)は、遺伝学の研究のために開発された最も基本的な技術の一つであり、研究者はこれによってDNA断片中のヌクレオチド配列を決定することができるようになった。1977年にフレデリック・サンガーが率いた研究チームによって開発された連鎖停止配列決定法(chain-termination sequencing)は、現在もDNA断片の配列決定に日常的に使用されている。この技術により、多くのヒト疾患に関連する分子配列の研究が可能となった[116]。
配列決定の費用が下がったことで、研究者はゲノムアセンブリ(genome assembly)と呼ばれる手法を用いて、多くの生物のゲノム配列を決定した。これは、コンピュータを使用して、さまざまなDNA断片の配列をつなぎ合わせる技術である[117]。これらの技術は、2003年に完了したヒトゲノム・プロジェクトにおいてヒトゲノムの配列決定に使用された[41]。新しいハイスループット配列決定技術により、DNA配列決定の費用が劇的に低下し、多くの研究者はヒトゲノムの再配列決定の費用を1,000ドルまで引き下げたいと考えている[118]。次世代配列決定法(超並列シークエンシング)は、配列決定の低コスト化に対する需要の高まりにより誕生した。
これらの配列決定技術により、同時に何百万もの塩基配列を生成することが可能となった[119][120]。大量の配列データを利用して、生物のゲノム全体にわたるパターンを検索・分析するコンピュータツールを使用するゲノミクスという研究分野も生まれた。ゲノミクスは、大量の生物学データを分析するために計算手法を使用するバイオインフォマティクスの亜分野とも考えられる。これらの研究分野に共通する課題は、被験者データや個人を特定しうる情報の管理と共有方法である[要出典]。
社会と文化
2015年3月19日、主要な生物学者グループが、遺伝可能な形でヒトゲノムを編集する手法、特にCRISPRとジンクフィンガーの臨床使用を世界的に禁止するよう求めた[121][122][123][124]。2015年4月、中国の研究者が、CRISPRを使用して生育不能なヒト胚のDNAを編集する基礎研究の結果を報告した[125][126]。
脚注
注釈
出典
- ^ “Genetics and the Organism: Introduction”. An Introduction to Genetic Analysis (7th ed.). New York: W.H. Freeman. (2000). ISBN 978-0-7167-3520-5
- ^ Hartl D, Jones E (2005)
- ^ “the definition of genetics” (英語). www.dictionary.com. 25 October 2018閲覧。
- ^ “Genetikos (γενετ-ικός)”. Henry George Liddell, Robert Scott, A Greek-English Lexicon. Perseus Digital Library, Tufts University. 15 June 2010時点のオリジナルよりアーカイブ。20 February 2012閲覧。
- ^ “Genesis (γένεσις)”. Henry George Liddell, Robert Scott, A Greek-English Lexicon. Perseus Digital Library, Tufts University. 15 June 2010時点のオリジナルよりアーカイブ。20 February 2012閲覧。
- ^ "Genetic". Online Etymology Dictionary. 2011年8月23日時点のオリジナルよりアーカイブ。2012年2月20日閲覧。
- ^ Science: The Definitive Visual Guide. Penguin. (2009). p. 362. ISBN 978-0-7566-6490-9
- ^ Poczai P, Santiago-Blay JA (July 2022). “Themes of Biological Inheritance in Early Nineteenth Century Sheep Breeding as Revealed by J. M. Ehrenfels”. Genes 13 (8): 1311. doi:10.3390/genes13081311. PMC 9332421. PMID 35893050.
- ^ Weiling F (July 1991). “Historical study: Johann Gregor Mendel 1822-1884”. American Journal of Medical Genetics 40 (1): 1–25; discussion 26. doi:10.1002/ajmg.1320400103. PMID 1887835.
- ^ a b Poczai P, Santiago-Blay JA (October 2021). “Principles and biological concepts of heredity before Mendel”. Biology Direct 16 (1): 19. doi:10.1186/s13062-021-00308-4. PMC 8532317. PMID 34674746.
 Text was copied from this source, which is available under a Creative Commons Attribution 4.0 International License Archived 16 October 2017 at the Wayback Machine..
Text was copied from this source, which is available under a Creative Commons Attribution 4.0 International License Archived 16 October 2017 at the Wayback Machine..
- ^ Szabó AT, Poczai P (June 2019). “The emergence of genetics from Festetics' sheep through Mendel's peas to Bateson's chickens”. Journal of Genetics 98 (2): 63. doi:10.1007/s12041-019-1108-z. hdl:10138/324962. PMID 31204695.
- ^ Poczai P, Bell N, Hyvönen J (January 2014). “Imre Festetics and the Sheep Breeders' Society of Moravia: Mendel's Forgotten "Research Network"”. PLOS Biology 12 (1): e1001772. doi:10.1371/journal.pbio.1001772. PMC 3897355. PMID 24465180.
- ^ Poczai P (2022). Heredity Before Mendel: Festetics and the Question of Sheep's Wool in Central Europe. Boca Raton, Florida: CRC Press. p. 113. ISBN 978-1-032-02743-2 30 August 2022閲覧。
- ^ Poczai P, Santiago-Blay JA, Sekerák J, Bariska I, Szabó AT (October 2022). “Mimush Sheep and the Spectre of Inbreeding: Historical Background for Festetics's Organic and Genetic Laws Four Decades Before Mendel's Experiments in Peas”. Journal of the History of Biology 55 (3): 495–536. doi:10.1007/s10739-022-09678-5. PMC 9668798. PMID 35670984.
- ^ Poczai P, Santiago-Blay JA (2022). “Chip Off the Old Block: Generation, Development, and Ancestral Concepts of Heredity”. Frontiers in Genetics 13: 814436. doi:10.3389/fgene.2022.814436. PMC 8959437. PMID 35356423.
- ^ Hamilton H (2011). Population Genetics. Georgetown University. p. 26. ISBN 978-1-4443-6245-9
- ^ Lamarck, J-B (2008). In Encyclopædia Britannica. Retrieved from Encyclopædia Britannica Online Archived 14 April 2020 at the Wayback Machine. on 16 March 2008.
- ^ Peter J. Bowler, The Mendelian Revolution: The Emergency of Hereditarian Concepts in Modern Science and Society (Baltimore: Johns Hopkins University Press, 1989): chapters 2 & 3.
- ^ a b Blumberg RB. “Mendel's Paper in English”. 13 January 2016時点のオリジナルよりアーカイブ。2009年9月28日閲覧。
- ^ genetics, n., Oxford English Dictionary, 3rd ed.
- ^ Bateson W. “Letter from William Bateson to Alan Sedgwick in 1905”. The John Innes Centre. 13 October 2007時点のオリジナルよりアーカイブ。15 March 2008閲覧。 The letter was to an Adam Sedgwick, a zoologist and "Reader in Animal Morphology" at Trinity College, Cambridge
- ^ genetic, adj., Oxford English Dictionary, 3rd ed.
- ^ Richmond ML (November 2007). “Opportunities for women in early genetics”. Nature Reviews. Genetics 8 (11): 897–902. doi:10.1038/nrg2200. PMID 17893692. オリジナルの16 May 2008時点におけるアーカイブ。.
- ^ Bateson W (1907). "The Progress of Genetic Research". In Wilks, W (ed.). Report of the Third 1906 International Conference on Genetics: Hybridization (the cross-breeding of genera or species), the cross-breeding of varieties, and general plant breeding. London: Royal Horticultural Society. :Initially titled the "International Conference on Hybridisation and Plant Breeding", the title was changed as a result of Bateson's speech. See: Cock AG, Forsdyke DR (2008). Treasure your exceptions: the science and life of William Bateson. Springer. p. 248. ISBN 978-0-387-75687-5
- ^ a b c “Nettie Stevens: A Discoverer of Sex Chromosomes”. Scitable. Nature Education. 8 June 2020閲覧。
- ^ Moore JA (1983). “Thomas Hunt Morgan – The Geneticist”. Integrative and Comparative Biology 23 (4): 855–865. doi:10.1093/icb/23.4.855.
- ^ Sturtevant AH (1913). “The linear arrangement of six sex-linked factors in Drosophila, as shown by their mode of association”. Journal of Experimental Biology 14 (1): 43–59. Bibcode: 1913JEZ....14...43S. doi:10.1002/jez.1400140104. オリジナルの27 February 2008時点におけるアーカイブ。.
- ^ Avery OT, Macleod CM, McCarty M (February 1944). “STUDIES ON THE CHEMICAL NATURE OF THE SUBSTANCE INDUCING TRANSFORMATION OF PNEUMOCOCCAL TYPES : INDUCTION OF TRANSFORMATION BY A DESOXYRIBONUCLEIC ACID FRACTION ISOLATED FROM PNEUMOCOCCUS TYPE III”. The Journal of Experimental Medicine 79 (2): 137–158. doi:10.1084/jem.79.2.137. PMC 2135445. PMID 19871359. Reprint: Avery OT, MacLeod CM, McCarty M (February 1979). “Studies on the chemical nature of the substance inducing transformation of pneumococcal types. Inductions of transformation by a desoxyribonucleic acid fraction isolated from pneumococcus type III”. The Journal of Experimental Medicine 149 (2): 297–326. doi:10.1084/jem.149.2.297. PMC 2184805. PMID 33226.
- ^ Khanna P (2008). Cell and Molecular Biology. I.K. International Pvt Ltd. p. 221. ISBN 978-81-89866-59-4
- ^ Hershey AD, Chase M (May 1952). “Independent functions of viral protein and nucleic acid in growth of bacteriophage”. The Journal of General Physiology 36 (1): 39–56. doi:10.1085/jgp.36.1.39. PMC 2147348. PMID 12981234.
- ^ Judson H (1979). The Eighth Day of Creation: Makers of the Revolution in Biology. Cold Spring Harbor Laboratory Press. pp. 51–169. ISBN 978-0-87969-477-7
- ^ Watson JD, Crick FH (April 1953). “Molecular structure of nucleic acids; a structure for deoxyribose nucleic acid”. Nature 171 (4356): 737–738. Bibcode: 1953Natur.171..737W. doi:10.1038/171737a0. PMID 13054692. オリジナルの4 February 2007時点におけるアーカイブ。.
- ^ Watson JD, Crick FH (May 1953). “Genetical implications of the structure of deoxyribonucleic acid”. Nature 171 (4361): 964–967. Bibcode: 1953Natur.171..964W. doi:10.1038/171964b0. PMID 13063483. オリジナルの21 June 2003時点におけるアーカイブ。.
- ^ Stratmann SA, van Oijen AM (February 2014). “DNA replication at the single-molecule level”. Chemical Society Reviews 43 (4): 1201–1220. doi:10.1039/c3cs60391a. PMID 24395040. オリジナルの2017-07-06時点におけるアーカイブ。.
- ^ Frederick B (2010). Managing Science: Methodology and Organization of Research. Springer. p. 76. ISBN 978-1-4419-7488-4
- ^ Rice SA (2009). Encyclopedia of Evolution. Infobase Publishing. p. 134. ISBN 978-1-4381-1005-9
- ^ Sarkar S (1998). Genetics and Reductionism. Cambridge University Press. p. 140. ISBN 978-0-521-63713-8
- ^ Ohta T (November 1973). “Slightly deleterious mutant substitutions in evolution”. Nature 246 (5428): 96–98. Bibcode: 1973Natur.246...96O. doi:10.1038/246096a0. PMID 4585855.
- ^ Sanger F, Nicklen S, Coulson AR (December 1977). “DNA sequencing with chain-terminating inhibitors”. Proceedings of the National Academy of Sciences of the United States of America 74 (12): 5463–5467. Bibcode: 1977PNAS...74.5463S. doi:10.1073/pnas.74.12.5463. PMC 431765. PMID 271968.
- ^ Saiki RK, Scharf S, Faloona F, Mullis KB, Horn GT, Erlich HA, Arnheim N (December 1985). “Enzymatic amplification of beta-globin genomic sequences and restriction site analysis for diagnosis of sickle cell anemia”. Science 230 (4732): 1350–1354. Bibcode: 1985Sci...230.1350S. doi:10.1126/science.2999980. PMID 2999980.
- ^ a b “Human Genome Project Information”. Human Genome Project. 15 March 2008時点のオリジナルよりアーカイブ。15 March 2008閲覧。
- ^ “The sequence of the human genome”. Science 291.
- ^ “Patterns of Inheritance: Introduction”. An Introduction to Genetic Analysis (7th ed.). New York: W.H. Freeman. (2000). ISBN 978-0-7167-3520-5
- ^ “Mendel's experiments”. An Introduction to Genetic Analysis (7th ed.). New York: W.H. Freeman. (2000). ISBN 978-0-7167-3520-5
- ^ a b c “Mendelian genetics in eukaryotic life cycles”. An Introduction to Genetic Analysis (7th ed.). New York: W.H. Freeman. (2000). ISBN 978-0-7167-3520-5
- ^ a b 日本遺伝学会『遺伝学用語改訂について』(レポート)2017年9月11日、1–3頁。2024年8月9日閲覧。
- ^ “Interactions between the alleles of one gene”. An Introduction to Genetic Analysis (7th ed.). New York: W.H. Freeman. (2000). ISBN 978-0-7167-3520-5
- ^ “Probabilities in genetics (article)”. Khan Academy. 2022年9月28日閲覧。
- ^ Cheney RW. “Genetic Notation”. Christopher Newport University. 3 January 2008時点のオリジナルよりアーカイブ。18 March 2008閲覧。
- ^ Müller-Wille S, Parolini G (2020-12-09). “Punnett squares and hybrid crosses: how Mendelians learned their trade by the book”. Learning by the Book: Manuals and Handbooks in the History of Science. BJHS Themes. 5. British Society for the History of Science / Cambridge University Press. pp. 149–165. doi:10.1017/bjt.2020.12. オリジナルの2021-03-29時点におけるアーカイブ。 2021年3月29日閲覧。
- ^ “Human Genetics”. An Introduction to Genetic Analysis (7th ed.). New York: W.H. Freeman. (2000). ISBN 978-0-7167-3520-5
- ^ “Gene interaction and modified dihybrid ratios”. An Introduction to Genetic Analysis (7th ed.). New York: W.H. Freeman. (2000). ISBN 978-0-7167-3520-5
- ^ Mayeux R (June 2005). “Mapping the new frontier: complex genetic disorders”. The Journal of Clinical Investigation 115 (6): 1404–1407. doi:10.1172/JCI25421. PMC 1137013. PMID 15931374.
- ^ “Quantifying heritability”. An Introduction to Genetic Analysis (7th ed.). New York: W. H. Freeman. (2000). ISBN 978-0-7167-3520-5
- ^ Luke A, Guo X, Adeyemo AA, Wilks R, Forrester T, Lowe W, Comuzzie AG, Martin LJ, Zhu X, Rotimi CN, Cooper RS (July 2001). “Heritability of obesity-related traits among Nigerians, Jamaicans and US black people”. International Journal of Obesity and Related Metabolic Disorders 25 (7): 1034–1041. doi:10.1038/sj.ijo.0801650. PMID 11443503.
- ^ Urry L, Cain M, Wasserman S, Minorsky P, Reece J, Campbell N. “Campbell Biology”. plus.pearson.com. 2022年9月28日閲覧。
- ^ Pearson H (May 2006). “Genetics: what is a gene?”. Nature 441 (7092): 398–401. Bibcode: 2006Natur.441..398P. doi:10.1038/441398a. PMID 16724031.
- ^ “Histone” (英語). Genome.gov. 2022年9月28日閲覧。
- ^ Prescott LM, Harley JP, Klein DA (1996). Microbiology (3rd ed.). Wm. C. Brown. p. 343. ISBN 0-697-21865-1
- ^ “Mechanism of DNA Replication”. An Introduction to Genetic Analysis (7th ed.). New York: W.H. Freeman. (2000). ISBN 978-0-7167-3520-5
- ^ Gregory SG, Barlow KF, McLay KE, Kaul R, Swarbreck D, Dunham A, Scott CE, Howe KL, Woodfine K, Spencer CC, Jones MC, Gillson C, Searle S, Zhou Y, Kokocinski F, McDonald L, Evans R, Phillips K, Atkinson A, Cooper R, Jones C, Hall RE, Andrews TD, Lloyd C, Ainscough R, Almeida JP, Ambrose KD, Anderson F, Andrew RW, Ashwell RI, Aubin K, Babbage AK, Bagguley CL, Bailey J, Beasley H, Bethel G, Bird CP, Bray-Allen S, Brown JY, Brown AJ, Buckley D, Burton J, Bye J, Carder C, Chapman JC, Clark SY, Clarke G, Clee C, Cobley V, Collier RE, Corby N, Coville GJ, Davies J, Deadman R, Dunn M, Earthrowl M, Ellington AG, Errington H, Frankish A, Frankland J, French L, Garner P, Garnett J, Gay L, Ghori MR, Gibson R, Gilby LM, Gillett W, Glithero RJ, Grafham DV, Griffiths C, Griffiths-Jones S, Grocock R, Hammond S, Harrison ES, Hart E, Haugen E, Heath PD, Holmes S, Holt K, Howden PJ, Hunt AR, Hunt SE, Hunter G, Isherwood J, James R, Johnson C, Johnson D, Joy A, Kay M, Kershaw JK, Kibukawa M, Kimberley AM, King A, Knights AJ, Lad H, Laird G, Lawlor S, Leongamornlert DA, Lloyd DM, Loveland J, Lovell J, Lush MJ, Lyne R, Martin S, Mashreghi-Mohammadi M, Matthews L, Matthews NS, McLaren S, Milne S, Mistry S, Moore MJ, Nickerson T, O'Dell CN, Oliver K, Palmeiri A, Palmer SA, Parker A, Patel D, Pearce AV, Peck AI, Pelan S, Phelps K, Phillimore BJ, Plumb R, Rajan J, Raymond C, Rouse G, Saenphimmachak C, Sehra HK, Sheridan E, Shownkeen R, Sims S, Skuce CD, Smith M, Steward C, Subramanian S, Sycamore N, Tracey A, Tromans A, Van Helmond Z, Wall M, Wallis JM, White S, Whitehead SL, Wilkinson JE, Willey DL, Williams H, Wilming L, Wray PW, Wu Z, Coulson A, Vaudin M, Sulston JE, Durbin R, Hubbard T, Wooster R, Dunham I, Carter NP, McVean G, Ross MT, Harrow J, Olson MV, Beck S, Rogers J, Bentley DR, Banerjee R, Bryant SP, Burford DC, Burrill WD, Clegg SM, Dhami P, Dovey O, Faulkner LM, Gribble SM, Langford CF, Pandian RD, Porter KM, Prigmore E (May 2006). “The DNA sequence and biological annotation of human chromosome 1”. Nature 441 (7091): 315–321. Bibcode: 2006Natur.441..315G. doi:10.1038/nature04727. PMID 16710414.
- ^ Alberts, Bruce; Johnson, Alexander; Lewis, Julian; Raff, Martin; Roberts, Keith; Walter, Peter (2002) (英語), Chromosomal DNA and Its Packaging in the Chromatin Fiber, Garland Science 2024年7月25日閲覧。
- ^ a b c “Ruth Sager”. Encyclopaedia Britannica. 8 June 2020閲覧。
- ^ “Sex chromosomes and sex-linked inheritance”. An Introduction to Genetic Analysis (7th ed.). New York: W.H. Freeman. (2000). ISBN 978-0-7167-3520-5
- ^ a b Rastan S (February 2015). “Mary F. Lyon (1925-2014)”. Nature (Springer Nature Limited) 518 (7537): 36. Bibcode: 2015Natur.518...36R. doi:10.1038/518036a. PMID 25652989.
- ^ “clone”. Merriam-Webster Dictionary. 13 November 2023閲覧。
- ^ “Haploid” (英語). www.genome.gov. 2024年2月10日閲覧。
- ^ “Bacterial conjugation”. An Introduction to Genetic Analysis (7th ed.). New York: W.H. Freeman. (2000). ISBN 978-0-7167-3520-5
- ^ “Bacterial transformation”. An Introduction to Genetic Analysis (7th ed.). New York: W.H. Freeman. (2000). ISBN 978-0-7167-3520-5
- ^ a b c Bernstein H, Bernstein C, Michod RE (January 2018). “Sex in microbial pathogens”. Infection, Genetics and Evolution 57: 8–25. Bibcode: 2018InfGE..57....8B. doi:10.1016/j.meegid.2017.10.024. PMID 29111273.
- ^ “Nature of crossing-over”. An Introduction to Genetic Analysis (7th ed.). New York: W. H. Freeman. (2000). ISBN 978-0-7167-3520-5
- ^ Creighton HB, McClintock B (August 1931). “A Correlation of Cytological and Genetical Crossing-Over in Zea Mays”. Proceedings of the National Academy of Sciences of the United States of America 17 (8): 492–497. Bibcode: 1931PNAS...17..492C. doi:10.1073/pnas.17.8.492. PMC 1076098. PMID 16587654.
- ^ Staub JE (1994). Crossover: Concepts and Applications in Genetics, Evolution, and Breeding. University of Wisconsin Press. p. 55. ISBN 978-0-299-13564-5
- ^ “Linkage maps”. An Introduction to Genetic Analysis (7th ed.). New York: W. H. Freeman. (2000). ISBN 978-0-7167-3520-5
- ^ Berg JM, Tymoczko JL, Stryer L, Clarke ND (2002). “I. 5. DNA, RNA, and the Flow of Genetic Information: Amino Acids Are Encoded by Groups of Three Bases Starting from a Fixed Point”. Biochemistry (5th ed.). New York: W.H. Freeman and Company. オリジナルの11 April 2006時点におけるアーカイブ。
- ^ Crick F (August 1970). “Central dogma of molecular biology”. Nature 227 (5258): 561–563. Bibcode: 1970Natur.227..561C. doi:10.1038/227561a0. PMID 4913914. オリジナルの15 February 2006時点におけるアーカイブ。.
- ^ Alberts et al. (2002年). “I.3. Proteins: The Shape and Structure of Proteins”. 2023年1月1日時点のオリジナルよりアーカイブ。2024年8月9日閲覧。
- ^ Alberts et al. (2002年). “Proteins: Protein Function”. 2006年4月25日時点のI.3. オリジナルよりアーカイブ。2024年8月9日閲覧。
- ^ “How Does Sickle Cell Cause Disease?”. Brigham and Women's Hospital: Information Center for Sickle Cell and Thalassemic Disorders (11 April 2002). 23 September 2010時点のオリジナルよりアーカイブ。23 July 2007閲覧。
- ^ Imes DL, Geary LA, Grahn RA, Lyons LA (April 2006). “Albinism in the domestic cat (Felis catus) is associated with a tyrosinase (TYR) mutation”. Animal Genetics 37 (2): 175–178. doi:10.1111/j.1365-2052.2005.01409.x. PMC 1464423. PMID 16573534.
- ^ “MedlinePlus: Phenylketonuria”. NIH: National Library of Medicine. 25 July 2008時点のオリジナルよりアーカイブ。15 March 2008閲覧。
- ^ For example, Ridley M (2003). Nature via Nurture: Genes, Experience and What Makes Us Human. Fourth Estate. p. 73. ISBN 978-1-84115-745-0
- ^ Rosenthal D (1964). “The Genain Quadruplets: A Case Study and Theoretical Analysis of Heredity and Environment in Schizophrenia”. Behavioral Science 9 (4): 371. doi:10.1002/bs.3830090407.
- ^ Brivanlou AH, Darnell JE (February 2002). “Signal transduction and the control of gene expression”. Science 295 (5556): 813–818. Bibcode: 2002Sci...295..813B. doi:10.1126/science.1066355. PMID 11823631.
- ^ Alberts et al. (2002), II.3. Control of Gene Expression – The Tryptophan Repressor is a Simple Switch That Turns Genes On and Off in Bacteria Archived 29 June 2007 at the Wayback Machine.
- ^ Jaenisch R, Bird A (March 2003). “Epigenetic regulation of gene expression: how the genome integrates intrinsic and environmental signals”. Nature Genetics 33 (Suppl): 245–254. doi:10.1038/ng1089. PMID 12610534.
- ^ Chandler VL (February 2007). “Paramutation: from maize to mice”. Cell 128 (4): 641–645. doi:10.1016/j.cell.2007.02.007. PMID 17320501.
- ^ “Spontaneous mutations”. An Introduction to Genetic Analysis (7th ed.). New York: W.H. Freeman. (2000). ISBN 978-0-7167-3520-5
- ^ Freisinger E, Grollman AP, Miller H, Kisker C (April 2004). “Lesion (in)tolerance reveals insights into DNA replication fidelity”. The EMBO Journal 23 (7): 1494–1505. doi:10.1038/sj.emboj.7600158. PMC 391067. PMID 15057282.
- ^ “Induced mutations”. An Introduction to Genetic Analysis (7th ed.). New York: W. H. Freeman. (2000). ISBN 978-0-7167-3520-5
- ^ Cadet J, Wagner JR (February 2013). “DNA base damage by reactive oxygen species, oxidizing agents, and UV radiation”. Cold Spring Harbor Perspectives in Biology 5 (2): a012559. doi:10.1101/cshperspect.a012559. PMC 3552502. PMID 23378590.
- ^ Jena NR (July 2012). “DNA damage by reactive species: Mechanisms, mutation and repair”. Journal of Biosciences 37 (3): 503–517. doi:10.1007/s12038-012-9218-2. PMID 22750987.
- ^ “Chromosome Mutation I: Changes in Chromosome Structure: Introduction”. An Introduction to Genetic Analysis (7th ed.). New York: W.H. Freeman. (2000). ISBN 978-0-7167-3520-5
- ^ Schaechter M (2009). Encyclopedia of Microbiology. Academic Press. p. 551. ISBN 978-0-12-373944-5
- ^ Calver M, Lymbery A, McComb J, Bamford M (2009). Environmental Biology. Cambridge University Press. p. 118. ISBN 978-0-521-67982-4
- ^ Sawyer SA, Parsch J, Zhang Z, Hartl DL (April 2007). “Prevalence of positive selection among nearly neutral amino acid replacements in Drosophila”. Proceedings of the National Academy of Sciences of the United States of America 104 (16): 6504–6510. Bibcode: 2007PNAS..104.6504S. doi:10.1073/pnas.0701572104. PMC 1871816. PMID 17409186.
- ^ “Variation and its modulation”. An Introduction to Genetic Analysis (7th ed.). New York: W.H. Freeman. (2000). ISBN 978-0-7167-3520-5
- ^ “Selection”. An Introduction to Genetic Analysis (7th ed.). New York: W. H. Freeman. (2000). ISBN 978-0-7167-3520-5
- ^ Gillespie JH (November 2001). “Is the population size of a species relevant to its evolution?”. Evolution; International Journal of Organic Evolution 55 (11): 2161–2169. doi:10.1111/j.0014-3820.2001.tb00732.x. PMID 11794777.
- ^ “Random events”. An Introduction to Genetic Analysis (7th ed.). New York: W.H. Freeman. (2000). ISBN 978-0-7167-3520-5
- ^ Darwin C (1859). On the Origin of Species. London: John Murray. p. 1. ISBN 978-0-8014-1319-3. オリジナルの12 December 2006時点におけるアーカイブ。
Earlier related ideas were acknowledged in Darwin C (1861). On the Origin of Species (3rd ed.). London: John Murray. p. xiii. ISBN 978-0-8014-1319-3. オリジナルの23 February 2011時点におけるアーカイブ。 - ^ Gavrilets S (October 2003). “Perspective: models of speciation: what have we learned in 40 years?”. Evolution; International Journal of Organic Evolution 57 (10): 2197–2215. doi:10.1554/02-727. PMID 14628909.
- ^ Wolf YI, Rogozin IB, Grishin NV, Koonin EV (September 2002). “Genome trees and the tree of life”. Trends in Genetics 18 (9): 472–479. doi:10.1016/S0168-9525(02)02744-0. PMID 12175808.
- ^ “The Use of Model Organisms in Instruction”. University of Wisconsin: Wisconsin Outreach Research Modules. 13 March 2008時点のオリジナルよりアーカイブ。15 March 2008閲覧。
- ^ “NCBI: Genes and Disease”. NIH: National Center for Biotechnology Information. 20 February 2007時点のオリジナルよりアーカイブ。15 March 2008閲覧。
- ^ Smith GD, Ebrahim S (February 2003). “'Mendelian randomization': can genetic epidemiology contribute to understanding environmental determinants of disease?”. International Journal of Epidemiology 32 (1): 1–22. doi:10.1093/ije/dyg070. PMID 12689998.
- ^ “Pharmacogenetics Fact Sheet”. NIH: National Institute of General Medical Sciences. 12 May 2008時点のオリジナルよりアーカイブ。15 March 2008閲覧。
- ^ Frank SA (October 2004). “Genetic predisposition to cancer - insights from population genetics”. Nature Reviews. Genetics 5 (10): 764–772. doi:10.1038/nrg1450. PMID 15510167.
- ^ Strachan T, Read AP (1999). Human Molecular Genetics 2 (second ed.). John Wiley & Sons Inc. Chapter 18: Cancer Genetics Archived 26 September 2005 at the Wayback Machine.
- ^ Lodish et al. (2000), Chapter 7: 7.1. DNA Cloning with Plasmid Vectors Archived 27 May 2009 at the Wayback Machine.
- ^ “Gel electrophoresis (article)” (英語). Khan Academy. 2024年2月21日閲覧。
- ^ Keefer CL (July 2015). “Artificial cloning of domestic animals”. Proceedings of the National Academy of Sciences of the United States of America 112 (29): 8874–8878. Bibcode: 2015PNAS..112.8874K. doi:10.1073/pnas.1501718112. PMC 4517265. PMID 26195770.
- ^ Lodish et al. (2000), Chapter 7: 7.7. Polymerase Chain Reaction: An Alternative to Cloning
- ^ Chang, Dingran; Tram, Kha; Li, Ben; Feng, Qian; Shen, Zhifa; Lee, Christine H.; Salena, Bruno J.; Li, Yingfu (2017-06-08). “Detection of DNA Amplicons of Polymerase Chain Reaction Using Litmus Test”. Scientific Reports 7 (3110): 3110. Bibcode: 2017NatSR...7.3110C. doi:10.1038/s41598-017-03009-z. PMC 5465217. PMID 28596600.
- ^ Garibyan, Lilit; Nidhi (March 2013). “Polymerase Chain Reaction”. Journal of Investigative Dermatology 133 (3): 1–4. doi:10.1038/jid.2013.1. PMC 4102308. PMID 23399825 2024年2月27日閲覧。.
- ^ Brown TA (2002). “Section 2, Chapter 6: 6.1. The Methodology for DNA Sequencing”. Genomes 2 (2nd ed.). Oxford: Bios. ISBN 978-1-85996-228-2
- ^ Brown (2002年). “Section 2, Chapter 6: 6.2. Assembly of a Contiguous DNA Sequence”. 2007年2月8日時点のオリジナルよりアーカイブ。2024年8月9日閲覧。
- ^ Service RF (March 2006). “Gene sequencing. The race for the $1000 genome”. Science 311 (5767): 1544–1546. doi:10.1126/science.311.5767.1544. PMID 16543431.
- ^ Hall N (May 2007). “Advanced sequencing technologies and their wider impact in microbiology”. The Journal of Experimental Biology 210 (Pt 9): 1518–1525. doi:10.1242/jeb.001370. PMID 17449817.
- ^ Church GM (January 2006). “Genomes for all”. Scientific American 294 (1): 46–54. Bibcode: 2006SciAm.294a..46C. doi:10.1038/scientificamerican0106-46. PMID 16468433.(
 要購読契約)
要購読契約)
- ^ Wade N (19 March 2015). “Scientists Seek Ban on Method of Editing the Human Genome”. The New York Times. オリジナルの19 March 2015時点におけるアーカイブ。 20 March 2015閲覧。
- ^ Pollack A (3 March 2015). “A Powerful New Way to Edit DNA”. The New York Times. オリジナルの26 March 2015時点におけるアーカイブ。 20 March 2015閲覧。
- ^ Baltimore D, Berg P, Botchan M, Carroll D, Charo RA, Church G, Corn JE, Daley GQ, Doudna JA, Fenner M, Greely HT, Jinek M, Martin GS, Penhoet E, Puck J, Sternberg SH, Weissman JS, Yamamoto KR (April 2015). “Biotechnology. A prudent path forward for genomic engineering and germline gene modification”. Science 348 (6230): 36–38. Bibcode: 2015Sci...348...36B. doi:10.1126/science.aab1028. PMC 4394183. PMID 25791083.
- ^ Lanphier E, Urnov F, Haecker SE, Werner M, Smolenski J (March 2015). “Don't edit the human germ line”. Nature 519 (7544): 410–411. Bibcode: 2015Natur.519..410L. doi:10.1038/519410a. PMID 25810189.
- ^ Kolata G (23 April 2015). “Chinese Scientists Edit Genes of Human Embryos, Raising Concerns”. The New York Times. オリジナルの24 April 2015時点におけるアーカイブ。 24 April 2015閲覧。
- ^ Liang P, Xu Y, Zhang X, Ding C, Huang R, Zhang Z, Lv J, Xie X, Chen Y, Li Y, Sun Y, Bai Y, Songyang Z, Ma W, Zhou C, Huang J (May 2015). “CRISPR/Cas9-mediated gene editing in human tripronuclear zygotes”. Protein & Cell 6 (5): 363–372. doi:10.1007/s13238-015-0153-5. PMC 4417674. PMID 25894090.
推薦文献
日本語:
- Daniel L. Hartl 著、中村千春, 岡田清孝 訳『エッセンシャル遺伝学・ゲノム科学(原著第7版)』化学同人、2021年。ISBN 978-4759820485。
- Alberts, Johnson, Lewis, Raff, Roberts, Walter 著、中村桂子, 松原謙一 監訳 訳『細胞の分子生物学 第6版』ニュートンプレス、2017年。ISBN 978-4315520620。
- H. Lodish ほか 著、田利明, 須藤和夫, 山本啓一 訳『分子細胞生物学 第9版』東京化学同人、2023年7月31日。ISBN 978-4807920518。
英語:
- Alberts B, Bray D, Hopkin K, Johnson A, Lewis J, Raff M, Roberts K, Walter P (2013). Essential Cell Biology, 4th Edition. Garland Science. ISBN 978-1-317-80627-1
- An Introduction to Genetic Analysis (7th ed.). New York: W. H. Freeman. (2000). ISBN 978-0-7167-3520-5
- Hartl D, Jones E (2005). Genetics: Analysis of Genes and Genomes (6th ed.). Jones & Bartlett. ISBN 978-0-7637-1511-3
- King RC, Mulligan PK, Stansfield WD (2013). A Dictionary of Genetics (8th ed.). New York: Oxford University Press. ISBN 978-0-19-976644-4
- Lodish H, Berk A, Zipursky LS, Matsudaira P, Baltimore D, Darnell J (2000). Molecular Cell Biology (4th ed.). New York: Scientific American Books. ISBN 978-0-7167-3136-8
関連項目
- 細菌ゲノム - 細菌のゲノム研究に関する話題
- 動物遺伝資源の凍結保存 - 家畜の遺伝子を保護・保存するための、域外保全戦略
- 優生学 - ヒトの遺伝的素質の改善を目指す取り組み
- 発生学 - 配偶子、胚および胎児の成長を研究する生物学の一分野
- 遺伝子疾患 - ゲノムの異常によって引き起こされる健康上の問題
- 遺伝的多様性 - ある生物種の遺伝子構成に含まれる遺伝的特性の総数
- 遺伝子工学 - 技術を用いて生物の遺伝子を改変・操作すること
- ヒトの遺伝子強化 - 遺伝子改変によるヒトの能力強化
- 細胞生物学および分子生物学の用語集 - 細胞生物学、分子生物学、分子遺伝学、生化学、微生物学などの研究で用いられる用語や概念のまとめ
- 遺伝学関連記事の索引
- 遺伝医学 - 遺伝性疾患の診断と管理を行う医学の一分野
- 核酸法 - DNAやRNAのような核酸を研究するための技術
- 神経エピジェネティクス - 遺伝子のエピジェネティックな変化が神経系に及ぼす影響を研究する学問
- 遺伝学のあらまし - 遺伝学に関連する記事の一覧 (英語)
- 遺伝学の歴史年表 - 1850年代~ゲノム時代までの遺伝学の出来事
- 植物遺伝資源 - 人為的および自然選択の結果として主に農作物に生じた遺伝的変異


