核酸
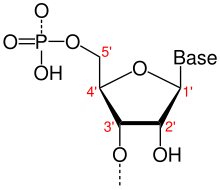
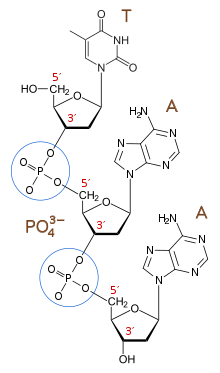

核酸(かくさん、英: nucleic acid)は、リボ核酸 (RNA)とデオキシリボ核酸 (DNA)の総称で、塩基と糖、リン酸からなるヌクレオチドがホスホジエステル結合で連なった生体高分子である。糖の部分がリボースであるものがRNA、リボースの2'位の水酸基が水素基に置換された2-デオキシリボースであるものがDNAである。RNAは2'位が水酸基であるため、加水分解を受けることにより、DNAよりも反応性が高く、熱力学的に不安定である。糖の 1'位には塩基(核酸塩基)が結合している。さらに糖の 3'位と隣の糖の 5'位はリン酸エステル構造で結合しており、その結合が繰り返されて長い鎖状になる。転写や翻訳は 5'位から 3'位への方向へ進む。
なお、糖鎖の両端のうち、5'にリン酸が結合して切れている側のほうを 5'末端、反対側を 3'末端と呼んで区別する。また、隣り合う核酸上の領域の、5'側を上流、3'側を下流という。
構造
[編集]一次構造
[編集]核酸の一次構造とは、(デオキシ)ヌクレオシド成分がホスホジエステル結合によって、連続的に連結され、枝分かれのない、ポリヌクレオチド(ヌクレオチドの重合体。核酸と区別して、20程度の短いものを指すことがある)鎖を形成させるような(デオキシ)ヌクレオシド配列である。
二次構造
[編集]核酸の二次構造とは、一本鎖の主にホモポリヌクレオチド(塩基成分が同一のヌクレオチド重合体)の場合には、塩基間の相互作用によって規定されるヌクレオシド成分の空間的配置をさす。2本の相補鎖の場合には、同一の鎖の隣接塩基間の相互作用と、互いに平行している鎖の対向塩基間の水素結合により安定化された規則的な二重螺旋(DNAには三重、四重螺旋も存在する)を意味する。
三次構造
[編集]核酸の三次構造は、固定化された二重螺旋とそれ以外のタイプの配列で形成される。
四次構造
[編集]核酸の四次構造は、リボソームやヌクレオソームのような核蛋白質と相互作用している高分子の空間的配置を意味する。特に、ポリヌクレオチドとポリペプチドの相互依存による高分子構造を指す。
核酸塩基
[編集]核酸塩基 (nucleobase) は核酸 (DNA, RNA) を構成する塩基成分で、主なものにアデニン、グアニン、シトシン、チミン、ウラシルがあり、それぞれ A, G, C, T, U と略す。構造の骨格からプリン塩基 (A, G) とピリミジン塩基 (C, T, U) とに分けられる。
| 塩基 | 略号 | 分類 | 構造式 | DNA or RNA |
ヌクレオシド | リボヌクレオチド | デオキシリボヌクレオチド |
|---|---|---|---|---|---|---|---|
| アデニン | A | プリン塩基 | 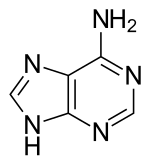
|
DNA and RNA |
アデノシン | アデノシン一リン酸 (AMP) アデノシン二リン酸 (ADP) アデノシン三リン酸 (ATP) |
デオキシアデノシン一リン酸 (dAMP) デオキシアデノシン二リン酸 (dADP) デオキシアデノシン三リン酸 (dATP) |
| グアニン | G | 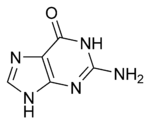
|
グアノシン | グアノシン一リン酸 (GMP) グアノシン二リン酸 (GDP) グアノシン三リン酸 (GTP) |
デオキシグアノシン一リン酸 (dGMP) デオキシグアノシン二リン酸 (dGDP) デオキシグアノシン三リン酸 (dGTP) | ||
| チミン | T | ピリミジン塩基 | 
|
DNA | チミジン または 5-メチルウリジン |
5-メチルウリジン一リン酸 (TMP) 5-メチルウリジン二リン酸 (TDP) 5-メチルウリジン三リン酸 (TTP) |
チミジン一リン酸 (dTMP) チミジン二リン酸 (dTDP) チミジン三リン酸 (dTTP) |
| シトシン | C | 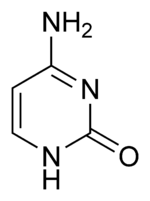
|
DNA and RNA |
シチジン | シチジン一リン酸 (CMP) シチジン二リン酸 (CDP) シチジン三リン酸 (CTP) |
デオキシシチジン一リン酸 (dCMP) デオキシシチジン二リン酸 (dCDP) デオキシシチジン三リン酸 (dCTP) | |
| ウラシル | U | 
|
RNA | ウリジン | ウリジン一リン酸 (UMP) ウリジン二リン酸 (UDP) ウリジン三リン酸 (UTP) |
デオキシウリジン一リン酸 (dUMP) デオキシウリジン二リン酸 (dUDP) デオキシウリジン三リン酸 (dUTP) |
核酸やヌクレオチドの構成単位(の繰り返し数)として、たとえば、10塩基(1本鎖の場合)または10塩基対(2重鎖の場合)などと便宜的に用いる。
塩基対における水素結合
[編集]| 略号 | 塩基(略称の由来) |
|---|---|
| A | アデニン (Adenine) |
| T | チミン (Thymine) |
| G | グアニン (Guanine) |
| C | シトシン (Cytosine) |
| U | ウラシル (Uracil) |
| R | プリン (puRine) |
| Y | ピリミジン (pYrimidine) |
| M | A あるいは C (aMino) |
| K | G あるいは T (Keto) |
| S | G あるいは C (G と C の結合は強い (Strong)) |
| W | A あるいは T (A と T の結合は弱い (Weak)) |
| B | G あるいは T あるいは C (A の次は B) |
| H | A あるいは T あるいは C (G の次は H) |
| V | A あるいは G あるいは C (TU の次は V) |
| D | A あるいは G あるいは T (C の次は D) |
| N | AGTCのどれか (aNy) |
DNAの場合、アデニン (A) とチミン (T)、グアニン (G) とシトシン (C) は水素結合を形成する。AT対が二つの水素結合を形成するのに対し、GC対は三つの水素結合を形成する。そのため、GC含有量が大きい領域では安定性が高まる。略号の A + T が Weak の頭文字W、G + C が Strong の頭文字Sとなっているわけである。
一方、RNAは、アデニン (A) とウラシル (U)、グアニン (G) とシトシン (C) で塩基対を形成する。塩基としてチミンではなくウラシルで構成されるが、ウラシルもチミン同様ピリミジン骨格であり、アデニンと塩基対を形成する。ウラシルは、チミンのメチル基が水素基に置換された塩基である。
比較的広範囲で使われている略号を示した。分野によってはこれと異なった略号を用いることもある(修飾塩基など)。また、塩基とヌクレオシドを区別したい場合は三文字の略号を使う場合もある。
化学的性質
[編集]変性
[編集]核酸や蛋白質などの巨大分子に起こる現象の一つで、一般的に二次以上の構造に関係している非共有結合交互作用の破壊を指し、核酸の場合では二本鎖から一本鎖の変換を意味し、[注 1]慣用的に融解といわれる。変性の化学的外因は紫外線、熱、加圧、攪拌、酸・塩基、溶媒のイオンなどである。これらのような刺激を与え続ければ、核酸の螺旋構造(以下、単に螺旋構造といえば二重螺旋の二次構造を指し、螺旋分子といえばその構造を持った核酸分子を意味する)は解けてゆき、最終的には平行していた鎖が完全に解離し、一本鎖となるだろう。この遷移の所要時間をその螺旋構造の安定性といえる。鎖の解離は対向塩基間の水素結合の切断によって進行するが、G/C塩基対の3本の結合より、A/T塩基対の2本の塩基対の破壊が容易であることは明らかである。スタッキング相互作用も安定性に関わるが、それはの項で詳述する。
また、溶液のイオン強度にも影響を受ける。螺旋分子の主鎖には負電荷を持つリン酸基があり、2本の鎖上のこれらの負電荷は互いに近くにあるので、遮蔽されていなければ鎖同士を反発させようとし、分離を促す。イオン濃度が高いと、陽イオンによって負電荷を遮断し、螺旋は安定化される。
G/C含量が増えるたびに、また溶液のイオン強度が強くなるたびに、変性にかかる時間は増加する。溶液のイオン濃度(他に温度、pHなども)を一定に保てばこの時間は塩基組成に依存するので、測定により、その螺旋構造の安定性を定量化することができる。安定性の指標として主に、温度、pH、塩基組成からの計算などがあり、それぞれ、Tm、pHm、と表す。以下にそれぞれの詳細を記述する。
融解温度という。螺旋分子溶液を徐々に加熱すると、そのポリヌクレオチドに特異的な一定の温度範囲内で、その溶液の性質が急変する。温度の増加に伴う種種の性質の変化は螺旋構造の崩壊の進行に比例する。加熱前の螺旋分子の温度と、変性完了の瞬間の温度の、中間の温度が融解温度なのである。熱変性には旋光度や粘度の減少、沈降定数の増大などを伴うが、この遷移の経過の検出に最も広く用いられる変化は吸光度の増加である。そこで、吸光度の観測実験を例に取り上げ、Tmの具体的な説明をする。
種種の螺旋分子の溶液を加熱したときの吸光度の変化を観察すると、明らかに狭い温度範囲で吸光度の増加が起こり、ある温度から再び吸光度は一定になる、という特徴が見られる。上昇が止まった吸光度は二次構造の完全な崩壊を意味するので、遷移の途中での螺旋部分の割合(θ)と、非螺旋部分の割合(1-θ)は次の式で求められる。
ここでD∞, Dt, D0は、完全に変性した分子の吸光度、ある中間温度でのポリヌクレオチド溶液の吸光度、低温でのポリヌクレオチドの吸光度である。 上で「変性完了の瞬間の温度の、中間の温度が融解温度」と述べたが、この式から表現すると、融解温度とは「螺旋部分の割合と非螺旋部分の割合が等しくなる(θ = 1 - θ = 0.5)温度」である。
Tmの値は、一定の外部条件化では一定であり、ためにその構造のみで規定される螺旋分子の安定性を指標することができる。
pHm
[編集]pHmは、上昇前のpHと、変性の完了の瞬間のpHの、中間のpHの値である。定義については上のTmで、温度をpH、TmをpHmを代入したものと同様であるので、pHm について特に解説することはない。以下に、両者の変性過程に共通して関わることを述べる。
螺旋分子の変性の遷移過程の特徴として、nativeの状態から変性状態へ遷移するときの遷移間隔の幅(⊿Tm、⊿pHm)があげられる。螺旋分子の変性過程を、上で示した吸光度の観測実験のように解析した結果において、1-θ曲線に対する点での接点が、直線1-θ=1(全変性)、および1-θ=0(未変性)と交差する温度の差から求められる。これは遷移の協力性[注 2]、すなわち温度(pH)の上昇に伴う螺旋構造の要素のすべてが崩壊する同時性の度合いを反映する。螺旋構造がある温度で同時に消失するとき、⊿Tm(⊿pHm) = 0となる。DNAは決してそのような融解はしない。
今まで二重螺旋のことばかり扱ってきたが、核酸には一重や、三重、四重螺旋も存在し、また部分的に二重螺旋を持つ三次構造も存在する。それらと比べ、単一の種類の螺旋分子の未変性温度およびpHは極めて低く、また⊿Tmは特徴的に低い(3〜7℃)ので、他の構造とほとんど区別できる。
- Δ G37°
[編集]構造安定エネルギーという。上で示した通り、螺旋構造の安定性はG/C含量に依存することを述べたが、実はそれだけでなく、スタッキング相互作用も関与している。水素結合は螺旋の軸に垂直に、スタッキング相互作用はほぼ平行に形成されるため、両者の、安定性への寄与を分けて考えることが可能である。は37度における構造形成の自由エネルギーを意味し、は水素結合とスタッキング相互作用の両者の寄与から予想された、安定性の指標の一つである。
この指標はI. Tinocoら[注 3]が1971年に最塩基対モデルとして提案され、このモデルは「核酸の塩基対形成に関して最も影響を与えるのは既に生成している隣の塩基対である」という考えを基本にしている。なぜなら、水素結合の強度は1塩基対における二つの塩基の組み合わせに決定され、スタッキング相互作用は距離の6乗に反比例するので、ある塩基対と隣接塩基対のさらに隣の塩基対との間に働く力は無視できると考えられるためである。すなわち、螺旋構造の安定性は、隣接する塩基対の足し合わせによって求められると考えられた。
螺旋構造において可能な最近接塩基対の組は、DNA/DNAおよびRNA/RNAで10種類、DNA/RNAで16種類である。[2]
- DNA/DNA二重螺旋
DNA DNA DNA DNA
- RNA/RNA二重螺旋
RNA RNA RNA RNA
- RNA/DNA二重螺旋
RNA DNA RNA DNA
もし螺旋構造の安定性がこのモデルに従えば、異なる塩基配列を持つ螺旋分子同士でも、同じ最近接塩基対の組成を持つのなら安定性は等しい。最近接塩基対モデルから、上図に示した最近接塩基対の組の構造安定エネルギーの実験的測定の網羅から、構造安定性は解読されている。
存在
[編集]ほぼすべての生物に含まれていると考えられる。重量比では、酵母(Baker's yeast/Saccharomyces cerevisiae)、海苔(Purple laver)、白子(鮭)、牡蠣、大豆、肝臓(豚)などでの検出値が高い。[3]
注釈
[編集]- ^ 蛋白質の変性については変性#変性(生体高分子)参照
- ^ КООПБРАТИВНОСТЬの暫定的和訳。英語ではcooperativeness
- ^ I. Tinoco, Jr., O. C. Uhlenbeck, M. D. Levine
出典
[編集]- ^ N. K. カチェトコフ/E. I. ブドフスキー 編、橋爪たけし 監訳「核酸の有機化学 上」 1974年 講談社出版
- ^ 下の図のアイディアは杉本直己「遺伝子化学」2002年 p36 に書かれている図3.9から流用
- ^ “Nucleic Acid Contents of Japanese Foods”. NIPPON SHOKUHIN KOGYO GAKKAISHI 36 (11): Table 2. (1989). doi:10.3136/nskkk1962.36.11_934.



























