クロマチン
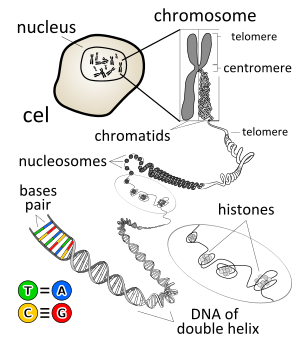
クロマチン(chromatin)は、真核細胞内に存在するDNAとタンパク質からなる構造である。日本語では染色質と訳される。
定義
[編集]クロマチンとは、元来『細胞核内の染色されやすい物質』を指す語として、ヴァルター・フレミング(Walther Flemming)によって初めて導入された[1]。クロマチンと共によく使われる語に染色体(chromosome)があるが、染色体とは元来、有糸分裂期の細胞においてクロマチンが構造変換して作り出される棒状の構造体を指す。このように原義をたどると、chromatinが不可算名詞であるのに対してchromosomeが可算名詞であることは理解しやすい。
その後の研究の発展と共にクロマチンという語のもつ意味合いは変わってきた。クロマチンに含まれるDNAが遺伝情報の担体であると認識されてからは、その貯蔵形態としての役割が強調されてきたが、最近では、遺伝子の発現・複製・分離・修復等、DNAが関わるあらゆる機能の制御に積極的な役割を果たしていると考えられるようになってきた。
クロマチンの構造
[編集]
ヌクレオソーム構造
[編集]ヒト二倍体細胞に納められているDNAの総延長はおよそ2 mに達する。これを直径約10 μmの核に収納するための構造がクロマチンである。クロマチンを構築するうえで最も基本となる構造が、ヌクレオソーム(nucleosome)である。まず、4種類のコアヒストン(H2A、H2B、H3、H4)が2コピーずつ集まって八量体(オクタマー)を形成し、その周りを約146bpのコアDNAが約1.65回左巻きに巻きつく(ヒストンおよびDNA超らせんの項参照)。この構造はヌクレオソームコア粒子(core particle)と呼ばれる。2つのヌクレオソーム(コア粒子)の間を繋ぐDNAがリンカーDNA(linker DNA)、そこに結合するヒストンがリンカーヒストンである。多数のヌクレオソームがリンカーDNAを介してアレイ状につながった構造を電子顕微鏡で観察すると、いわゆる beads-on-a-string 状の形態が観察される。この構造は、その直径から10 nm ファイバー(10 nm fiber)と呼ばれる。また、ヌクレオソーム・リンカーDNA・リンカーヒストンの複合体をひとつのユニットとしてクロマトソーム(chromatosome)と呼ぶことがある。
30 nm ファイバー構造
[編集]
ヌクレオソーム繊維(10 nm ファイバー)はさらに折り畳まれ、直径約30 nmの30 nm ファイバー(30 nm fiber)を形成する。30 nm ファイバーの折り畳みについては、ソレノイドモデル(solenoid model)、ジグザグモデル(zig-zag model)等のモデルが提出されているが、いまだ定説はない[2]。最近では、規則的に折り畳まれた30 nm ファイバーの存在そのものにも疑念が提出されている[3]。
高次クロマチン構造
[編集]さらに巨視的に眺めた場合、クロマチンは凝集の度合いによりヘテロクロマチン(heterochromatin)とユークロマチン(euchromatin)に分類される。遺伝子密度が低い領域や遺伝子発現が抑制されている領域は、強く折り畳まれてヘテロクロマチンを形成する傾向にある。一方、遺伝子の転写が活発な領域のクロマチンは比較的緩んでおり、ユークロマチンと呼ばれる。細胞分裂期にはいると、クロマチンは組織的に折り畳まれて、よりコンパクトな棒状の構造体(すなわち染色体)に変換される。この過程は染色体凝縮と呼ばれ、姉妹染色分体を正確に分離するために重要な過程である。
遺伝子発現におけるクロマチンの役割
[編集]クロマチン構造は遺伝子発現の調節に関与している。
例えば、遺伝子の発現・抑制を制御する機構のひとつとしてヒストンの翻訳後修飾が知られている。ヒストンは強い塩基性のタンパク質であり、酸性のDNAとの高い親和性を示す。それぞれのコアヒストンは球形のカルボキシル末端と、決まった構造をとらないアミノ末端(ヒストンテール)から構成されている。ヒストンテールはアセチル化、メチル化、リン酸化、ユビキチン化といった様々な化学修飾を受けることにより、遺伝子発現など様々なクロマチン機能の制御に関わる(ヒストンの項参照)。複数の修飾の組み合わせがそれぞれ特異的な機能を引き出すという仮説は、ヒストンコード仮説と呼ばれている[4]。
一方、ATP依存的にヌクレオソーム構造を変化させる活性が知られており、この活性を担うタンパク質複合体は、クロマチン・リモデリング複合体(chromatin remodeling complexes)あるいはヌクレオソーム・リモデリング複合体(nucleosome remodeling complexes)と呼ばれる。クロマチン・リモデリング複合体はヒストン修飾酵素と協調して、クロマチンのダイナミックな構造変換とそれに伴う機能制御に関わる。
クロマチン研究の歴史
[編集]- 1882年、ドイツの細胞学者フレミング (Walther Flemming)が、特異的な染料によって染められる細胞核内の構成要素を示す用語として、クロマチンという言葉を提案した[1]。
- 1974年、オリンズら (Ada & Donald Olins) は、電子顕微鏡を用いクロマチンのビーズ状構造を初めて可視化した[5]。
- 1974年、コーンバーグ(Roger Kornberg)は、X線回折、生化学、ヌクレアーゼ消化実験の結果をもとに、ヒストンとDNAから構成されるクロマチンの繰り返し構造のモデルを提出した[6]。
- 1975年、シャンボン (Pierre Chambon) らにより、この繰り返しのユニットを表す用語として、ヌクレオソームという言葉が提案された[7]。
- 1976年、クルーグ (Aaron Klug) らは、電子顕微鏡観察をもとにして、30 nmファイバーのソレノイドモデルを提出した[8]。
- 1997年、リッチモンド (Timothy Richmond) らは、ヌクレオソームの結晶構造を2.8オングストロームの解像度で決定した[9]。
- 1990年半ば以降、ヌクレオソームをダイナミックに変化させる活性(クロマチン・リモデリング活性)[10]やヒストンを修飾する活性[11][12]が相次いで発見され、クロマチン構造の機能的な重要性が再認識されるようになった(ヒストンの項参照)。
関連項目
[編集]引用文献
[編集]- ^ a b Flemming, W (1882). Zellsubstantz, Kern und Zelltheilung. F.C.W. Vogel, Leipzig, Germany.
- ^ Bian Q, Belmont AS (2012). “Revisiting higher-order and large-scale chromatin organization”. Curr. Opin. Cell Biol. 24: 359-366. PMID 22459407.
- ^ Joti Y, Hikima T, Nishino Y, Kamada F, Hihara S, Takata H, Ishikawa T, Maeshima K (2012). “Chromosomes without a 30-nm chromatin fiber”. Nucleus 3: 404-410. PMID 22825571.
- ^ Strahl BD, Allis CD (2000). “The language of covalent histone modifications”. Nature 403: 41-45. PMID 10638745.
- ^ Olins AL, Olins DE (1974). “Spheroid chromatin units (v bodies)”. Science 183: 330-332. PMID 4128918.
- ^ Kornberg RD (1974). “Chromatin structure: a repeating unit of histones and DNA”. Science 184: 868-871. PMID 4825889.
- ^ Oudet P, Gross-Bellard M, Chambon P (1975). “Electron microscopic and biochemical evidence that chromatin structure is a repeating unit”. Cell 4: 281-300. PMID 1122558.
- ^ Finch JT, Klug A (1975). “Solenoidal model for superstructure in chromatin”. Proc Natl Acad Sci USA 73: 1897-1901. PMID 1064861.
- ^ Luger K, Mäder AW, Richmond RK, Sargent DF, Richmond TJ (1997). “Crystal structure of the nucleosome core particle at 2.8 A resolution”. Nature 389: 251-260. PMID 9305837.
- ^ Tsukiyama T, Becker PB, Wu C (1994). “ATP-dependent nucleosome disruption at a heat-shock promoter mediated by binding of GAGA transcription factor”. Nature 367: 525-532. PMID 8107823.
- ^ Brownell JE, Zhou J, Ranalli T, Kobayashi R, Edmondson DG, Roth SY, Allis CD (1996). “Tetrahymena histone acetyltransferase A: a homolog to yeast Gcn5p linking histone acetylation to gene activation”. Cell 84: 843-851. PMID 8601308.
- ^ Taunton J, Hassig CA, Schreiber SL (1996). “A mammalian histone deacetylase related to the yeast transcriptional regulator Rpd3p”. Science 272: 408-411. PMID 8602529.
参考図書
[編集]- J. Watson他 著(中村桂子 監訳)『遺伝子の分子生物学 第6版』東京電機大学出版局、2010年。
- B. Alberts他 著(中村桂子・松原謙一 監訳)『細胞の分子生物学 第6版』ニュートンプレス、2017年。
- B. Alberts他 著(中村桂子・松原謙一 監訳)『Essential 細胞生物学 原書第4版』南江堂、2016年。
- 平岡泰・原口徳子 編『染色体と細胞核のダイナミクス』化学同人、2013年。
- 平野達也・胡桃坂仁志 編(実験医学増刊号)『教科書を書き換えろ!染色体の新常識』羊土社、2018年。
