クロマチンリモデリング
クロマチンリモデリング(英: chromatin remodeling)は、クロマチン構造の動的な調節である。クロマチンリモデリングは凝縮したゲノムDNAに対する転写調節装置のタンパク質のアクセスを可能にし、遺伝子発現の制御が行われる。こうしたリモデリングは主に、(1) 特異的酵素による共有結合的なヒストン修飾(ヒストンアセチル化酵素、脱アセチル化酵素、メチル化酵素、キナーゼなどによるもの)、(2) ヌクレオソームを動かしたり、除去したり、再構築したりするATP依存的なクロマチン構造のリモデリング、によって行われる[1]。クロマチン構造の動的なリモデリングは、遺伝子発現の活発な調節の他にも、卵細胞のDNA複製や修復、アポトーシス、染色体分離、発生や多能性など、いくつかの重要な生物学的過程のエピジェネティックな調節を可能にする。クロマチンリモデリングタンパク質の異常は、がんを含むヒトの疾患と関係していることが判明している。いくつかのがんに対しては、クロマチンリモデリング経路を標的とした治療戦略の進化が続いている。
概要
[編集]ゲノムの転写調節は主に転写開始前の段階、DNAのコアプロモーター配列へのコア転写装置(すなわちRNAポリメラーゼ、転写因子、アクチベーターとリプレッサー)の結合の制御によって行われている。しかし、核内のDNAはしっかりとパッケージングされており、主にヒストンタンパク質の助けによってヌクレオソームの反復単位が形成され、それらがさらに束ねられて凝縮したクロマチン構造が形成されている。こうした凝縮構造は多くのDNA調節タンパク質を排除し、転写装置との相互作用や遺伝子発現の調節はできない状態となっている。クロマチンリモデリングと呼ばれる過程は、この問題を克服して凝縮DNAに対して動的なアクセスを行うことを目的として行われ、ヌクレオソーム構造を変化させて転写調節のためのDNA領域を露出させたり隠したりする。
定義として、クロマチンリモデリングはヌクレオソームDNAへのアクセスを促進する酵素的過程であり、ヌクレオソームの構造、構成、配置のリモデリングが行われる。
分類
[編集]ヌクレオソームDNAへのアクセスは大きく2種類のタンパク質複合体によって行われる。
- 共有結合によってヒストンを修飾する複合体
- ATP依存的なクロマチンリモデリング複合体
共有結合によってヒストンを修飾する複合体
[編集]ヒストン修飾複合体と呼ばれる特異的なタンパク質複合体が、ヒストンに対するさまざまな化学的要素の付加や除去を触媒する。こうした酵素的な修飾にはアセチル化、メチル化、リン酸化、ユビキチン化が含まれ、主に修飾はヒストンのN末端のテール領域に対して行われる。こうした修飾はヒストンとDNAの間の結合親和性に影響を与え、ヒストンに巻き付いている凝縮したDNA構造を緩めたり引き締めたりする。例えば、ヒストンH3とH4の特定のリジン残基のメチル化はヒストン周囲のDNAのさらなる凝縮を引き起こし、転写因子のDNAへの結合を阻害し遺伝子発現を抑制する。反対に、ヒストンのアセチル化はクロマチンの凝縮を緩め、転写因子が結合できるようにDNAを露出させ、遺伝子発現を増加させる[2]。
既知の修飾
[編集]よく知られたヒストン修飾には次のようなものがある[3]。
- メチル化
リジン残基とアルギニン残基の双方がメチル化を受けることが知られている。メチル化リジンはヒストンコードの中で最もよく理解されている標識の1つであり、特定のリジン残基のメチル化状態は遺伝子の発現状態とよく一致する。H3K4とH3K36のメチル化は転写の活性化と相関している一方、H3K4の脱メチル化はゲノム領域のサイレンシングと相関している。H3K9とH3K27のメチル化は転写抑制と相関している[4]。特に、H3K9のトリメチル化は構成的ヘテロクロマチンと高度の相関がみられる[5]。
- アセチル化と脱アセチル化
アセチル化されたヒストンは脱アセチル化ヒストンと同じようにうまくパッキングすることはできないため、クロマチンが「開いた」構造となる傾向がある。
- リン酸化
- ユビキチン化
ヒストン修飾にはさらに多くの種類が存在し、高感度の質量分析によって近年その種類は大きく広がった[6]。
ヒストンコード仮説
[編集]ヒストンコード仮説は、DNAにコードされている遺伝情報の転写が部分的にはヒストンタンパク質、主にその構造をとらない末端部の化学修飾によって調節される、という仮説である。DNAのメチル化などの類似した修飾とともに、エピジェネティックコードの一部を構成する。
多くの研究の蓄積により、こうしたコードはヒストンをメチル化したりアセチル化したりする特定の酵素によって書き込まれ(ライター)、脱メチル化や脱アセチル化活性を持つ他の酵素によって消去され(イレーザー)、そして最終的に特定のドメイン(ブロモドメイン、クロモドメインなど)を介してこうした修飾へリクルートされて結合するタンパク質によって読み取られる(リーダー)ことが示唆されている。これらライター、イレーザー、リーダーによる3つの作用によって、転写調節やDNA損傷修復などに適した局所的環境が確立される[7]。
ヒストンコード仮説の重要なコンセプトは、ヒストン修飾は単にヒストンとDNAの相互作用を安定化したり不安定化したりするのではなく、専用のタンパク質ドメインによって修飾を特異的に認識する他のタンパク質をリクルートするために利用される、という点である。こうしてリクルートされたタンパク質はその後、クロマチン構造を活発に変化させたり、転写を促進したりする。
遺伝子発現に関するヒストンコードの非常に基礎的な概要を下に示す。
| 修飾の種類 | ヒストン | ||||||
|---|---|---|---|---|---|---|---|
| H3K4 | H3K9 | H3K14 | H3K27 | H3K79 | H4K20 | H2BK5 | |
| モノメチル化 | 活性化[8] | 活性化[9] | 活性化[9] | 活性化[9][10] | 活性化[9] | 活性化[9] | |
| ジメチル化 | 抑制[4] | 抑制[4] | 活性化[10] | ||||
| トリメチル化 | 活性化[11] | 抑制[9] | 抑制[9] | 活性化[10]、 抑制[9] |
抑制[4] | ||
| アセチル化 | 活性化[11] | 活性化[11] | |||||
ATP依存性クロマチンリモデリング
[編集]ATP依存性クロマチンリモデリング複合体は、ヌクレオソームを移動させるか、除去するか、再構築するかによって遺伝子発現を調節する。これらのタンパク質複合体は共通したATPアーゼドメインを持っており、ATPの加水分解によるエネルギーによってヌクレオソームをDNAに沿って再配置したり(ヌクレオソームスライディング(nucleosome sliding)とも呼ばれる)、ヒストンを組み立てたり除去したり、ヒストンバリアントの交換を促進したりし、遺伝子の活性化のためにヌクレオソームが存在しないDNA領域を作り出す[12]。いくつかのリモデリング因子はDNAを移動させる活性を持っている[13]。
全てのATP依存性クロマチンリモデリング複合体には、SNF2スーパーファミリーに属するATPアーゼサブユニットが含まれている。これらのタンパク質には2つの主要なグループが存在しており、SWI2/SNF2(SWI/SNF)グループとISWI(imitation SWI)グループとして知られている。近年記載されたものの中には、脱アセチル化活性も示すものもある[14]。
既知のクロマチンリモデリング複合体
[編集]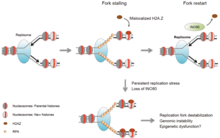
真核生物のクロマチンリモデリング因子には少なくとも5つのファミリー(SWI/SNF、ISWI、Mi-2/NuRD/CHD、INO80、SWR1)が存在し、最初の2つに関しては特に酵母モデルでよく研究が行われている。リモデリング因子には共通したATPアーゼドメインが存在するが、それらはいくつかの生物学的過程(DNA修復、アポトーシスなど)において特異的に機能する。これは各リモデリング因子のATPアーゼ領域には特有のタンパク質ドメイン(ヘリカーゼ、ブロモドメインなど)が存在し、また異なるサブユニットを介してリクルートが行われるためである。
特異的機能
[編集]- いくつかのin vitroでの実験からはISWIリモデリング因子はヌクレオソームを適切な束へと組織化し、ヌクレオソームの均等な配置を作り出すが、SWI/SNFリモデリング因子はヌクレオソーム構造を無秩序化することが示唆されている。
- ISWIファミリーのリモデリング因子はDNA複製後のクロマチンの組み立てとクロマチンの高次構造の維持に中心的な役割を果たすことが示されている。
- INO80ファミリーとSWI/SNFファミリーのリモデリング因子はDNA二本鎖切断修復とヌクレオチド除去修復に関与し、p53を介したDNA損傷応答に重要な役割を果たす。
- Mi-2/NuRD/CHDリモデリング複合体は主に核内での転写抑制を媒介し、胚性幹細胞の多能性の維持に必要である[12]。
意義
[編集]正常な生物学的過程
[編集]クロマチンリモデリングはしっかりとパッケージされたゲノムに対して転写装置の動的なアクセスを可能にし、遺伝子発現調節において中心的な役割を果たしている。さらに、クロマチンリモデリング因子によるヌクレオソームの移動は、染色体の集合と分離、DNAの複製と修復、胚発生と多能性、細胞周期の進行など、いくつかの重要な生物学的過程に必要不可欠である。クロマチンリモデリングの調節異常によって、適切な細胞機能に必要とされるこうした重要なチェックポイントでの転写調節の喪失が引き起こされ、それによってがんを含むさまざまな疾患が引き起こされる。
DNA損傷への応答
[編集]クロマチン構造の緩和は、DNA損傷に対する最初期の細胞応答である[15]。この緩和はPARP1によって開始されるようであり、PARP1のDNA損傷部位への蓄積はDNA損傷の発生後1.6秒以内に最大半値に達する[16]。続いてADPリボース結合ドメインを持つクロマチンリモデリング因子ALC1がPARPの反応産物であるポリADPリボース鎖に迅速に結合する。ALC1のDNA損傷部位へのリクルートは損傷後10秒以内に最大値に達する[15]。ALC1によるものと考えられるクロマチン構造の緩和は10秒以内に最大半値に達する[15]。二本鎖切断部位でのPARP1の作用によって、2つのDNA修復酵素MRE11とNBS1がリクルートされる。これら2つのDNA修復酵素のリクルートは、MRE11に関しては13秒、NBS1に関しては28秒で最大半値に達する[16]。
DNA二本鎖切断の形成後のクロマチン構造の緩和の他の過程には、H2AXのリン酸化型であるγH2AXが関与している。ヒストンバリアントH2AXは、ヒトのクロマチン中のH2Aヒストンの約10%を構成している[17]。γH2AX(セリン139番残基がリン酸化されたH2AX)の蓄積はガンマ線照射による二本鎖切断の形成後20秒で検出され、1分で最大半値に達する[17]。γH2AXを含むクロマチンの範囲はDNA二本鎖切断部位の周辺約 2 Mbpにわたる[17]。
γH2AXはそれ自身がクロマチンの脱凝縮を引き起こすわけではないが、照射後数秒以内にMDC1がγH2AXに特異的に結合する[18][19]。それと同時にRNF8とNBS1が蓄積する。NBS1は、γH2AXに結合したMDC1に結合する[20]。RNF8は、ヌクレオソームリモデリング・ヒストン脱アセチル化複合体NuRDの構成要素であるCHD4との相互作用によって、広範囲のクロマチン脱凝縮を媒介する。二本鎖切断部位へのCHD4の蓄積は迅速であり、照射後40秒以内に最大半値に達する[21]。
DNA損傷に伴う迅速なクロマチン構造の緩和とDNA修復の開始後にはゆっくりと再凝縮が行われ、約20分でクロマチンは損傷前の状態に近い凝縮状態を回復する[15]。
がん
[編集]クロマチンリモデリングは、細胞周期の進行、DNA修復や染色体分離など、細胞の成長と分裂の重要な段階の微調整を行い、それによって腫瘍形成を抑制する機能を発揮する。こうしたクロマチンリモデリング因子の変異やヒストン修飾の調節異常によって、細胞増殖が自己充足的となり、成長調節シグナルによる制御を受けない状態となる可能性がある。これらはがんの2つの重要な特徴である[22]。
- ヒトのSWI/SNFリモデリング複合体の構成要素であるSMARCB1(hSNF5/INI1)を不活性化する変異は、悪性ラブドイド腫瘍の多くでみられ、一般的には小児に影響を与えることが多い[23]。同様の変異は脈絡叢乳頭腫、髄芽腫などの他の小児がんや急性白血病の一部でもみられる。さらに、ノックアウトマウスでの研究もSMARCB1ががん抑制タンパク質であることを強く支持している。ラブトイド腫瘍でSMARCB1の変異が観察されて以降、広範囲の新生物でヒトのSWI/SNFリモデリング複合体の他のサブユニットでも変異が発見されている[24]。
- SWI/SNF型ATPアーゼBRG1(SMARCA4)は、がんで最も高頻度で変異がみられるクロマチンリモデリングATPアーゼである[25]。この遺伝子の変異は、副腎[26]と肺[27]に由来するがん細胞株で初めて発見された。がんにおけるBRG1の変異は、ATPアーゼドメインを標的としたミスセンス変異に対する非常に高い選択性を示す[25][28]。変異は高度に保存されたATPアーゼ配列[29]、すなわちATPポケットやDNA結合面など機能的に重要な表面で多くみられる[28]。これらの変異は優性に作用し、エンハンサー[28]とプロモーター[29]でのクロマチン調節機能を変化させる。
- がん抑制因子であるRbタンパク質はSWI/SNF型酵素BRG1、ヒストン脱アセチル化酵素、DNAメチルトランスフェラーゼをリクルートすることで機能する。BRG1の変異はRbのがん抑制作用の喪失を引き起こすことがいくつかのがんで報告されている[30]。
治療介入
[編集]クロマチンリモデリングの調節異常によって引き起こされるエピジェネティックな不安定性について、乳がん、大腸がん、膵臓がんを含むいくつかのがんで研究が行われている。こうした不安定性は広範囲にわたる遺伝子のサイレンシングを引き起こし、主にがん抑制遺伝子に影響を与える。そのため、ヒストン脱アセチル化酵素阻害剤(HDI)とDNA脱メチル化剤との相乗効果によってエピジェネティックなサイレンシングを克服する戦略がとられている。HDIはいくつかのタイプのがんで主に補助療法として利用されている[31][32]。HDIは、p53のがん抑制活性の調節因子であるp21(WAF1)の発現を誘導する。ヒストン脱アセチル化酵素はRbタンパク質が細胞増殖を抑制する経路に関与している[33]。エストロゲンはエストロゲン受容体α(ERα)に結合し、乳がんの形成と進行への関与することが示唆されている分裂促進因子として良く知られている。近年のデータからは、ヒストン脱アセチル化とDNAメチル化によるクロマチン不活性化がヒトの乳がん細胞におけるERαのサイレンシングの重要な要素であることが示されている[34]。
HDIとして、ボリノスタットとロミデプシンは、アメリカ食品医薬品局(FDA)から皮膚T細胞性リンパ腫(CTCL)の治療に対する承認を受けている[35][36]。ベリノスタット(PXD101)は末梢性T細胞リンパ腫に対し2014年7月にFDAの承認が行われた。パノビノスタット(LBH589)は2015年2月に多発性骨髄腫に対してFDAの迅速承認が行われている[37][38]。バルプロ酸は子宮頸がんと乳がんに対する臨床試験が行われている[39][40]。
ヒストンリジンメチルトランスフェラーゼとアルギニンメチルトランスフェラーゼは新たな薬剤標的の有力な候補である[41]。
他の疾患
[編集]- ATR-X症候群とαサラセミア骨髄異形成症候群(α-thalassemia myelodysplasia syndrome、ATMDS)は、SNF2関連ATPアーゼであるATRXの変異によって引き起こされる。
- 常染色体優性遺伝するCHARGE症候群は、CGDファミリーのATPアーゼCHD7のハプロ不全との関連が近年示されている[42]。
老化
[編集]クロマチン構造のリモデリングは細胞老化の過程への関与が示唆されている。細胞老化は、個体レベルでの老化と関連しているものの異なる過程である。複製老化は恒久的な細胞周期の停止を意味し、有糸分裂を終えた細胞は代謝的に活発な状態で存在し続けるが、増殖することはできない[43][44]。細胞老化は、加齢と関連した疾患、テロメアの短縮、プロジェリア、前がん状態、他の損傷や疾患によっても生じる。老化細胞には明確に抑制的な表現型の変化が生じ、クロマチン構成の変化やリモデリング因子の存在量の変動、エピジェネティックな修飾の変化が生じた損傷細胞やがん性細胞の増殖を防いでいる可能性がある[43][45][46]。老化細胞では、構成的ヘテロクロマチンが核の中心部に移動し、ユークロマチンと条件的ヘテロクロマチンが核の周縁部に移動するという、クロマチン配置の変化が生じる。これによってクロマチンとラミンの間の相互作用が破壊され、活発に有糸分裂を行う細胞で見られるパターンとは反転した配置となる[45][47]。この移動によってラミン結合ドメイン(LAD)とトポロジカルドメイン(TAD)は破壊され、ゲノム間のシスの相互作用に影響が生じる[48]。さらに、全体的に典型的ヒストンが喪失したパターンが生じ、ヌクレオソームでは特にヒストンH3とH4、リンカーヒストンH1が喪失する[47]。老化細胞では2つのエクソンからなるヒストンバリアントがアップレギュレーションされてヌクレオソームの組み立てに変化が生じ、老化状態の確立に必要なpermissiveなクロマチン構造への変化に寄与する[48]。ヒストンバリアントの転写は上昇するが、典型的ヒストンは細胞周期のS期にのみ合成されるため、有糸分裂を終えた老化細胞では発現しない[47]。老化時には、染色体の一部は核から輸送されてリソソームでの分解が行われ、より大きな構成の変化とクロマチン相互作用の破壊が引き起こされる[46]。
クロマチンリモデリング因子の存在量は細胞老化に影響を与える可能性がある。酵母、C. elegans、マウス、ヒトの培養細胞において、NuRD、ACF1、SWI/SNFなどのATP依存性リモデリング因子のノックダウンやノックアウトによってDNA損傷と老化表現型が生じる[46][49][50]。老化細胞ではACF1とNuRDはダウンレギュレーションされており、有糸分裂の維持にはクロマチンリモデリングが必要不可欠であることが示唆される[49][50]。老化シグナル伝達に関与する遺伝子のサイレンシングはクロマチン構造とポリコーム抑制複合体(PRC)とによっても行われており、p16がPRC1/PRC2によってサイレンシングされているのはその1例である[51]。特定のリモデリング因子の欠失は、サイレンシングの維持の喪失によって増殖性の遺伝子の活性化を引き起こす[46]。一部のリモデリング因子は特定の遺伝子座というよりはエンハンサー領域に対して作用し、調節領域周辺に濃密なヘテロクロマチン領域を形成することで細胞周期の再進行を防いでいる[52]。
出典
[編集]- ^ “Predicting nucleosome positions on the DNA: combining intrinsic sequence preferences and remodeler activities”. Nucleic Acids Research 37 (17): 5641–55. (September 2009). doi:10.1093/nar/gkp610. PMC 2761276. PMID 19625488.
- ^ “Chromatin remodeling and cancer, Part I: Covalent histone modifications”. Trends in Molecular Medicine 13 (9): 363–72. (September 2007). doi:10.1016/j.molmed.2007.07.003. PMID 17822958.
- ^ “The language of covalent histone modifications”. Nature 403 (6765): 41–5. (January 2000). Bibcode: 2000Natur.403...41S. doi:10.1038/47412. PMID 10638745.
- ^ a b c d “Determination of enriched histone modifications in non-genic portions of the human genome”. BMC Genomics 10: 143. (March 2009). doi:10.1186/1471-2164-10-143. PMC 2667539. PMID 19335899.
- ^ Hublitz, Philip; Albert, Mareike; Peters, Antoine (28 April 2009). “Mechanisms of Transcriptional Repression by Histone Lysine Methylation”. The International Journal of Developmental Biology 10 (1387): 335–354. ISSN 1696-3547.
- ^ “Identification of 67 histone marks and histone lysine crotonylation as a new type of histone modification”. Cell 146 (6): 1016–28. (September 2011). doi:10.1016/j.cell.2011.08.008. PMC 3176443. PMID 21925322.
- ^ “Translating the histone code”. Science 293 (5532): 1074–80. (August 2001). doi:10.1126/science.1063127. PMID 11498575.
- ^ “Histone H3K4 demethylases are essential in development and differentiation”. Biochemistry and Cell Biology 85 (4): 435–43. (August 2007). doi:10.1139/o07-057. PMID 17713579.
- ^ a b c d e f g h “High-resolution profiling of histone methylations in the human genome”. Cell 129 (4): 823–37. (May 2007). doi:10.1016/j.cell.2007.05.009. PMID 17512414.
- ^ a b c “DOT1L/KMT4 recruitment and H3K79 methylation are ubiquitously coupled with gene transcription in mammalian cells”. Molecular and Cellular Biology 28 (8): 2825–39. (April 2008). doi:10.1128/MCB.02076-07. PMC 2293113. PMID 18285465.
- ^ a b c “The landscape of histone modifications across 1% of the human genome in five human cell lines”. Genome Research 17 (6): 691–707. (June 2007). doi:10.1101/gr.5704207. PMC 1891331. PMID 17567990.
- ^ a b “Chromatin remodeling and cancer, Part II: ATP-dependent chromatin remodeling”. Trends in Molecular Medicine 13 (9): 373–80. (September 2007). doi:10.1016/j.molmed.2007.07.004. PMC 4337864. PMID 17822959.
- ^ “Chromatin remodelling: the industrial revolution of DNA around histones”. Nature Reviews Molecular Cell Biology 7 (6): 437–47. (June 2006). doi:10.1038/nrm1945. PMID 16723979.
- ^ Vignali, M.; Hassan, A. H.; Neely, K. E.; Workman, J. L. (2000-03-15). “ATP-Dependent Chromatin-Remodeling Complexes”. Molecular and Cellular Biology 20 (6): 1899–1910. doi:10.1128/mcb.20.6.1899-1910.2000. ISSN 0270-7306. PMC 110808. PMID 10688638.
- ^ a b c d “The poly(ADP-ribose)-dependent chromatin remodeler Alc1 induces local chromatin relaxation upon DNA damage”. Mol. Biol. Cell 27 (24): 3791–3799. (2016). doi:10.1091/mbc.E16-05-0269. PMC 5170603. PMID 27733626.
- ^ a b “PARP1-dependent kinetics of recruitment of MRE11 and NBS1 proteins to multiple DNA damage sites”. J. Biol. Chem. 283 (2): 1197–208. (2008). doi:10.1074/jbc.M706734200. PMID 18025084.
- ^ a b c “DNA double-stranded breaks induce histone H2AX phosphorylation on serine 139”. J. Biol. Chem. 273 (10): 5858–68. (1998). doi:10.1074/jbc.273.10.5858. PMID 9488723.
- ^ “RNF8 ubiquitylates histones at DNA double-strand breaks and promotes assembly of repair proteins”. Cell 131 (5): 887–900. (2007). doi:10.1016/j.cell.2007.09.040. PMID 18001824.
- ^ “MDC1 directly binds phosphorylated histone H2AX to regulate cellular responses to DNA double-strand breaks”. Cell 123 (7): 1213–26. (2005). doi:10.1016/j.cell.2005.09.038. PMID 16377563.
- ^ “Phospho-dependent interactions between NBS1 and MDC1 mediate chromatin retention of the MRN complex at sites of DNA damage”. EMBO Rep. 9 (8): 795–801. (2008). doi:10.1038/embor.2008.103. PMC 2442910. PMID 18583988.
- ^ “The NuRD chromatin-remodeling complex regulates signaling and repair of DNA damage”. J. Cell Biol. 190 (5): 741–9. (2010). doi:10.1083/jcb.201001048. PMC 2935570. PMID 20805320.
- ^ “The hallmarks of cancer”. Cell 100 (1): 57–70. (January 2000). doi:10.1016/S0092-8674(00)81683-9. PMID 10647931.
- ^ “Truncating mutations of hSNF5/INI1 in aggressive paediatric cancer”. Nature 394 (6689): 203–6. (July 1998). Bibcode: 1998Natur.394..203V. doi:10.1038/28212. PMID 9671307.
- ^ “The spectrum of SWI/SNF mutations, ubiquitous in human cancers”. PLOS ONE 8 (1): e55119. (2013). Bibcode: 2013PLoSO...855119S. doi:10.1371/journal.pone.0055119. PMC 3552954. PMID 23355908.
- ^ a b “The Many Roles of BAF (mSWI/SNF) and PBAF Complexes in Cancer”. Cold Spring Harbor Perspectives in Medicine 6 (8): a026930. (August 2016). doi:10.1101/cshperspect.a026930. PMC 4968166. PMID 27413115.
- ^ “The retinoblastoma protein and BRG1 form a complex and cooperate to induce cell cycle arrest”. Cell 79 (1): 119–30. (October 1994). doi:10.1016/0092-8674(94)90405-7. PMID 7923370.
- ^ “Frequent BRG1/SMARCA4-inactivating mutations in human lung cancer cell lines”. Human Mutation 29 (5): 617–22. (May 2008). doi:10.1002/humu.20730. PMID 18386774.
- ^ a b c “Dominant-negative SMARCA4 mutants alter the accessibility landscape of tissue-unrestricted enhancers”. Nature Structural & Molecular Biology 25 (1): 61–72. (January 2018). doi:10.1038/s41594-017-0007-3. PMC 5909405. PMID 29323272.
- ^ a b “Smarca4 ATPase mutations disrupt direct eviction of PRC1 from chromatin”. Nature Genetics 49 (2): 282–288. (February 2017). doi:10.1038/ng.3735. PMC 5373480. PMID 27941795.
- ^ “Chromatin remodeling: why it is important in cancer”. Oncogene 20 (24): 2988–90. (May 2001). doi:10.1038/sj.onc.1204322. PMID 11420713.
- ^ “Histone deacetylase inhibitors: discovery and development as anticancer agents”. Expert Opinion on Investigational Drugs 14 (12): 1497–511. (December 2005). doi:10.1517/13543784.14.12.1497. PMID 16307490.
- ^ “Histone deacetylase inhibitors: a new class of potential therapeutic agents for cancer treatment”. Clinical Cancer Research 8 (3): 662–4. (2002). PMID 11895892.
- ^ “Histone deacetylase inhibitor selectively induces p21WAF1 expression and gene-associated histone acetylation”. Proceedings of the National Academy of Sciences of the United States of America 97 (18): 10014–9. (August 2000). Bibcode: 2000PNAS...9710014R. doi:10.1073/pnas.180316197. PMC 27656. PMID 10954755.
- ^ “Quantitation of HDAC1 mRNA expression in invasive carcinoma of the breast*”. Breast Cancer Research and Treatment 94 (1): 11–6. (November 2005). doi:10.1007/s10549-005-6001-1. PMID 16172792.
- ^ “Zolinza (vorinostat) dosing, indications, interactions, adverse effects, and more”. reference.medscape.com. 2020年9月20日閲覧。
- ^ “New Drug Approvals - Pt. XXII - Romidepsin (Istodax)”. chembl.blogspot.com. 2020年9月20日閲覧。
- ^ Research, Center for Drug Evaluation and (2020-07-30). “Drug Trials Snapshot: FARYDAK (panobinostat)” (英語). FDA.
- ^ “FDA Approves Panobinostat for Some Patients with Multiple Myeloma - National Cancer Institute” (英語). www.cancer.gov (2015年3月19日). 2020年9月20日閲覧。
- ^ Coronel, Jaime; Cetina, Lucely; Pacheco, Irlanda; Trejo-Becerril, Catalina; González-Fierro, Aurora; de la Cruz-Hernandez, Erick; Perez-Cardenas, Enrique; Taja-Chayeb, Lucia et al. (2011-12). “A double-blind, placebo-controlled, randomized phase III trial of chemotherapy plus epigenetic therapy with hydralazine valproate for advanced cervical cancer. Preliminary results”. Medical Oncology (Northwood, London, England) 28 Suppl 1: S540–546. doi:10.1007/s12032-010-9700-3. ISSN 1559-131X. PMID 20931299.
- ^ Munster, Pamela; Marchion, Douglas; Bicaku, Elona; Lacevic, Mira; Kim, Jongphil; Centeno, Barbara; Daud, Adil; Neuger, Anthony et al. (2009-04-01). “Clinical and biological effects of valproic acid as a histone deacetylase inhibitor on tumor and surrogate tissues: phase I/II trial of valproic acid and epirubicin/FEC”. Clinical Cancer Research: An Official Journal of the American Association for Cancer Research 15 (7): 2488–2496. doi:10.1158/1078-0432.CCR-08-1930. ISSN 1078-0432. PMID 19318486.
- ^ “Toward the development of potent and selective bisubstrate inhibitors of protein arginine methyltransferases”. Bioorganic & Medicinal Chemistry Letters 20 (7): 2103–5. (April 2010). doi:10.1016/j.bmcl.2010.02.069. PMID 20219369.
- ^ “The biology of chromatin remodeling complexes”. Annual Review of Biochemistry 78: 273–304. (2009). doi:10.1146/annurev.biochem.77.062706.153223. PMID 19355820.
- ^ a b Parry, Aled John; Narita, Masashi (2016). “Old cells, new tricks: chromatin structure in senescence”. Mammalian Genome 27 (7–8): 320–331. doi:10.1007/s00335-016-9628-9. ISSN 0938-8990. PMC 4935760. PMID 27021489.
- ^ Hayflick, L.; Moorhead, P. S. (1961-12-01). “The serial cultivation of human diploid cell strains”. Experimental Cell Research 25 (3): 585–621. doi:10.1016/0014-4827(61)90192-6. ISSN 0014-4827. PMID 13905658.
- ^ a b Chandra, Tamir; Ewels, Philip Andrew; Schoenfelder, Stefan; Furlan-Magaril, Mayra; Wingett, Steven William; Kirschner, Kristina; Thuret, Jean-Yves; Andrews, Simon et al. (2015-01-29). “Global Reorganization of the Nuclear Landscape in Senescent Cells”. Cell Reports 10 (4): 471–483. doi:10.1016/j.celrep.2014.12.055. ISSN 2211-1247. PMC 4542308. PMID 25640177.
- ^ a b c d Sun, Luyang; Yu, Ruofan; Dang, Weiwei (2018-04-16). “Chromatin Architectural Changes during Cellular Senescence and Aging”. Genes 9 (4): 211. doi:10.3390/genes9040211. ISSN 2073-4425. PMC 5924553. PMID 29659513.
- ^ a b c Criscione, Steven W.; Teo, Yee Voan; Neretti, Nicola (2016). “The chromatin landscape of cellular senescence”. Trends in Genetics 32 (11): 751–761. doi:10.1016/j.tig.2016.09.005. ISSN 0168-9525. PMC 5235059. PMID 27692431.
- ^ a b Yang, Na; Sen, Payel (2018-11-03). “The senescent cell epigenome”. Aging (Albany NY) 10 (11): 3590–3609. doi:10.18632/aging.101617. ISSN 1945-4589. PMC 6286853. PMID 30391936.
- ^ a b Basta, Jeannine; Rauchman, Michael (2015). “The Nucleosome Remodeling and Deacetylase (NuRD) Complex in Development and Disease”. Translational Research 165 (1): 36–47. doi:10.1016/j.trsl.2014.05.003. ISSN 1931-5244. PMC 4793962. PMID 24880148.
- ^ a b Li, Xueping; Ding, Dong; Yao, Jun; Zhou, Bin; Shen, Ting; Qi, Yun; Ni, Ting; Wei, Gang (2019-07-15). “Chromatin remodeling factor BAZ1A regulates cellular senescence in both cancer and normal cells”. Life Sciences 229: 225–232. doi:10.1016/j.lfs.2019.05.023. ISSN 1879-0631. PMID 31085244.
- ^ H, Rayess (2012年4月15日). “Cellular senescence and tumor suppressor gene p16” (英語). International journal of cancer. doi:10.1002/ijc.27316. 2020年9月21日閲覧。
- ^ Tasdemir, Nilgun; Banito, Ana; Roe, Jae-Seok; Alonso-Curbelo, Direna; Camiolo, Matthew; Tschaharganeh, Darjus F.; Huang, Chun-Hao; Aksoy, Ozlem et al. (2016). “BRD4 Connects Enhancer Remodeling to Senescence Immune Surveillance”. Cancer Discovery 6 (6): 612–629. doi:10.1158/2159-8290.CD-16-0217. ISSN 2159-8290. PMC 4893996. PMID 27099234.
関連文献
[編集]- “Chromatin modifiers and remodellers: regulators of cellular differentiation”. Nature Reviews Genetics 15 (2): 93–106. (February 2014). doi:10.1038/nrg3607. PMC 3999985. PMID 24366184.
関連項目
[編集]- エピジェネティクス
- ヒストン
- ヌクレオソーム
- クロマチン
- ヒストンアセチル化酵素
- 転写因子
- CAF-1(chromatin assembly factor-1)- クロマチンリモデリングを調整する役割を果たすヒストンシャペロン
- クロマチン再構成複合体
