「抗生物質」の版間の差分
4th protocol (会話 | 投稿記録) 編集の要約なし タグ: 2017年版ソースエディター |
Karasunoko (会話 | 投稿記録) 推敲と加筆 |
||
| (9人の利用者による、間の99版が非表示) | |||
| 1行目: | 1行目: | ||
{{一部転記|抗菌薬|抗生物質|date=2021年9月}} |
|||
[[ファイル:Staphylococcus aureus (AB Test).jpg|200px|right|thumb|[[培地]]上での実験。抗生物質を含むディスクでは、[[黄色ブドウ球菌]]の繁殖が抑制される。菌が繁殖していない円形の部分を'''阻止円'''と呼ぶ。]] |
|||
[[File:Staphylococcus aureus (AB Test).jpg|200px|right|thumb|[[培地]]上での実験。抗生物質を含むディスクでは、[[黄色ブドウ球菌]]の繁殖が抑制される。菌が繁殖していない円形の部分を'''阻止円'''と呼ぶ。]] |
|||
'''抗生物質'''(こうせいぶっしつ、{{lang-en|antibiotics}})とは、[[微生物]]が産生し、ほかの微生物の発育を阻害する[[物質]]と定義される。広義には、微生物が産生したものを化学修飾したり人工的に合成された[[抗菌薬]]、腫瘍細胞のようなほかの微生物以外の[[細胞]]の増殖や機能を阻害する物質を含めることもある<ref name="SeikagakuDic471-3">[[抗生物質#生化学辞典(2版)|生化学辞典第2版]]、p.471【抗生物質】</ref>。通俗的に[[抗ウイルス薬]]と混同されることもあるが誤りである。 |
|||
'''抗生物質'''(こうせいぶっしつ、{{lang-en|antibiotics}})とは、[[微生物]]が産生し、ほかの微生物の発育を阻害する[[物質]]と定義される。広義には、微生物が産生したものを化学修飾したり人工的に合成した[[抗菌薬]]、腫瘍細胞のような微生物以外の[[細胞]]の増殖や機能を阻害する物質を含めることもある<ref name="SeikagakuDic471-3">[[抗生物質#生化学辞典(2版)|生化学辞典第2版]]、p.471【抗生物質】</ref>。また、抗生物質の作用を利用した薬剤を指して'''抗生剤'''と呼ばれることもある。 |
|||
[[アレクサンダー・フレミング]]が[[1928年]]に[[アオカビ]]から見つけた[[ペニシリン]]が世界初の抗生物質である。ペニシリンの発見から実用化までの間には10年もの歳月を要したものの、いったん実用化されたのちは[[ストレプトマイシン]]などの抗生物質を用いた抗菌薬が次々と開発され、人類の医療に革命をもたらした。ペニシリンの開発は20世紀でもっとも偉大な発見のひとつで「奇跡の薬」と呼ばれることがあるのも、このことによる{{R|Spending}}。 |
[[アレクサンダー・フレミング]]が[[1928年]]に[[アオカビ]]から見つけた[[ペニシリン]]が世界初の抗生物質である。ペニシリンの発見から実用化までの間には10年もの歳月を要したものの、いったん実用化されたのちは[[ストレプトマイシン]]などの抗生物質を用いた抗菌薬が次々と開発され、人類の医療に革命をもたらした。ペニシリンの開発は20世紀でもっとも偉大な発見のひとつで「奇跡の薬」と呼ばれることがあるのも、このことによる{{R|Spending}}。 |
||
1990年頃には、天然由来の抗生物質は5,000〜6,000種類があると言われ、約70種類(微量成分を含めると約100種類)が実用に使われている。この他にも半合成抗生物質も80種が利用されている{{R|SeikagakuDic471-3}}。しかし乱用が指摘されており、抗生物質処方の50%以上は不適切であるとOECDは報告している<ref name="Spending">{{Cite|title=Tackling Wasteful Spending on Health|publisher=OECD|date=2017-01|isbn=9789264266599|doi=10.1787/9789264266414-en|loc=Chapt.3}}</ref>。WHOやCDCはガイドラインを作成し、適切な利用を呼び掛けている。厚生労働省も2017年ガイドライン第1版を公開した<ref name="日本ガイドライン1版"/>。[[薬剤耐性|薬剤耐性菌]]を生む問題があり、感染症でもないのに使用することを戒めている<ref name="日本ガイドライン1版"/>。 |
1990年頃には、天然由来の抗生物質は5,000〜6,000種類があると言われ、約70種類(微量成分を含めると約100種類)が実用に使われている。この他にも半合成抗生物質も80種が利用されている{{R|SeikagakuDic471-3}}。しかし乱用が指摘されており、抗生物質処方の50%以上は不適切であるとOECDは報告している<ref name="Spending">{{Cite|title=Tackling Wasteful Spending on Health|publisher=OECD|date=2017-01|isbn=9789264266599|doi=10.1787/9789264266414-en|loc=Chapt.3}}</ref>。WHOやアメリカ合衆国のCDCはガイドラインを作成し、適切な利用を呼び掛けている。日本の厚生労働省も2017年ガイドライン第1版を公開した<ref name="日本ガイドライン1版"/>。[[薬剤耐性|薬剤耐性菌]]を生む問題があり、感染症でもないのに使用することを戒めている<ref name="日本ガイドライン1版"/>。 |
||
== 名称と定義 == |
== 名称と定義 == |
||
[[細菌]]や[[真菌]]などの微生物がある環境に2種類存在する場合に、一方の生育が阻害されることがある。この抑制的な作用を'''抗生'''(antibiosis; '''抗生現象'''・'''抗生作用'''とも<ref>{{Cite journal|和書|author=吉川昌之介|date=1995|title=抗生物質耐性菌の生態学 抗生物質と抗生物質耐性に関する生態学的考察; 変異 ・伝達 ・転移 ・選択|url=http://www.jstage.jst.go.jp/article/microbes1986/10/3/10_3_137/_article|journal=Bulletin of Japanese Society of Microbial Ecology|volume=10|issue=3|pages=141-148|language=|doi=10.1264/microbes1986.10.137|issn=0911-7830}}</ref>)と呼ばれ<ref>{{Cite journal|last=Kong|first=Kok-Fai|last2=Schneper|first2=Lisa|last3=Mathee|first3=Kalai|date=2010-01|title=Beta-lactam antibiotics: from antibiosis to resistance and bacteriology: BETA-LACTAM RESISTANCE|url=https://onlinelibrary.wiley.com/doi/10.1111/j.1600-0463.2009.02563.x|journal=APMIS|volume=118|issue=1|pages=1–36|language=en|doi=10.1111/j.1600-0463.2009.02563.x|pmid=20041868|pmc=PMC2894812}}</ref>、例として[[アオカビ]]による細菌の発育抑制が知られる<ref>{{Cite journal|last=Foster|first=W.|last2=Raoult|first2=A.|date=1974-12|title=Early descriptions of antibiosis|url=https://pubmed.ncbi.nlm.nih.gov/4618289|journal=The Journal of the Royal College of General Practitioners|volume=24|issue=149|pages=889–894|issn=0035-8797|pmid=4618289|pmc=2157443}}</ref>。'''抗生物質''' (antibiotic) は、微生物が産生する物質で抗生作用を持つものを指す用語であり<ref>{{Cite journal|last=Davies|first=Julian|date=2006-07|title=Are antibiotics naturally antibiotics?|url=https://academic.oup.com/jimb/article/33/7/496-499/5992967|journal=Journal of Industrial Microbiology & Biotechnology|volume=33|issue=7|pages=496–499|language=en|doi=10.1007/s10295-006-0112-5|issn=1367-5435}}</ref>、前述したアオカビによる細菌の発育抑制は、[[アレクサンダー・フレミング]]によってアオカビから発見された抗生物質である[[ペニシリン]]によるものである<ref name=":1" />。抗生物質の単語を初めて定義したのは、抗生物質の一種[[ストレプトマイシン]]を発見してノーベル賞を受賞した[[セルマン・ワクスマン]]である。彼は「微生物が産生し、ほかの微生物の発育を阻害する[[物質]]」の名称として抗生物質の単語を定義した<ref name=":7">{{Cite journal|last=Davies|first=Julian|last2=Davies|first2=Dorothy|date=2010-09|title=Origins and Evolution of Antibiotic Resistance|url=https://journals.asm.org/doi/10.1128/MMBR.00016-10|journal=Microbiology and Molecular Biology Reviews|volume=74|issue=3|pages=417–433|language=en|doi=10.1128/MMBR.00016-10|issn=1092-2172|pmid=20805405|pmc=PMC2937522}}</ref>。ただし、この定義は抗生物質のヒトによる利用を前提としたものであり、抗生物質が高い濃度で存在しない自然界において抗生物質は抗生作用を示さないことが知られる<ref name=":7" /><ref>{{Cite journal|last=Davies|first=Julian|date=2006-07|title=Are antibiotics naturally antibiotics?|url=https://academic.oup.com/jimb/article/33/7/496-499/5992967|journal=Journal of Industrial Microbiology & Biotechnology|volume=33|issue=7|pages=496–499|language=en|doi=10.1007/s10295-006-0112-5|issn=1367-5435}}</ref>。一方で、細菌の代謝系を選択的に阻害して宿主の代謝系を阻害しない抗生物質は、細菌感染症の治療薬として使用される<ref>{{Cite book|edition=Sixth edition|title=Molecular biology of the cell|url=https://www.worldcat.org/oclc/887605755|date=2015|location=New York, NY|isbn=978-0-8153-4432-2|oclc=887605755|first=Bruce|last=Alberts|publisher=|chapter=Chapter 23: Pathogens and Infection}}</ref>。2012年の推定によると、これまでに6万-8万種類の微生物に由来する[[天然化合物]]が知られているが、その40%は抗生物質としての機能を有するとされ、その内200-220種程度の物質が微生物に直接由来する抗生物質として治療に用いられてきた<ref>{{Cite journal|last=Bérdy|first=János|date=2012-08|title=Thoughts and facts about antibiotics: Where we are now and where we are heading|url=http://www.nature.com/articles/ja201227|journal=The Journal of Antibiotics|volume=65|issue=8|pages=385–395|language=en|doi=10.1038/ja.2012.27|issn=0021-8820}}</ref>。また、「細菌に対して作用して感染症の治療、予防に使用されている薬剤」の総称として「抗菌薬」 (antibacterial agents) が用いられる他、「抗生物質の抗菌作用を利用した薬剤」を指す通称として「'''抗生剤'''」という用語が使用される。ただし、抗菌薬、抗生物質、抗生剤の3つは細菌に対する作用を示す薬剤の総称として厳密には区別されずに使用されている<ref name="日本ガイドライン1版"/>。 |
|||
antibioticsの単語は、抗生物質の一種[[ストレプトマイシン]]を発見した[[セルマン・ワクスマン]]が1942年の[[アメリカ合衆国|アメリカ]]細菌学会で、二種の[[細菌]]が同じ場所に存在する際に生じる拮抗する現象({{lang-en|antibiosis}})につき報告した際、「微生物が産生し、ほかの微生物の発育を阻害する[[物質]]」の名称として用いたことによる。 |
|||
近年では[[化学合成]]で生産されるものや、天然の[[誘導体]]から半合成されるものもある{{R|SeikagakuDic471-3}}。ワクスマンは微生物によって産生される物質を抗生物質と定義したが、多くのβラクタム系抗菌薬やマクロライド系抗菌薬に代表される、天然物へ人工的に修飾を加えた半合成の抗菌薬も抗生物質と呼ばれる<ref name=":3">{{Cite journal|last=Yoneyama|first=Hiroshi|last2=Katsumata|first2=Ryoichi|date=2006-05-23|title=Antibiotic Resistance in Bacteria and Its Future for Novel Antibiotic Development|url=https://academic.oup.com/bbb/article/70/5/1060-1075/5953912|journal=Bioscience, Biotechnology, and Biochemistry|volume=70|issue=5|pages=1060–1075|language=en|doi=10.1271/bbb.70.1060|issn=0916-8451}}</ref>。また、ピリドンカルボン酸系([[キノロン系]]、[[ニューキノロン系]])や[[サルファ剤]]など、完全に人工的に合成された抗菌性物質は、厳密には抗生物質には含まず「合成抗菌薬」と呼ぶが、抗生物質として扱われることもある<ref name=":7" /><ref name=":3" /><ref name="hiramatsu" />。一方、[[ポリエン系抗真菌薬|ポリエンマクロライド系]]のように細菌ではなく[[真菌]]に毒性を示して真菌感染症の治療に用いられる物質や、[[イベルメクチン]]の基となった物質で抗寄生虫作用を持つ[[アベルメクチン]]、「ほかの微生物」のみならず抗腫瘍活性を持つ[[アクチノマイシン]]、[[ラパマイシン]]のように免疫抑制効果や抗炎症作用を示す物質も微生物に由来する薬剤として利用されている<ref>{{Cite journal|last=Pham|first=Janette V.|last2=Yilma|first2=Mariamawit A.|last3=Feliz|first3=Adriana|last4=Majid|first4=Murtadha T.|last5=Maffetone|first5=Nicholas|last6=Walker|first6=Jorge R.|last7=Kim|first7=Eunji|last8=Cho|first8=Hyo Je|last9=Reynolds|first9=Jared M.|date=2019-06-20|title=A Review of the Microbial Production of Bioactive Natural Products and Biologics|url=https://www.frontiersin.org/article/10.3389/fmicb.2019.01404/full|journal=Frontiers in Microbiology|volume=10|pages=1404|doi=10.3389/fmicb.2019.01404|issn=1664-302X|pmid=31281299|pmc=PMC6596283}}</ref>。 |
|||
近年では[[化学合成]]で生産されるものや、天然の[[誘導体]]から半合成されるものもある{{R|SeikagakuDic471-3}}。ピリドンカルボン酸系([[キノロン系]]、[[ニューキノロン系]])や[[サルファ剤]]など、完全に人工的に合成された抗菌性物質も、一般的に「抗生物質」と呼ばれることが多いが、厳密には「合成抗菌薬」と呼ぶのが正しい。抗菌性の抗生物質、合成抗菌薬をあわせて、広義の[[抗菌薬]]と呼ぶ。 |
|||
なお、アルコールなどの[[消毒薬]] (disinfectant) も微生物を死滅・不活化させる働きを持つが、一般に強い毒性を持つために服用はできず、抗生物質を含めた抗菌薬とは区別される<ref>{{Cite book|和書|title=標準微生物学|author=平松啓一・中込治 編集|edition=10|year=2009|ISBN=978-4-260-00638-5|chapter=第II章 環境と微生物}}</ref>。 |
|||
一方、[[アクチノマイシン]]のように、微生物が産生し、「ほかの微生物」のみならず抗腫瘍活性を持つ抗生物質も存在する。 |
|||
== 分類 == |
== 分類 == |
||
[[File:Antibiotics action ja.svg|サムネイル|各抗生物質が細菌の細胞内におけるどの分子を標的とするか示した模式図]] |
|||
抗生物質の分類は、化学構造からの分類と作用による分類の2つがある{{R|SeikagakuDic471-3}}。 |
|||
抗生物質の分類は、化学構造からの分類と作用による分類の2つがある{{R|SeikagakuDic471-3}}。前者は新しい抗生物質の分類ができず、後者では作用機序が厳密に調べられていない抗生物質が分類できないことがある。従って両者を考慮した分類が理想的とされる<ref>{{Cite book|title=Antimicrobial Drugs|first=Amanda J.|editor2-first=Lionel|editor-last=Mozayani|editor-first=Ashraf|last2=Valentine|first2=Jimmie L.|last=Jenkins|language=en|url=http://link.springer.com/10.1007/978-1-61779-222-9_10|doi=10.1007/978-1-61779-222-9_10|pages=385–411|isbn=978-1-61779-221-2|location=Totowa, NJ|date=2012|publisher=Humana Press|editor2-last=Raymon}}</ref>。 |
|||
化学構造からの分類では、[[β-ラクタム系抗生物質|β-ラクタム系]]、[[アミノグリコシド系抗生物質|アミノグリコシド系]]、[[マクロライド系抗生物質|マクロライド系]]、[[テトラサイクリン系抗生物質|テトラサイクリン系]]、[[ペプチド]]系、[[核酸]]系、[[ポリエン系抗真菌薬|ポリエン系]]などに大別されるが、さらに細かく[[ペニシリン]]系、[[セフェム系]]、[[モノバクタム]]系を加える場合もある<ref name="SeikagakuDic471-3" />。 |
化学構造からの分類では、[[β-ラクタム系抗生物質|β-ラクタム系]]、[[アミノグリコシド系抗生物質|アミノグリコシド系]]、[[マクロライド系抗生物質|マクロライド系]]、[[テトラサイクリン系抗生物質|テトラサイクリン系]]、[[ペプチド]]系、[[核酸]]系、[[ポリエン系抗真菌薬|ポリエン系]]などに大別されるが、さらに細かく[[ペニシリン]]系、[[セフェム系]]、[[モノバクタム]]系を加える場合もある<ref name="SeikagakuDic471-3" />。 |
||
| 20行目: | 22行目: | ||
作用からの分類では、抗細菌性、抗[[カビ]]([[菌類|真菌]])性、抗腫瘍性などに分けられる。用途を重視する場合は、医療用、動物用、農業用などで分類される。作用域から、広範囲・狭域で区分される事もある<ref name="SeikagakuDic471-3" />。[[作用機序]]から、細胞壁作用性などの呼称もある{{R|SeikagakuDic471-3}}。 |
作用からの分類では、抗細菌性、抗[[カビ]]([[菌類|真菌]])性、抗腫瘍性などに分けられる。用途を重視する場合は、医療用、動物用、農業用などで分類される。作用域から、広範囲・狭域で区分される事もある<ref name="SeikagakuDic471-3" />。[[作用機序]]から、細胞壁作用性などの呼称もある{{R|SeikagakuDic471-3}}。 |
||
[[細菌]]に対する作用機序による抗生物質の分類の一例としては、細胞壁合成阻害薬、タンパク質合成阻害薬、核酸合成阻害薬の3つに大きく分けるものがある<ref name=":4">{{Cite journal|last=Kapoor|first=Garima|last2=Saigal|first2=Saurabh|last3=Elongavan|first3=Ashok|date=2017|title=Action and resistance mechanisms of antibiotics: A guide for clinicians|url=http://www.joacp.org/text.asp?2017/33/3/300/214313|journal=Journal of Anaesthesiology Clinical Pharmacology|volume=33|issue=3|pages=300|language=en|doi=10.4103/joacp.JOACP_349_15|issn=0970-9185|pmid=29109626|pmc=PMC5672523}}</ref>。また、葉酸代謝阻害薬を加えて4つに分類することもある<ref name=":3" />。 |
|||
作用機序の分類としては、核酸合成阻害薬、細胞壁合成阻害薬、蛋白合成阻害薬に大きく分けられる。 |
|||
; 核酸合成阻害薬 |
|||
===細胞壁合成阻害薬=== |
|||
: [[リファンピシン]] |
|||
細胞壁合成阻害薬に分類される抗生物質としてβラクタム系、[[ホスホマイシン]]、[[バンコマイシン]]がある。 |
|||
; 細胞壁合成阻害薬 |
|||
==== 細胞壁の合成経路 ==== |
|||
: βラクタム系、[[ホスホマイシン]]、[[バンコマイシン]] |
|||
ほとんどの細菌は[[細胞膜]]の外側に[[細胞壁]]と呼ばれる構造を持つが、動物細胞はこれを持たない。細菌は一般に[[グラム染色]]の染色像によりグラム陽性菌とグラム陰性菌に分類され、両者は細胞壁の構造の違いから区別されるが、いずれの細胞壁も共通してペプチドグリカンという[[高分子]]を構成成分として持つ。細菌の細胞は高い内部[[浸透圧]]を持ち、ペプチドグリカンはこの浸透圧から細菌を保護する働きを持つ。従ってペプチドグリカンを欠く細菌は細胞膜が破裂して死んでしまう<ref name="hiramatsu" />。 |
|||
; 蛋白合成阻害薬 |
|||
: テトラサイクリン系、マクロライド系、アミノグリコシド系、[[クロラムフェニコール]] |
|||
細菌の細胞壁はムレインとも呼ばれ、2つの[[アミノ糖]]と10個の[[アミノ酸]]から構成されるムレインモノマーがレンガのように組み立てられることで細胞壁が構成される。ムレインモノマーは細胞内で合成された後に細胞外へ輸送され、[[グリコシルトランスフェラーゼ]] (GT) と呼ばれる酵素と[[ペニシリン結合タンパク質]] (PBP) と呼ばれる酵素の両者の働きによって既存の細胞壁へ架橋され、細胞壁の合成が進められる。この2つの酵素は必ずしも別の酵素であるとは限らず、[[大腸菌]]の場合はPBPが2つの酵素の働きを兼ねる。細胞壁合成阻害薬のうち、β-ラクタム系とバンコマイシンはPBPの作用を阻害するが、ホスホマイシンは細胞内におけるムレインモノマーの合成を阻害する<ref name="hiramatsu">{{Cite book|和書|title=標準微生物学|author=平松啓一・中込治 編集|edition=10|year=2009|ISBN=978-4-260-00638-5|chapter=第III章 細菌学総論}}</ref>。 |
|||
==== β-ラクタム系 ==== |
|||
[[File:Penicillines General Formula V1.svg|サムネイル|βラクタム系の代表格、ペニシリン系の骨格。赤く示された部分がβラクタム環である。左上のRがペニシリン系の側鎖であり、側鎖を変更することで様々なペニシリン系の誘導体が開発された。]] |
|||
[[File:Cephalosporin core structure.svg|サムネイル|βラクタム系の下位分類であるセフェム系の骨格。ペニシリン系と異なりラクタム環に付随する環は六員環である。また、改変しうる側鎖を2つ持つ点でも異なる。]] |
|||
β-ラクタム系の抗生物質は最も普及した抗生物質で、アメリカ合衆国で処方される抗菌薬の65%はこの系統に属する。β-ラクタム系の中でも[[セフェム系]]は特に処方されることが多く、β-ラクタム系の処方のうちおよそ半分はセフェム系の抗生物質である<ref name=":9">{{Cite journal|last=Bush|first=Karen|last2=Bradford|first2=Patricia A.|date=2016-08|title=β-Lactams and β-Lactamase Inhibitors: An Overview|url=http://perspectivesinmedicine.cshlp.org/lookup/doi/10.1101/cshperspect.a025247|journal=Cold Spring Harbor Perspectives in Medicine|volume=6|issue=8|pages=a025247|language=en|doi=10.1101/cshperspect.a025247|issn=2157-1422|pmid=27329032|pmc=PMC4968164}}</ref>。 |
|||
β-ラクタム系はPBPの作用を阻害することでその薬理効果を発揮する。PBPは、ムレインモノマーの分子中に存在するD-アラニル-D-アラニンを認識して架橋を形成し細胞壁の合成を進めるため、D-アラニル-D-アラニンは細胞壁合成において重要な役割を果たす。[[ペニシリン]]に代表されるβ-ラクタム系の抗菌薬はこのD-アラニル-D-アラニンに類似した構造をしているため、PBPに結合し、PBPはムレインモノマーに結合できなくなってしまう。結果的に細胞壁の架橋が不十分になり、細菌は破裂死する。これがβ-ラクタム系の作用機序である<ref name="hiramatsu" /><ref name=":4" />。 |
|||
β-ラクタム系はその名の通り、β-ラクタム環と呼ばれる構造を持っている。β-ラクタム系ではこれに付随する[[側鎖]]の構造を変えることで抗菌スペクトルが異なる様々な抗菌薬が派生して開発されている<ref name="hiramatsu" />。副作用は主にアレルギー反応であり、特に[[アンピシリン]]と[[セファレキシン]]の組み合わせの様に側鎖が類似したペニシリン系とセフェム系同士では交差アレルギー反応が発現しやすい。一方、ペニシリン系やセフェム系と異なり、β-ラクタム環に付随する5員環または6員環を持たない[[モノバクタム]]はアレルギー反応が少なく、ペニシリンに対しアレルギーを示す患者にも使用される<ref name=":9" /><ref>{{Cite journal|last=Mirakian|first=R.|last2=Leech|first2=S. C.|last3=Krishna|first3=M. T.|last4=Richter|first4=A. G.|last5=Huber|first5=P. A. J.|last6=Farooque|first6=S.|last7=Khan|first7=N.|last8=Pirmohamed|first8=M.|last9=Clark|first9=A. T.|date=2015-02|title=Management of allergy to penicillins and other beta-lactams|url=https://onlinelibrary.wiley.com/doi/10.1111/cea.12468|journal=Clinical & Experimental Allergy|volume=45|issue=2|pages=300–327|language=en|doi=10.1111/cea.12468}}</ref><ref>{{Cite journal|last=Trubiano|first=Jason A.|last2=Stone|first2=Cosby A.|last3=Grayson|first3=M. Lindsay|last4=Urbancic|first4=Karen|last5=Slavin|first5=Monica A.|last6=Thursky|first6=Karin A.|last7=Phillips|first7=Elizabeth J.|date=2017-11|title=The 3 Cs of Antibiotic Allergy—Classification, Cross-Reactivity, and Collaboration|url=https://linkinghub.elsevier.com/retrieve/pii/S2213219817305019|journal=The Journal of Allergy and Clinical Immunology: In Practice|volume=5|issue=6|pages=1532–1542|language=en|doi=10.1016/j.jaip.2017.06.017|pmid=28843343|pmc=PMC5681410}}</ref><ref>{{Cite journal|last=Jeimy|first=Samira|last2=Ben-Shoshan|first2=Moshe|last3=Abrams|first3=Elissa M.|last4=Ellis|first4=Anne K.|last5=Connors|first5=Lori|last6=Wong|first6=Tiffany|date=2020-12|title=Practical guide for evaluation and management of beta-lactam allergy: position statement from the Canadian Society of Allergy and Clinical Immunology|url=https://aacijournal.biomedcentral.com/articles/10.1186/s13223-020-00494-2|journal=Allergy, Asthma & Clinical Immunology|volume=16|issue=1|pages=95|language=en|doi=10.1186/s13223-020-00494-2|issn=1710-1492|pmid=33292466|pmc=PMC7653726}}</ref>。 |
|||
==== バンコマイシン ==== |
|||
[[File:Vancomycin.svg|サムネイル|バンコマイシンの構造式]] |
|||
β-ラクタム系がPBPと結合して細胞壁の合成を阻害するのに対し、[[バンコマイシン]]はムレインモノマーの一部であるD-アラニル-D-アラニンと結合し、GTによるムレインモノマーの重合を阻害することで作用するとされる。分子が大きいため細胞外膜を通過しにくいという難点や副作用から「最後の手段」と呼ばれることもあるが、β-ラクタム系と作用機序が異なるため、[[メチシリン耐性黄色ブドウ球菌]]の様にβ-ラクタム系の抗菌薬に対し耐性を示す細菌の感染に対し、治療薬として使用される<ref name="hiramatsu"/><ref>{{Cite journal|last=Butler|first=Mark S|last2=Hansford|first2=Karl A|last3=Blaskovich|first3=Mark A T|last4=Halai|first4=Reena|last5=Cooper|first5=Matthew A|date=2014-09|title=Glycopeptide antibiotics: Back to the future|url=http://www.nature.com/articles/ja2014111|journal=The Journal of Antibiotics|volume=67|issue=9|pages=631–644|language=en|doi=10.1038/ja.2014.111|issn=0021-8820}}</ref>。 |
|||
==== ホスホマイシン ==== |
|||
上記2系統の細胞壁合成阻害薬と異なり、[[ホスホマイシン]]はムレインモノマーの部品となる[[N-アセチルムラミン酸]]の産生を阻害する。β-ラクタム系と併用することで相乗効果を示す<ref name="hiramatsu"/><ref>{{Cite journal|last=Falagas|first=Matthew E.|last2=Vouloumanou|first2=Evridiki K.|last3=Samonis|first3=George|last4=Vardakas|first4=Konstantinos Z.|date=2016-04|title=Fosfomycin|url=https://journals.asm.org/doi/10.1128/CMR.00068-15|journal=Clinical Microbiology Reviews|volume=29|issue=2|pages=321–347|language=en|doi=10.1128/CMR.00068-15|issn=0893-8512|pmid=26960938|pmc=PMC4786888}}</ref>。 |
|||
===タンパク質合成阻害薬=== |
|||
[[File:Erythromycin A.svg|サムネイル|マクロライド系の代表例、エリスロマイシンA]] |
|||
[[File:Tetracycline skeletal.svg|サムネイル|テトラサイクリンの構造式]] |
|||
生物のDNAに保存された情報は[[転写 (生物学)|転写]]により[[伝令RNA|mRNA]]に変換され、mRNAは[[翻訳 (生物学)|翻訳]]されて[[タンパク質]]の合成に用いられる。[[リボソーム]]はタンパク質合成の場であり、細菌の場合70Sリボソームが30Sサブユニットと50Sサブユニットの組み合わせによって構成される<ref name=":4" />。細菌のリボソームはヒトのリボソームとは部分的に異なった構造を持つため、タンパク質合成阻害薬は細菌のリボソームに高い親和性を持って作用する。タンパク質合成阻害薬の選択性は単に親和性に依存しており、量的な選択毒性を示す<ref name="hiramatsu" />。タンパク質合成阻害薬はその阻害対象によって30Sサブユニットを対象とするものと、50Sサブユニットを対象とするものの2つに大きく分類できる。前者にはアミノ配糖体とテトラサイクリン系が、後者にはクロラムフェニコール、マクロライド系が含まれる<ref name=":4" />。[[アミノグリコシド系抗生物質|アミノ配糖体]](アミノグリコシド系)は1943年に''Streptomyces griseus''から分離された[[ストレプトマイシン]]に代表される抗生物質で、グラム陽性菌及びグラム陰性菌両者に対する広い抗菌スペクトルを持つ<ref>{{Cite journal|last=Jospe-Kaufman|first=Moriah|last2=Siomin|first2=Liza|last3=Fridman|first3=Micha|date=2020-07-01|title=The relationship between the structure and toxicity of aminoglycoside antibiotics|url=https://pubmed.ncbi.nlm.nih.gov/32360102|journal=Bioorganic & Medicinal Chemistry Letters|volume=30|issue=13|pages=127218|doi=10.1016/j.bmcl.2020.127218|issn=1464-3405|pmid=32360102|pmc=7194799}}</ref>。一方、アミノ配糖体の細胞内への取り込みには好気呼吸が必要であり、嫌気性菌に対しては有効性を欠く<ref>{{Cite journal|last=Ramirez|first=Maria S.|last2=Tolmasky|first2=Marcelo E.|date=2010-12|title=Aminoglycoside modifying enzymes|url=https://pubmed.ncbi.nlm.nih.gov/20833577|journal=Drug Resistance Updates: Reviews and Commentaries in Antimicrobial and Anticancer Chemotherapy|volume=13|issue=6|pages=151–171|doi=10.1016/j.drup.2010.08.003|issn=1532-2084|pmid=20833577|pmc=2992599}}</ref><ref>{{Cite journal|last=Krause|first=Kevin M.|last2=Serio|first2=Alisa W.|last3=Kane|first3=Timothy R.|last4=Connolly|first4=Lynn E.|date=2016-06|title=Aminoglycosides: An Overview|url=http://perspectivesinmedicine.cshlp.org/lookup/doi/10.1101/cshperspect.a027029|journal=Cold Spring Harbor Perspectives in Medicine|volume=6|issue=6|pages=a027029|language=en|doi=10.1101/cshperspect.a027029|issn=2157-1422|pmid=27252397|pmc=PMC4888811}}</ref>。[[マクロライド系]]は、12-16の原子によって構成される大環状ラクトンと呼ばれる構造を持つ大きな分子で<ref name=":10">{{Cite journal|last=Vázquez-Laslop|first=Nora|last2=Mankin|first2=Alexander S.|date=2018-09|title=How Macrolide Antibiotics Work|url=https://pubmed.ncbi.nlm.nih.gov/30054232|journal=Trends in Biochemical Sciences|volume=43|issue=9|pages=668–684|doi=10.1016/j.tibs.2018.06.011|issn=0968-0004|pmid=30054232|pmc=6108949}}</ref>、毒性が低く<ref>{{Cite journal|last=Brook|first=Itzhak|last2=Wexler|first2=Hannah M.|last3=Goldstein|first3=Ellie J. C.|date=2013-07|title=Antianaerobic antimicrobials: spectrum and susceptibility testing|url=https://pubmed.ncbi.nlm.nih.gov/23824372|journal=Clinical Microbiology Reviews|volume=26|issue=3|pages=526–546|doi=10.1128/CMR.00086-12|issn=1098-6618|pmid=23824372|pmc=3719496}}</ref>、ブドウ球菌などのグラム陽性菌に優れた抗菌力を示す<ref>{{Cite journal|和書|author=西野 武志|year=2014|title=薬剤耐性菌の耐性機構に関する研究―とくに自然耐性機構の解明―|url=http://www.chemotherapy.or.jp/journal/jjc/06202/062020177.pdf|journal=日本化学療法学会雑誌|volume=62|issue=2|page=177-191}}</ref>。代表例として1952年に発見された[[エリスロマイシン]]などが知られる<ref name=":10" />。 [[テトラサイクリン]]系も極めて抗菌スペクトルの広い抗生物質で、4つの連なった環状構造を核として持つ。テトラサイクリンの他、テトラサイクリンの側鎖を変更して脂溶性を高めた[[ドキシサイクリン]]、[[ミノサイクリン]]が知られる。テトラサイクリン系抗生物質はリボソームと結合し、アミノアシル-tRNAとリボソームの結合を阻害することでタンパク質合成を阻害する<ref>{{Cite journal|last=Griffin|first=Michael O.|last2=Fricovsky|first2=Eduardo|last3=Ceballos|first3=Guillermo|last4=Villarreal|first4=Francisco|date=2010-09|title=Tetracyclines: a pleitropic family of compounds with promising therapeutic properties. Review of the literature|url=https://www.physiology.org/doi/10.1152/ajpcell.00047.2010|journal=American Journal of Physiology-Cell Physiology|volume=299|issue=3|pages=C539–C548|language=en|doi=10.1152/ajpcell.00047.2010|issn=0363-6143|pmid=20592239|pmc=PMC2944325}}</ref>。 [[クロラムフェニコール]]は極めて広い抗菌スペクトルを持つ抗生物質である。しかしながら、骨髄毒性を示すなど毒性が強く、治療目的で使用されることは多くない<ref name="hiramatsu" /><ref>{{Cite book|title=Chloramphenicol|url=http://www.ncbi.nlm.nih.gov/books/NBK555966/|publisher=StatPearls Publishing|date=2021|location=Treasure Island (FL)|pmid=32310426|first=Ginny C.|last=Oong|first2=Prasanna|last2=Tadi}}</ref>。 |
|||
===核酸合成阻害薬=== |
|||
核酸合成阻害薬はRNA合成阻害薬とDNA合成阻害薬に分類され、いずれも量的な選択毒性を示す。前者は[[RNAポリメラーゼ]]を阻害して[[伝令RNA|mRNA]]の合成を抑制する。[[リファンピシン]]はこの代表例で、抗結核薬として重要である<ref name="hiramatsu" />。 |
|||
===その他の抗菌薬=== |
|||
キノロン系や[[サルファ剤]]は核酸合成阻害を機序とした'''合成抗菌薬'''であり、狭義の抗生物質とは異なる。 |
キノロン系や[[サルファ剤]]は核酸合成阻害を機序とした'''合成抗菌薬'''であり、狭義の抗生物質とは異なる。 |
||
キノロン系はDNA合成阻害薬でもあり、[[DNAジャイレース]]と[[DNAトポイソメラーゼ|トポイソメラーゼIV]]を阻害することでDNAの複製を阻害する。葉酸代謝系阻害薬はヒトが持たない[[葉酸]]代謝系を阻害するため、高い選択毒性を持つ。サルファ剤は葉酸代謝系阻害薬であり、同じ葉酸代謝系の別の経路を阻害する[[トリメトプリム]]と共に[[ST合剤]]として使用される。ST合剤はグラム陽性・グラム陰性菌の他、[[原虫]]や[[菌類|真菌]]にも効果を示す<ref name="hiramatsu" />。 |
|||
=== 抗菌薬以外の抗生物質 === |
|||
[[ポリエン系抗真菌薬|ポリエンマクロライド系]]は[[エルゴステロール]]と呼ばれる真菌の細胞膜に特徴的な[[ステロール]]に結合する。この結合によりエルゴステロールが細胞膜から奪われ、機能を阻害することで真菌に対する毒性を示す<ref name=":16">{{Cite journal|last=Robbins|first=Nicole|last2=Caplan|first2=Tavia|last3=Cowen|first3=Leah E.|date=2017-09-08|title=Molecular Evolution of Antifungal Drug Resistance|url=http://www.annualreviews.org/doi/10.1146/annurev-micro-030117-020345|journal=Annual Review of Microbiology|volume=71|issue=1|pages=753–775|language=en|doi=10.1146/annurev-micro-030117-020345|issn=0066-4227}}</ref><ref>{{Cite journal|last=Ellis|first=David|date=2002-01-01|title=Amphotericin B: spectrum and resistance|url=https://academic.oup.com/jac/article/49/suppl_1/7/2473430|journal=Journal of Antimicrobial Chemotherapy|volume=49|issue=suppl_1|pages=7–10|language=en|doi=10.1093/jac/49.suppl_1.7|issn=1460-2091}}</ref>。代表例として [[アムホテリシンB]]が知られ、重篤な全身性の真菌感染症の治療に使用される<ref name=":16" />。 |
|||
[[マイトマイシン]]は細胞内で[[還元]]されて活性化するとDNAを架橋する働きを持つ抗生物質である。マイトマイシンを活性化する酵素は全身に分布するが、酸素が豊富な環境では還元が抑制される。従って相対的に低酸素状態にある[[がん|固形がん]]に対し選択的に毒性を示すため、特に[[マイトマイシンC]]は抗がん剤として利用される<ref>{{Cite journal|last=Tomasz|first=M.|date=1995-09|title=Mitomycin C: small, fast and deadly (but very selective)|url=https://pubmed.ncbi.nlm.nih.gov/9383461|journal=Chemistry & Biology|volume=2|issue=9|pages=575–579|doi=10.1016/1074-5521(95)90120-5|issn=1074-5521|pmid=9383461}}</ref><ref>{{Cite journal|last=Kono|first=Motomichi|last2=Kasai|first2=Masaji|date=1990|title=Studies on the chemistry of mitomycins.|url=http://www.jstage.jst.go.jp/article/yukigoseikyokaishi1943/48/9/48_9_824/_article/-char/ja/|journal=Journal of Synthetic Organic Chemistry, Japan|volume=48|issue=9|pages=824–833|doi=10.5059/yukigoseikyokaishi.48.824|issn=0037-9980}}</ref>。 |
|||
== 薬理 == |
== 薬理 == |
||
[[File:Antibiotic sensitivity test.jpg|サムネイル|薬剤感受性試験の一例。寒天培地上に置かれた白い紙のディスクにはディスク毎に異なる抗生物質が含まれており、細菌がその抗生物質に感受性だとその周りでは細菌が増殖できない。この細菌が増殖できない範囲が阻止円である。]] |
|||
抗生物質を含む抗菌剤は、細菌が増殖するのに必要な[[代謝経路]]に作用することで細菌にのみ選択的に[[毒性]]を示す[[化学物質]]である。例えば、β-ラクタム系抗生物質は細菌特有の[[細胞壁]]の合成を阻害するが、人体の細胞に対してはほとんど毒性を示さない。[[アルコール]]、[[ポビドンヨード]]などのように、単に化学的な作用で細菌を死滅させる[[殺菌剤]]、[[消毒薬]]とは区別される。 |
|||
抗生物質を含む抗菌剤は、細菌が増殖するのに必要な[[代謝経路]]に作用することで、選択毒性、つまり細菌にのみ選択的に[[毒性]]を示す[[化学物質]]である。例えば、β-ラクタム系抗生物質はPBPとの親和性を持ち、[[細胞壁]]の合成を阻害するが、そのいずれもが原核生物に特有のため、人体の細胞に対してはほとんど毒性を示さない<ref name=":11">{{Cite journal|last=Dalhoff|first=Axel|date=2021-02|title=Selective toxicity of antibacterial agents-still a valid concept or do we miss chances and ignore risks?|url=https://pubmed.ncbi.nlm.nih.gov/33367978|journal=Infection|volume=49|issue=1|pages=29–56|doi=10.1007/s15010-020-01536-y|issn=1439-0973|pmid=33367978|pmc=7851017}}</ref>。 |
|||
もっとも、抗生物質の中には抗菌性のみならず、抗ウイルス、抗真菌、抗寄生虫、抗腫瘍活性を示すものが存在する<ref name=":11" />。また、選択毒性を示さずに、全ての生物に対して毒性を示す抗生物質も存在する。例えば[[ピューロマイシン]]は[[転移RNA|tRNA]]にアミノ酸を付加したアミノアシルtRNAに類似した構造を持つ、[[放線菌]]に由来する抗生物質だが、産生菌を含む全ての生物においてタンパク質合成を阻害する働きを持つ。このような選択毒性を持たない抗生物質が感染症治療に利用されることはないが、タンパク質合成系の研究などの研究用途では広く用いられる<ref>{{Cite journal|last=Aviner|first=Ranen|date=2020|title=The science of puromycin: From studies of ribosome function to applications in biotechnology|url=https://linkinghub.elsevier.com/retrieve/pii/S2001037020300921|journal=Computational and Structural Biotechnology Journal|volume=18|pages=1074–1083|language=en|doi=10.1016/j.csbj.2020.04.014|pmid=32435426|pmc=PMC7229235}}</ref>。 |
|||
また、抗菌剤の作用は一般に殺菌と静菌に分類される。殺菌的な抗菌剤はその名の通り細菌を死滅させる。一方、静菌的な抗菌剤は細菌の増殖を抑制するのみにとどまり、静菌的な抗菌剤の濃度が低下するなどの条件下で細菌は再び増殖することができる。また、抗菌剤が効く細菌の範囲を示す用語として抗菌スペクトルが用いられる。抗菌スペクトルは細菌の分類体系に従って記述される<ref name=":2" />。 |
|||
人類の最大の脅威であった細菌感染を克服し、[[平均寿命]]を大幅に伸ばすこととなった<ref>[[トマス・マキューン|McKeown. T.]] (1979). ''The role of medicine''. Oxford, Basil Blackwell.</ref>。しかし、感染症との戦いは終わったわけではなく、治療法の開発されていない[[新興感染症]]、抗生物質の効力が薄くなるなどした[[再興感染症]]などが問題となっている。 |
人類の最大の脅威であった細菌感染を克服し、[[平均寿命]]を大幅に伸ばすこととなった<ref>[[トマス・マキューン|McKeown. T.]] (1979). ''The role of medicine''. Oxford, Basil Blackwell.</ref>。しかし、感染症との戦いは終わったわけではなく、治療法の開発されていない[[新興感染症]]、抗生物質の効力が薄くなるなどした[[再興感染症]]などが問題となっている。 |
||
| 36行目: | 75行目: | ||
また、抗生物質は病原性を示していない細菌にも作用するため、多量に使用すると体内の[[常在菌]]のバランスを崩してしまう場合がある。それにより常在菌が極端に減少すると、他の細菌や真菌(カビ)などが爆発的に繁殖し、病原性を示す場合もある。さらに、生き残った菌が耐性化する[[耐性菌]]の出現も問題となっている。 |
また、抗生物質は病原性を示していない細菌にも作用するため、多量に使用すると体内の[[常在菌]]のバランスを崩してしまう場合がある。それにより常在菌が極端に減少すると、他の細菌や真菌(カビ)などが爆発的に繁殖し、病原性を示す場合もある。さらに、生き残った菌が耐性化する[[耐性菌]]の出現も問題となっている。 |
||
== |
=== 薬剤感受性 === |
||
細菌感染症に対する化学療法に抗生物質を用いる場合は、感染起因菌の薬剤感受性を調べた上で投与する抗生物質を選択する。迅速に当たりをつけるためには[[グラム染色]]による検体の塗抹染色を行う。正確に薬剤感受性を調べるためには、[[最小発育阻止濃度]] (Minimum Inhibitory Concentration; MIC) の測定を行う。これは細菌の増殖を抑制しうる最小の抗生物質濃度を割り出す方法であり、液体希釈法と寒天平板希釈法の2種が知られる他、簡易的な感受性ディスク法が医療現場では広く用いられている<ref name="hiramatsu" />。抗菌性を評価する指標には他に[[最小殺菌濃度]] (Minimum Bacteicidal Concentration; MBC) もあり、これは細菌の増殖を抑制するのみならず殺すために必要な抗菌剤の最小濃度を意味する。一般にMICに比べMBCは高い値を取り、その差が小さい時には抗菌剤が殺菌的、大きい時には静菌的であることを意味する<ref name=":2">{{Citation|title=抗菌剤の特性と抗菌メカニズム|url=https://doi.org/10.11338/mls.23.21|publisher=マテリアルライフ学会|date=2011-02-28|accessdate=2021-08-24|doi=10.11338/mls.23.21|language=ja|first=恒雄|last=石田}}</ref>。これらの指標は臨床の現場で薬剤耐性を調べる目的のみならず、新規に開発された抗菌剤の活性を決定するためにも用いられる<ref>{{Cite journal|last=Andrews|first=Jennifer M.|date=2001-07-01|title=Determination of minimum inhibitory concentrations|url=https://academic.oup.com/jac/article/48/suppl_1/5/2473513|journal=Journal of Antimicrobial Chemotherapy|volume=48|issue=suppl_1|pages=5–16|language=en|doi=10.1093/jac/48.suppl_1.5|issn=1460-2091}}</ref>。 |
|||
== 医療における利用 == |
|||
{{main2|細菌に対する薬物療法|化学療法 (細菌)}} |
{{main2|細菌に対する薬物療法|化学療法 (細菌)}} |
||
{{main2|悪性腫瘍に対する薬物療法|抗がん剤}} |
{{main2|悪性腫瘍に対する薬物療法|抗がん剤}} |
||
| 43行目: | 85行目: | ||
その他、ポリエンマクロライド系抗生物質は真菌の治療に使用される。また、癌治療には[[マイトマイシンC]]や[[ブレオマイシン]]、[[アドリアマイシン]]、[[ドキソルビシン]]などの抗生物質が使用される。また[[シクロスポリン]]、[[タクロリムス]]、[[エベロリムス]]も抗生物質であり、[[免疫抑制剤]]として[[膠原病]]、[[自己免疫疾患]]、移植医療の現場で活躍している。 |
その他、ポリエンマクロライド系抗生物質は真菌の治療に使用される。また、癌治療には[[マイトマイシンC]]や[[ブレオマイシン]]、[[アドリアマイシン]]、[[ドキソルビシン]]などの抗生物質が使用される。また[[シクロスポリン]]、[[タクロリムス]]、[[エベロリムス]]も抗生物質であり、[[免疫抑制剤]]として[[膠原病]]、[[自己免疫疾患]]、移植医療の現場で活躍している。 |
||
===抗生物質による治療=== |
|||
抗生物質は細菌感染を治療したり予防するために用いられるが<ref name="Antibiotic">{{cite book|title=Antibiotics Simplified.|date=2011|publisher=Jones & Bartlett Publishers|isbn=978-1-4496-1459-1|pages=15–17|url=https://books.google.com/books?id=vIRgA57q414C&q=Antibiotics}}</ref>、[[メトロニダゾール]]の様に[[原虫|原虫感染症]]に効果を示すものもある。ある症状が感染に起因することが疑われ、かつそれを起因する病原体が明らかでない場合は[[経験的治療]]が行われることもある<ref name="General principles">{{cite journal | vauthors = Leekha S, Terrell CL, Edson RS | title = General principles of antimicrobial therapy | journal = Mayo Clinic Proceedings | volume = 86 | issue = 2 | pages = 156–67 | date = February 2011 | pmid = 21282489 | pmc = 3031442 | doi = 10.4065/mcp.2010.0639 }}</ref>。経験的治療においては結果が出るのに数日かかる培養検査の結果を待たずに、症状に基づいて広域スペクトル抗生物質が投与される<ref name="Antibiotic" /><ref name="General principles" />。厳密に感染起因菌を特定するためには培養などによる検査が必要だが、症状から病原体の推定が可能なこともある。例えば、[[蜂巣炎]]の病原体はレンサ球菌やブドウ球菌が尤もらしいと推定できるため、培養で陽性が得られなくとも抗菌薬による治療を開始できる<ref name="General principles" />。重篤な感染を生じている場合などはできるだけ速やかに抗生物質を投与することが推奨される。そのため、多くの救急部門で抗生物質を備えている<ref>{{cite journal|date=December 2018|title=Cross-sectional study on emergency department management of sepsis|journal=Hong Kong Medical Journal = Xianggang Yi Xue Za Zhi|volume=24|issue=6|pages=571–578|doi=10.12809/hkmj177149|pmid=30429360|vauthors=Hung KK, Lam RP, Lo RS, Tenney JW, Yang ML, Tai MC, Graham CA|doi-access=free}}</ref>。 |
|||
病原微生物が予めわかっていたり、検査により特定された場合には、抗菌スペクトルの狭い抗生物質が投与される。抗生物質投与の費用と毒性を抑え、かつ耐性菌の出現を抑制するためには、病原体の特定が重要となる<ref name="General principles" />。また、手術を避けるために[[急性虫垂炎]]に対して処方されることもある<ref>{{cite journal | vauthors = Rollins KE, Varadhan KK, Neal KR, Lobo DN | title = Antibiotics Versus Appendicectomy for the Treatment of Uncomplicated Acute Appendicitis: An Updated Meta-Analysis of Randomised Controlled Trials | journal = World Journal of Surgery | volume = 40 | issue = 10 | pages = 2305–18 | date = October 2016 | pmid = 27199000 | doi = 10.1007/s00268-016-3561-7 | s2cid = 4802473 }}</ref>。 |
|||
培養によって病原体が特定された場合、次に[[薬剤感受性試験]]を行い、病原体が特定の抗菌薬の存在下で発育可能か試験する。薬剤感受性試験で得られたMICの値を基に、病原体が各薬剤に対し、感受性か、耐性か、あるいは中間かを決定する。感受性の場合は通常投与される抗菌薬の量で感染を治療できることを意味する。通常、この過程を経ることで有効な抗菌薬を絞り込むことが可能となる<ref name="General principles" />。 |
|||
抗生物質が予防的に用いられることもあるが、予防的な投与は[[免疫抑制薬]]を服薬中の者、[[がん]]患者、[[手術]]を受けた患者のような免疫系の弱った者への投与に限定され、特に[[ヒト免疫不全ウイルス]]感染者における[[肺炎]]の防止のために投与される<ref name="Antibiotic" />。外科手術における抗生物質の投与は[[切開]]部位の感染を防止する。予防的な抗生物質の投与は口腔外科的な手術で重要な役割を担い、菌血症やそれに続く[[感染性心内膜炎]]を防止する。また、[[好中球減少症]]における感染防止にも使用され、これは特に[[化学療法 (悪性腫瘍)|化学療法]]によるがん治療を受けるものに対して行われる<ref>{{cite journal | vauthors = Flowers CR, Seidenfeld J, Bow EJ, Karten C, Gleason C, Hawley DK, Kuderer NM, Langston AA, Marr KA, Rolston KV, Ramsey SD | display-authors = 6 | title = Antimicrobial prophylaxis and outpatient management of fever and neutropenia in adults treated for malignancy: American Society of Clinical Oncology clinical practice guideline | journal = Journal of Clinical Oncology | volume = 31 | issue = 6 | pages = 794–810 | date = February 2013 | pmid = 23319691 | doi = 10.1200/JCO.2012.45.8661 }}</ref><ref>{{cite journal | vauthors = Bow EJ | title = Infection in neutropenic patients with cancer | journal = Critical Care Clinics | volume = 29 | issue = 3 | pages = 411–41 | date = July 2013 | pmid = 23830647 | doi = 10.1016/j.ccc.2013.03.002 }}</ref><ref>{{Cite journal|last=Freifeld|first=Alison G.|last2=Bow|first2=Eric J.|last3=Sepkowitz|first3=Kent A.|last4=Boeckh|first4=Michael J.|last5=Ito|first5=James I.|last6=Mullen|first6=Craig A.|last7=Raad|first7=Issam I.|last8=Rolston|first8=Kenneth V.|last9=Young|first9=Jo-Anne H.|date=2011-02-15|title=Clinical Practice Guideline for the Use of Antimicrobial Agents in Neutropenic Patients with Cancer: 2010 Update by the Infectious Diseases Society of America|url=https://academic.oup.com/cid/article/52/4/e56/382256|journal=Clinical Infectious Diseases|volume=52|issue=4|pages=e56–e93|language=en|doi=10.1093/cid/cir073|issn=1058-4838}}</ref>。ただし、薬剤耐性菌の問題が大きくなってからは、それ以前に比べて予防投与の効果が低減している可能性もある<ref>{{Cite journal|和書|author=冲中 敬二|year=2020|title=抗がん剤治療患者における感染症対策について|url=http://www.chemotherapy.or.jp/journal/jjc/06801/068010132.pdf|journal=日本化学療法学会雑誌|volume=68|issue=1|page=132-142}}</ref>。 |
|||
===投与経路=== |
|||
抗生物質は様々な[[投与経路]]を持つ。通常は[[経口投与]]されることが多いが、[[全身感染症]]の場合などで[[点滴静脈注射|点滴]]や注射によって投与されることもある<ref name="General principles" />。感染部位が露出しているような場合は抗生物質が局所投与されることもあり、例えば[[結膜炎]]の際には[[結膜]]に対して[[目薬]]として、急性の[[外耳炎]]の場合には[[点耳薬]]として投与される。また、[[ニキビ]]や[[蜂巣炎]]のような皮膚疾患の治療には[[外用薬]]として抗生物質が用いられることがある<ref>{{cite journal | vauthors = Pangilinan R, Tice A, Tillotson G | title = Topical antibiotic treatment for uncomplicated skin and skin structure infections: review of the literature | journal = Expert Review of Anti-Infective Therapy | volume = 7 | issue = 8 | pages = 957–65 | date = October 2009 | pmid = 19803705 | doi = 10.1586/eri.09.74 | s2cid = 207217730 }}</ref>。局所投与の利点は抗生物質の投与部位における濃度を高く、長く保つことができる点などにある。これにより全身的な吸収や毒性を抑え、抗生物質の投与量を減少し、それゆえに乱用の恐れを減ずることができる<ref name="Treating chronic wounds">{{cite journal | vauthors = Lipsky BA, Hoey C | title = Topical antimicrobial therapy for treating chronic wounds | journal = Clinical Infectious Diseases | volume = 49 | issue = 10 | pages = 1541–9 | date = November 2009 | pmid = 19842981 | doi = 10.1086/644732 | doi-access = free }}</ref>。手術創に対する抗生物質の局所投与は、術創感染のリスクを軽減すると報告されてきた<ref>{{cite journal | vauthors = Heal CF, Banks JL, Lepper PD, Kontopantelis E, van Driel ML | title = Topical antibiotics for preventing surgical site infection in wounds healing by primary intention | journal = The Cochrane Database of Systematic Reviews | volume = 11 | issue = 11 | pages = CD011426 | date = November 2016 | pmid = 27819748 | pmc = 6465080 | doi = 10.1002/14651858.CD011426.pub2 }}</ref>。しかしながら、抗生物質の局所投与に対しては一般的に懸念材料が存在する。抗生物質が吸収されて全身へ移行する可能性もあり、その場合には抗生物質の投与量の正確な調節が困難となる。また、局所性の[[過敏感反応|過敏反応]]や、[[接触性皮膚炎]]を生じる可能性もある<ref name="Treating chronic wounds" />。 |
|||
=== 併用療法 === |
|||
結核などの感染症の治療においては数種類の抗生物質を同時に使用する[[併用療法]]が行われることがある<ref>{{Cite journal|last=Kerantzas|first=Christopher A.|last2=Jacobs|first2=William R.|editor-last=Rubin|editor-first=Eric J.|editor2-last=Collier|editor2-first=R. John|date=2017-05-03|title=Origins of Combination Therapy for Tuberculosis: Lessons for Future Antimicrobial Development and Application|url=https://journals.asm.org/doi/10.1128/mBio.01586-16|journal=mBio|volume=8|issue=2|language=en|doi=10.1128/mBio.01586-16|issn=2161-2129|pmid=28292983|pmc=PMC5350467}}</ref>。併用療法は経験的治療における抗菌スペクトラムの拡大、相乗効果による治療効果の増大、耐性菌出現の抑制などを目的として行われる<ref name=":14">{{Cite journal|last=Tamma|first=Pranita D.|last2=Cosgrove|first2=Sara E.|last3=Maragakis|first3=Lisa L.|date=2012-07|title=Combination Therapy for Treatment of Infections with Gram-Negative Bacteria|url=https://journals.asm.org/doi/10.1128/CMR.05041-11|journal=Clinical Microbiology Reviews|volume=25|issue=3|pages=450–470|language=en|doi=10.1128/CMR.05041-11|issn=0893-8512|pmid=22763634|pmc=PMC3416487}}</ref>。急性の細菌感染においては、治療効果の向上のために、単剤よりも効果の大きい複数の抗生物質の組み合わせが相乗効果を狙って投与され<ref name="Antagonism between bacteriostatic">{{cite journal | vauthors = Ocampo PS, Lázár V, Papp B, Arnoldini M, Abel zur Wiesch P, Busa-Fekete R, Fekete G, Pál C, Ackermann M, Bonhoeffer S | display-authors = 6 | title = Antagonism between bacteriostatic and bactericidal antibiotics is prevalent | journal = Antimicrobial Agents and Chemotherapy | volume = 58 | issue = 8 | pages = 4573–82 | date = August 2014 | pmid = 24867991 | pmc = 4135978 | doi = 10.1128/AAC.02463-14 }}</ref><ref name="Bollenbach - interactions">{{cite journal | vauthors = Bollenbach T | title = Antimicrobial interactions: mechanisms and implications for drug discovery and resistance evolution | journal = Current Opinion in Microbiology | volume = 27 | pages = 1–9 | date = October 2015 | pmid = 26042389 | doi = 10.1016/j.mib.2015.05.008 | doi-access = free }}</ref>、[[メチシリン耐性黄色ブドウ球菌]]の感染では[[フシジン酸]]と[[リファンピシン]]の併用により治療が行われる<ref name="Antagonism between bacteriostatic"/>。グラム陰性菌感染に対して併用療法による治療を行う場合はβラクタム系にアミノ配糖体かフルオロキノロンが組み合わされる<ref name=":14" />。また、抗生物質の組み合わせが単剤投与の場合よりも低下する場合もあり、これを拮抗作用と呼ぶ<ref name="Antagonism between bacteriostatic"/>。一般的には静菌作用を持つ抗生物質と殺菌作用を持つ抗生物質の組み合わせは拮抗的である<ref name="Antagonism between bacteriostatic"/><ref name="Bollenbach - interactions"/>。ただし、併用療法の有効性は実験的条件下においてのみ実証されている場合があり、例えばグラム陰性菌に対する併用療法の臨床における効果については疑問視する意見もある<ref name=":14" />。 |
|||
抗生物質と他の抗生物質の組み合わせに加え、抗生物質が抗生物質への耐性を抑える薬剤と共に用いられることもある。例えば、[[β-ラクタマーゼ]]を持つ細菌に感染した患者に対しては、βラクタム系の抗生物質が[[クラブラン酸]]や[[スルバクタム]]のような[[β-ラクタマーゼ阻害薬]]と併用されることがある<ref>{{cite journal | vauthors = Drawz SM, Bonomo RA | title = Three decades of beta-lactamase inhibitors | journal = Clinical Microbiology Reviews | volume = 23 | issue = 1 | pages = 160–201 | date = January 2010 | pmid = 20065329 | pmc = 2806661 | doi = 10.1128/CMR.00037-09 }}</ref>。 |
|||
== 動植物に対する使用 == |
|||
抗生物質はヒトの医療においてのみならず、動物や植物に対しても使用される<ref name=":17" /><ref name=":18">{{Cite journal|last=Teuber|first=M|date=2001-10-01|title=Veterinary use and antibiotic resistance|url=https://linkinghub.elsevier.com/retrieve/pii/S1369527400002411|journal=Current Opinion in Microbiology|volume=4|issue=5|pages=493–499|doi=10.1016/S1369-5274(00)00241-1}}</ref>。中にはヒトのみに使用されるもの、動物に対してのみ使用されるものも存在するが、多くの抗生物質はヒトとその他の動物の両者に使用される。抗生物質が投与され得る動物としてヒト以外の[[哺乳類]]、[[鳥類]]、[[魚類]]、[[昆虫]]などが例示される。また、テトラサイクリン系やストレプトマイシンなど一部の抗生物質は果樹に対しても使用される<ref name=":17">{{Cite journal|last=McEwen|first=Scott A.|last2=Collignon|first2=Peter J.|editor-last=Aarestrup|editor-first=Frank Møller|editor2-last=Schwarz|editor2-first=Stefan|editor3-last=Shen|editor3-first=Jianzhong|editor4-last=Cavaco|editor4-first=Lina|date=2018-04-06|title=Antimicrobial Resistance: a One Health Perspective|url=https://journals.asm.org/doi/10.1128/microbiolspec.ARBA-0009-2017|journal=Microbiology Spectrum|volume=6|issue=2|language=en|doi=10.1128/microbiolspec.ARBA-0009-2017|issn=2165-0497}}</ref><ref name=":19">{{Cite journal|last=Sundin|first=George W.|last2=Wang|first2=Nian|date=2018-08-25|title=Antibiotic Resistance in Plant-Pathogenic Bacteria|url=https://www.annualreviews.org/doi/10.1146/annurev-phyto-080417-045946|journal=Annual Review of Phytopathology|volume=56|issue=1|pages=161–180|language=en|doi=10.1146/annurev-phyto-080417-045946|issn=0066-4286}}</ref>。1997年の統計によると、ヨーロッパではヒトの医療用途で5,460,000 kgの抗生物質が使用された一方、動物への使用量も5,040,000 kgに上り、世界的に見ておよそ50%の抗生物質が動物に対して使用されると推定される<ref name=":18" />。また、[[アメリカ食品医薬品局]]によると、2019年の一年間でアメリカ合衆国内において動物用に販売された、医療用にも使用される抗菌薬の量は6,189,260 kgに上り、その内67%をテトラサイクリン系抗生物質が占めていた。なお、動物に対する抗菌薬の使用量は2015年の9,702,943 kgが最大となっており、それと比べると36%減少している。また、動物の種別では牛と豚に対する抗菌薬の使用がそれぞれ2,529,281 kgと2,582,399 kgに及び、これは動物に対する抗菌薬の使用量のそれぞれ41%と42%を占めている<ref>{{Cite web|title=2019 Summary Report on Antimicrobials Sold or Distributed for Use in Food-Producing Animals {{!}} FDA|url=https://www.fda.gov/media/144427/download|website=www.fda.gov|accessdate=2021-09-29}}</ref>。 |
|||
上述の通り、ヒトに対して抗菌薬を用いる場合、抗菌薬の投与は原則的に治療を目的とする。一方、ヒト以外の動物に対して用いる場合は事情が異なる。動物の中でも犬や猫のような[[ペット]]に対して抗菌薬を用いる場合、使用方針はヒトと同様であり、原則的に感染の治療を目的として個々の動物に対して抗菌薬が用いられる。例外的に予防的投与が行われることもあるが、これは手術後など特定の条件に限られる。一方、食肉を目的として飼育される動物の場合、群の一部の個体が症状を示していて、大多数の個体が無症状でも、餌や水を通して抗菌薬が群全体に投与されることがある。このような集団単位での抗菌薬の使用がヒトに対して行われるのは稀であり、その場合も濃厚接触がある個人など特定の個人にしか用いられない<ref name=":17" />。 |
|||
最も議論を招いているのは成長促進を目的とした[[経済動物]]に対する長期の低容量の抗菌薬の使用である。これは動物の治療を目指すものではなく、経済的利点から抗生物質が使用される。低容量の抗菌薬の長期にわたる使用は耐性菌を生じやすく、また耐性菌は動物の間のみならず食事や環境を通してヒトにも伝播しうる<ref name=":17" />。例えば、バンコマイシンに類似した抗生物質である[[アボパルシン]]はグラム陽性菌に効果を示す抗生物質として家禽やブタの成長促進用途で使用されるが、アボパルシンを使用した農場では[[バンコマイシン耐性腸球菌]]が検出されやすくなる。バンコマイシン耐性腸球菌はイギリス、ドイツ、デンマークの家畜から検出さており、この耐性菌が欧米の医療施設で急速に拡散したと考えられている<ref name=":20">{{Cite journal|last=Wegener|first=Henrik C|date=2003-10|title=Antibiotics in animal feed and their role in resistance development|url=https://linkinghub.elsevier.com/retrieve/pii/S1369527403001206|journal=Current Opinion in Microbiology|volume=6|issue=5|pages=439–445|language=en|doi=10.1016/j.mib.2003.09.009}}</ref>。加えて抗菌薬の使用による経済的な利得もないか、あっても耐性の出現に比して小さいものである<ref name=":17" />。一方、ヨーロッパでは2006年から成長促進を目的とした抗菌薬の使用を全面的に禁止している<ref>{{Cite journal|last=Castanon|first=J.I.R.|date=2007-11|title=History of the Use of Antibiotic as Growth Promoters in European Poultry Feeds|url=https://linkinghub.elsevier.com/retrieve/pii/S0032579119390716|journal=Poultry Science|volume=86|issue=11|pages=2466–2471|language=en|doi=10.3382/ps.2007-00249}}</ref>。デンマークでの研究では家畜の成長促進を目的としたアボパルシンの使用禁止のみではバンコマイシン耐性腸球菌の検出率は下がらなかったが、さらにマクロライド系抗菌薬の使用も禁止したところ、バンコマイシン耐性腸球菌の検出率が減少した。これはバンコマイシン耐性遺伝子''vanA''とマクロライド耐性遺伝子''ermB''が[[遺伝的連鎖|連鎖]]して伝播することによって説明されている<ref name=":20" />。 |
|||
畜産における抗生物質の使用は1950年代から始まっているが、植物に対してもペニシリン、ストレプトマイシン、[[クロルテトラサイクリン]]、クロラムフェニコール、[[オキシテトラサイクリン]]などが病気から植物を守るために使用できないか1940年代後半から検討されてきた。しかしながら低容量では効果がない、高容量では毒性が問題となる、他の防除法と比して費用がかかるといった点から、実際にはストレプトマイシンとオキシテトラサイクリンが特定の病気に使用される様になったのみである。ストレプトマイシンは植物の疾患制御に使われる主要な抗生物質で、リンゴやナシの[[火傷病]]を引き起こす''[[Erwinia amylovora]]''や、リンゴやナシの花弁・果実に感染する''[[Pseudomonas syringae]]''、トマトなどの[[斑点細菌病]]の原因菌である''[[Xanthomonas campestris]]''などの病原体に対して使用される。またモモなどの斑点細菌病に対してはオキシテトラサイクリンが用いられる<ref name=":19" />。 |
|||
== 耐性と乱用 == |
== 耐性と乱用 == |
||
=== 薬剤耐性のメカニズム === |
|||
[[ファイル:CDC Get Smart poster healthy adult.png|thumb|米国CDCの"Get Smart"キャンペーンポスター。抗生物質は[[風邪]]に効かないことを警告している。]] |
|||
{{See Also|抗微生物薬耐性}} |
|||
[[File:Antibiotic resistance ja.svg|サムネイル|[[自然選択説|自然選択]]による抗生物質耐性の増強を説明する模式図]] |
|||
細菌学において抗菌薬が効かないことを耐性といい、耐性を持つ細菌のことを耐性菌と呼ぶ。2009年現在において使用されてきたすべての抗生物質のいずれに対しても耐性菌が報告されており、これは合成抗菌薬についても同様である<ref name="hiramatsu" />。例えば1940年代には事実上すべてのグラム陽性菌がペニシリンに感受性だったが<ref name=":8">{{Cite journal|last=Palumbi|first=S. R.|date=2001-09-07|title=Humans as the World's Greatest Evolutionary Force|url=https://www.sciencemag.org/lookup/doi/10.1126/science.293.5536.1786|journal=Science|volume=293|issue=5536|pages=1786–1790|doi=10.1126/science.293.5536.1786}}</ref>、1991年までに病院で検査される[[黄色ブドウ球菌]]の38%がペニシリンより強力なβラクタム系抗生物質であるメチシリンに対して耐性を示すようになった<ref name=":8" /><ref>{{Cite journal|last=Abramson|first=Murray A.|last2=Sexton|first2=Daniel J.|date=1999-06|title=Nosocomial Methicillin-Resistant and Methicillin-Susceptible Staphylococcus Aureus Primary Bacteremia: At What Costs?|url=https://www.cambridge.org/core/product/identifier/S0195941700070430/type/journal_article|journal=Infection Control & Hospital Epidemiology|volume=20|issue=6|pages=408–411|language=en|doi=10.1086/501641|issn=0899-823X}}</ref>。細菌の持つ抗生物質への耐性は、その細菌が生来持つものと、新たに獲得されるものとがある。前者の例としては[[緑膿菌]]の細胞外膜の透過性が低いことによる、多くの抗生物質への自然発生的な耐性があげられる。後者の耐性獲得に関わる機構としては、[[プラスミド]]や[[トランスポゾン]]といった外来性遺伝子の取り込むによるものに加え、[[染色体]]上の変異によって発生することもある<ref name=":3" />。 |
|||
外来遺伝子の取り込みは[[遺伝子の水平伝播]]とも呼ばれ、細菌の[[進化]]に重要な役割を果たすが、これによってしばしば耐性遺伝子が伝達される。抗生物質は土壌などの環境中に存在する微生物に由来するが、生態学的[[ニッチ]]を共有する微生物はその抗生物質に対する耐性遺伝子を持っており、その様な遺伝子が医療現場で検出される病原体の耐性遺伝子の元となる可能性が高い。また、変異により耐性を獲得する場合、感受性を持つ細菌集団の中から抗生物質の活性に影響を及ぼす遺伝子変異を起こす細胞が出現し、その細胞が抗生物質に耐えて生き残る。生き残った細胞は抗生物質の存在下では[[自然選択説|選択圧]]により感受性を持つ細菌を駆逐して優先となるが、耐性遺伝子は一般にコストが大きいため、抗生物質が存在しないと維持されない<ref name=":13">{{Cite journal|last=Munita|first=Jose M.|last2=Arias|first2=Cesar A.|editor-last=Kudva|editor-first=Indira T.|editor2-last=Zhang|editor2-first=Qijing|date=2016-03-25|title=Mechanisms of Antibiotic Resistance|url=https://journals.asm.org/doi/10.1128/microbiolspec.VMBF-0016-2015|journal=Microbiology Spectrum|volume=4|issue=2|language=en|doi=10.1128/microbiolspec.VMBF-0016-2015|issn=2165-0497|pmid=27227291|pmc=PMC4888801}}</ref>。 |
|||
薬剤耐性のメカニズムは大きく(1)抗菌薬の取り込み低下や排出促進による抗菌薬の蓄積防止、(2)抗菌薬の分解や修飾による不活化、(3)抗菌薬の標的分子の変異や修飾による親和性の低下や過剰生産による抗菌薬の量的無効化に分類される<ref name=":3" /><ref name=":4" />。 |
|||
抗菌薬の取り込み低下や排出促進による抗菌薬の蓄積防止による耐性機構の一例として[[緑膿菌]]の自然耐性がある。全ての抗生物質は細菌の外膜を通過し、菌体内で蓄積することで機能を発揮するが、緑膿菌の外膜は抗生物質の透過性が低く、一般に抗生物質が効きにくい。また、細胞内へ透過したβラクタム系抗生物質やキノロン系抗菌薬を排出することでも耐性を持つ<ref name=":3" /><ref>{{Cite journal|last=Lambert|first=P. A.|date=2002|title=Mechanisms of antibiotic resistance in Pseudomonas aeruginosa|url=https://pubmed.ncbi.nlm.nih.gov/12216271|journal=Journal of the Royal Society of Medicine|volume=95 Suppl 41|pages=22–26|issn=0141-0768|pmid=12216271|pmc=1308633}}</ref>。 |
|||
抗菌薬の分解や修飾による不活化は、βラクタム系のような天然の抗生物質に対する耐性の主要なメカニズムである。典型的な例として[[Β-ラクタマーゼ|βラクタマーゼ]]によるβラクタム系抗生物質に対する耐性機構が知られており、βラクタマーゼはベータラクタム環構造を加水分解することで、ペニシリンをはじめとしたβラクタム系抗生物質とPBPの結合を阻害し、細菌に耐性をもたらす<ref name=":3" />。これまでに数百種類のラクタマーゼが発見されており、一般的にはA、B、C、Dの4種類のクラスに分類される<ref name="hiramatsu" /><ref name=":4" /><ref name=":5">{{Cite journal|last=Alekshun|first=Michael N.|last2=Levy|first2=Stuart B.|date=2007-03|title=Molecular Mechanisms of Antibacterial Multidrug Resistance|url=https://linkinghub.elsevier.com/retrieve/pii/S009286740700311X|journal=Cell|volume=128|issue=6|pages=1037–1050|language=en|doi=10.1016/j.cell.2007.03.004}}</ref>。特に[[ニューデリー・メタロベータラクタマーゼ|ニューデリー・メタロβラクタマーゼ-1]] (NDM-1) と呼ばれるβラクタマーゼは他のラクタマーゼと異なり特定の菌種のみならず多数の菌種に共有される、NDM-1の遺伝子を持つプラスミドが他の系統の耐性遺伝子も持つためにプラスミドを保持する細菌が多剤耐性となる、子どもの下痢の原因となる大腸菌にも伝播しうるために環境中に広がりやすいといった特徴を持ち、世界的に保健衛生上の脅威として認識されている<ref>{{Cite journal|last=Nordmann|first=Patrice|last2=Poirel|first2=Laurent|last3=Carrër|first3=Amélie|last4=Toleman|first4=Mark A.|last5=Walsh|first5=Timothy R.|date=2011-02|title=How To Detect NDM-1 Producers|url=https://journals.asm.org/doi/10.1128/JCM.01773-10|journal=Journal of Clinical Microbiology|volume=49|issue=2|pages=718–721|language=en|doi=10.1128/JCM.01773-10|issn=0095-1137|pmid=21123531|pmc=PMC3043507}}</ref><ref name=":15">{{Cite journal|last=Moellering|first=Robert C.|date=2010-12-16|title=NDM-1 — A Cause for Worldwide Concern|url=https://doi.org/10.1056/NEJMp1011715|journal=New England Journal of Medicine|volume=363|issue=25|pages=2377–2379|doi=10.1056/NEJMp1011715|issn=0028-4793|pmid=21158655}}</ref>。 |
|||
天然物に由来する抗生物質と異なり、サルファ剤やキノロン系などの合成抗菌薬を分解・修飾する酵素は発見されていない。このような抗菌薬に対する耐性は、抗菌薬の標的分子の変異や修飾による親和性の低下や過剰生産による抗菌薬の量的無効化によって獲得される<ref name=":3" />。例えばキノロン系抗菌薬への耐性は[[DNAジャイレース]]や[[DNAトポイソメラーゼ]]のような酵素をコードする[[遺伝子]]に変異が生じることで発生する<ref name=":4" />。合成抗菌薬のみならず、天然物に由来する抗生物質に対する耐性も同様の機構で獲得されることがある。例えば[[テトラサイクリン]]は[[16SリボソームRNA]]と結合することでタンパク質合成を阻害する抗生物質であるが、[[アクネ菌]]や[[ヘリコバクター・ピロリ]]で16SリボソームRNA遺伝子の変異による耐性獲得が報告されている<ref name=":5" />。 |
|||
=== 多剤耐性菌 === |
|||
近年においては[[メチシリン耐性黄色ブドウ球菌]]や[[多剤耐性結核菌]]のように、複数の抗菌薬に対し耐性を示す細菌が出現している。複数の抗菌薬に対し耐性を示すことを多剤耐性 (multidrug-resistant; MDR) と呼び、また多剤耐性を持つ細菌を[[多剤耐性菌]]と呼ぶ。加えて多剤耐性菌よりもさらに耐性の多い細菌を超多剤耐性 (extensively drug-resistant; XDR) 菌、全ての抗生物質に対し耐性を示す細菌を汎耐性 (pandrug-resistant; PDR) 菌と呼び、公衆衛生上の脅威となっている<ref>{{Cite journal|last=Magiorakos|first=A.-P.|last2=Srinivasan|first2=A.|last3=Carey|first3=R.B.|last4=Carmeli|first4=Y.|last5=Falagas|first5=M.E.|last6=Giske|first6=C.G.|last7=Harbarth|first7=S.|last8=Hindler|first8=J.F.|last9=Kahlmeter|first9=G.|date=2012-03|title=Multidrug-resistant, extensively drug-resistant and pandrug-resistant bacteria: an international expert proposal for interim standard definitions for acquired resistance|url=https://linkinghub.elsevier.com/retrieve/pii/S1198743X14616323|journal=Clinical Microbiology and Infection|volume=18|issue=3|pages=268–281|language=en|doi=10.1111/j.1469-0691.2011.03570.x}}</ref><ref>{{Cite journal|last=俊英|first=岡島|last2=雅之|first2=五十嵐|last3=陽子|first3=江口|last4=龍太郎|first4=内海|date=2019|title=多剤耐性細菌に有効な次世代型抗菌薬|url=https://www.jstage.jst.go.jp/article/kagakutoseibutsu/57/7/57_570706/_article/-char/ja/|journal=化学と生物|volume=57|issue=7|pages=416–427|doi=10.1271/kagakutoseibutsu.57.416}}</ref>。例えば、[[アメリカ疾病予防管理センター]]はアメリカ合衆国内で年間23,000人以上が多剤耐性を示す細菌の感染によって死亡していると推定している<ref name=":13" />。[[結核菌]]をはじめとした多数の細菌において多剤耐性の菌株が出現しており、治療用の抗生物質への耐性のために罹患率と死亡率の増加した微生物はスーパーバグと呼ばれることもある<ref name=":7" />。メチシリン耐性黄色ブドウ球菌や頭文字を取ってESKAPEと呼ばれる一群の細菌種(''[[Enterococcus faecium]]、[[黄色ブドウ球菌|Staphylococcus aureus]]、[[Klebsiella pneumoniae]]''、''[[Acinetobacter baumannii]]、[[Pseudomonas aeruginosa]]、''および[[エンテロバクター属|エンテロバクター属菌]])がこれに含まれ、多剤耐性を示す院内感染起因菌として問題視される<ref name=":15" /><ref>{{Cite journal|last=Rice|first=Louis B.|date=2008-04-15|title=Federal Funding for the Study of Antimicrobial Resistance in Nosocomial Pathogens: No ESKAPE|url=https://academic.oup.com/jid/article-lookup/doi/10.1086/533452|journal=The Journal of Infectious Diseases|volume=197|issue=8|pages=1079–1081|language=en|doi=10.1086/533452|issn=0022-1899}}</ref>。 |
|||
=== 乱用防止キャンペーン === |
|||
{{main|[[:en:Antibiotic misuse]]}} |
{{main|[[:en:Antibiotic misuse]]}} |
||
[[File:CDC Get Smart poster healthy adult.png|thumb|米国CDCの"Get Smart"キャンペーンポスター。抗生物質は[[風邪]]に効かないことを警告している。]] |
|||
耐性菌問題に関する組織は、不必要な抗生物質の使用を削減するキャンペーンを行っている<ref name="Larson2007">{{cite journal|author=Larson E|year=2007|title=Community factors in the development of antibiotic resistance.|url=|journal=Annu Rev Public Health|volume=28|issue=|pages=435–447|doi=10.1146/annurev.publhealth.28.021406.144020|pmid=17094768}}</ref>。耐性菌問題への対応のため、米国では省庁横断の耐性菌タスクフォースが作られた。タスクフォースには[[アメリカ疾病予防管理センター]] (CDC)、[[アメリカ食品医薬品局]] (FDA)、[[アメリカ国立衛生研究所]] (NIH)、などの機関が参加している<ref name="pharmguide">{{cite report|url=http://www.cdc.gov/drugresistance/index.html|title=CDC - Antibiotic / Antimicrobial Resistance|publisher=[[アメリカ疾病予防管理センター]]|date=2009-03-12}}</ref>。 |
耐性菌問題に関する組織は、不必要な抗生物質の使用を削減するキャンペーンを行っている<ref name="Larson2007">{{cite journal|author=Larson E|year=2007|title=Community factors in the development of antibiotic resistance.|url=|journal=Annu Rev Public Health|volume=28|issue=|pages=435–447|doi=10.1146/annurev.publhealth.28.021406.144020|pmid=17094768}}</ref>。耐性菌問題への対応のため、米国では省庁横断の耐性菌タスクフォースが作られた。タスクフォースには[[アメリカ疾病予防管理センター]] (CDC)、[[アメリカ食品医薬品局]] (FDA)、[[アメリカ国立衛生研究所]] (NIH)、などの機関が参加している<ref name="pharmguide">{{cite report|url=http://www.cdc.gov/drugresistance/index.html|title=CDC - Antibiotic / Antimicrobial Resistance|publisher=[[アメリカ疾病予防管理センター]]|date=2009-03-12}}</ref>。 |
||
| 99行目: | 186行目: | ||
=== 家畜への投与等 === |
=== 家畜への投与等 === |
||
1950年代から、米国の農家で薬用に満たない低用量の抗生物質の家畜への投与が家畜の体重増加を大幅に早めることに利用されてきた。このことは薬剤耐性菌リスクを高めることになる。EUは2006年に家畜を肥育させる目的での抗生物質の使用を禁止した<ref name=rob>ロブ・ナイト等、山田卓司等訳、「細菌が人をつくる」p139、TEDブックス、2018年5月30日、ISBN 978-4-255-01057-1</ref>。 |
1950年代から、米国の農家で薬用に満たない低用量の抗生物質の家畜への投与が家畜の体重増加を大幅に早めることに利用されてきた。このことは薬剤耐性菌リスクを高めることになる。EUは2006年に家畜を肥育させる目的での抗生物質の使用を禁止した<ref name="rob">ロブ・ナイト等、山田卓司等訳、「細菌が人をつくる」p139、TEDブックス、2018年5月30日、ISBN 978-4-255-01057-1</ref>。 |
||
家畜においても、薬剤耐性菌リスク軽減のために農林水産省は「責任ある慎重使用」を求めている<ref>{{Cite web|publisher=農林水産省|date=2016-10-27|title=家畜に使用する抗菌性物質について|url=http://www.maff.go.jp/j/syouan/tikusui/yakuzi/koukinzai.html|accessdate=2016-11-01}}</ref>。なお、実験動物のマウスへの抗生物質の低用量投与でも体重増加を示した。生後6か月のヒトの幼児でも抗生物質の投与と体重増加が関連を示していた<ref name=rob/>。 |
家畜においても、薬剤耐性菌リスク軽減のために日本の農林水産省は「責任ある慎重使用」を求めている<ref>{{Cite web|publisher=農林水産省|date=2016-10-27|title=家畜に使用する抗菌性物質について|url=http://www.maff.go.jp/j/syouan/tikusui/yakuzi/koukinzai.html|accessdate=2016-11-01}}</ref>。なお、実験動物のマウスへの抗生物質の低用量投与でも体重増加を示した。生後6か月のヒトの幼児でも抗生物質の投与と体重増加が関連を示していた<ref name=rob/>。 |
||
==副作用と疾病との関連== |
|||
細菌の治療において、抗生物質は病原性の細菌を殺したり増殖を抑えたりすることを期待して用いられるが、時に投与を受けた者に危害を与えることもある。ほとんどの抗生物質が経口投与により下痢を引き起こす様に普遍的な[[副作用]]もあるが、抗生物質によっては固有の副作用を生じる場合がある<ref name=":12">{{Cite journal|last=Barnhill|first=Alison E.|last2=Brewer|first2=Matt T.|last3=Carlson|first3=Steve A.|date=2012-08|title=Adverse Effects of Antimicrobials via Predictable or Idiosyncratic Inhibition of Host Mitochondrial Components|url=https://journals.asm.org/doi/10.1128/AAC.00678-12|journal=Antimicrobial Agents and Chemotherapy|volume=56|issue=8|pages=4046–4051|language=en|doi=10.1128/AAC.00678-12|issn=0066-4804|pmid=22615289|pmc=PMC3421593}}</ref>。しばしば抗生物質使用による副作用は[[アレルギー]]と同義的に扱われるが、アレルギー反応は抗生物質による副作用の一部に過ぎない。抗生物質による副作用は直接的なものと間接的なものに分けられる<ref name="General principles" />。 |
|||
アレルギー反応は抗生物質使用による直接的な副作用の代表である。[[IgE]]依存的な[[即時型アレルギー反応]]と、[[細胞性免疫]]による[[遅延型アレルギー反応]]の両者が生じうるが、特に重篤となるのは即時型アレルギー反応によるアナフィラキシーショックである。2008年にアメリカ合衆国で行われた調査<ref>{{Cite journal|last=Shehab|first=Nadine|last2=Patel|first2=Priti R.|last3=Srinivasan|first3=Arjun|last4=Budnitz|first4=Daniel S.|date=2008-09-15|title=Emergency Department Visits for Antibiotic‐Associated Adverse Events|url=https://academic.oup.com/cid/article-lookup/doi/10.1086/591126|journal=Clinical Infectious Diseases|volume=47|issue=6|pages=735–743|language=en|doi=10.1086/591126|issn=1058-4838}}</ref> では、薬剤の有害事象による救急外来の受診のうち19%が抗生物質と関係しており、その内79%がアレルギー反応に分類された<ref name="General principles" />。 |
|||
抗生物質の毒性による副作用も直接的なものであり、投与される抗生物質の量が多かったり、投与期間が長かったりする際に生じる。特に[[腎臓]]や[[肝臓]]の機能低下が生じて抗生物質の[[クリアランス (医学)|クリアランス]]に支障が生じている患者の治療で使用する際に注意が必要となる<ref name="General principles" />。軽度の副作用としてはテトラサイクリン系による歯の黄染、エリスロマイシンによる消化管の[[蠕動]]充進、リファンピシンによる色素沈着などが知られる。より重篤な副作用としてはアミノ配糖体による聴覚障害、フルオロキノロンによる関節毒性と網膜症、メトリニダゾールや[[リネゾリド]]による末梢神経障害、リネゾリドによる[[代謝性アシドーシス|乳酸アシドーシス]]や[[セロトニン症候群]]などがある<ref name=":12" />。 |
|||
間接的な副作用は[[細菌叢]]に及ぼす影響に起因するもので、クロストリジウム・ディフィシルによる腸炎に代表され<ref name="General principles" />、他にも[[性器カンジダ症|外陰膣カンジダ症]]との関連が知られる<ref>{{Cite journal|last=Gonçalves|first=Bruna|last2=Ferreira|first2=Carina|last3=Alves|first3=Carlos Tiago|last4=Henriques|first4=Mariana|last5=Azeredo|first5=Joana|last6=Silva|first6=Sónia|date=2016-11|title=Vulvovaginal candidiasis: Epidemiology, microbiology and risk factors|url=https://www.tandfonline.com/doi/full/10.3109/1040841X.2015.1091805|journal=Critical Reviews in Microbiology|volume=42|issue=6|pages=905–927|language=en|doi=10.3109/1040841X.2015.1091805|issn=1040-841X}}</ref>。 |
|||
==疾病との関連== |
|||
===クロストリジウム・ディフィシル腸炎=== |
===クロストリジウム・ディフィシル腸炎=== |
||
この[[クロストリジウム・ディフィシル腸炎]]は、抗生物質の投与等で正常な[[腸内細菌|腸内細菌叢]]が撹乱されて菌交代症が生ずる事で発生すると考えられている<ref name="MM1010_01">{{PDFlink|[http://www.eiken.co.jp/modern_media/backnumber/pdf/MM1010_01.pdf 話題の感染症 ディフィシル菌感染症の基礎と臨床] モダンメディア 2010年10月号(第56巻10号)}}</ref>。正常腸内細菌叢を掻き乱す事は、''C. difficile'' に増殖の機会を与えていることになる<ref name="eMed1942">{{Cite web|url=http://www.emedicine.com/med/topic1942.htm#section~introduction|author=Curry J|title=Pseudomembranous Colitis|publisher=WebMD|date=2007-07-20|accessdate=2008-11-17}}</ref>。つまり、この疾患は{{仮リンク|抗生物質関連下痢|en|antibiotic-associated diarrhea}}の一つである<ref name="nisshoshi.107.1897">鈴木康夫、[[doi:10.11405/nisshoshi.107.1897|抗生物質起因性腸炎の診療]] 日本消化器病学会雑誌 107巻 (2010) 12号 p.1897-1904, {{doi|10.11405/nisshoshi.107.1897}}</ref>。 |
この[[クロストリジウム・ディフィシル腸炎]]は、抗生物質の投与等で正常な[[腸内細菌|腸内細菌叢]]が撹乱されて菌交代症が生ずる事で発生すると考えられている<ref name="MM1010_01">{{PDFlink|[http://www.eiken.co.jp/modern_media/backnumber/pdf/MM1010_01.pdf 話題の感染症 ディフィシル菌感染症の基礎と臨床] モダンメディア 2010年10月号(第56巻10号)}}</ref>。正常腸内細菌叢を掻き乱す事は、''C. difficile'' に増殖の機会を与えていることになる<ref name="eMed1942">{{Cite web|url=http://www.emedicine.com/med/topic1942.htm#section~introduction|author=Curry J|title=Pseudomembranous Colitis|publisher=WebMD|date=2007-07-20|accessdate=2008-11-17}}</ref>。つまり、この疾患は{{仮リンク|抗生物質関連下痢|en|antibiotic-associated diarrhea}}の一つである<ref name="nisshoshi.107.1897">鈴木康夫、[[doi:10.11405/nisshoshi.107.1897|抗生物質起因性腸炎の診療]] 日本消化器病学会雑誌 107巻 (2010) 12号 p.1897-1904, {{doi|10.11405/nisshoshi.107.1897}}</ref>。 |
||
| 108行目: | 203行目: | ||
一部の研究者は、日常的な{{仮リンク|家畜への抗生物質使用|en|Use of antibiotics in livestock}}が''C. difficile'' などの流行に結び付く危険性があると指摘している<ref>{{Cite news|url=http://www.cbc.ca/health/story/2006/10/04/cdifficile-meat.html|publisher=CBC News|title=Scientists probe whether ''C. difficile'' is linked to eating meat|date=2006-10-04|deadurl=yes|archiveurl=https://web.archive.org/web/20061024034645/http://www.cbc.ca:80/health/story/2006/10/04/cdifficile-meat.html|archivedate=24 October 2006}}</ref>。 |
一部の研究者は、日常的な{{仮リンク|家畜への抗生物質使用|en|Use of antibiotics in livestock}}が''C. difficile'' などの流行に結び付く危険性があると指摘している<ref>{{Cite news|url=http://www.cbc.ca/health/story/2006/10/04/cdifficile-meat.html|publisher=CBC News|title=Scientists probe whether ''C. difficile'' is linked to eating meat|date=2006-10-04|deadurl=yes|archiveurl=https://web.archive.org/web/20061024034645/http://www.cbc.ca:80/health/story/2006/10/04/cdifficile-meat.html|archivedate=24 October 2006}}</ref>。 |
||
===自閉症との関連の可能性=== |
|||
[[自閉症]]児と健康児の[[腸内細菌]]を比較すると[[クロストリジウム属]]の細菌が平均して10倍程度多い状況が報告されている。乳幼児時に多種多量の抗生物質の投与により腸内細菌の組成が破壊され、クロストリジウム属の増殖とともに自閉症に至った例が紹介されている。幼い脳にダメージを与えるクロストリジウム属の神経毒素が原因であると指摘している<ref name="アランナ">アランナ・コリン著、矢野真千子訳『あなたの体は9割が細菌』 p111ほか、2016年8月30日、河出書房新社、ISBN 978-4-309-25352-7</ref>(詳細は[[自閉症]]を参照のこと)。 |
|||
== 歴史 == |
== 歴史 == |
||
{{ |
{{See also|抗菌剤の年表}} |
||
20世紀以前の世界において、感染症の治療は専ら[[伝統医学]]によって行われるものであった。抗菌性を持つ物質を利用した治療の記録は紀元前からすでに存在している<ref>{{Cite journal|last=Lindblad|first=William J.|date=2008-06|title=Review Paper: Considerations for Determining if a Natural Product Is an Effective Wound-Healing Agent|url=http://journals.sagepub.com/doi/10.1177/1534734608316028|journal=The International Journal of Lower Extremity Wounds|volume=7|issue=2|pages=75–81|language=en|doi=10.1177/1534734608316028|issn=1534-7346}}</ref>。[[古代エジプト]]や[[古代ギリシャ]]などの古代文明社会では、特定の[[カビ]]や植物を感染症の治療に利用した<ref>{{Cite journal|last=Forrest|first=R. D.|date=1982-03|title=Early history of wound treatment|url=https://pubmed.ncbi.nlm.nih.gov/7040656|journal=Journal of the Royal Society of Medicine|volume=75|issue=3|pages=198–205|issn=0141-0768|pmid=7040656|pmc=1437561}}</ref><ref>{{Cite journal|last=Wainwright|first=Milton|date=1989-01|title=Moulds in ancient and more recent medicine|url=https://linkinghub.elsevier.com/retrieve/pii/S0269915X89800102|journal=Mycologist|volume=3|issue=1|pages=21–23|language=en|doi=10.1016/S0269-915X(89)80010-2}}</ref>。また、[[ヌビア]]のミイラからは大量のテトラサイクリンが検出されている。これは当時生産されていた発酵食品などに由来するテトラサイクリンが蓄積したものであると推測されており<ref>{{Cite journal|last=Nelson|first=Mark L.|last2=Dinardo|first2=Andrew|last3=Hochberg|first3=Jeffery|last4=Armelagos|first4=George J.|date=2010-09|title=Brief communication: Mass spectroscopic characterization of tetracycline in the skeletal remains of an ancient population from Sudanese Nubia 350-550 CE|url=https://onlinelibrary.wiley.com/doi/10.1002/ajpa.21340|journal=American Journal of Physical Anthropology|volume=143|issue=1|pages=151–154|language=en|doi=10.1002/ajpa.21340}}</ref>、彼らが食事を通じたテトラサイクリンの摂取により感染症から守られていた可能性が指摘されている<ref name=":0">{{Cite journal|last=Aminov|first=Rustam I.|date=2010|title=A Brief History of the Antibiotic Era: Lessons Learned and Challenges for the Future|url=http://journal.frontiersin.org/article/10.3389/fmicb.2010.00134/abstract|journal=Frontiers in Microbiology|volume=1|doi=10.3389/fmicb.2010.00134|issn=1664-302X|pmid=21687759|pmc=PMC3109405}}</ref>。古くから行われていた治療法には有効性を検証されているものもあり、1000年前のレシピに従って野菜、ワイン、胆汁を混ぜて作った薬が[[メチシリン耐性黄色ブドウ球菌]]に対して有効性を示したとする報告が2015年になされている<ref name=":6">{{Cite journal|last=Hutchings|first=Matthew I|last2=Truman|first2=Andrew W|last3=Wilkinson|first3=Barrie|date=2019-10|title=Antibiotics: past, present and future|url=https://linkinghub.elsevier.com/retrieve/pii/S1369527419300190|journal=Current Opinion in Microbiology|volume=51|pages=72–80|language=en|doi=10.1016/j.mib.2019.10.008}}</ref><ref>{{Cite journal|last=Harrison|first=Freya|last2=Roberts|first2=Aled E. L.|last3=Gabrilska|first3=Rebecca|last4=Rumbaugh|first4=Kendra P.|last5=Lee|first5=Christina|last6=Diggle|first6=Stephen P.|editor-last=Newman|editor-first=Dianne K.|date=2015-09|title=A 1,000-Year-Old Antimicrobial Remedy with Antistaphylococcal Activity|url=https://journals.asm.org/doi/10.1128/mBio.01129-15|journal=mBio|volume=6|issue=4|language=en|doi=10.1128/mBio.01129-15|issn=2161-2129|pmid=26265721|pmc=PMC4542191}}</ref>。抗生物質への耐性の歴史も非常に古く、抗生物質が発見されるはるか昔、数十億年前からある種のβラクタマーゼは存在していたと推定されている<ref name=":0" /><ref>{{Cite journal|last=Garau|first=Gianpiero|last2=Di Guilmi|first2=Anne Marie|last3=Hall|first3=Barry G.|date=2005-07|title=Structure-based phylogeny of the metallo-beta-lactamases|url=https://pubmed.ncbi.nlm.nih.gov/15980349|journal=Antimicrobial Agents and Chemotherapy|volume=49|issue=7|pages=2778–2784|doi=10.1128/AAC.49.7.2778-2784.2005|issn=0066-4804|pmid=15980349|pmc=1168685}}</ref>。 |
|||
抗生物質の発見の前に微生物が他の微生物の増殖を抑制する現象は知られていた。例えば、1887年にはルイ・パスツールらが[[炭疽菌]]を他の好気性細菌と一緒に培養すると増殖が抑制される現象を発見している。また、1889年には Jean Paul Vuilleminが「ある生物が生存のために他の生物を殺す関係性」を抗生と定義している<ref>{{Cite journal|last=Durand|first=Guillaume André|last2=Raoult|first2=Didier|last3=Dubourg|first3=Grégory|date=2019-04|title=Antibiotic discovery: history, methods and perspectives|url=https://linkinghub.elsevier.com/retrieve/pii/S0924857918303352|journal=International Journal of Antimicrobial Agents|volume=53|issue=4|pages=371–382|language=en|doi=10.1016/j.ijantimicag.2018.11.010}}</ref>。1890年代には緑膿菌の抽出物が多くの患者に対して使用した報告がなされており、抗生物質の臨床応用に関するおそらく世界初の報告とも言われる<ref name=":6" />。 |
|||
[[ファイル:Paul Ehrlich and Sahachiro Hata.jpg|サムネイル|[[サルバルサン]]を開発したエーリッヒと秦]] |
|||
近代的な抗生物質の歴史は[[サルバルサン]]を開発した[[ポール・エーリッヒ]]と、ペニシリンを発見した[[アレクサンダー・フレミング]]の2人と結びつけられることが多く<ref name=":0" />、まずは色素に由来する合成抗菌薬が発見された<ref>{{Cite journal|last=Limbird|first=L. E.|date=2004-12-01|title=The Receptor Concept: A Continuing Evolution|url=http://molinterv.aspetjournals.org/cgi/doi/10.1124/mi.4.6.6|journal=Molecular Interventions|volume=4|issue=6|pages=326–336|language=en|doi=10.1124/mi.4.6.6|issn=1534-0384}}</ref><ref>{{Cite journal|last=Williams|first=K. J.|date=2009-08|title=The introduction of 'chemotherapy' using arsphenamine - the first magic bullet|url=https://pubmed.ncbi.nlm.nih.gov/19679737|journal=Journal of the Royal Society of Medicine|volume=102|issue=8|pages=343–348|doi=10.1258/jrsm.2009.09k036|issn=1758-1095|pmid=19679737|pmc=2726818}}</ref><ref>{{Cite journal|last=Bosch|first=Fèlix|last2=Rosich|first2=Laia|date=2008|title=The Contributions of Paul Ehrlich to Pharmacology: A Tribute on the Occasion of the Centenary of His Nobel Prize|url=https://www.karger.com/Article/FullText/149583|journal=Pharmacology|volume=82|issue=3|pages=171–179|language=english|doi=10.1159/000149583|issn=0031-7012|pmid=18679046|pmc=PMC2790789}}</ref>。エーリッヒらは当時重大な副作用の代償にわずかな効果しか得られない[[水銀|無機水銀塩]]によって治療されていた[[梅毒]]の治療薬を開発するため、[[秦佐八郎]]らと共に今日で言うところの化合物スクリーニングを1904年に開始した。彼らが1909年に試験した606番目の化合物は、梅毒に罹患したウサギに有効性を示し、後に[[ヘキスト (化学メーカー)|ヘキスト]]社によってサルバルサンとして販売される。エーリッヒはサルバルサンの開発で成功を収め、改良版であるネオサルバルサンは1940年代まで最も多く処方される治療薬だった<ref name=":0" /><ref>{{Cite journal|last=Singh|first=Ameeta E.|last2=Romanowski|first2=Barbara|date=1999-04|title=Syphilis: Review with Emphasis on Clinical, Epidemiologic, and Some Biologic Features|url=https://journals.asm.org/doi/10.1128/CMR.12.2.187|journal=Clinical Microbiology Reviews|volume=12|issue=2|pages=187–209|language=en|doi=10.1128/CMR.12.2.187|issn=0893-8512}}</ref>。彼らのスクリーニングを用いた治療薬開発の手法は他の合成抗菌薬の開発にも応用され、色素として開発された[[プロントジル]]が感染症治療薬としても有用であることが[[ゲルハルト・ドーマク]]らによって明らかにされるなど、[[サルファ剤]]を始めとした様々な抗菌薬が発見されていった<ref name=":0" />。プロントジルの抗菌性を見出したドーマクは1939年に[[ノーベル生理・医学賞]]を受賞している(ただしドーマクは[[ナチス]]の圧力を受けて一度受賞を辞退し、1947年に改めて受賞した)<ref>{{Cite journal|date=1964-11|title=Gerhard Domagk, 1895-1964|url=https://royalsocietypublishing.org/doi/10.1098/rsbm.1964.0003|journal=Biographical Memoirs of Fellows of the Royal Society|volume=10|pages=39–50|language=en|doi=10.1098/rsbm.1964.0003|issn=0080-4606}}</ref>。エーリッヒは選択毒性に基づく感染症の化学療法という概念を初めてもたらした人物でもある<ref name="hiramatsu" /><ref>{{Cite journal|last=Aminov|first=Rustam|date=2017-06|title=History of antimicrobial drug discovery: Major classes and health impact|url=https://linkinghub.elsevier.com/retrieve/pii/S0006295216303318|journal=Biochemical Pharmacology|volume=133|pages=4–19|language=en|doi=10.1016/j.bcp.2016.10.001}}</ref>。 |
|||
[[ファイル:Alexander Fleming.jpg|サムネイル|[[ペニシリン]]を発見した[[アレクサンダー・フレミング|フレミング]]]] |
|||
1928年9月3日の[[アレクサンダー・フレミング|フレミング]]による[[ペニシリン]]の発見は一つの失敗を機に成されたものであり、[[セレンディピティ]]としても知られる<ref name=":0" /><ref name=":1">{{Cite journal|last=Lobanovska|first=Mariya|last2=Pilla|first2=Giulia|date=2017-03|title=Penicillin's Discovery and Antibiotic Resistance: Lessons for the Future?|url=https://pubmed.ncbi.nlm.nih.gov/28356901|journal=The Yale Journal of Biology and Medicine|volume=90|issue=1|pages=135–145|issn=1551-4056|pmid=28356901|pmc=5369031}}</ref>。フレミングは休日を終えて当時の職場である[[セント・メアリーズ病院]]に出勤し、実験台で培養していたペトリ皿の[[ブドウ球菌]]にカビが[[コンタミネーション|コンタミ]]がしていることに気づく。この時、フレミングはコンタミしたカビが周囲の細菌の増殖を抑制している様子を観察し、この増殖抑制が[[アオカビ]]の産生する物質によるものであることと、その物質をペニシリンと名付けたことを論文として投稿した<ref name=":1" /><ref>{{Cite journal|last=Fleming|first=Alexander|date=1929-06|title=On the Antibacterial Action of Cultures of a Penicillium, with Special Reference to their Use in the Isolation of B. influenzæ|url=https://www.ncbi.nlm.nih.gov/pmc/articles/PMC2048009/|journal=British journal of experimental pathology|volume=10|issue=3|pages=226–236|issn=0007-1021|pmc=2048009}}</ref>。その後[[オックスフォード大学]]の[[ハワード・フローリー]]と[[エルンスト・ボリス・チェーン]]らの研究により大量生産が可能になると、フローリーらはペニシリンの臨床試験を1941年から1942年にかけて実施する。この臨床試験でペニシリンはなんら副作用を示さずに絶大な効果を発揮した。ペニシリンは第二次世界大戦後には広く使われる様になり、1945年にはフレミング、フローリー、チェーンの3名がペニシリンの発見とその後の研究によって[[ノーベル生理学・医学賞]]を受賞している<ref name=":1" />。 |
|||
サルバルサン、プロントジル、ペニシリンの3つの抗菌薬の発見はその後の抗菌薬の開発研究に大きな影響を与え、1950年代から1970年代にかけて抗生物質研究は黄金期を迎える<ref name=":0" />。1930年代の終わりには[[セルマン・ワクスマン]]が抗生物質の探索を開始する<ref name=":6" />。1940年代に抗生物質を定義したワクスマンは<ref name=":3" /><ref>{{Cite journal|last=Clardy|first=Jon|last2=Fischbach|first2=Michael A.|last3=Currie|first3=Cameron R.|date=2009-06|title=The natural history of antibiotics|url=https://linkinghub.elsevier.com/retrieve/pii/S096098220900918X|journal=Current Biology|volume=19|issue=11|pages=R437–R441|language=en|doi=10.1016/j.cub.2009.04.001|pmid=19515346|pmc=PMC2731226}}</ref>、[[結核]]に有効な[[ネオマイシン]]や[[ストレプトマイシン]]など多数の抗生物質を発見し<ref name=":6" />、その貢献に対して1952年にはノーベル生理学・医学賞が授与された<ref>{{Cite journal|last=Kresge|first=Nicole|last2=Simoni|first2=Robert D.|last3=Hill|first3=Robert L.|date=2004-11|title=Selman Waksman: the Father of Antibiotics|url=https://linkinghub.elsevier.com/retrieve/pii/S0021925820678619|journal=Journal of Biological Chemistry|volume=279|issue=48|pages=e7–e8|language=en|doi=10.1016/S0021-9258(20)67861-9}}</ref>。 |
|||
この時代の抗生物質の発見は土壌のスクリーニングを行って有用な微生物を発見することによって成し遂げられた。そのため、この時代の製薬会社は世界中から土壌試料を集めて回っている。例えば[[エリスロマイシン]]を産生する[[放線菌]]は、[[イーライリリー・アンド・カンパニー]]が雇っていたフィリピンの医師が1949年に庭で発見したものである<ref>{{Cite journal|last=Katz|first=Leonard|last2=Baltz|first2=Richard H|date=2016-03-01|title=Natural product discovery: past, present, and future|url=https://academic.oup.com/jimb/article/43/2-3/155/5995722|journal=Journal of Industrial Microbiology and Biotechnology|volume=43|issue=2-3|pages=155–176|language=en|doi=10.1007/s10295-015-1723-5|issn=1476-5535}}</ref>。放線菌は抗生物質を産生する主要な微生物として知られ、1945年から1978年までの間に発見された抗生物質のうち55%は放線菌に由来するものである<ref name=":6" />。この時代に発見・開発された新しい系統の抗生物質・合成抗菌剤として[[アミノグリコシド系抗生物質|アミノ配糖体]]、[[セファロスポリン]]、[[クロラムフェニコール]]、[[テトラサイクリン]]、[[マクロライド系抗菌薬|マクロマイド]]、[[キノロン]]、[[トリメトプリム]]などが挙げられる。抗生物質開発の黄金期を迎えた研究者の中には感染症の克服を期待した者もいたが、それ以降、新しい系統の抗生物質の発見はほとんどなく、一方で1990年代頃から新興感染症や薬物耐性の問題は大きくなっていった<ref>{{Cite journal|last=Conly|first=Jm|last2=Johnston|first2=Bl|date=2005|title=Where are all the new antibiotics? The new antibiotic paradox|url=http://www.hindawi.com/journals/cjidmm/2005/892058/abs/|journal=Canadian Journal of Infectious Diseases and Medical Microbiology|volume=16|issue=3|pages=159–160|language=en|doi=10.1155/2005/892058|issn=1712-9532|pmid=18159536|pmc=PMC2095020}}</ref>。 |
|||
抗生物質に対する耐性菌の出現や、新規に開発される抗生物質の減少を受けて、抗生物質の代替がこれまでに研究されている。この文脈における代替とは抗菌薬の様な化合物で細菌を制御するものではなく、細菌が感染する宿主の体を標的とした化合物や、細菌を標的とする従来の抗生物質とは異なる物質のことをいう。代表的な例として、細菌を標的とする[[抗体]]、宿主に健康上の利点をもたらす微生物と定義される[[プロバイオティクス]]、[[ファージ]]が産生して細菌を溶解する働きを持つ[[ライシン]]やファージ自体、[[自然免疫系]]を活性化する免疫賦活剤、感染を防ぐための[[ワクチン]]などが挙げられる<ref>{{Cite journal|last=Czaplewski|first=Lloyd|last2=Bax|first2=Richard|last3=Clokie|first3=Martha|last4=Dawson|first4=Mike|last5=Fairhead|first5=Heather|last6=Fischetti|first6=Vincent A|last7=Foster|first7=Simon|last8=Gilmore|first8=Brendan F|last9=Hancock|first9=Robert E W|date=2016-02|title=Alternatives to antibiotics—a pipeline portfolio review|url=https://linkinghub.elsevier.com/retrieve/pii/S1473309915004661|journal=The Lancet Infectious Diseases|volume=16|issue=2|pages=239–251|language=en|doi=10.1016/S1473-3099(15)00466-1}}</ref>。 |
|||
== 脚注 == |
== 脚注 == |
||
| 122行目: | 227行目: | ||
* {{Citation|和書|title=抗菌薬の考え方、使い方 |publisher=[[中外医学社]] |isbn=4-498-01758-7 |date=2004年8月 |year=2004 |author1=[[岩田健太郎]] |author2=宮入烈 }} |
* {{Citation|和書|title=抗菌薬の考え方、使い方 |publisher=[[中外医学社]] |isbn=4-498-01758-7 |date=2004年8月 |year=2004 |author1=[[岩田健太郎]] |author2=宮入烈 }} |
||
* {{Cite book|和書|author = |title = 生化学辞典第2版|edition = 第2版第6刷|year = 1995|publisher = [[東京化学同人]]|isbn = 4-8079-0340-3|page = |ref = 生化学辞典(2版)}} |
* {{Cite book|和書|author = |title = 生化学辞典第2版|edition = 第2版第6刷|year = 1995|publisher = [[東京化学同人]]|isbn = 4-8079-0340-3|page = |ref = 生化学辞典(2版)}} |
||
* {{Cite book|和書|title=標準微生物学|author=平松啓一・中込治 編集|edition=10|year=2009|publisher=医学書院|ISBN=978-4-260-00638-5}} |
|||
== 関連項目 == |
== 関連項目 == |
||
| 144行目: | 250行目: | ||
{{authority control}} |
{{authority control}} |
||
{{ |
{{DEFAULTSORT:こうせいふつしつ}} |
||
[[Category:薬理学]] |
[[Category:薬理学]] |
||
[[Category:抗生物質|*]] |
[[Category:抗生物質|*]] |
||
2021年9月29日 (水) 09:55時点における版

抗生物質(こうせいぶっしつ、英語: antibiotics)とは、微生物が産生し、ほかの微生物の発育を阻害する物質と定義される。広義には、微生物が産生したものを化学修飾したり人工的に合成した抗菌薬、腫瘍細胞のような微生物以外の細胞の増殖や機能を阻害する物質を含めることもある[1]。また、抗生物質の作用を利用した薬剤を指して抗生剤と呼ばれることもある。
アレクサンダー・フレミングが1928年にアオカビから見つけたペニシリンが世界初の抗生物質である。ペニシリンの発見から実用化までの間には10年もの歳月を要したものの、いったん実用化されたのちはストレプトマイシンなどの抗生物質を用いた抗菌薬が次々と開発され、人類の医療に革命をもたらした。ペニシリンの開発は20世紀でもっとも偉大な発見のひとつで「奇跡の薬」と呼ばれることがあるのも、このことによる[2]。
1990年頃には、天然由来の抗生物質は5,000〜6,000種類があると言われ、約70種類(微量成分を含めると約100種類)が実用に使われている。この他にも半合成抗生物質も80種が利用されている[1]。しかし乱用が指摘されており、抗生物質処方の50%以上は不適切であるとOECDは報告している[2]。WHOやアメリカ合衆国のCDCはガイドラインを作成し、適切な利用を呼び掛けている。日本の厚生労働省も2017年ガイドライン第1版を公開した[3]。薬剤耐性菌を生む問題があり、感染症でもないのに使用することを戒めている[3]。
名称と定義
細菌や真菌などの微生物がある環境に2種類存在する場合に、一方の生育が阻害されることがある。この抑制的な作用を抗生(antibiosis; 抗生現象・抗生作用とも[4])と呼ばれ[5]、例としてアオカビによる細菌の発育抑制が知られる[6]。抗生物質 (antibiotic) は、微生物が産生する物質で抗生作用を持つものを指す用語であり[7]、前述したアオカビによる細菌の発育抑制は、アレクサンダー・フレミングによってアオカビから発見された抗生物質であるペニシリンによるものである[8]。抗生物質の単語を初めて定義したのは、抗生物質の一種ストレプトマイシンを発見してノーベル賞を受賞したセルマン・ワクスマンである。彼は「微生物が産生し、ほかの微生物の発育を阻害する物質」の名称として抗生物質の単語を定義した[9]。ただし、この定義は抗生物質のヒトによる利用を前提としたものであり、抗生物質が高い濃度で存在しない自然界において抗生物質は抗生作用を示さないことが知られる[9][10]。一方で、細菌の代謝系を選択的に阻害して宿主の代謝系を阻害しない抗生物質は、細菌感染症の治療薬として使用される[11]。2012年の推定によると、これまでに6万-8万種類の微生物に由来する天然化合物が知られているが、その40%は抗生物質としての機能を有するとされ、その内200-220種程度の物質が微生物に直接由来する抗生物質として治療に用いられてきた[12]。また、「細菌に対して作用して感染症の治療、予防に使用されている薬剤」の総称として「抗菌薬」 (antibacterial agents) が用いられる他、「抗生物質の抗菌作用を利用した薬剤」を指す通称として「抗生剤」という用語が使用される。ただし、抗菌薬、抗生物質、抗生剤の3つは細菌に対する作用を示す薬剤の総称として厳密には区別されずに使用されている[3]。
近年では化学合成で生産されるものや、天然の誘導体から半合成されるものもある[1]。ワクスマンは微生物によって産生される物質を抗生物質と定義したが、多くのβラクタム系抗菌薬やマクロライド系抗菌薬に代表される、天然物へ人工的に修飾を加えた半合成の抗菌薬も抗生物質と呼ばれる[13]。また、ピリドンカルボン酸系(キノロン系、ニューキノロン系)やサルファ剤など、完全に人工的に合成された抗菌性物質は、厳密には抗生物質には含まず「合成抗菌薬」と呼ぶが、抗生物質として扱われることもある[9][13][14]。一方、ポリエンマクロライド系のように細菌ではなく真菌に毒性を示して真菌感染症の治療に用いられる物質や、イベルメクチンの基となった物質で抗寄生虫作用を持つアベルメクチン、「ほかの微生物」のみならず抗腫瘍活性を持つアクチノマイシン、ラパマイシンのように免疫抑制効果や抗炎症作用を示す物質も微生物に由来する薬剤として利用されている[15]。
なお、アルコールなどの消毒薬 (disinfectant) も微生物を死滅・不活化させる働きを持つが、一般に強い毒性を持つために服用はできず、抗生物質を含めた抗菌薬とは区別される[16]。
分類

抗生物質の分類は、化学構造からの分類と作用による分類の2つがある[1]。前者は新しい抗生物質の分類ができず、後者では作用機序が厳密に調べられていない抗生物質が分類できないことがある。従って両者を考慮した分類が理想的とされる[17]。
化学構造からの分類では、β-ラクタム系、アミノグリコシド系、マクロライド系、テトラサイクリン系、ペプチド系、核酸系、ポリエン系などに大別されるが、さらに細かくペニシリン系、セフェム系、モノバクタム系を加える場合もある[1]。
作用からの分類では、抗細菌性、抗カビ(真菌)性、抗腫瘍性などに分けられる。用途を重視する場合は、医療用、動物用、農業用などで分類される。作用域から、広範囲・狭域で区分される事もある[1]。作用機序から、細胞壁作用性などの呼称もある[1]。
細菌に対する作用機序による抗生物質の分類の一例としては、細胞壁合成阻害薬、タンパク質合成阻害薬、核酸合成阻害薬の3つに大きく分けるものがある[18]。また、葉酸代謝阻害薬を加えて4つに分類することもある[13]。
細胞壁合成阻害薬
細胞壁合成阻害薬に分類される抗生物質としてβラクタム系、ホスホマイシン、バンコマイシンがある。
細胞壁の合成経路
ほとんどの細菌は細胞膜の外側に細胞壁と呼ばれる構造を持つが、動物細胞はこれを持たない。細菌は一般にグラム染色の染色像によりグラム陽性菌とグラム陰性菌に分類され、両者は細胞壁の構造の違いから区別されるが、いずれの細胞壁も共通してペプチドグリカンという高分子を構成成分として持つ。細菌の細胞は高い内部浸透圧を持ち、ペプチドグリカンはこの浸透圧から細菌を保護する働きを持つ。従ってペプチドグリカンを欠く細菌は細胞膜が破裂して死んでしまう[14]。
細菌の細胞壁はムレインとも呼ばれ、2つのアミノ糖と10個のアミノ酸から構成されるムレインモノマーがレンガのように組み立てられることで細胞壁が構成される。ムレインモノマーは細胞内で合成された後に細胞外へ輸送され、グリコシルトランスフェラーゼ (GT) と呼ばれる酵素とペニシリン結合タンパク質 (PBP) と呼ばれる酵素の両者の働きによって既存の細胞壁へ架橋され、細胞壁の合成が進められる。この2つの酵素は必ずしも別の酵素であるとは限らず、大腸菌の場合はPBPが2つの酵素の働きを兼ねる。細胞壁合成阻害薬のうち、β-ラクタム系とバンコマイシンはPBPの作用を阻害するが、ホスホマイシンは細胞内におけるムレインモノマーの合成を阻害する[14]。
β-ラクタム系


β-ラクタム系の抗生物質は最も普及した抗生物質で、アメリカ合衆国で処方される抗菌薬の65%はこの系統に属する。β-ラクタム系の中でもセフェム系は特に処方されることが多く、β-ラクタム系の処方のうちおよそ半分はセフェム系の抗生物質である[19]。
β-ラクタム系はPBPの作用を阻害することでその薬理効果を発揮する。PBPは、ムレインモノマーの分子中に存在するD-アラニル-D-アラニンを認識して架橋を形成し細胞壁の合成を進めるため、D-アラニル-D-アラニンは細胞壁合成において重要な役割を果たす。ペニシリンに代表されるβ-ラクタム系の抗菌薬はこのD-アラニル-D-アラニンに類似した構造をしているため、PBPに結合し、PBPはムレインモノマーに結合できなくなってしまう。結果的に細胞壁の架橋が不十分になり、細菌は破裂死する。これがβ-ラクタム系の作用機序である[14][18]。
β-ラクタム系はその名の通り、β-ラクタム環と呼ばれる構造を持っている。β-ラクタム系ではこれに付随する側鎖の構造を変えることで抗菌スペクトルが異なる様々な抗菌薬が派生して開発されている[14]。副作用は主にアレルギー反応であり、特にアンピシリンとセファレキシンの組み合わせの様に側鎖が類似したペニシリン系とセフェム系同士では交差アレルギー反応が発現しやすい。一方、ペニシリン系やセフェム系と異なり、β-ラクタム環に付随する5員環または6員環を持たないモノバクタムはアレルギー反応が少なく、ペニシリンに対しアレルギーを示す患者にも使用される[19][20][21][22]。
バンコマイシン

β-ラクタム系がPBPと結合して細胞壁の合成を阻害するのに対し、バンコマイシンはムレインモノマーの一部であるD-アラニル-D-アラニンと結合し、GTによるムレインモノマーの重合を阻害することで作用するとされる。分子が大きいため細胞外膜を通過しにくいという難点や副作用から「最後の手段」と呼ばれることもあるが、β-ラクタム系と作用機序が異なるため、メチシリン耐性黄色ブドウ球菌の様にβ-ラクタム系の抗菌薬に対し耐性を示す細菌の感染に対し、治療薬として使用される[14][23]。
ホスホマイシン
上記2系統の細胞壁合成阻害薬と異なり、ホスホマイシンはムレインモノマーの部品となるN-アセチルムラミン酸の産生を阻害する。β-ラクタム系と併用することで相乗効果を示す[14][24]。
タンパク質合成阻害薬
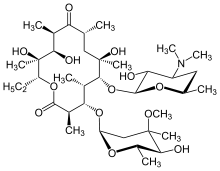
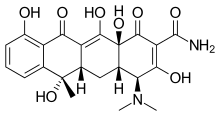
生物のDNAに保存された情報は転写によりmRNAに変換され、mRNAは翻訳されてタンパク質の合成に用いられる。リボソームはタンパク質合成の場であり、細菌の場合70Sリボソームが30Sサブユニットと50Sサブユニットの組み合わせによって構成される[18]。細菌のリボソームはヒトのリボソームとは部分的に異なった構造を持つため、タンパク質合成阻害薬は細菌のリボソームに高い親和性を持って作用する。タンパク質合成阻害薬の選択性は単に親和性に依存しており、量的な選択毒性を示す[14]。タンパク質合成阻害薬はその阻害対象によって30Sサブユニットを対象とするものと、50Sサブユニットを対象とするものの2つに大きく分類できる。前者にはアミノ配糖体とテトラサイクリン系が、後者にはクロラムフェニコール、マクロライド系が含まれる[18]。アミノ配糖体(アミノグリコシド系)は1943年にStreptomyces griseusから分離されたストレプトマイシンに代表される抗生物質で、グラム陽性菌及びグラム陰性菌両者に対する広い抗菌スペクトルを持つ[25]。一方、アミノ配糖体の細胞内への取り込みには好気呼吸が必要であり、嫌気性菌に対しては有効性を欠く[26][27]。マクロライド系は、12-16の原子によって構成される大環状ラクトンと呼ばれる構造を持つ大きな分子で[28]、毒性が低く[29]、ブドウ球菌などのグラム陽性菌に優れた抗菌力を示す[30]。代表例として1952年に発見されたエリスロマイシンなどが知られる[28]。 テトラサイクリン系も極めて抗菌スペクトルの広い抗生物質で、4つの連なった環状構造を核として持つ。テトラサイクリンの他、テトラサイクリンの側鎖を変更して脂溶性を高めたドキシサイクリン、ミノサイクリンが知られる。テトラサイクリン系抗生物質はリボソームと結合し、アミノアシル-tRNAとリボソームの結合を阻害することでタンパク質合成を阻害する[31]。 クロラムフェニコールは極めて広い抗菌スペクトルを持つ抗生物質である。しかしながら、骨髄毒性を示すなど毒性が強く、治療目的で使用されることは多くない[14][32]。
核酸合成阻害薬
核酸合成阻害薬はRNA合成阻害薬とDNA合成阻害薬に分類され、いずれも量的な選択毒性を示す。前者はRNAポリメラーゼを阻害してmRNAの合成を抑制する。リファンピシンはこの代表例で、抗結核薬として重要である[14]。
その他の抗菌薬
キノロン系やサルファ剤は核酸合成阻害を機序とした合成抗菌薬であり、狭義の抗生物質とは異なる。
キノロン系はDNA合成阻害薬でもあり、DNAジャイレースとトポイソメラーゼIVを阻害することでDNAの複製を阻害する。葉酸代謝系阻害薬はヒトが持たない葉酸代謝系を阻害するため、高い選択毒性を持つ。サルファ剤は葉酸代謝系阻害薬であり、同じ葉酸代謝系の別の経路を阻害するトリメトプリムと共にST合剤として使用される。ST合剤はグラム陽性・グラム陰性菌の他、原虫や真菌にも効果を示す[14]。
抗菌薬以外の抗生物質
ポリエンマクロライド系はエルゴステロールと呼ばれる真菌の細胞膜に特徴的なステロールに結合する。この結合によりエルゴステロールが細胞膜から奪われ、機能を阻害することで真菌に対する毒性を示す[33][34]。代表例として アムホテリシンBが知られ、重篤な全身性の真菌感染症の治療に使用される[33]。
マイトマイシンは細胞内で還元されて活性化するとDNAを架橋する働きを持つ抗生物質である。マイトマイシンを活性化する酵素は全身に分布するが、酸素が豊富な環境では還元が抑制される。従って相対的に低酸素状態にある固形がんに対し選択的に毒性を示すため、特にマイトマイシンCは抗がん剤として利用される[35][36]。
薬理

抗生物質を含む抗菌剤は、細菌が増殖するのに必要な代謝経路に作用することで、選択毒性、つまり細菌にのみ選択的に毒性を示す化学物質である。例えば、β-ラクタム系抗生物質はPBPとの親和性を持ち、細胞壁の合成を阻害するが、そのいずれもが原核生物に特有のため、人体の細胞に対してはほとんど毒性を示さない[37]。
もっとも、抗生物質の中には抗菌性のみならず、抗ウイルス、抗真菌、抗寄生虫、抗腫瘍活性を示すものが存在する[37]。また、選択毒性を示さずに、全ての生物に対して毒性を示す抗生物質も存在する。例えばピューロマイシンはtRNAにアミノ酸を付加したアミノアシルtRNAに類似した構造を持つ、放線菌に由来する抗生物質だが、産生菌を含む全ての生物においてタンパク質合成を阻害する働きを持つ。このような選択毒性を持たない抗生物質が感染症治療に利用されることはないが、タンパク質合成系の研究などの研究用途では広く用いられる[38]。
また、抗菌剤の作用は一般に殺菌と静菌に分類される。殺菌的な抗菌剤はその名の通り細菌を死滅させる。一方、静菌的な抗菌剤は細菌の増殖を抑制するのみにとどまり、静菌的な抗菌剤の濃度が低下するなどの条件下で細菌は再び増殖することができる。また、抗菌剤が効く細菌の範囲を示す用語として抗菌スペクトルが用いられる。抗菌スペクトルは細菌の分類体系に従って記述される[39]。
人類の最大の脅威であった細菌感染を克服し、平均寿命を大幅に伸ばすこととなった[40]。しかし、感染症との戦いは終わったわけではなく、治療法の開発されていない新興感染症、抗生物質の効力が薄くなるなどした再興感染症などが問題となっている。
また、抗生物質は病原性を示していない細菌にも作用するため、多量に使用すると体内の常在菌のバランスを崩してしまう場合がある。それにより常在菌が極端に減少すると、他の細菌や真菌(カビ)などが爆発的に繁殖し、病原性を示す場合もある。さらに、生き残った菌が耐性化する耐性菌の出現も問題となっている。
薬剤感受性
細菌感染症に対する化学療法に抗生物質を用いる場合は、感染起因菌の薬剤感受性を調べた上で投与する抗生物質を選択する。迅速に当たりをつけるためにはグラム染色による検体の塗抹染色を行う。正確に薬剤感受性を調べるためには、最小発育阻止濃度 (Minimum Inhibitory Concentration; MIC) の測定を行う。これは細菌の増殖を抑制しうる最小の抗生物質濃度を割り出す方法であり、液体希釈法と寒天平板希釈法の2種が知られる他、簡易的な感受性ディスク法が医療現場では広く用いられている[14]。抗菌性を評価する指標には他に最小殺菌濃度 (Minimum Bacteicidal Concentration; MBC) もあり、これは細菌の増殖を抑制するのみならず殺すために必要な抗菌剤の最小濃度を意味する。一般にMICに比べMBCは高い値を取り、その差が小さい時には抗菌剤が殺菌的、大きい時には静菌的であることを意味する[39]。これらの指標は臨床の現場で薬剤耐性を調べる目的のみならず、新規に開発された抗菌剤の活性を決定するためにも用いられる[41]。
医療における利用
抗生物質の大部分は抗菌薬として使用される。抗菌薬の投与方法は臨床薬理学の考え方が適用されている。細菌感染症に対する抗生物質の投与は、抗生物質は化学療法剤とは異なるものの、臨床医学的にはまとめて化学療法と呼ばれている。
その他、ポリエンマクロライド系抗生物質は真菌の治療に使用される。また、癌治療にはマイトマイシンCやブレオマイシン、アドリアマイシン、ドキソルビシンなどの抗生物質が使用される。またシクロスポリン、タクロリムス、エベロリムスも抗生物質であり、免疫抑制剤として膠原病、自己免疫疾患、移植医療の現場で活躍している。
抗生物質による治療
抗生物質は細菌感染を治療したり予防するために用いられるが[42]、メトロニダゾールの様に原虫感染症に効果を示すものもある。ある症状が感染に起因することが疑われ、かつそれを起因する病原体が明らかでない場合は経験的治療が行われることもある[43]。経験的治療においては結果が出るのに数日かかる培養検査の結果を待たずに、症状に基づいて広域スペクトル抗生物質が投与される[42][43]。厳密に感染起因菌を特定するためには培養などによる検査が必要だが、症状から病原体の推定が可能なこともある。例えば、蜂巣炎の病原体はレンサ球菌やブドウ球菌が尤もらしいと推定できるため、培養で陽性が得られなくとも抗菌薬による治療を開始できる[43]。重篤な感染を生じている場合などはできるだけ速やかに抗生物質を投与することが推奨される。そのため、多くの救急部門で抗生物質を備えている[44]。
病原微生物が予めわかっていたり、検査により特定された場合には、抗菌スペクトルの狭い抗生物質が投与される。抗生物質投与の費用と毒性を抑え、かつ耐性菌の出現を抑制するためには、病原体の特定が重要となる[43]。また、手術を避けるために急性虫垂炎に対して処方されることもある[45]。
培養によって病原体が特定された場合、次に薬剤感受性試験を行い、病原体が特定の抗菌薬の存在下で発育可能か試験する。薬剤感受性試験で得られたMICの値を基に、病原体が各薬剤に対し、感受性か、耐性か、あるいは中間かを決定する。感受性の場合は通常投与される抗菌薬の量で感染を治療できることを意味する。通常、この過程を経ることで有効な抗菌薬を絞り込むことが可能となる[43]。
抗生物質が予防的に用いられることもあるが、予防的な投与は免疫抑制薬を服薬中の者、がん患者、手術を受けた患者のような免疫系の弱った者への投与に限定され、特にヒト免疫不全ウイルス感染者における肺炎の防止のために投与される[42]。外科手術における抗生物質の投与は切開部位の感染を防止する。予防的な抗生物質の投与は口腔外科的な手術で重要な役割を担い、菌血症やそれに続く感染性心内膜炎を防止する。また、好中球減少症における感染防止にも使用され、これは特に化学療法によるがん治療を受けるものに対して行われる[46][47][48]。ただし、薬剤耐性菌の問題が大きくなってからは、それ以前に比べて予防投与の効果が低減している可能性もある[49]。
投与経路
抗生物質は様々な投与経路を持つ。通常は経口投与されることが多いが、全身感染症の場合などで点滴や注射によって投与されることもある[43]。感染部位が露出しているような場合は抗生物質が局所投与されることもあり、例えば結膜炎の際には結膜に対して目薬として、急性の外耳炎の場合には点耳薬として投与される。また、ニキビや蜂巣炎のような皮膚疾患の治療には外用薬として抗生物質が用いられることがある[50]。局所投与の利点は抗生物質の投与部位における濃度を高く、長く保つことができる点などにある。これにより全身的な吸収や毒性を抑え、抗生物質の投与量を減少し、それゆえに乱用の恐れを減ずることができる[51]。手術創に対する抗生物質の局所投与は、術創感染のリスクを軽減すると報告されてきた[52]。しかしながら、抗生物質の局所投与に対しては一般的に懸念材料が存在する。抗生物質が吸収されて全身へ移行する可能性もあり、その場合には抗生物質の投与量の正確な調節が困難となる。また、局所性の過敏反応や、接触性皮膚炎を生じる可能性もある[51]。
併用療法
結核などの感染症の治療においては数種類の抗生物質を同時に使用する併用療法が行われることがある[53]。併用療法は経験的治療における抗菌スペクトラムの拡大、相乗効果による治療効果の増大、耐性菌出現の抑制などを目的として行われる[54]。急性の細菌感染においては、治療効果の向上のために、単剤よりも効果の大きい複数の抗生物質の組み合わせが相乗効果を狙って投与され[55][56]、メチシリン耐性黄色ブドウ球菌の感染ではフシジン酸とリファンピシンの併用により治療が行われる[55]。グラム陰性菌感染に対して併用療法による治療を行う場合はβラクタム系にアミノ配糖体かフルオロキノロンが組み合わされる[54]。また、抗生物質の組み合わせが単剤投与の場合よりも低下する場合もあり、これを拮抗作用と呼ぶ[55]。一般的には静菌作用を持つ抗生物質と殺菌作用を持つ抗生物質の組み合わせは拮抗的である[55][56]。ただし、併用療法の有効性は実験的条件下においてのみ実証されている場合があり、例えばグラム陰性菌に対する併用療法の臨床における効果については疑問視する意見もある[54]。
抗生物質と他の抗生物質の組み合わせに加え、抗生物質が抗生物質への耐性を抑える薬剤と共に用いられることもある。例えば、β-ラクタマーゼを持つ細菌に感染した患者に対しては、βラクタム系の抗生物質がクラブラン酸やスルバクタムのようなβ-ラクタマーゼ阻害薬と併用されることがある[57]。
動植物に対する使用
抗生物質はヒトの医療においてのみならず、動物や植物に対しても使用される[58][59]。中にはヒトのみに使用されるもの、動物に対してのみ使用されるものも存在するが、多くの抗生物質はヒトとその他の動物の両者に使用される。抗生物質が投与され得る動物としてヒト以外の哺乳類、鳥類、魚類、昆虫などが例示される。また、テトラサイクリン系やストレプトマイシンなど一部の抗生物質は果樹に対しても使用される[58][60]。1997年の統計によると、ヨーロッパではヒトの医療用途で5,460,000 kgの抗生物質が使用された一方、動物への使用量も5,040,000 kgに上り、世界的に見ておよそ50%の抗生物質が動物に対して使用されると推定される[59]。また、アメリカ食品医薬品局によると、2019年の一年間でアメリカ合衆国内において動物用に販売された、医療用にも使用される抗菌薬の量は6,189,260 kgに上り、その内67%をテトラサイクリン系抗生物質が占めていた。なお、動物に対する抗菌薬の使用量は2015年の9,702,943 kgが最大となっており、それと比べると36%減少している。また、動物の種別では牛と豚に対する抗菌薬の使用がそれぞれ2,529,281 kgと2,582,399 kgに及び、これは動物に対する抗菌薬の使用量のそれぞれ41%と42%を占めている[61]。
上述の通り、ヒトに対して抗菌薬を用いる場合、抗菌薬の投与は原則的に治療を目的とする。一方、ヒト以外の動物に対して用いる場合は事情が異なる。動物の中でも犬や猫のようなペットに対して抗菌薬を用いる場合、使用方針はヒトと同様であり、原則的に感染の治療を目的として個々の動物に対して抗菌薬が用いられる。例外的に予防的投与が行われることもあるが、これは手術後など特定の条件に限られる。一方、食肉を目的として飼育される動物の場合、群の一部の個体が症状を示していて、大多数の個体が無症状でも、餌や水を通して抗菌薬が群全体に投与されることがある。このような集団単位での抗菌薬の使用がヒトに対して行われるのは稀であり、その場合も濃厚接触がある個人など特定の個人にしか用いられない[58]。
最も議論を招いているのは成長促進を目的とした経済動物に対する長期の低容量の抗菌薬の使用である。これは動物の治療を目指すものではなく、経済的利点から抗生物質が使用される。低容量の抗菌薬の長期にわたる使用は耐性菌を生じやすく、また耐性菌は動物の間のみならず食事や環境を通してヒトにも伝播しうる[58]。例えば、バンコマイシンに類似した抗生物質であるアボパルシンはグラム陽性菌に効果を示す抗生物質として家禽やブタの成長促進用途で使用されるが、アボパルシンを使用した農場ではバンコマイシン耐性腸球菌が検出されやすくなる。バンコマイシン耐性腸球菌はイギリス、ドイツ、デンマークの家畜から検出さており、この耐性菌が欧米の医療施設で急速に拡散したと考えられている[62]。加えて抗菌薬の使用による経済的な利得もないか、あっても耐性の出現に比して小さいものである[58]。一方、ヨーロッパでは2006年から成長促進を目的とした抗菌薬の使用を全面的に禁止している[63]。デンマークでの研究では家畜の成長促進を目的としたアボパルシンの使用禁止のみではバンコマイシン耐性腸球菌の検出率は下がらなかったが、さらにマクロライド系抗菌薬の使用も禁止したところ、バンコマイシン耐性腸球菌の検出率が減少した。これはバンコマイシン耐性遺伝子vanAとマクロライド耐性遺伝子ermBが連鎖して伝播することによって説明されている[62]。
畜産における抗生物質の使用は1950年代から始まっているが、植物に対してもペニシリン、ストレプトマイシン、クロルテトラサイクリン、クロラムフェニコール、オキシテトラサイクリンなどが病気から植物を守るために使用できないか1940年代後半から検討されてきた。しかしながら低容量では効果がない、高容量では毒性が問題となる、他の防除法と比して費用がかかるといった点から、実際にはストレプトマイシンとオキシテトラサイクリンが特定の病気に使用される様になったのみである。ストレプトマイシンは植物の疾患制御に使われる主要な抗生物質で、リンゴやナシの火傷病を引き起こすErwinia amylovoraや、リンゴやナシの花弁・果実に感染するPseudomonas syringae、トマトなどの斑点細菌病の原因菌であるXanthomonas campestrisなどの病原体に対して使用される。またモモなどの斑点細菌病に対してはオキシテトラサイクリンが用いられる[60]。
耐性と乱用
薬剤耐性のメカニズム
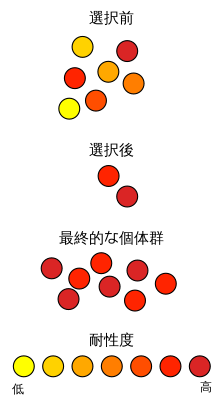
細菌学において抗菌薬が効かないことを耐性といい、耐性を持つ細菌のことを耐性菌と呼ぶ。2009年現在において使用されてきたすべての抗生物質のいずれに対しても耐性菌が報告されており、これは合成抗菌薬についても同様である[14]。例えば1940年代には事実上すべてのグラム陽性菌がペニシリンに感受性だったが[64]、1991年までに病院で検査される黄色ブドウ球菌の38%がペニシリンより強力なβラクタム系抗生物質であるメチシリンに対して耐性を示すようになった[64][65]。細菌の持つ抗生物質への耐性は、その細菌が生来持つものと、新たに獲得されるものとがある。前者の例としては緑膿菌の細胞外膜の透過性が低いことによる、多くの抗生物質への自然発生的な耐性があげられる。後者の耐性獲得に関わる機構としては、プラスミドやトランスポゾンといった外来性遺伝子の取り込むによるものに加え、染色体上の変異によって発生することもある[13]。
外来遺伝子の取り込みは遺伝子の水平伝播とも呼ばれ、細菌の進化に重要な役割を果たすが、これによってしばしば耐性遺伝子が伝達される。抗生物質は土壌などの環境中に存在する微生物に由来するが、生態学的ニッチを共有する微生物はその抗生物質に対する耐性遺伝子を持っており、その様な遺伝子が医療現場で検出される病原体の耐性遺伝子の元となる可能性が高い。また、変異により耐性を獲得する場合、感受性を持つ細菌集団の中から抗生物質の活性に影響を及ぼす遺伝子変異を起こす細胞が出現し、その細胞が抗生物質に耐えて生き残る。生き残った細胞は抗生物質の存在下では選択圧により感受性を持つ細菌を駆逐して優先となるが、耐性遺伝子は一般にコストが大きいため、抗生物質が存在しないと維持されない[66]。
薬剤耐性のメカニズムは大きく(1)抗菌薬の取り込み低下や排出促進による抗菌薬の蓄積防止、(2)抗菌薬の分解や修飾による不活化、(3)抗菌薬の標的分子の変異や修飾による親和性の低下や過剰生産による抗菌薬の量的無効化に分類される[13][18]。
抗菌薬の取り込み低下や排出促進による抗菌薬の蓄積防止による耐性機構の一例として緑膿菌の自然耐性がある。全ての抗生物質は細菌の外膜を通過し、菌体内で蓄積することで機能を発揮するが、緑膿菌の外膜は抗生物質の透過性が低く、一般に抗生物質が効きにくい。また、細胞内へ透過したβラクタム系抗生物質やキノロン系抗菌薬を排出することでも耐性を持つ[13][67]。
抗菌薬の分解や修飾による不活化は、βラクタム系のような天然の抗生物質に対する耐性の主要なメカニズムである。典型的な例としてβラクタマーゼによるβラクタム系抗生物質に対する耐性機構が知られており、βラクタマーゼはベータラクタム環構造を加水分解することで、ペニシリンをはじめとしたβラクタム系抗生物質とPBPの結合を阻害し、細菌に耐性をもたらす[13]。これまでに数百種類のラクタマーゼが発見されており、一般的にはA、B、C、Dの4種類のクラスに分類される[14][18][68]。特にニューデリー・メタロβラクタマーゼ-1 (NDM-1) と呼ばれるβラクタマーゼは他のラクタマーゼと異なり特定の菌種のみならず多数の菌種に共有される、NDM-1の遺伝子を持つプラスミドが他の系統の耐性遺伝子も持つためにプラスミドを保持する細菌が多剤耐性となる、子どもの下痢の原因となる大腸菌にも伝播しうるために環境中に広がりやすいといった特徴を持ち、世界的に保健衛生上の脅威として認識されている[69][70]。
天然物に由来する抗生物質と異なり、サルファ剤やキノロン系などの合成抗菌薬を分解・修飾する酵素は発見されていない。このような抗菌薬に対する耐性は、抗菌薬の標的分子の変異や修飾による親和性の低下や過剰生産による抗菌薬の量的無効化によって獲得される[13]。例えばキノロン系抗菌薬への耐性はDNAジャイレースやDNAトポイソメラーゼのような酵素をコードする遺伝子に変異が生じることで発生する[18]。合成抗菌薬のみならず、天然物に由来する抗生物質に対する耐性も同様の機構で獲得されることがある。例えばテトラサイクリンは16SリボソームRNAと結合することでタンパク質合成を阻害する抗生物質であるが、アクネ菌やヘリコバクター・ピロリで16SリボソームRNA遺伝子の変異による耐性獲得が報告されている[68]。
多剤耐性菌
近年においてはメチシリン耐性黄色ブドウ球菌や多剤耐性結核菌のように、複数の抗菌薬に対し耐性を示す細菌が出現している。複数の抗菌薬に対し耐性を示すことを多剤耐性 (multidrug-resistant; MDR) と呼び、また多剤耐性を持つ細菌を多剤耐性菌と呼ぶ。加えて多剤耐性菌よりもさらに耐性の多い細菌を超多剤耐性 (extensively drug-resistant; XDR) 菌、全ての抗生物質に対し耐性を示す細菌を汎耐性 (pandrug-resistant; PDR) 菌と呼び、公衆衛生上の脅威となっている[71][72]。例えば、アメリカ疾病予防管理センターはアメリカ合衆国内で年間23,000人以上が多剤耐性を示す細菌の感染によって死亡していると推定している[66]。結核菌をはじめとした多数の細菌において多剤耐性の菌株が出現しており、治療用の抗生物質への耐性のために罹患率と死亡率の増加した微生物はスーパーバグと呼ばれることもある[9]。メチシリン耐性黄色ブドウ球菌や頭文字を取ってESKAPEと呼ばれる一群の細菌種(Enterococcus faecium、Staphylococcus aureus、Klebsiella pneumoniae、Acinetobacter baumannii、Pseudomonas aeruginosa、およびエンテロバクター属菌)がこれに含まれ、多剤耐性を示す院内感染起因菌として問題視される[70][73]。
乱用防止キャンペーン

耐性菌問題に関する組織は、不必要な抗生物質の使用を削減するキャンペーンを行っている[74]。耐性菌問題への対応のため、米国では省庁横断の耐性菌タスクフォースが作られた。タスクフォースにはアメリカ疾病予防管理センター (CDC)、アメリカ食品医薬品局 (FDA)、アメリカ国立衛生研究所 (NIH)、などの機関が参加している[75]。
| 透析 | 12 - 37% |
| 小児科 | 4.0 - 46.7% |
| クリティカルケア | 14 - 60% |
| 外来 | 10.5 - 69.0% |
| 病院・三次医療機関 | 21 - 73% |
| 長期ケア施設 | 21 - 73% |
| 総合診療 (GP) | 45 - 90% |
OECDは抗生物質処方の50%以上は不適切であるとしている[2]。最も不適切な処方が行われているのは総合診療(GP)であった[2]。
一般市民を対象としたキャンペーンも行われ、アメリカではChoosing Wisely、フランスでは政府による“Antibiotics are not automatic” キャンペーンが開始され(2002年)、不必要な抗生物質の処方削減をめざしている[2][76]。
臨床ガイドライン
The first rule of antibiotics is try not to use them, and the second rule is try not to use too many of them.[77]
(抗生物質の第一のルールは使わないようにすること、第二のルールは使う種類を多くしすぎないようにすることである)—Paul L. Marino、ICUブック 第3版[78]
Choosing Wisely勧告では、呼吸器ウイルス感染症に対して抗生物質を処方してはならない[2]。米国家庭医学会(AAFP)ガイドラインでは「児童・成人の風邪に対して抗生物質を使用してはならない(should not be used, エビデンスレベルA)と勧告している[79]。米国品質保証委員会(NCQA)によるHEDISにおいては2005年から「急性気管支炎への処方はゼロにすべき(should be zero)」と勧告している[80]。
英国国立医療技術評価機構(NICE)ガイドラインでは、抗生物質の処方を控える、もしくは遅らせるべき患者として、急性中耳炎、 急性咽喉炎/急性咽頭炎/急性扁桃炎、 風邪、 急性鼻副鼻腔炎、 急性咳/急性気管支炎を挙げている[81]。日本感染症学会と日本化学療法学会の合同ガイドラインでは、ウイルス性急性気管支炎に対しては、ほかに慢性呼吸器疾患を抱えていない限り抗生物質の投与を原則として推奨しない(推奨レベルA, エビデンスレベルI)[82]。
薬剤耐性菌を生む問題があり感染症においても適正使用が言われ、感染症でもない状況での抗生物質の不適切使用は戒められる[3]。
家畜への投与等
1950年代から、米国の農家で薬用に満たない低用量の抗生物質の家畜への投与が家畜の体重増加を大幅に早めることに利用されてきた。このことは薬剤耐性菌リスクを高めることになる。EUは2006年に家畜を肥育させる目的での抗生物質の使用を禁止した[83]。 家畜においても、薬剤耐性菌リスク軽減のために日本の農林水産省は「責任ある慎重使用」を求めている[84]。なお、実験動物のマウスへの抗生物質の低用量投与でも体重増加を示した。生後6か月のヒトの幼児でも抗生物質の投与と体重増加が関連を示していた[83]。
副作用と疾病との関連
細菌の治療において、抗生物質は病原性の細菌を殺したり増殖を抑えたりすることを期待して用いられるが、時に投与を受けた者に危害を与えることもある。ほとんどの抗生物質が経口投与により下痢を引き起こす様に普遍的な副作用もあるが、抗生物質によっては固有の副作用を生じる場合がある[85]。しばしば抗生物質使用による副作用はアレルギーと同義的に扱われるが、アレルギー反応は抗生物質による副作用の一部に過ぎない。抗生物質による副作用は直接的なものと間接的なものに分けられる[43]。
アレルギー反応は抗生物質使用による直接的な副作用の代表である。IgE依存的な即時型アレルギー反応と、細胞性免疫による遅延型アレルギー反応の両者が生じうるが、特に重篤となるのは即時型アレルギー反応によるアナフィラキシーショックである。2008年にアメリカ合衆国で行われた調査[86] では、薬剤の有害事象による救急外来の受診のうち19%が抗生物質と関係しており、その内79%がアレルギー反応に分類された[43]。
抗生物質の毒性による副作用も直接的なものであり、投与される抗生物質の量が多かったり、投与期間が長かったりする際に生じる。特に腎臓や肝臓の機能低下が生じて抗生物質のクリアランスに支障が生じている患者の治療で使用する際に注意が必要となる[43]。軽度の副作用としてはテトラサイクリン系による歯の黄染、エリスロマイシンによる消化管の蠕動充進、リファンピシンによる色素沈着などが知られる。より重篤な副作用としてはアミノ配糖体による聴覚障害、フルオロキノロンによる関節毒性と網膜症、メトリニダゾールやリネゾリドによる末梢神経障害、リネゾリドによる乳酸アシドーシスやセロトニン症候群などがある[85]。
間接的な副作用は細菌叢に及ぼす影響に起因するもので、クロストリジウム・ディフィシルによる腸炎に代表され[43]、他にも外陰膣カンジダ症との関連が知られる[87]。
クロストリジウム・ディフィシル腸炎
このクロストリジウム・ディフィシル腸炎は、抗生物質の投与等で正常な腸内細菌叢が撹乱されて菌交代症が生ずる事で発生すると考えられている[88]。正常腸内細菌叢を掻き乱す事は、C. difficile に増殖の機会を与えていることになる[89]。つまり、この疾患は抗生物質関連下痢の一つである[90]。 C. difficile 腸炎の発生は、抗生物質であるニューキノロン、セファロスポリン、クリンダマイシンの使用と強く相関している[91]。
一部の研究者は、日常的な家畜への抗生物質使用がC. difficile などの流行に結び付く危険性があると指摘している[92]。
歴史
20世紀以前の世界において、感染症の治療は専ら伝統医学によって行われるものであった。抗菌性を持つ物質を利用した治療の記録は紀元前からすでに存在している[93]。古代エジプトや古代ギリシャなどの古代文明社会では、特定のカビや植物を感染症の治療に利用した[94][95]。また、ヌビアのミイラからは大量のテトラサイクリンが検出されている。これは当時生産されていた発酵食品などに由来するテトラサイクリンが蓄積したものであると推測されており[96]、彼らが食事を通じたテトラサイクリンの摂取により感染症から守られていた可能性が指摘されている[97]。古くから行われていた治療法には有効性を検証されているものもあり、1000年前のレシピに従って野菜、ワイン、胆汁を混ぜて作った薬がメチシリン耐性黄色ブドウ球菌に対して有効性を示したとする報告が2015年になされている[98][99]。抗生物質への耐性の歴史も非常に古く、抗生物質が発見されるはるか昔、数十億年前からある種のβラクタマーゼは存在していたと推定されている[97][100]。
抗生物質の発見の前に微生物が他の微生物の増殖を抑制する現象は知られていた。例えば、1887年にはルイ・パスツールらが炭疽菌を他の好気性細菌と一緒に培養すると増殖が抑制される現象を発見している。また、1889年には Jean Paul Vuilleminが「ある生物が生存のために他の生物を殺す関係性」を抗生と定義している[101]。1890年代には緑膿菌の抽出物が多くの患者に対して使用した報告がなされており、抗生物質の臨床応用に関するおそらく世界初の報告とも言われる[98]。

近代的な抗生物質の歴史はサルバルサンを開発したポール・エーリッヒと、ペニシリンを発見したアレクサンダー・フレミングの2人と結びつけられることが多く[97]、まずは色素に由来する合成抗菌薬が発見された[102][103][104]。エーリッヒらは当時重大な副作用の代償にわずかな効果しか得られない無機水銀塩によって治療されていた梅毒の治療薬を開発するため、秦佐八郎らと共に今日で言うところの化合物スクリーニングを1904年に開始した。彼らが1909年に試験した606番目の化合物は、梅毒に罹患したウサギに有効性を示し、後にヘキスト社によってサルバルサンとして販売される。エーリッヒはサルバルサンの開発で成功を収め、改良版であるネオサルバルサンは1940年代まで最も多く処方される治療薬だった[97][105]。彼らのスクリーニングを用いた治療薬開発の手法は他の合成抗菌薬の開発にも応用され、色素として開発されたプロントジルが感染症治療薬としても有用であることがゲルハルト・ドーマクらによって明らかにされるなど、サルファ剤を始めとした様々な抗菌薬が発見されていった[97]。プロントジルの抗菌性を見出したドーマクは1939年にノーベル生理・医学賞を受賞している(ただしドーマクはナチスの圧力を受けて一度受賞を辞退し、1947年に改めて受賞した)[106]。エーリッヒは選択毒性に基づく感染症の化学療法という概念を初めてもたらした人物でもある[14][107]。
1928年9月3日のフレミングによるペニシリンの発見は一つの失敗を機に成されたものであり、セレンディピティとしても知られる[97][8]。フレミングは休日を終えて当時の職場であるセント・メアリーズ病院に出勤し、実験台で培養していたペトリ皿のブドウ球菌にカビがコンタミがしていることに気づく。この時、フレミングはコンタミしたカビが周囲の細菌の増殖を抑制している様子を観察し、この増殖抑制がアオカビの産生する物質によるものであることと、その物質をペニシリンと名付けたことを論文として投稿した[8][108]。その後オックスフォード大学のハワード・フローリーとエルンスト・ボリス・チェーンらの研究により大量生産が可能になると、フローリーらはペニシリンの臨床試験を1941年から1942年にかけて実施する。この臨床試験でペニシリンはなんら副作用を示さずに絶大な効果を発揮した。ペニシリンは第二次世界大戦後には広く使われる様になり、1945年にはフレミング、フローリー、チェーンの3名がペニシリンの発見とその後の研究によってノーベル生理学・医学賞を受賞している[8]。
サルバルサン、プロントジル、ペニシリンの3つの抗菌薬の発見はその後の抗菌薬の開発研究に大きな影響を与え、1950年代から1970年代にかけて抗生物質研究は黄金期を迎える[97]。1930年代の終わりにはセルマン・ワクスマンが抗生物質の探索を開始する[98]。1940年代に抗生物質を定義したワクスマンは[13][109]、結核に有効なネオマイシンやストレプトマイシンなど多数の抗生物質を発見し[98]、その貢献に対して1952年にはノーベル生理学・医学賞が授与された[110]。
この時代の抗生物質の発見は土壌のスクリーニングを行って有用な微生物を発見することによって成し遂げられた。そのため、この時代の製薬会社は世界中から土壌試料を集めて回っている。例えばエリスロマイシンを産生する放線菌は、イーライリリー・アンド・カンパニーが雇っていたフィリピンの医師が1949年に庭で発見したものである[111]。放線菌は抗生物質を産生する主要な微生物として知られ、1945年から1978年までの間に発見された抗生物質のうち55%は放線菌に由来するものである[98]。この時代に発見・開発された新しい系統の抗生物質・合成抗菌剤としてアミノ配糖体、セファロスポリン、クロラムフェニコール、テトラサイクリン、マクロマイド、キノロン、トリメトプリムなどが挙げられる。抗生物質開発の黄金期を迎えた研究者の中には感染症の克服を期待した者もいたが、それ以降、新しい系統の抗生物質の発見はほとんどなく、一方で1990年代頃から新興感染症や薬物耐性の問題は大きくなっていった[112]。
抗生物質に対する耐性菌の出現や、新規に開発される抗生物質の減少を受けて、抗生物質の代替がこれまでに研究されている。この文脈における代替とは抗菌薬の様な化合物で細菌を制御するものではなく、細菌が感染する宿主の体を標的とした化合物や、細菌を標的とする従来の抗生物質とは異なる物質のことをいう。代表的な例として、細菌を標的とする抗体、宿主に健康上の利点をもたらす微生物と定義されるプロバイオティクス、ファージが産生して細菌を溶解する働きを持つライシンやファージ自体、自然免疫系を活性化する免疫賦活剤、感染を防ぐためのワクチンなどが挙げられる[113]。
脚注
- ^ a b c d e f g 生化学辞典第2版、p.471【抗生物質】
- ^ a b c d e f g Tackling Wasteful Spending on Health, OECD, (2017-01), doi:10.1787/9789264266414-en, ISBN 9789264266599
- ^ a b c d 厚生労働省健康局結核感染症課 (2017-06). 抗微生物薬適正使用の手引き 第一版 (pdf) (Report). 厚生労働省. 2017-12-10閲覧。
{{cite report}}:|date=の日付が不正です。 (説明) - ^ 吉川昌之介「抗生物質耐性菌の生態学 抗生物質と抗生物質耐性に関する生態学的考察; 変異 ・伝達 ・転移 ・選択」『Bulletin of Japanese Society of Microbial Ecology』第10巻第3号、1995年、141-148頁、doi:10.1264/microbes1986.10.137、ISSN 0911-7830。
- ^ Kong, Kok-Fai; Schneper, Lisa; Mathee, Kalai (2010-01). “Beta-lactam antibiotics: from antibiosis to resistance and bacteriology: BETA-LACTAM RESISTANCE” (英語). APMIS 118 (1): 1–36. doi:10.1111/j.1600-0463.2009.02563.x. PMC PMC2894812. PMID 20041868.
- ^ Foster, W.; Raoult, A. (1974-12). “Early descriptions of antibiosis”. The Journal of the Royal College of General Practitioners 24 (149): 889–894. ISSN 0035-8797. PMC 2157443. PMID 4618289.
- ^ Davies, Julian (2006-07). “Are antibiotics naturally antibiotics?” (英語). Journal of Industrial Microbiology & Biotechnology 33 (7): 496–499. doi:10.1007/s10295-006-0112-5. ISSN 1367-5435.
- ^ a b c d Lobanovska, Mariya; Pilla, Giulia (2017-03). “Penicillin's Discovery and Antibiotic Resistance: Lessons for the Future?”. The Yale Journal of Biology and Medicine 90 (1): 135–145. ISSN 1551-4056. PMC 5369031. PMID 28356901.
- ^ a b c d Davies, Julian; Davies, Dorothy (2010-09). “Origins and Evolution of Antibiotic Resistance” (英語). Microbiology and Molecular Biology Reviews 74 (3): 417–433. doi:10.1128/MMBR.00016-10. ISSN 1092-2172. PMC PMC2937522. PMID 20805405.
- ^ Davies, Julian (2006-07). “Are antibiotics naturally antibiotics?” (英語). Journal of Industrial Microbiology & Biotechnology 33 (7): 496–499. doi:10.1007/s10295-006-0112-5. ISSN 1367-5435.
- ^ Alberts, Bruce (2015). “Chapter 23: Pathogens and Infection”. Molecular biology of the cell (Sixth edition ed.). New York, NY. ISBN 978-0-8153-4432-2. OCLC 887605755
- ^ Bérdy, János (2012-08). “Thoughts and facts about antibiotics: Where we are now and where we are heading” (英語). The Journal of Antibiotics 65 (8): 385–395. doi:10.1038/ja.2012.27. ISSN 0021-8820.
- ^ a b c d e f g h i Yoneyama, Hiroshi; Katsumata, Ryoichi (2006-05-23). “Antibiotic Resistance in Bacteria and Its Future for Novel Antibiotic Development” (英語). Bioscience, Biotechnology, and Biochemistry 70 (5): 1060–1075. doi:10.1271/bbb.70.1060. ISSN 0916-8451.
- ^ a b c d e f g h i j k l m n o 平松啓一・中込治 編集「第III章 細菌学総論」『標準微生物学』(10版)、2009年。ISBN 978-4-260-00638-5。
- ^ Pham, Janette V.; Yilma, Mariamawit A.; Feliz, Adriana; Majid, Murtadha T.; Maffetone, Nicholas; Walker, Jorge R.; Kim, Eunji; Cho, Hyo Je et al. (2019-06-20). “A Review of the Microbial Production of Bioactive Natural Products and Biologics”. Frontiers in Microbiology 10: 1404. doi:10.3389/fmicb.2019.01404. ISSN 1664-302X. PMC PMC6596283. PMID 31281299.
- ^ 平松啓一・中込治 編集「第II章 環境と微生物」『標準微生物学』(10版)、2009年。ISBN 978-4-260-00638-5。
- ^ Jenkins, Amanda J.; Valentine, Jimmie L. (2012). Mozayani, Ashraf; Raymon, Lionel. eds (英語). Antimicrobial Drugs. Totowa, NJ: Humana Press. pp. 385–411. doi:10.1007/978-1-61779-222-9_10. ISBN 978-1-61779-221-2
- ^ a b c d e f g Kapoor, Garima; Saigal, Saurabh; Elongavan, Ashok (2017). “Action and resistance mechanisms of antibiotics: A guide for clinicians” (英語). Journal of Anaesthesiology Clinical Pharmacology 33 (3): 300. doi:10.4103/joacp.JOACP_349_15. ISSN 0970-9185. PMC PMC5672523. PMID 29109626.
- ^ a b Bush, Karen; Bradford, Patricia A. (2016-08). “β-Lactams and β-Lactamase Inhibitors: An Overview” (英語). Cold Spring Harbor Perspectives in Medicine 6 (8): a025247. doi:10.1101/cshperspect.a025247. ISSN 2157-1422. PMC PMC4968164. PMID 27329032.
- ^ Mirakian, R.; Leech, S. C.; Krishna, M. T.; Richter, A. G.; Huber, P. A. J.; Farooque, S.; Khan, N.; Pirmohamed, M. et al. (2015-02). “Management of allergy to penicillins and other beta-lactams” (英語). Clinical & Experimental Allergy 45 (2): 300–327. doi:10.1111/cea.12468.
- ^ Trubiano, Jason A.; Stone, Cosby A.; Grayson, M. Lindsay; Urbancic, Karen; Slavin, Monica A.; Thursky, Karin A.; Phillips, Elizabeth J. (2017-11). “The 3 Cs of Antibiotic Allergy—Classification, Cross-Reactivity, and Collaboration” (英語). The Journal of Allergy and Clinical Immunology: In Practice 5 (6): 1532–1542. doi:10.1016/j.jaip.2017.06.017. PMC PMC5681410. PMID 28843343.
- ^ Jeimy, Samira; Ben-Shoshan, Moshe; Abrams, Elissa M.; Ellis, Anne K.; Connors, Lori; Wong, Tiffany (2020-12). “Practical guide for evaluation and management of beta-lactam allergy: position statement from the Canadian Society of Allergy and Clinical Immunology” (英語). Allergy, Asthma & Clinical Immunology 16 (1): 95. doi:10.1186/s13223-020-00494-2. ISSN 1710-1492. PMC PMC7653726. PMID 33292466.
- ^ Butler, Mark S; Hansford, Karl A; Blaskovich, Mark A T; Halai, Reena; Cooper, Matthew A (2014-09). “Glycopeptide antibiotics: Back to the future” (英語). The Journal of Antibiotics 67 (9): 631–644. doi:10.1038/ja.2014.111. ISSN 0021-8820.
- ^ Falagas, Matthew E.; Vouloumanou, Evridiki K.; Samonis, George; Vardakas, Konstantinos Z. (2016-04). “Fosfomycin” (英語). Clinical Microbiology Reviews 29 (2): 321–347. doi:10.1128/CMR.00068-15. ISSN 0893-8512. PMC PMC4786888. PMID 26960938.
- ^ Jospe-Kaufman, Moriah; Siomin, Liza; Fridman, Micha (2020-07-01). “The relationship between the structure and toxicity of aminoglycoside antibiotics”. Bioorganic & Medicinal Chemistry Letters 30 (13): 127218. doi:10.1016/j.bmcl.2020.127218. ISSN 1464-3405. PMC 7194799. PMID 32360102.
- ^ Ramirez, Maria S.; Tolmasky, Marcelo E. (2010-12). “Aminoglycoside modifying enzymes”. Drug Resistance Updates: Reviews and Commentaries in Antimicrobial and Anticancer Chemotherapy 13 (6): 151–171. doi:10.1016/j.drup.2010.08.003. ISSN 1532-2084. PMC 2992599. PMID 20833577.
- ^ Krause, Kevin M.; Serio, Alisa W.; Kane, Timothy R.; Connolly, Lynn E. (2016-06). “Aminoglycosides: An Overview” (英語). Cold Spring Harbor Perspectives in Medicine 6 (6): a027029. doi:10.1101/cshperspect.a027029. ISSN 2157-1422. PMC PMC4888811. PMID 27252397.
- ^ a b Vázquez-Laslop, Nora; Mankin, Alexander S. (2018-09). “How Macrolide Antibiotics Work”. Trends in Biochemical Sciences 43 (9): 668–684. doi:10.1016/j.tibs.2018.06.011. ISSN 0968-0004. PMC 6108949. PMID 30054232.
- ^ Brook, Itzhak; Wexler, Hannah M.; Goldstein, Ellie J. C. (2013-07). “Antianaerobic antimicrobials: spectrum and susceptibility testing”. Clinical Microbiology Reviews 26 (3): 526–546. doi:10.1128/CMR.00086-12. ISSN 1098-6618. PMC 3719496. PMID 23824372.
- ^ 西野 武志「薬剤耐性菌の耐性機構に関する研究―とくに自然耐性機構の解明―」『日本化学療法学会雑誌』第62巻第2号、2014年、177-191頁。
- ^ Griffin, Michael O.; Fricovsky, Eduardo; Ceballos, Guillermo; Villarreal, Francisco (2010-09). “Tetracyclines: a pleitropic family of compounds with promising therapeutic properties. Review of the literature” (英語). American Journal of Physiology-Cell Physiology 299 (3): C539–C548. doi:10.1152/ajpcell.00047.2010. ISSN 0363-6143. PMC PMC2944325. PMID 20592239.
- ^ Oong, Ginny C.; Tadi, Prasanna (2021). Chloramphenicol. Treasure Island (FL): StatPearls Publishing. PMID 32310426
- ^ a b Robbins, Nicole; Caplan, Tavia; Cowen, Leah E. (2017-09-08). “Molecular Evolution of Antifungal Drug Resistance” (英語). Annual Review of Microbiology 71 (1): 753–775. doi:10.1146/annurev-micro-030117-020345. ISSN 0066-4227.
- ^ Ellis, David (2002-01-01). “Amphotericin B: spectrum and resistance” (英語). Journal of Antimicrobial Chemotherapy 49 (suppl_1): 7–10. doi:10.1093/jac/49.suppl_1.7. ISSN 1460-2091.
- ^ Tomasz, M. (1995-09). “Mitomycin C: small, fast and deadly (but very selective)”. Chemistry & Biology 2 (9): 575–579. doi:10.1016/1074-5521(95)90120-5. ISSN 1074-5521. PMID 9383461.
- ^ Kono, Motomichi; Kasai, Masaji (1990). “Studies on the chemistry of mitomycins.”. Journal of Synthetic Organic Chemistry, Japan 48 (9): 824–833. doi:10.5059/yukigoseikyokaishi.48.824. ISSN 0037-9980.
- ^ a b Dalhoff, Axel (2021-02). “Selective toxicity of antibacterial agents-still a valid concept or do we miss chances and ignore risks?”. Infection 49 (1): 29–56. doi:10.1007/s15010-020-01536-y. ISSN 1439-0973. PMC 7851017. PMID 33367978.
- ^ Aviner, Ranen (2020). “The science of puromycin: From studies of ribosome function to applications in biotechnology” (英語). Computational and Structural Biotechnology Journal 18: 1074–1083. doi:10.1016/j.csbj.2020.04.014. PMC PMC7229235. PMID 32435426.
- ^ a b 石田恒雄『抗菌剤の特性と抗菌メカニズム』マテリアルライフ学会、2011年2月28日。doi:10.11338/mls.23.21。2021年8月24日閲覧。
- ^ McKeown. T. (1979). The role of medicine. Oxford, Basil Blackwell.
- ^ Andrews, Jennifer M. (2001-07-01). “Determination of minimum inhibitory concentrations” (英語). Journal of Antimicrobial Chemotherapy 48 (suppl_1): 5–16. doi:10.1093/jac/48.suppl_1.5. ISSN 1460-2091.
- ^ a b c Antibiotics Simplified.. Jones & Bartlett Publishers. (2011). pp. 15–17. ISBN 978-1-4496-1459-1
- ^ a b c d e f g h i j “General principles of antimicrobial therapy”. Mayo Clinic Proceedings 86 (2): 156–67. (February 2011). doi:10.4065/mcp.2010.0639. PMC 3031442. PMID 21282489.
- ^ “Cross-sectional study on emergency department management of sepsis”. Hong Kong Medical Journal = Xianggang Yi Xue Za Zhi 24 (6): 571–578. (December 2018). doi:10.12809/hkmj177149. PMID 30429360.
- ^ “Antibiotics Versus Appendicectomy for the Treatment of Uncomplicated Acute Appendicitis: An Updated Meta-Analysis of Randomised Controlled Trials”. World Journal of Surgery 40 (10): 2305–18. (October 2016). doi:10.1007/s00268-016-3561-7. PMID 27199000.
- ^ “Antimicrobial prophylaxis and outpatient management of fever and neutropenia in adults treated for malignancy: American Society of Clinical Oncology clinical practice guideline”. Journal of Clinical Oncology 31 (6): 794–810. (February 2013). doi:10.1200/JCO.2012.45.8661. PMID 23319691.
- ^ “Infection in neutropenic patients with cancer”. Critical Care Clinics 29 (3): 411–41. (July 2013). doi:10.1016/j.ccc.2013.03.002. PMID 23830647.
- ^ Freifeld, Alison G.; Bow, Eric J.; Sepkowitz, Kent A.; Boeckh, Michael J.; Ito, James I.; Mullen, Craig A.; Raad, Issam I.; Rolston, Kenneth V. et al. (2011-02-15). “Clinical Practice Guideline for the Use of Antimicrobial Agents in Neutropenic Patients with Cancer: 2010 Update by the Infectious Diseases Society of America” (英語). Clinical Infectious Diseases 52 (4): e56–e93. doi:10.1093/cid/cir073. ISSN 1058-4838.
- ^ 冲中 敬二「抗がん剤治療患者における感染症対策について」『日本化学療法学会雑誌』第68巻第1号、2020年、132-142頁。
- ^ “Topical antibiotic treatment for uncomplicated skin and skin structure infections: review of the literature”. Expert Review of Anti-Infective Therapy 7 (8): 957–65. (October 2009). doi:10.1586/eri.09.74. PMID 19803705.
- ^ a b “Topical antimicrobial therapy for treating chronic wounds”. Clinical Infectious Diseases 49 (10): 1541–9. (November 2009). doi:10.1086/644732. PMID 19842981.
- ^ “Topical antibiotics for preventing surgical site infection in wounds healing by primary intention”. The Cochrane Database of Systematic Reviews 11 (11): CD011426. (November 2016). doi:10.1002/14651858.CD011426.pub2. PMC 6465080. PMID 27819748.
- ^ Kerantzas, Christopher A.; Jacobs, William R. (2017-05-03). Rubin, Eric J.; Collier, R. John. eds. “Origins of Combination Therapy for Tuberculosis: Lessons for Future Antimicrobial Development and Application” (英語). mBio 8 (2). doi:10.1128/mBio.01586-16. ISSN 2161-2129. PMC PMC5350467. PMID 28292983.
- ^ a b c Tamma, Pranita D.; Cosgrove, Sara E.; Maragakis, Lisa L. (2012-07). “Combination Therapy for Treatment of Infections with Gram-Negative Bacteria” (英語). Clinical Microbiology Reviews 25 (3): 450–470. doi:10.1128/CMR.05041-11. ISSN 0893-8512. PMC PMC3416487. PMID 22763634.
- ^ a b c d “Antagonism between bacteriostatic and bactericidal antibiotics is prevalent”. Antimicrobial Agents and Chemotherapy 58 (8): 4573–82. (August 2014). doi:10.1128/AAC.02463-14. PMC 4135978. PMID 24867991.
- ^ a b “Antimicrobial interactions: mechanisms and implications for drug discovery and resistance evolution”. Current Opinion in Microbiology 27: 1–9. (October 2015). doi:10.1016/j.mib.2015.05.008. PMID 26042389.
- ^ “Three decades of beta-lactamase inhibitors”. Clinical Microbiology Reviews 23 (1): 160–201. (January 2010). doi:10.1128/CMR.00037-09. PMC 2806661. PMID 20065329.
- ^ a b c d e McEwen, Scott A.; Collignon, Peter J. (2018-04-06). Aarestrup, Frank Møller; Schwarz, Stefan; Shen, Jianzhong et al.. eds. “Antimicrobial Resistance: a One Health Perspective” (英語). Microbiology Spectrum 6 (2). doi:10.1128/microbiolspec.ARBA-0009-2017. ISSN 2165-0497.
- ^ a b Teuber, M (2001-10-01). “Veterinary use and antibiotic resistance”. Current Opinion in Microbiology 4 (5): 493–499. doi:10.1016/S1369-5274(00)00241-1.
- ^ a b Sundin, George W.; Wang, Nian (2018-08-25). “Antibiotic Resistance in Plant-Pathogenic Bacteria” (英語). Annual Review of Phytopathology 56 (1): 161–180. doi:10.1146/annurev-phyto-080417-045946. ISSN 0066-4286.
- ^ “2019 Summary Report on Antimicrobials Sold or Distributed for Use in Food-Producing Animals | FDA”. www.fda.gov. 2021年9月29日閲覧。
- ^ a b Wegener, Henrik C (2003-10). “Antibiotics in animal feed and their role in resistance development” (英語). Current Opinion in Microbiology 6 (5): 439–445. doi:10.1016/j.mib.2003.09.009.
- ^ Castanon, J.I.R. (2007-11). “History of the Use of Antibiotic as Growth Promoters in European Poultry Feeds” (英語). Poultry Science 86 (11): 2466–2471. doi:10.3382/ps.2007-00249.
- ^ a b Palumbi, S. R. (2001-09-07). “Humans as the World's Greatest Evolutionary Force”. Science 293 (5536): 1786–1790. doi:10.1126/science.293.5536.1786.
- ^ Abramson, Murray A.; Sexton, Daniel J. (1999-06). “Nosocomial Methicillin-Resistant and Methicillin-Susceptible Staphylococcus Aureus Primary Bacteremia: At What Costs?” (英語). Infection Control & Hospital Epidemiology 20 (6): 408–411. doi:10.1086/501641. ISSN 0899-823X.
- ^ a b Munita, Jose M.; Arias, Cesar A. (2016-03-25). Kudva, Indira T.; Zhang, Qijing. eds. “Mechanisms of Antibiotic Resistance” (英語). Microbiology Spectrum 4 (2). doi:10.1128/microbiolspec.VMBF-0016-2015. ISSN 2165-0497. PMC PMC4888801. PMID 27227291.
- ^ Lambert, P. A. (2002). “Mechanisms of antibiotic resistance in Pseudomonas aeruginosa”. Journal of the Royal Society of Medicine 95 Suppl 41: 22–26. ISSN 0141-0768. PMC 1308633. PMID 12216271.
- ^ a b Alekshun, Michael N.; Levy, Stuart B. (2007-03). “Molecular Mechanisms of Antibacterial Multidrug Resistance” (英語). Cell 128 (6): 1037–1050. doi:10.1016/j.cell.2007.03.004.
- ^ Nordmann, Patrice; Poirel, Laurent; Carrër, Amélie; Toleman, Mark A.; Walsh, Timothy R. (2011-02). “How To Detect NDM-1 Producers” (英語). Journal of Clinical Microbiology 49 (2): 718–721. doi:10.1128/JCM.01773-10. ISSN 0095-1137. PMC PMC3043507. PMID 21123531.
- ^ a b Moellering, Robert C. (2010-12-16). “NDM-1 — A Cause for Worldwide Concern”. New England Journal of Medicine 363 (25): 2377–2379. doi:10.1056/NEJMp1011715. ISSN 0028-4793. PMID 21158655.
- ^ Magiorakos, A.-P.; Srinivasan, A.; Carey, R.B.; Carmeli, Y.; Falagas, M.E.; Giske, C.G.; Harbarth, S.; Hindler, J.F. et al. (2012-03). “Multidrug-resistant, extensively drug-resistant and pandrug-resistant bacteria: an international expert proposal for interim standard definitions for acquired resistance” (英語). Clinical Microbiology and Infection 18 (3): 268–281. doi:10.1111/j.1469-0691.2011.03570.x.
- ^ 俊英, 岡島; 雅之, 五十嵐; 陽子, 江口; 龍太郎, 内海 (2019). “多剤耐性細菌に有効な次世代型抗菌薬”. 化学と生物 57 (7): 416–427. doi:10.1271/kagakutoseibutsu.57.416.
- ^ Rice, Louis B. (2008-04-15). “Federal Funding for the Study of Antimicrobial Resistance in Nosocomial Pathogens: No ESKAPE” (英語). The Journal of Infectious Diseases 197 (8): 1079–1081. doi:10.1086/533452. ISSN 0022-1899.
- ^ Larson E (2007). “Community factors in the development of antibiotic resistance.”. Annu Rev Public Health 28: 435–447. doi:10.1146/annurev.publhealth.28.021406.144020. PMID 17094768.
- ^ CDC - Antibiotic / Antimicrobial Resistance (Report). アメリカ疾病予防管理センター. 12 March 2009.
- ^ Sabuncu E, David J, Bernède-Bauduin C et al. (2009). Klugman, Keith P.. ed. “Significant reduction of antibiotic use in the community after a nationwide campaign in France, 2002–2007”. PLoS Med 6 (6): e1000084. doi:10.1371/journal.pmed.1000084. PMC 2683932. PMID 19492093.
- ^ Marino PL (2007). “Antimicrobial therapy”. The ICU book. Hagerstown, MD: Lippincott Williams & Wilkins. p. 817. ISBN 978-0-7817-4802-5
- ^ ポール L. マリノ『ICUブック 第3版』メディカル・サイエンス・インターナショナル、2008年3月。ISBN 978-4-89592-500-6。
- ^ Fashner J, Ericson K, Werner S (2012). “Treatment of the common cold in children and adults”. Am Fam Physician 86 (2): 153–9. PMID 22962927.
- ^ Barnett, Michael L.; Linder, Jeffrey A. (2014). “Antibiotic Prescribing for Adults With Acute Bronchitis in the United States, 1996-2010”. JAMA 311 (19): 2020. doi:10.1001/jama.2013.286141. ISSN 0098-7484.
- ^ CG69: Respiratory tract infections (self-limiting): prescribing antibiotics (Report). 英国国立医療技術評価機構. 2008-07.
{{cite report}}:|date=の日付が不正です。 (説明) - ^ 一般社団法人日本感染症学会、公益社団法人日本化学療法学会 JAID/JSC感染症治療ガイド・ガイドライン作成委員会「JAID/JSC感染症治療ガイドライン―呼吸器感染症―」『日本化学療法学会雑誌』第62巻、一般社団法人日本感染症学会、公益社団法人日本化学療法学会、2014年1月、71頁。
- ^ a b ロブ・ナイト等、山田卓司等訳、「細菌が人をつくる」p139、TEDブックス、2018年5月30日、ISBN 978-4-255-01057-1
- ^ “家畜に使用する抗菌性物質について”. 農林水産省 (2016年10月27日). 2016年11月1日閲覧。
- ^ a b Barnhill, Alison E.; Brewer, Matt T.; Carlson, Steve A. (2012-08). “Adverse Effects of Antimicrobials via Predictable or Idiosyncratic Inhibition of Host Mitochondrial Components” (英語). Antimicrobial Agents and Chemotherapy 56 (8): 4046–4051. doi:10.1128/AAC.00678-12. ISSN 0066-4804. PMC PMC3421593. PMID 22615289.
- ^ Shehab, Nadine; Patel, Priti R.; Srinivasan, Arjun; Budnitz, Daniel S. (2008-09-15). “Emergency Department Visits for Antibiotic‐Associated Adverse Events” (英語). Clinical Infectious Diseases 47 (6): 735–743. doi:10.1086/591126. ISSN 1058-4838.
- ^ Gonçalves, Bruna; Ferreira, Carina; Alves, Carlos Tiago; Henriques, Mariana; Azeredo, Joana; Silva, Sónia (2016-11). “Vulvovaginal candidiasis: Epidemiology, microbiology and risk factors” (英語). Critical Reviews in Microbiology 42 (6): 905–927. doi:10.3109/1040841X.2015.1091805. ISSN 1040-841X.
- ^ 話題の感染症 ディフィシル菌感染症の基礎と臨床 モダンメディア 2010年10月号(第56巻10号) (PDF)
- ^ Curry J (2007年7月20日). “Pseudomembranous Colitis”. WebMD. 2008年11月17日閲覧。
- ^ 鈴木康夫、抗生物質起因性腸炎の診療 日本消化器病学会雑誌 107巻 (2010) 12号 p.1897-1904, doi:10.11405/nisshoshi.107.1897
- ^ Luciano, JA; Zuckerbraun, BS (December 2014). “Clostridium difficile infection: prevention, treatment, and surgical management”. The Surgical clinics of North America 94 (6): 1335–49. doi:10.1016/j.suc.2014.08.006. PMID 25440127.
- ^ “Scientists probe whether C. difficile is linked to eating meat”. CBC News. (2006年10月4日). オリジナルの24 October 2006時点におけるアーカイブ。
- ^ Lindblad, William J. (2008-06). “Review Paper: Considerations for Determining if a Natural Product Is an Effective Wound-Healing Agent” (英語). The International Journal of Lower Extremity Wounds 7 (2): 75–81. doi:10.1177/1534734608316028. ISSN 1534-7346.
- ^ Forrest, R. D. (1982-03). “Early history of wound treatment”. Journal of the Royal Society of Medicine 75 (3): 198–205. ISSN 0141-0768. PMC 1437561. PMID 7040656.
- ^ Wainwright, Milton (1989-01). “Moulds in ancient and more recent medicine” (英語). Mycologist 3 (1): 21–23. doi:10.1016/S0269-915X(89)80010-2.
- ^ Nelson, Mark L.; Dinardo, Andrew; Hochberg, Jeffery; Armelagos, George J. (2010-09). “Brief communication: Mass spectroscopic characterization of tetracycline in the skeletal remains of an ancient population from Sudanese Nubia 350-550 CE” (英語). American Journal of Physical Anthropology 143 (1): 151–154. doi:10.1002/ajpa.21340.
- ^ a b c d e f g Aminov, Rustam I. (2010). “A Brief History of the Antibiotic Era: Lessons Learned and Challenges for the Future”. Frontiers in Microbiology 1. doi:10.3389/fmicb.2010.00134. ISSN 1664-302X. PMC PMC3109405. PMID 21687759.
- ^ a b c d e Hutchings, Matthew I; Truman, Andrew W; Wilkinson, Barrie (2019-10). “Antibiotics: past, present and future” (英語). Current Opinion in Microbiology 51: 72–80. doi:10.1016/j.mib.2019.10.008.
- ^ Harrison, Freya; Roberts, Aled E. L.; Gabrilska, Rebecca; Rumbaugh, Kendra P.; Lee, Christina; Diggle, Stephen P. (2015-09). Newman, Dianne K.. ed. “A 1,000-Year-Old Antimicrobial Remedy with Antistaphylococcal Activity” (英語). mBio 6 (4). doi:10.1128/mBio.01129-15. ISSN 2161-2129. PMC PMC4542191. PMID 26265721.
- ^ Garau, Gianpiero; Di Guilmi, Anne Marie; Hall, Barry G. (2005-07). “Structure-based phylogeny of the metallo-beta-lactamases”. Antimicrobial Agents and Chemotherapy 49 (7): 2778–2784. doi:10.1128/AAC.49.7.2778-2784.2005. ISSN 0066-4804. PMC 1168685. PMID 15980349.
- ^ Durand, Guillaume André; Raoult, Didier; Dubourg, Grégory (2019-04). “Antibiotic discovery: history, methods and perspectives” (英語). International Journal of Antimicrobial Agents 53 (4): 371–382. doi:10.1016/j.ijantimicag.2018.11.010.
- ^ Limbird, L. E. (2004-12-01). “The Receptor Concept: A Continuing Evolution” (英語). Molecular Interventions 4 (6): 326–336. doi:10.1124/mi.4.6.6. ISSN 1534-0384.
- ^ Williams, K. J. (2009-08). “The introduction of 'chemotherapy' using arsphenamine - the first magic bullet”. Journal of the Royal Society of Medicine 102 (8): 343–348. doi:10.1258/jrsm.2009.09k036. ISSN 1758-1095. PMC 2726818. PMID 19679737.
- ^ Bosch, Fèlix; Rosich, Laia (2008). “The Contributions of Paul Ehrlich to Pharmacology: A Tribute on the Occasion of the Centenary of His Nobel Prize” (english). Pharmacology 82 (3): 171–179. doi:10.1159/000149583. ISSN 0031-7012. PMC PMC2790789. PMID 18679046.
- ^ Singh, Ameeta E.; Romanowski, Barbara (1999-04). “Syphilis: Review with Emphasis on Clinical, Epidemiologic, and Some Biologic Features” (英語). Clinical Microbiology Reviews 12 (2): 187–209. doi:10.1128/CMR.12.2.187. ISSN 0893-8512.
- ^ “Gerhard Domagk, 1895-1964” (英語). Biographical Memoirs of Fellows of the Royal Society 10: 39–50. (1964-11). doi:10.1098/rsbm.1964.0003. ISSN 0080-4606.
- ^ Aminov, Rustam (2017-06). “History of antimicrobial drug discovery: Major classes and health impact” (英語). Biochemical Pharmacology 133: 4–19. doi:10.1016/j.bcp.2016.10.001.
- ^ Fleming, Alexander (1929-06). “On the Antibacterial Action of Cultures of a Penicillium, with Special Reference to their Use in the Isolation of B. influenzæ”. British journal of experimental pathology 10 (3): 226–236. ISSN 0007-1021. PMC 2048009.
- ^ Clardy, Jon; Fischbach, Michael A.; Currie, Cameron R. (2009-06). “The natural history of antibiotics” (英語). Current Biology 19 (11): R437–R441. doi:10.1016/j.cub.2009.04.001. PMC PMC2731226. PMID 19515346.
- ^ Kresge, Nicole; Simoni, Robert D.; Hill, Robert L. (2004-11). “Selman Waksman: the Father of Antibiotics” (英語). Journal of Biological Chemistry 279 (48): e7–e8. doi:10.1016/S0021-9258(20)67861-9.
- ^ Katz, Leonard; Baltz, Richard H (2016-03-01). “Natural product discovery: past, present, and future” (英語). Journal of Industrial Microbiology and Biotechnology 43 (2-3): 155–176. doi:10.1007/s10295-015-1723-5. ISSN 1476-5535.
- ^ Conly, Jm; Johnston, Bl (2005). “Where are all the new antibiotics? The new antibiotic paradox” (英語). Canadian Journal of Infectious Diseases and Medical Microbiology 16 (3): 159–160. doi:10.1155/2005/892058. ISSN 1712-9532. PMC PMC2095020. PMID 18159536.
- ^ Czaplewski, Lloyd; Bax, Richard; Clokie, Martha; Dawson, Mike; Fairhead, Heather; Fischetti, Vincent A; Foster, Simon; Gilmore, Brendan F et al. (2016-02). “Alternatives to antibiotics—a pipeline portfolio review” (英語). The Lancet Infectious Diseases 16 (2): 239–251. doi:10.1016/S1473-3099(15)00466-1.
参考文献
- 岩田健太郎; 宮入烈『抗菌薬の考え方、使い方』中外医学社、2004年8月。ISBN 4-498-01758-7。
- 『生化学辞典第2版』(第2版第6刷)東京化学同人、1995年。ISBN 4-8079-0340-3。
- 平松啓一・中込治 編集『標準微生物学』(10版)医学書院、2009年。ISBN 978-4-260-00638-5。
関連項目
- 抗菌薬
- 抗ウイルス薬
- 抗真菌薬
- 抗寄生虫薬
- 感染症
- プロバイオティクス
- 殺菌 - 殺菌剤
- 消毒 - 消毒薬
- バクテリオシン
- 薬剤耐性
- 抗微生物薬耐性 antimicrobial resistance (抗菌剤耐性)
- フルクロキサシリン flucloxacillin
