マンガン酸塩
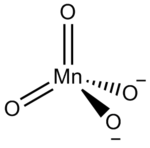
マンガン酸塩(マンガンさんえん、英: manganate)とは、マンガンのオキソアニオンの塩である[1]。ただし、通常は酸化数+6のマンガン(VI)を含むマンガン(VI)酸塩、テトラオキソマンガン(VI)酸塩を指す[1]。マンガン酸は唯一知られているマンガン(VI)化合物である[2]。
マンガン(VI)酸塩
[編集]
マンガン(VI)酸イオン、マンガン酸イオン MnO42- は四面体形で、硫酸イオンやクロム酸イオンに類似している。このことは1831年にアルハード・ミッチェルリヒによって指摘された[3]。塩はマンガン酸塩と呼ばれる。Mn-O 結合長は165.9 pmであり、過マンガン酸イオンのものより3 pm長い[3]。d1 イオンで常磁性であるが、X線回折によって検出されるヤーン・テラー効果は非常に小さい[3]。暗緑色で、可視光吸収の極大は λmax = 606 nm (ε = 1710 dm3 mol-1 cm-1) である[4][5]。ラマン分光法でも同様の報告がなされた[6]。
合成
[編集]実験室では、通常ナトリウムやカリウムのマンガン酸塩は、濃厚な水酸化物溶液 (5-10 M) と過マンガン酸塩を混合したものを24時間攪拌する[4]か、加熱する[7]ことによって合成されている。
マンガン酸カリウムは、工業的には溶融水酸化カリウムと二酸化マンガンの混合物を硝酸カリウムあるいは空気によって酸化することにより、過マンガン酸カリウムの中間生成物として合成されている[2]。
利用
[編集]マンガン酸塩、特に不溶性のマンガン酸バリウム BaMnO4 は、有機合成において酸化剤として使われている。これは一級アルコールをアルデヒド、そしてカルボン酸に、二級アルコールをケトンに酸化する[8][9]。また、ヒドラゾンをジアゾ化合物に酸化するために使われている[10]。
不均化
[編集]マンガン酸塩は、塩基性水溶液中を除いて、全て不均化に対して不安定である[2]。最終生成物は過マンガン酸塩と二酸化マンガンであるが、動力学は複雑であり、この機構にはプロトン化およびマンガン(V)種が関与している可能性がある[11][12]。
マンガン酸
[編集]MnO42- はマンガン酸 H2MnO4 の共役塩基だが、遊離酸は不安定で単離できない。しかし、放射線分解によって第二段階解離の酸解離定数が見積もられている[13]。MnO42- は酢酸イオンに比べて約100倍塩基性である[7]。
- pKa
マンガン酸は無水マンガン酸(MnO3、酸化マンガン(VI))として無水物の形を取る。無水マンガン酸は暗赤色の固体であり、過マンガン酸カリウムと炭酸ナトリウムを硫酸溶液中で反応させることで得られる。不安定な物質であり、水と容易に反応して二酸化マンガンと過マンガン酸に分解する[14]。
マンガン(V)酸塩
[編集]マンガン(V)酸イオン MnO43- の塩は、通常次亜マンガン酸塩またはテトラオキソマンガン(V)酸塩と呼ばれる明青色の塩である[15]。可視光吸収の極大は λmax = 670 nm (ε = 900 dm3 mol-1 cm-1) である[4][5]。塩基性溶液中で不安定で、マンガン(IV)酸塩と二酸化マンガンに不均化するが、この反応は非常に遅い (c(OH-) = 5–10 mol dm-3)[15]。
次亜マンガン酸塩は、マンガン酸塩を亜硫酸塩[15]、過酸化水素[16]、マンデル酸塩[5]によって注意深く還元することで得られる。次亜マンガン酸塩の中で十分に研究されたのは次亜マンガン酸カリウムのみである。次亜マンガン酸はその速い不均化のため単離できないが、放射線分解によって第三段階解離の酸解離定数が見積もられている[13]。
- pKa
過マンガン酸塩によるアルケンの酸化では、中間体として次亜マンガン酸の環状エステルが生じていると考えられている[5]。
マンガン(IV)酸塩・マンガン(III)酸塩
[編集]マンガン(IV)酸アニオンは、希過マンガン酸カリウム溶液を放射線分解することで得られる[13][16]。これは希溶液中で単核であり、紫外域で強い吸収、650 nmで弱い吸収が見られる[13]。
大抵のいわゆる「亜マンガン酸塩」は単独のオキソアニオンを含まない。ペロブスカイト型構造 (LaMnIIIO3, CaMnIVO3)、スピネル型構造 (LiMnIII,IV
2O4)、塩化ナトリウム型構造 (LiMnIIIO2, NaMnIIIO2) の亜マンガン酸塩は混合酸化物を形成している。1つの例外が二マンガン酸カリウム K6Mn2O6 で、これは単独の Mn2O66- アニオンを含む[17]。
脚注
[編集]- ^ a b International Union of Pure and Applied Chemistry (2005). Nomenclature of Inorganic Chemistry (IUPAC Recommendations 2005). Cambridge (UK): RSC–IUPAC. ISBN 0-85404-438-8. pp. 74–75, 77–78, 313, 338. Electronic version..
- ^ a b c Cotton, F. Albert; Wilkinson, Geoffrey (1980), Advanced Inorganic Chemistry (4th ed.), New York: Wiley, p. 746, ISBN 0-471-02775-8.
- ^ a b c Palenik, Gus J. (1967), “Crystal structure of potassium manganate”, Inorg. Chem. 6 (3): 507–11, doi:10.1021/ic50049a016.
- ^ a b c Carrington, A.; Symons, M. C. R. (1956), “Structure and reactivity of the oxy-anions of transition metals. Part I. The manganese oxy-anions”, J. Chem. Soc.: 3373–80, doi:10.1039/JR9560003373.
- ^ a b c d Lee, Donald G.; Chen, Tao (1993), “Reduction of manganate(VI) by mandelic acid and its significance for development of a general mechanism of oxidation of organic compounds by high-valent transition metal oxides”, J. Am. Chem. Soc. 115 (24): 11231–36, doi:10.1021/ja00077a023.
- ^ Juberta, A. H.; Varettia, E. L. (1982), “Normal and resonance Raman spectra of some manganates”, J. Mol. Struct. 79: 285–88, doi:10.1016/0022-2860(82)85067-9.
- ^ a b Nyholm, R. S.; Woolliams, P. R. (1986), “Manganates(VI)”, Inorg. Synth. 11: 56–61.
- ^ Procter, G.; Ley, S. V.; Castle, G. H. (2004), “Barium Manganate”, in Paquette, L., Encyclopedia of Reagents for Organic Synthesis, New York: Wiley, doi:10.1002/047084289.
- ^ Firouzabadi, Habib; Mostafavipoor, Zohreh (1983), “Barium Manganate. A Versatile Oxidant in Organic Synthesis”, Bull. Chem. Soc. Jpn. 56 (3): 914–17, doi:10.1246/bcsj.56.914.
- ^ Guziec, Frank S., Jr.; Murphy, Christopher J.; Cullen, Edward R. (1985), “Thermal and photochemical studies of symmetrical and unsymmetrical dihydro-1,3,4-selenadiazoles”, J. Chem. Soc., Perkin Trans. 1: 107–13, doi:10.1039/P19850000107.
- ^ Sutter, Joan H.; Colquitt, Kevin; Sutter, John R. (1974), “Kinetics of the disproportionation of manganate in acid solution”, Inorg. Chem. 13 (6): 1444–46, doi:10.1021/ic50136a037.
- ^ Sekula-Brzezińska, K.; Wrona, P. K.; Galus, Z. (1979), “Rate of the MnO4-/MnO42- and MnO42-/MnO43- electrode reactions in alkaline solutions at solid electrodes”, Electrochim. Acta 24 (5): 555–63, doi:10.1016/0013-4686(79)85032-X.
- ^ a b c d Rush, J. D.; Bielski, B. H. J. (1995), “Studies of Manganate(V), -(VI), and -(VII) Tetraoxyanions by Pulse Radiolysis. Optical Spectra of Protonated Forms”, Inorg. Chem. 34 (23): 5832–38, doi:10.1021/ic00127a022.
- ^ Anil Kumar De (2007). A Textbook Of Inorganic Chemistry. New Age International. p. 709. ISBN 8122413846
- ^ a b c Greenwood, Norman N.; Earnshaw, A. (1984), Chemistry of the Elements, Oxford: Pergamon, pp. 1221–22, ISBN 0-08-022057-6.
- ^ a b Lee, Donald G.; Chen, Tao (1989), “Oxidation of hydrocarbons. 18. Mechanism of the reaction between permanganate and carbon-carbon double bonds”, J. Am. Chem. Soc. 111 (19): 7534–38, doi:10.1021/ja00201a039.
- ^ Brachtel, G.; Hoppe, R. (1976), “Das erste Oxomanganat(III) mit Inselstruktur: K6[Mn2O6]”, Naturwissenschaften 63 (7): 339, doi:10.1007/BF00597313.
参考文献
[編集]- G. Procter, S. V. Ley, G. H. Castle “Barium Manganate” in Encyclopedia of Reagents for Organic Synthesis (Ed: L. Paquette) 2004, J. Wiley & Sons, New York. DOI: 10.1002/047084289.
- Holleman, A. F.; Wiberg, E. "Inorganic Chemistry" Academic Press: San Diego, 2001. ISBN 0-12-352651-5.







