バナドセン
| バナドセン | |
|---|---|

| |
Bis(cyclopentadienyl)vanadium | |
別称 Vanadocene | |
| 識別情報 | |
| CAS登録番号 | 1277-47-0 |
| PubChem | 18667909 |
| UNII | GZ5K54AP9L |
| |
| 特性 | |
| 化学式 | V(C5H5)2 |
| モル質量 | 181.128 g/mol |
| 外観 | 紫色結晶 |
| 融点 |
167 °C, 440 K, 333 °F |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
バナドセン(Vanadocene)またはビス(η5-シクロペンタジエニルバナジウム(Bis(η5-cyclopentadienyl) vanadium)は、有機金属化合物であり、化学式はV(C5H5)2である。Cp2Vと略される。紫色の結晶で、常磁性を持つ固体である。用途は比較的限られているものの、盛んに研究されている。
構造と結合
[編集]バナドセンは、金属イオンを2つのシクロペンタジエニル環で挟んだメタロセンの一つである。固体状態では、D5d対称性を持つ。バナジウム(II)中心は、2つのシクロペンタジエニル環から等距離で、反転中心に位置する。V-C結合長の平均は、226 pmである[1]。バナドセンのシクロペンタジエニル環は、170 K以上では動的に無秩序な状態で、108 Kまで冷やすと完全に整列する。
合成
[編集]バナドセンは1954年にバーミンガム、フィッシャー、ジェフリー・ウィルキンソンにより、二塩化バナドセンを水素化アルミニウムで還元し、その後、真空中100℃で昇華させることで合成することができる[2]。より大量生産が可能な最近の合成法では、[V2Cl3(THF)6]2[Zn2Cl6]をシクロペンタジエニルナトリウムで処理する[3]。
- 2 [V2Cl3(THF)6]2[Zn2Cl6] + 8 NaCp + THF → 4 Cp2V
性質
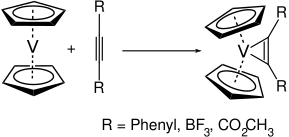
[編集]バナドセンは反応性の高い分子である。15個の価電子しか使えないが、多くの配位子と容易に反応する。例えば、アルキンと反応し、バナジウム-シクロプロペン錯体を形成する[4]。
不活性雰囲気中での一酸化炭素の関与するある反応では、イオン性のバナドセン誘導体が得られる。
- Cp2V + V(CO)6 → [Cp2V(CO)2][V(CO)6]
トルエン中で、フェロセニウム塩で処理することで容易に酸化し、モノカチオンを与える[5]。
- VCp2 + [FeCp2]BR4 → [VCp2]BR4 + FeCp2 (R = Ph or 4-C6H4F)
これらのモノカチオンは、非常に空気反応性が高く、酸化還元電位は、-1.10 Vである[5]。
高圧の一酸化炭素と反応し、CpV(CO)4を与える[6]。
出典
[編集]- ^ Robin D. Rogers; Jerry L. Atwood; Don Foust & Marvin D. Rausch (1981). “Crystal Structure of Vanadocene”. Journal of Crystal and Molecular Structure 11 (5-6): 183-188. doi:10.1007/BF01210393.
- ^ Birmingham, J. M., A. K. Fischer, and G. Wilkinson (1955). “The Reduction of Bis-cyclopentadienyl Compounds”. Naturwissenschaften 42 (4): 96. doi:10.1007/BF00617242.
- ^ Lorber, C. "Vanadium Organometallics." Chapter 5.01. Comprehensive Organometallic Chemistry III. Elsevier, 2007. 1-60.
- ^ Jordan, Markus (2009). Azine in der Koordinationssphare von Vanadocenderivaten unterschiedlicher Oxidationsstufen (PhD thesis). Universitat Oldenburg.
- ^ a b Calderazzo, Fausto, Isabella Ferri, Guido Pampaloni, and Ulli Englert (1999). “Oxidation Products of Vanadocene and of Its Permethylated Analogue, Including the Isolation and the Reactivity of the Unsolvated [VCp]Cation”. Organometallics 18 (13): 2452-2458. doi:10.1021/om9809320.
- ^ King, R.B.; Stone, F.G.A. (1963). “Cyclopentadienyl Metal Carbonyls and Some Derivatives”. Inorg. Synth. 7: 99. doi:10.1002/9780470132388.ch31.