トリフェニルホスフィン
| トリフェニルホスフィン | |
|---|---|
| |

| |

| |
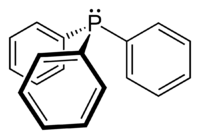
Triphenylphosphane | |
| 識別情報 | |
| CAS登録番号 | 603-35-0 |
| PubChem | 11776 |
| ChemSpider | 11283 |
| EC番号 | 210-036-0 |
| RTECS番号 | SZ3500000 |
| |
| |
| 特性 | |
| 化学式 | C18H15P |
| モル質量 | 262.29 g mol−1 |
| 外観 | 白色の固体 |
| 密度 | 1.1 g cm−3, 固体 |
| 融点 |
80 °C, 353 K, 176 °F |
| 沸点 |
377 °C, 650 K, 711 °F |
| 水への溶解度 | 溶けない |
| 屈折率 (nD) | 1.59; εr, etc. |
| 構造 | |
| 分子の形 | 三角錐形 |
| 双極子モーメント | 1.4 - 1.44 D [1] |
| 危険性 | |
| 安全データシート(外部リンク) | JT Baker |
| EU分類 | Not Listed |
| Rフレーズ | R20 R22 R40 R43 R50 R53 |
| Sフレーズ | S36 S37 S45 S57 S60 |
| 引火点 | 180 °C |
| 関連する物質 | |
| 関連するホスフィン | トリメチルホスフィン ホスフィン |
| 関連物質 | トリフェニルアミン トリフェニルアルシン |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
トリフェニルホスフィン (triphenylphosphine) は、分子式 Ph3P(Ph はフェニル基を示す)で表される一般的な有機リン化合物である。IUPACではトリフェニルホスファン (triphenylphosphane) という名称が推奨されている。TPPと省略されることもある。空気に対しても比較的安定で、室温では結晶性の固体であり、ベンゼンなどの非極性有機溶媒に可溶である。
合成法
[編集]安価であり容易に入手可能であるが、実験室では三塩化リンと臭素化フェニルマグネシウムまたはフェニルリチウムを反応させることにより合成できる。工業的には三塩化リンとベンゼンのフリーデル・クラフツ反応で作られる。熱エタノールやイソプロピルアルコールから再結晶することができる。この精製法は、しばしばトリフェニルホスフィンが空気により徐々に酸化されてできるトリフェニルホスフィンオキシド (Ph3P=O) を取り除くために用いられる。
主な有機化学反応
[編集]トリフェニルホスフィンは有機合成で広く用いられている。ハロゲン化アルキルと反応させるとホスホニウム塩を与える。
ホスホニウム塩と強塩基の反応によりイリドが生成する。これはウィッティヒ反応における重要な中間体であり、アルデヒドやケトンをアルケンに変換する際に用いられる。
また、塩素と反応させるとジクロロホスホラン Ph3PCl2 となり、反応系中で発生させておきアルコールをハロゲン化アルキルに変換するのに使われる。副生成物は と である。
アジドと反応させると窒素を発生し、P=N結合を生じる(シュタウディンガー反応)。
これを水と反応させるとアミンを遊離する(シュタウディンガー還元)。またカルボニル化合物と反応させるとイミンを形成する(アザ-ウィッティヒ反応)。
脱水縮合反応のひとつ、光延反応の試剤として DEAD とともに用いられる。
主な無機化学反応
[編集]様々な金属に対する配位子として配位化合物を作るのに使われる。ほとんどの遷移金属、特にパラジウム、白金、ロジウム、ニッケル、オスミウムに対して良く結合する。類縁体であるトリフェニルアミンの金属への結合能力は弱いことが知られている。この違いは、窒素原子はより小さいため立体的に混みあっており、金属への接近が阻害されるためである。
金属-トリフェニルホスフィン化合物を解析する際には 31P NMR 分光学が重要である。
単体硫黄 S8 を含む多くの硫黄化合物から硫黄を引き抜き、Ph3P=S を生成する。この反応は硫黄を定量するのに使うことができる。
有機リン化学
[編集]他の有機リン化合物の前駆体として一般的に用いられる。テトラヒドロフラン中でリチウムと、あるいは液体アンモニア中でナトリウムやカリウムと反応し、アルカリ金属ジフェニルホスフィド (M は Li, Na, K を表す)を与える。これらの反応では1等量のフェニルリチウムなどが副生してしまうが、注意深く酸で処理することによりベンゼンに変換することができる。調製したアルカリ金属ジフェニルホスフィドとハロゲン化アルキル RX を反応させれば が得られる。メチルジフェニルホスフィン などのホスフィン配位子はこのようにして合成できる。ジハロゲン化アルキルに対して同様の反応を行うと、ビス(ジフェニルホスフィノ)アルカンを与える。例えば1,2-ジブロモエタンと の反応では 1,2-ビス(ジフェニルホスフィノ)エタン が得られる。 に塩化アンモニウムなどの弱めの酸を加えるとジフェニルホスフィン が得られる。
トリフェニルホスフィンのスルホン化はトリス(3-スルホフェニル)ホスフィン を与える。このアニオン性のホスフィンは普通3ナトリウム塩として単離され、TPPTS (triphenylphosphine trisulfonate) として知られる。親水性の置換基を持つため、TPPTSはトリフェニルホスフィンに比べ水溶性が高い。TPPTSのロジウム錯体は工業的なヒドロホルミル化に用いられるが、これは水溶性の触媒は容易に有機溶媒から分離できるためである。
トリフェニルホスフィンを用いる人名反応
[編集]- アッペル反応 (Appel reaction)
- 光延反応
- ウィッティヒ反応
- シュタウディンガー反応 (Staudinger reaction)
- ヘック反応(パラジウムの配位子として)
- ウィルキンソン触媒やバスカ錯体 (Vaska's complex) の合成
出典
[編集]- ^ Warchol, Mark P.; DiCarlo, E.N.; Maryanoff, Cynthia A.; Mislow, Kurt (1975). “Evidence for the contribution of the lone pair to the molecular dipole moment of triarylphosphines”. Tetrahedron Letters 16 (11): 917–920. doi:10.1016/S0040-4039(00)72019-3. ISSN 00404039.

![{\displaystyle {\ce {{Ph3P}+ R-X -> \ [Ph3PR]^+ X^-}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/571231bce47c892214bd2ff54522c2f88b9e8052)








