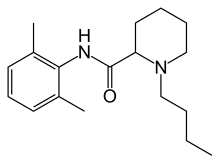
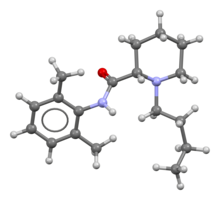
ブピバカイン
 | |
 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 発音 | [bjuːˈpɪvəkeɪn] |
| 販売名 | Marcaine, Sensorcaine, Posimir, others |
| Drugs.com | monograph |
| ライセンス | EMA:リンク、US Daily Med:リンク |
| 胎児危険度分類 | |
| 法的規制 | |
| 薬物動態データ | |
| 生物学的利用能 | n/a |
| 血漿タンパク結合 | 95% |
| 代謝 | 肝臓 |
| 作用発現 | 15分以内[4] |
| 半減期 | 3.1 hours (adults)[4] 8.1 hours (neonates)[4] |
| 作用持続時間 | 2 to 8 hr[5] |
| 排泄 | 腎臓、4–10% |
| データベースID | |
| CAS番号 |
38396-39-3 73360-54-0 |
| ATCコード | N01BB01 (WHO) |
| PubChem | CID: 2474 |
| IUPHAR/BPS | 2397 |
| DrugBank |
DB00297 |
| ChemSpider |
2380 |
| UNII |
Y8335394RO |
| KEGG |
D07552 |
| ChEBI |
CHEBI:60789 |
| ChEMBL |
CHEMBL1098 |
| 化学的データ | |
| 化学式 | C18H28N2O |
| 分子量 | 288.44 g·mol−1 |
| |
| 物理的データ | |
| 融点 | 107 - 108 °C (225 - 226 °F) |
ブピバカイン(英: Bupivacaine)とは、アミド型に分類される長時間作用型の局所麻酔薬の一つである[4]。商品名マーカイン。力価も毒性も強いが、低濃度では低い運動遮断効果と高い感覚遮断効果、すなわち分離麻酔作用が他の局所麻酔薬に比べて強い。力価は同じアミド型局所麻酔薬であるリドカインの4倍である[6]。区域麻酔では、麻酔目的の組織を支配する神経の周囲、または脊柱管の硬膜外腔に注射される[4]。すなわち、ブピバカインは浸潤麻酔、神経ブロック、硬膜外麻酔、脊髄くも膜下麻酔などに用いられる。少量のエピネフリンと混和して用いると作用持続時間が延長する[4]。通常、注入後15分以内に作用し始め、2~8時間持続する[4][5]。起こり得る副作用には、眠気、筋肉の痙攣、耳鳴り、視野の変化、低血圧、不整脈などがある[4]。高濃度ブピバカイン(0.75%)は産科麻酔には禁忌である[7]。ブピバカインは1957年に発見された[8]。世界保健機関(WHO)の必須医薬品モデル・リスト[9]に収載されている。 ブピバカインはジェネリック医薬品として入手可能である[4][10]。
適応
[編集]ブピバカインは局所浸潤、末梢神経ブロック、交感神経ブロック、硬膜外麻酔、仙骨麻酔に適応がある[7]。日本で承認されている麻酔方法は、硬膜外麻酔[11]、伝達麻酔[11]、脊髄くも膜下麻酔(腰椎麻酔)[11]、となっており、局所浸潤が含まれていない。硬膜外麻酔や伝達麻酔時の最大投与量(極量)は体重kgあたり2mgまでとされている[12]。血管への吸収を防ぎ作用時間を延長するためにエピネフリンと併用されることもある。 海外でのみ入手可能な0.75%(高濃度)の製剤は球後麻酔に使用される[13]。ブピバカインは陣痛時の硬膜外麻酔(無痛分娩)や術後の疼痛管理で最も一般的に使用されてきた局所麻酔薬であった[14]が、少なくとも日本においては、より毒性が低い長時間作用性局所麻酔薬である、レボブピバカインやロピバカインの使用が増えてきている。ブピバカインのリポソーム製剤(商品名EXPAREL)は、ブピバカインの通常の溶液よりも鎮痛効果が高いことが示されている[15][16](2023年現在、日本では未承認)。
ブピバカインとI型コラーゲンの 多剤混合薬(fixed-dose combination: FDC)(商品名ザラコール(Xaracoll))は、成人の鼠径ヘルニア手術後の術後24時間までの術後鎮痛に適応がある[17][18](2023年現在、日本では未承認)。
ブピバカイン(商品名ポジミール(Posimir))は、関節鏡視下で肩峰下腔に投与することで、鏡視下肩峰下除圧術後72時間までの術後鎮痛効果を得るために、成人において適応がある[19][20](2023年現在、日本では未承認)。なお、Posimirは5ml単回投与バイアル中に660mgのブピバカインを含有し、濃度は132mg/mLである[21]。日本でのブピバカイン製剤の最高濃度は1バイアル20ml中に100mgを含有する0.5%(5mg/mL)製剤[11]であり、これと比較すると桁違いに高濃度、高用量である。
日本麻酔科学会のガイドラインでは投与量上限は2mg/体重kgまでとなっている[22]。
硬膜外麻酔での使用
[編集]ブピバカインは1980年代から硬膜外麻酔に一般的に用いられるようになったが、これは低濃度で使用した場合、運動ブロックが軽微でも、十分な感覚ブロックが得られるためである(分離麻酔)[23]。反面、ブピバカインと同様に長時間作用性の局所麻酔薬であるエチドカインではブピバカインほどの分離麻酔効果は無い[23]。この特性は、患者の離床を妨げないので、硬膜外麻酔による無痛分娩や術後鎮痛に特に有用である[23]。

脊髄くも膜下麻酔への適応拡大
[編集]
日本では、商品名マーカインとして1969年に販売開始となっているが、適応は伝達麻酔と硬膜外麻酔に限られていた[11]。局所麻酔薬の主たる適応としては他に脊髄くも膜下麻酔があり、テトラカインやネオペルカミンSTMなどが用いられていた。一方、脊髄くも膜下麻酔に用いた際の優れた特性が報告され、1980年代から、他国で脊髄くも膜下麻酔にも用いられるようになった(米国での脊髄くも膜下麻酔への適応承認は1984年[25])。日本でも適応拡大が待望されていたが、マーカインは保存料であるパラベンを含有し、パラベンのくも膜下投与時の安全性が未確立であることから、長年適応外の状況が続いていた[26]。パラベンを含有しない脊髄くも膜下麻酔専用の製剤の治験が行われ、適応拡大となったのは初販後30年以上経過した2000年である[26]。なお、投与量の上限20mg(4mL)は、低血圧などの可逆的な有害事象が用量増加とともに増えることから臨床試験時に設定されたものである[27]。同じ濃度でも、比重が異なると力価が異なる。例えば、同じ運動ブロックを得るのに必要な量の比は高比重/等比重 = 0.72と等比重の方が力価が低い[28]。
禁忌
[編集]ブピバカインは、ブピバカインまたはアミド型局所麻酔薬に対する過敏反応既往の患者には禁忌である。 また、静脈内区域麻酔(Bierブロック)ではターニケット操作失敗による血中濃度上昇、産科の傍頸管ブロックでも、薬剤の全身吸収の懸念から、心停止が続発する危険性があるため禁忌である。 0.75%製剤は、蘇生抵抗性の心停止との関連があるため、分娩時の硬膜外麻酔では禁忌である[29]。硬膜外麻酔に用いる場合には、大量出血やショック状態の患者、注射部位やその周辺に炎症のある患者、敗血症の患者にも禁忌である[11]。脊髄くも膜下麻酔に用いる場合はさらに、髄膜炎、灰白脊髄炎、脊髄癆などの中枢神経系疾患を持つ患者や脊椎に結核、脊椎炎、転移性腫瘍などの活動性疾患のある患者に禁忌となる[30]。
副作用
[編集]他の局所麻酔薬と比較して、ブピバカインは著明な心毒性がある[31]。しかしながら、正しく投与されていれば薬物有害反応はまれである。ほとんどの反応は、注射部位からの吸収促進、偶発的血管内注入、または代謝分解の遅れによって引き起こされる。 しかし、アレルギー反応が起こることもまれにある[29]。
臨床的に重大な有害事象はブピバカインの血管経由での全身吸収に起因し、主に中枢神経系および心血管系が冒される。 通常、血漿中濃度が比較的低いときに中枢神経系が影響される。 初期には、皮質の抑制経路が選択的に阻害され、神経細胞の興奮症状を引き起こす。 血漿中濃度が高くなると、抑制性経路と興奮性経路の両方が抑制され、中枢神経系の抑制を引き起こし、昏睡状態に陥ることもある。 血漿中濃度が高くなると心血管系への影響も生じるが、心血管系の虚脱は低濃度でも起こりうる[32]。中枢神経系への有害作用は、心毒性が差し迫っていることを示している可能性があり、注意深く監視すべきである[29]。
毒性や副作用は、ブピバカインによる脊髄くも膜下麻酔中にも起こりうる。 これらの作用には、パレステジア、麻痺、無呼吸、呼吸抑制、便失禁、尿失禁などがある[注釈 1]。 さらに、ブピバカインは関節腔への持続注入後に軟骨融解を起こすことがある[29]。
ブピバカインは、硬膜外麻酔中に誤って静脈内投与された際に数人の死亡者を出している[33]。
過量投与の治療
[編集]動物実験[34][35]では、一般に入手可能な静脈内脂質乳剤であるイントラリピッドが、局所麻酔薬の過剰投与に続発する重篤な心毒性の治療に有効であることが示されており、この方法で成功したヒトの症例報告もある[36][37]。この治療をより広く普及させる計画が発表されている[38]。
妊産婦・授乳婦への使用
[編集]ブピバカインは胎盤を通過するため、胎児危険度分類Cの薬物である。 しかし、産科麻酔における正期産での使用は承認されている。 ブピバカインは母乳中に排泄される。 授乳を中止するリスクとブピバカインを中止するリスクについて医療者と患者は話し合うべきである[29]。
関節鏡下手術後の肩甲上腕関節の軟骨融解
[編集]ブピバカインは軟骨に対して毒性があり、その関節内注入は関節鏡下手術後の肩甲上腕関節の軟骨融解につながる可能性がある[39]。
薬理学
[編集]薬力学
[編集]ブピバカインは電位依存性ナトリウムチャネルの細胞内部分に結合し、神経細胞へのナトリウム流入を遮断することで脱分極を防ぐ。 脱分極がなければ、疼痛信号の開始や伝導は起こらない。
薬物動態学
[編集]ブピバカインおよび他の局所麻酔薬の全身吸収速度は、投与される薬物の用量および濃度、投与経路、投与部位の血管の多寡、製剤中のエピネフリンの有無に依存する[40]。酸解離定数pKaは8.2、蛋白結合率は95%、分配係数346と脂溶性も蛋白結合率も高い[12]。
- 作用発現(投与経路および用量に依存する):1~17分
- 作用時間(投与経路および用量に依存):2~9時間
- 力価: リドカインの4倍[6]。
- 半減期: 新生児:8.1時間、成人:2.7時間
- 血漿中濃度が最大に達するまでの時間(末梢神経ブロック、硬膜外ブロック、仙骨麻酔の場合):30~45分
- 代謝: 肝代謝
- 排泄: 腎 (6%が未変化)[29]
化学構造
[編集]リドカインと同様に、ブピバカインもアミド型局所麻酔薬である。芳香族残基と炭化水素鎖は、以前の局所麻酔薬のようにエステル結合ではなく、アミド結合で結合している。 その結果、アミド型局所麻酔薬は安定性が高く、アレルギー反応を起こしにくい。 リドカインとは異なり、ブピバカイン(およびメピバカイン、ロピバカイン、レボブピバカイン)の末端アミノ部分はピペリジン環内に含まれる。すなわち、これらの化合物はピペコリルキシリジンと総称される[14]。ブピバカインは光学異性体を持ち、ラセミ体として市販されている[41]。光学分割されてS(-)体のみとして商品化されたレボブピバカインはラセミ体のブピバカインやR(+)体のブピバカインよりも低毒性であり、日本では2008年に発売された[41]。
社会と文化
[編集]承認状況
[編集]2020年9月17日、欧州医薬品庁(EMA)の欧州医薬品委員会(CHMP)は、術後疼痛治療を目的とした医薬品Exparelの販売承認を推奨する肯定的意見を採択した[42]。この医薬品の申請者はPacira Ireland社である[42]。リポソーム製剤であるExparel liposomalは2020年11月に欧州連合(EU)で医療用として承認された[43]。
Durect社は、ブピバカインの術後用の生分解性放出制御薬物送達システムを開発している。 2010年第III相臨床試験を完了した[44]。徐放剤のSAVER-Bupicaineとして上市され、肩関節鏡視下術後疼痛への有効性が無作為化二重盲検プラセボ対照試験で証明されている[45]。
経済
[編集]ブピバカインはジェネリック医薬品として入手可能である[4][10]。
脚注
[編集]注釈
[編集]- ^ これらの作用は、脊髄全般への麻酔作用によるもので、この麻酔方法に付随する必発的なもので、一過性である。ただし、医師による厳重経過観察が必要である。
出典
[編集]- ^ “Marcaine- bupivacaine hydrochloride injection, solution Marcaine with epinephrine- bupivacaine hydrochloride and epinephrine bitartrate injection, solution”. DailyMed. 13 February 2021閲覧。
- ^ “Sensorcaine MPF- bupivacaine hydrochloride injection, solution”. DailyMed. 13 February 2021閲覧。
- ^ “Bupivacaine Use During Pregnancy”. Drugs.com (13 April 2020). 21 September 2020閲覧。
- ^ a b c d e f g h i j “Bupivacaine Hydrochloride”. The American Society of Health-System Pharmacists. 2015年6月30日時点のオリジナルよりアーカイブ。August 1, 2015閲覧。
- ^ a b Cambridge textbook of accident and emergency medicine. Cambridge: Cambridge University Press. (1997). p. 194. ISBN 9780521433792. オリジナルの2015-10-05時点におけるアーカイブ。
- ^ a b 正尚, 横山 (2007). “硬膜外麻酔に用いる局所麻酔薬の特徴”. 日本臨床麻酔学会誌 27 (5): 445–455. doi:10.2199/jjsca.27.445.
- ^ a b Shafiei, Fourutan T.; McAllister, Russell K.; Lopez, Javier (2023), Bupivacaine, StatPearls Publishing, PMID 30422478 2023年7月9日閲覧。
- ^ Pharmacology and physiology for anesthesia : foundations and clinical application. Philadelphia, PA: Elsevier/Saunders. (2013). p. 291. ISBN 9781437716795. オリジナルの2016-05-12時点におけるアーカイブ。
- ^ World Health Organization model list of essential medicines: 22nd list (2021). Geneva: World Health Organization. (2021). hdl:10665/345533. WHO/MHP/HPS/EML/2021.02
- ^ a b Tarascon Pocket Pharmacopoeia 2015 Deluxe Lab-Coat Edition. Jones & Bartlett Learning. (2015). p. 22. ISBN 9781284057560
- ^ a b c d e f “マーカイン注0.125%/マーカイン注0.25%/マーカイン注0.5%”. www.info.pmda.go.jp. 2023年7月9日閲覧。
- ^ a b 公益社団法人日本麻酔科学会 2019, p. 126.
- ^ Lexicomp. “Bupivacaine (Lexi-Drugs)”. 2014年4月10日時点のオリジナルよりアーカイブ。20 April 2014閲覧。
- ^ a b c Basics of Anesthesia. Churchill Livingstone. (November 2, 2006)
- ^ “Liposomal bupivacaine versus traditional bupivacaine for pain control after total hip arthroplasty: A meta-analysis”. Medicine 96 (25): e7190. (June 2017). doi:10.1097/MD.0000000000007190. PMC 5484209. PMID 28640101.
- ^ “Local Infiltration Analgesia With Liposomal Bupivacaine Improves Pain Scores and Reduces Opioid Use After Total Knee Arthroplasty: Results of a Randomized Controlled Trial”. The Journal of Arthroplasty 33 (1): 90–96. (January 2018). doi:10.1016/j.arth.2017.07.024. PMID 28802777.
- ^ “FDA approval letter”. U.S. Food and Drug Administration (FDA) (28 August 2020). 2 September 2020閲覧。
 この記事には現在パブリックドメインとなった次の出版物からの記述が含まれています。
この記事には現在パブリックドメインとなった次の出版物からの記述が含まれています。
- ^ "FDA Approves Xaracoll (bupivacaine HCl) Implant, a Non-opioid, Drug-device Treatment Option for Acute Postsurgical Pain Relief for up to 24 Hours Following Open Inguinal Hernia Repair in Adults" (Press release). Innocoll Pharmaceuticals. 31 August 2020. PR Newswireより2020年9月2日閲覧。
- ^ https://www.accessdata.fda.gov/drugsatfda_docs/appletter/2021/204803Orig1s000ltr.pdf en:Template:Bare URL PDF
- ^ "Durect Corporation Announces U.S. FDA Approval of Posimir For Post-Surgical Pain Reduction for up to 72 Hours Following Arthroscopic Subacromial Decompression" (Press release). Durect Corporation. 2 February 2021. PR Newswireより2021年2月13日閲覧。
- ^ https://www.facebook.com/Drugscom.+“Posimir Injection: Package Insert” (英語). Drugs.com. 2023年7月9日閲覧。
- ^ 日本麻酔科学会 2019, p. 126.
- ^ a b c Miller 2007, p. 461.
- ^ “https://twitter.com/chopper8111362/status/1699983903015268784”. X (formerly Twitter). 2023年9月9日閲覧。
- ^ “These highlights do not include all the information needed to use BUPIVACAINE SPINAL safely and effectively. See full prescribing information for BUPIVACAINE SPINAL. BUPIVACAINE SPINAL (bupivacaine hydrochloride in dextrose injection) for subarachnoid injection Initial U.S. Approval: 1984”. dailymed.nlm.nih.gov. 2023年8月19日閲覧。
- ^ a b “医薬インタビューフォーム マーカイン注脊麻用0.5%等比重 マーカイン注脊麻用0.5%高比重”. サンド株式会社. 2023年8月19日閲覧。
- ^ アストラゼネカ株式会社 2010, p. 215.
- ^ Parums, Dinah V. (2023-08-01). “Editorial: First Regulatory Approval for Allogeneic Pancreatic Islet Beta Cell Infusion for Adult Patients with Type 1 Diabetes Mellitus” (英語). Medical Science Monitor 29. doi:10.12659/MSM.941918. ISSN 1643-3750. PMC PMC10403990. PMID 37525584.
- ^ a b c d e f g “Bupivacaine (Lexi-Drugs)”. 2014年4月10日時点のオリジナルよりアーカイブ。20 April 2014閲覧。
- ^ “マーカイン注脊麻用0.5%等比重/マーカイン注脊麻用0.5%高比重”. www.info.pmda.go.jp. 2023年7月9日閲覧。
- ^ “[Cardiotoxicity of local anesthetics]”. Cahiers d'Anesthésiologie 41 (6): 589–598. (1993). PMID 8287299.
- ^ Australian Medicines Handbook. Adelaide. (2006). ISBN 978-0-9757919-2-9
- ^ “Filipino nurse dies in UK due to wrong use of anaesthetic”. ABS-CBN Interactive (28 January 2014). 9 July 2007時点のオリジナルよりアーカイブ。2014年1月28日閲覧。
- ^ “Pretreatment or resuscitation with a lipid infusion shifts the dose-response to bupivacaine-induced asystole in rats”. Anesthesiology 88 (4): 1071–1075. (April 1998). doi:10.1097/00000542-199804000-00028. PMID 9579517.
- ^ “Lipid emulsion infusion rescues dogs from bupivacaine-induced cardiac toxicity”. Regional Anesthesia and Pain Medicine 28 (3): 198–202. (2003). doi:10.1053/rapm.2003.50041. PMID 12772136.
- ^ “Successful use of a 20% lipid emulsion to resuscitate a patient after a presumed bupivacaine-related cardiac arrest”. Anesthesiology 105 (1): 217–218. (July 2006). doi:10.1097/00000542-200607000-00033. PMID 16810015.
- ^ “Successful resuscitation of a patient with ropivacaine-induced asystole after axillary plexus block using lipid infusion”. Anaesthesia 61 (8): 800–801. (August 2006). doi:10.1111/j.1365-2044.2006.04740.x. PMID 16867094.
- ^ “Lipid emulsion to treat overdose of local anaesthetic: the gift of the glob”. Anaesthesia 61 (2): 107–109. (February 2006). doi:10.1111/j.1365-2044.2005.04494.x. PMID 16430560.
- ^ “Articular cartilage and local anaesthetic: A systematic review of the current literature”. Journal of Orthopaedics 12 (Suppl 2): S200–S210. (December 2015). doi:10.1016/j.jor.2015.10.005. PMC 4796530. PMID 27047224.
- ^ “bupivacaine hydrochloride (Bupivacaine Hydrochloride) injection, solution”. FDA. 21 April 2014時点のオリジナルよりアーカイブ。20 April 2014閲覧。
- ^ a b 山蔭道明 (2009). “新しい局所麻酔薬レボブピバカイン概要”. 日本臨床麻酔学会誌 29: 275-289.
- ^ a b “Exparel: Pending EC decision”. European Medicines Agency (EMA) (17 September 2020). 21 September 2020閲覧。 Text was copied from this source which is © European Medicines Agency. Reproduction is authorized provided the source is acknowledged.
- ^ “Exparel liposomal EPAR”. European Medicines Agency (EMA) (15 September 2020). 11 December 2020閲覧。
- ^ “Bupivacaine Effectiveness and Safety in SABER Trial (BESST)”. ClinicalTrials.gov (20 January 2010). 2011年12月27日時点のオリジナルよりアーカイブ。2012年3月1日閲覧。
- ^ Ekelund, Anders; Peredistijs, Andrejs; Grohs, Josef; Meisner, Jon; Verity, Neil; Rasmussen, Sten (2022-05-01). “SABER-Bupivacaine Reduces Postoperative Pain and Opioid Consumption After Arthroscopic Subacromial Decompression: A Randomized, Placebo-Controlled Trial”. Journal of the American Academy of Orthopaedic Surgeons. Global Research & Reviews 6 (5): e21.00287. doi:10.5435/JAAOSGlobal-D-21-00287. ISSN 2474-7661. PMID 35584248.
参考文献
[編集]- アストラゼネカ株式会社『マーカイン注脊麻用0.5%等比重及びマーカイン注脊麻用0.5%等比重に関する資料』アストラゼネカ株式会社、2010年9月3日。
- 日本麻酔科学会「V 局所麻酔薬」『麻酔薬および麻酔関連薬使用ガイドライン』(第3版第4訂)公益社団法人日本麻酔科学会、2019年5月28日。
- Miller, Ronald 著、武田純三 訳『ミラー麻酔科学』メディカルサイエンスインターナショナル、2007年4月1日。ISBN 9784895924658。
外部リンク
[編集]- “Bupivacaine” (英語). PubChem. U.S. National Library of Medicine. 2023年7月9日閲覧。 - ブピバカインの特性について詳述されている。
