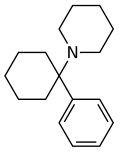
フェンサイクリジン
 | |
 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| Drugs.com | entry |
| 法的規制 |
|
| 嗜癖傾向 | 中程度[1] |
| 薬物動態データ | |
| 作用発現 | 2〜60分[2] |
| 半減期 | 7〜46時間 |
| 作用持続時間 | 6〜48時間[2] |
| データベースID | |
| CAS番号 |
77-10-1 |
| ATCコード | none |
| PubChem | CID: 6468 |
| IUPHAR/BPS | 4282 |
| DrugBank |
DB03575 |
| ChemSpider |
6224 |
| UNII |
J1DOI7UV76 |
| KEGG |
C07575 |
| ChEBI |
CHEBI:8058 |
| ChEMBL |
CHEMBL275528 |
| 化学的データ | |
| 化学式 | C17H25N |
| 分子量 | 243.387 g/mol |
| |
フェンサイクリジン(フェンシクリジン、英語: Phencyclidine、略称: PCP)は、ベンゼンとシクロヘキサンとピペリジンが結合したアリルシクロヘキシルアミン系の化合物である。静脈注射することによって作用を発揮する解離性麻酔薬であり、俗にエンジェルダストと呼ばれる。
近似の物質に麻酔薬のケタミンがある[3]。フェンサイクリジンによる、暴力など興奮性の副作用のため、後にケタミンが開発されている。これら解離性麻酔薬は呼吸を抑制する副作用がない点では安全である。ケタミンとともに「クラブドラッグ」に分類される場合が多い[4]。
向精神薬に関する条約のスケジュールIIに指定され、日本では麻薬及び向精神薬取締法の麻薬に指定されている[5]。NMDA受容体拮抗剤に分類される。
歴史
[編集]1952年にアメリカ合衆国の製薬会社パーク・デービス社により麻酔薬として開発された。1963年に外科手術麻酔薬としてセルニールという名称で認可されたが、麻酔から覚醒する際に妄想や突発的な暴力などの副作用が起こることが判明したために1965年にはヒトへの使用が断念された[3]。1967年から動物への麻酔薬としてセルニランという名称で販売されている[3]。
後に、幻覚剤として乱用されるようになった。しばしば自分の肉体を離れるなど解離の感覚が生じる[3]。乱用者の多くが統合失調症に類似した症状を呈するため、同障害のモデルとして使用されることがある。
薬理
[編集]ドーパミンD2受容体への結合親和性は、Ki=2.7nM[6]。ヒトクローン化D2受容体への親和性を有する[6]。D2(High)受容体パーシャルアゴニスト作用を有する[7]。
本来、ドーパミン神経細胞に対するフェンサイクリジンの急性作用は抑制性であるが、フェンサイクリジンの慢性投与は興奮性に転換し、その作用は薬剤投与の中止後も長期間持続することが示されている[8]。
乱用による症状
[編集]1978年の報告書では、外部刺激への感度、刺激、解離、高揚感、陶酔、鎮静、多幸感、知覚障害、不穏、見当識障害、不安、偏執病、過剰な興奮、易刺激性、錯乱、言語障害、構音障害、認知障害(持続的)、記憶障害(持続的)、吃音(約1年間)、自己表現困難(約1年間)、気分障害、うつ病、仕事や学校での能力低下、眼振、痙攣[9]。同報告書では、大麻よりも強力で、LSDに匹敵すると言われている[9]。
乱用者の多くが統合失調症の陽性症状と陰性症状に類似した症状を呈する[10]。
研究用途
[編集]統合失調症様のモデル動物を作成する際に用いられる[10][11][12][13][14][15]。
出典
[編集]- ^ “Chapter 15: Reinforcement and Addictive Disorders”. Molecular Neuropharmacology: A Foundation for Clinical Neuroscience (2nd ed.). New York: McGraw-Hill Medical. (2009). pp. 374–375. ISBN 9780071481274. "Phencyclidine (PCP or angel dust) and ketamine (also known as special K) are structurally related drugs that are classified as dissociative anesthetics. These drugs are distinguished from other psychotomimetic agents, such as hallucinogens, by their distinct spectrum of pharmacologic effects, including their reinforcing properties and risks related to compulsive abuse ... The reinforcing properties of PCP and ketamine are mediated by the binding of these drugs to specific sites in the channel of the NMDA glutamate receptor, where they act as noncompetitive antagonists. PCP is self-administered directly into the NAc, where its reinforcing effects are believed to result from the blockade of excitatory glutamatergic input to the same medium spiny NAc neurons inhibited by opioids and dopamine"
- ^ a b Riviello, Ralph J. (2010). Manual of forensic emergency medicine : a guide for clinicians. Sudbury, Mass.: Jones and Bartlett Publishers. pp. 41–42. ISBN 9780763744625
- ^ a b c d レスター・グリンスプーン、ジェームズ・B. バカラー 『サイケデリック・ドラッグ-向精神物質の科学と文化』 杵渕幸子訳、妙木浩之訳、工作舎、2000年。ISBN 978-4875023210。62-65頁。Psychedelic Drugs Reconsidered, 1979
- ^ Bertram G.Katzung 著、柳沢輝行ほか訳『カッツング薬理学 原書第10版』、丸善株式会社、平成21年3月25日 発行、P562
- ^ 麻薬、麻薬原料植物、向精神薬及び麻薬向精神薬原料を指定する政令(平成2年8月1日政令第238号 - e-Gov法令検索
- ^ a b c Seeman P, et al. (2005-9). “Dopamine receptor contribution to the action of PCP, LSD and ketamine psychotomimetics.”. en:Molecular Psychiatry. 10 (9): 877-83. doi:10.1038/sj.mp.4001682. PMID 15852061.
- ^ Seeman P, et al. (2009-8). “Dopamine D2High receptors stimulated by phencyclidines, lysergic acid diethylamide, salvinorin A, and modafinil.”. en:Synapse. 63 (8): 698-704. doi:10.1002/syn.20647. PMID 19391150.
- ^ “薬物依存の神経機序の発見:幻覚剤のドーパミン神経への作用は、慢性投与の結果、抑制から興奮に転換する”. 自治医科大学医学部 (2014年2月21日). 2016年12月13日閲覧。
- ^ a b Petersen RC, Stillman RC., ed (1978-8). “The phencyclidine psychosis: phenomenology and treatment.”. Phencyclidine (PCP) Abuse: An Appraisal. (Rockville, Maryland.: en:National Institute on Drug Abuse.).
- ^ a b “フェンサイクリジン作用機序におけるGluN2Dサブユニットの役割”. 東京都精神医学総合研究所. 2016年12月13日閲覧。
- ^ 野田幸裕名, 鍋島俊隆, 毛利彰宏、統合失調症様行動の評価法 『日本薬理学雑誌』 2007年 130巻 2号 p.117-123, doi:10.1254/fpj.130.117
- ^ 野田幸裕, 鍋島俊隆、フェンシクリジン誘発精神分裂病陰性症状動物モデルの神経精神薬理学的研究 『YAKUGAKU ZASSHI.』 2000 年 120 巻 8 号 p. 677-682, doi:10.1248/yakushi1947.120.8_677、日本薬学会
- ^ “精神分裂病モデル動物としてのフェンサイクリジン投与ラット脳の超微形態”. 日本学術振興会(JSPS). 2016年12月25日閲覧。
- ^ “統合失調症モデル動物:陰性症状の評価法”. 日本神経精神薬理学会 (2013年4月). 2016年12月25日閲覧。
- ^ “薬効薬理試験 » 中枢神経系関連 » 統合失調症”. 日本バイオリサーチセンター. 2016年12月25日閲覧。
関連項目
[編集]- ケタミン - フェンサイクリジンの副作用を改良した解離性麻酔薬
