ハロゲン結合
ハロゲン結合(ハロゲンけつごう、英: halogen bond、略称: XB)は、ハロゲン原子(ルイス酸)とルイス塩基との間に働く非共有結合性相互作用である。ハロゲンはその他の結合(例: 共有結合)にも関与するが、ハロゲン結合は特にハロゲンが求電子種として働く場合を指す。
結合
[編集]ハロゲン結合と水素結合の比較:
水素結合:
ハロゲン結合:
どちらの場合においても、D(ドナー、供与体)は、電子不足の化学種(HあるいはX)を提供する原子あるいは原子団、分子である。Hは水素結合に関与する水素原子であり、Xはハロゲン結合に関与するハロゲンである。A(アクセプター、受容体)は電子豊富な化学種を意味する。
ハロゲン結合と水素結合の類似関係は容易に見て取ることができる。どちらの結合でも、電子供与体/電子受容体の関係が存在する。この2種の結合の違いは、何の化学種が電子供与体/電子受容体として働くかである。水素結合では、水素原子が電子受容体として働き、電子豊富な部位(電子供与体)から電子密度を受け取り、非共有結合性相互作用を形成する。ハロゲン結合では、ハロゲン原子が電子受容体である。電子密度移動の結果として、ファンデルワールス半径より小さい距離まで原子間距離が近づく[1]。

ハロゲン結合に関与するハロゲン原子は、ヨウ素 (I)、臭素 (Br)、塩素 (Cl)、そしてたまにフッ素 (F) である。この4種のハロゲンは全てハロゲン結合供与体として作用できることが理論的、実験的に証明されており、結合の強さは一般的に F < Cl < Br < I の順で、通常ヨウ素が最も強い相互作用を形成する[2]。
ジハロゲン分子(I2、Br2他)は強いハロゲン結合を形成する傾向がある。塩素およびフッ素のハロゲン結合形成における強さと有効性は、ハロゲン結合供与体の性質に依存する。ハロゲン原子が電気陰性度の高い(電子求引性)部位と結合している場合は、強いハロゲン結合が形成されやすい[3]。
例えば、ヨウ化パーフルオロアルカン類はハロゲン結合結晶工学のためにうまくデザインされている。さらに、フッ素原子と結合したアルキルグループが電気陰性でないのが、F2が強いハロゲン結合供与体として働くのに対して、フッ化炭素が弱いハロゲン結合供与体である理由である。さらに、ルイス塩基(ハロゲン結合受容体)は、同様に電気的に陰性であり、アニオン(陰イオン)は中性分子よりもよいハロゲン結合受容体である。
ハロゲン結合は、強力かつ特異的、指向性を有する相互作用であり、よく明確に定義された構造を生じさせる。ハロゲン結合の強さは 5-180 kJ/molの範囲である。ハロゲン結合の強度は水素結合よりも少しだけ弱いが、競合できる。ハロゲン結合は180°の角度で形成されやすいことが、オッド・ハッセルによる1954年の臭素と1,4-ジオキサンに関する研究で示されている[4]。ハロゲン結合の強さに寄与するもう一つの因子は、ハロゲン(ルイス酸、ハロゲン結合供与体)とルイス塩基(ハロゲン結合受容体)との短い距離からくる。ハロゲン結合の引力的性質によって、供与体と受容体の距離がファンデルワールス半径の和よりも短くなる。ハロゲン結合相互作用はハロゲンとルイス塩基の距離が短くなるとより強くなる。
歴史
[編集]1814年、ジャン=ジャック・コリンは、乾燥した気体状アンモニアと乾燥したヨウ素を混合した時に金属光沢を持つ液体が形成されることを記述した。得られるI2...NH3錯体の正確な組成は50年後にフレデリック・ガスリーによって証明された[5]。実験でガスリーは、I2を液体アンモニアへ加えた。この分子相互作用の真の性質は、ロバート・マリケンの電荷移動相互作用の発見と、Odd Hasselによるそれらの詳細な説明によりわずか半世紀後に初めて理解された。
1950年代、ロバート・マリケンは、電子供与体-受容体複合体の詳細な理論を開発し、これらをouterとinner複合体に分類した[6][7][8]。Outer複合体は、電子ドナーとアクセプター間に働く分子内相互作用であり、弱くとても小さな電荷移動しかない。Inner複合体では、大きな電荷の再分布が起こっている。マリケンの理論はハロゲン結合形成が起こる理論を説明するのに用いられてきた。

マリケンが彼の理論を開発した同時期に、ハッセルが行った結晶学研究が、ハロゲン結合形成とその特性の理解に関するターニングポイントとなった。
ハッセルのグループによる初めてのX線結晶構造解析研究は1954年に発表された。この実験で、彼のグループはX線回折技術を用いることによって臭素-1.4-ジオキサン複合体の構造を示すことができた[4]。この実験によりジオキサンの酸素原子と臭素原子との間に短距離の分子間相互作用が存在することが明らかになった。結晶中のO-Br距離は2.71 Åと測定された。これは、臭素原子と酸素原子間の強い相互作用を示している。さらに、この距離は、酸素原子と臭素原子のファンデルワールス半径の和 (3.35 Å) よりも短い。O-Br結合とBr-Br結合の作る角度は約180°だった。これが、ハロゲン結合形成における典型的な特徴の初めての証拠であり、これによってハッセルは、電子対ドナー分子中の非共有電子対の軌道の軸と一致する結合角度を持つ電子対ドナーとハロゲン原子が直接結び付いていると結論づけた[9]。
1969年、ハッセルは、ハロゲンが求電子剤、電子受容体、そして電子供与体存在下で高度に一方向に組織化された結晶性電荷移動錯体へと自己組織化できるという極めて優れた発見に対してノーベル化学賞を授与された[10]。電子供与体-受容体に関する初期の総説は1968年にBentによって書かれた[11]。「ハロゲン結合」という用語は、有機溶媒中でのCCl4、CBr4、SiCl4、およびSiBr4とテトラヒドロフラン、テトラヒドロピラン、ピリジン、アニソール、およびジブチルエーテルとの錯体を研究したDumasらによって1978年に使われるようになった[12]。
しかしながら、ハロゲン結合の性質と応用が精力的に研究されるようになったのは1990年代中頃であった。マイクロ波分光法により気相において形成される様々なハロゲン結合付加体を研究したLegonらによる系統的で広範囲に及ぶ研究は、ハロゲン結合とよく知られている水素結合相互作用との間の類似性に注目を集めた[13]。PolitzerとMurrayによるコンピューター計算は、ハロゲン結合の高い指向性がハロゲン核周りの電子密度の異方的分布の結果であると明らかにし[14]、「σホール」の定義への道を開いた[15]ため特に重要であった。
現在、ハロゲン結合は幅広い機能応用(例えば、結晶工学、超分子化学、高分子科学、液晶、導電性素材、医薬品化学)のために利用されている[16][17]。
応用
[編集]結晶工学
[編集]結晶工学は、固体化学と超分子化学を橋渡しする成長研究分野である[18]。このユニークな研究分野は学際的であり、結晶学、有機化学、無機化学などの伝統的な分野を融合させる。1971年、Schmidtは固体における光二量化の論文で初めてこの分野を確立した[19]。より最近の定義では、結晶工学は結晶化や望んだ物理化学的特性を有する新規物質の開発における分子間相互作用の利用と見なしている。ハロゲン結合の発見以前は、液晶や固体結晶材料の開発を目指す結晶工学におけるこのようなアプローチとしては、水素結合や錯体化学、イオン間相互作用を利用していた。さらに、ハロゲン結合は、ラジカルカチオン塩の組織化や分子導体の設計、液晶構造物の作成などに用いられている。ハロゲン原子の発見され、新しい分子集合体が開発されている[20]。ハロゲン結合のユニークな化学的特性のため、この分子間相互作用は結晶工学の発展における補助手段としての役割を果たしている[21]。
液晶形成におけるハロゲン結合の利用に関する初めての論文はH. Loc Nguyenによるものであった[22]。
液晶を形成する目的で、アルコキシスチルバゾールやペンタフルオロヨードベンゼンが用いられた。MetrangoloとResnatiによる以前の研究では、固体構造へのペンタフルオロヨードベンゼンの有用性が明らかになった[1]。様々なアルコキシスチルバゾールは非線形光学およびメタロ液晶物質に利用されている[23]。Resnatiのもう一つの発見(例: N-I複合体が強力に形成される)を用いて、このグループはペンタフルオロヨードベンゼンと4-アルコキシスチルバゾールのハロゲン結合複合体を調製した。X線回折解析の結果、N—I間の距離は2.811(4) Åで結合角度は168.4°であることが明らかになった。同様のN-I間距離は固体粉末でも計測されている[24]。この発見されたN—I間距離は、窒素とヨウ素のファンデルワールス半径の和 (3.53 Å) よりも短い。この分子の単結晶構造は四重極子相互作用が存在しないことを示している。
ハロゲン結合の強度における分極率の関与を調べるため、ブロモペンタフルオロベンゼンがルイス塩基として用いられた。その結果、ハロゲン結合複合体の確証は得られなかった。このことは、ハロゲン結合が原子分極率に依存していることをより支持している。同様のドナー-アクセプター骨格を利用して、著者らは液晶状態でのハロゲン結合の強さが水素結合したメソゲンに匹敵することを証明している。
ポリ(ジヨードジアセチレン) (PIDA) の調製
[編集]
共役ポリマー(重合体)の特性を利用した応用は、Heeger、McDiaramid、白川英樹らの(材料の製造は困難であるが)ポリアセチレンが導電性を示すという発見から生まれた。それ以後、この共役ポリマーの主骨格(例: ポリ(p-フェニレンビニレン))を模倣する研究が行われた。共役ポリマーは、多くの実用的応用があり、光電池、有機エレクトロルミネッセンス、電界効果トランジスタ、化学センサなどに用いられている。Goroffらは、ハロゲン結合骨格によってモノマー(単量体、2)を事前に整列させ、秩序だったポリ(ジヨードジアセチレン) (PIDA, 1) を調製した。PIDAは、ヨウ素は容易に変換できるため、他の共役ポリマーの極めて優れた前駆体である。例えば、C-I結合の切断は電気化学的還元となりうる[25]。
モノマー (2) の結晶構造は、様々な組成や接続性を有し無秩序である。ホスト (3-7) の分子パッキングが、主にモノマー (2) とそれぞれのホスト分子との共結晶実験により調べられた。ホスト 3 と 4 がモノマー (2) と事前に調製されたが、ヨウ素周辺の立体的嵩高さにより、モノマーの位相的重合が得られなかった。ホスト 5-7 は水素結合とハロゲン結合を利用することで、モノマー (2) を重合しやすい適切な距離に固定した。
実際に、ホスト 7 を用いた場合、共結晶を単離するさいに自発的に重合が起こった。結晶構造では、ポリマー鎖が水素結合ネットワークに全て平行で、ホストのニトリルがそれぞれのヨウ素原子とハロゲン結合していることが示された。興味深いことに、ポリマー 1 の結晶中のヨウ素原子の半分はオキサルアミドの酸素原子と近接した位置に存在する。ホスト 7 の酸素原子は、水素結合とハロゲン結合の両方でアクセプターとして作用している。


多孔質構造
[編集]
多孔質構造には様々な用途がある。多くの化学者と材料科学者が、自動車で使用する水素の貯蔵のための金属有機構造体 (metal-Organic Framework, MOF) の改良に取り組んでいる。これらの高度に秩序だった結晶包摂錯体は、触媒や分子分離装置としての利用が期待されている。分子組織は、しばしば水素結合などの分子間力によって制御されている。しかしながら水素結合の利用は、しばしば密なパッキングにより利用できる孔の大きさの範囲を制限する。
Piggeらは、アミン、含窒素複素環化合物、カルボニル基とその他のハロゲン化有機化合物との間のハロゲン結合相互作用を利用して、多孔質構造を構築した。これは、水素結合よりも著しく弱い相互作用であるハロゲン結合が介在する有機結晶ネットワークは珍しいため、意義深い[26]。
ジクロロメタンやピリジン、ベンゼンなど様々な溶媒中での1と2(図-上)の結晶構造が得られた。著者らは、多孔包摂錯体は明らかに、部分的には前例のないI-π相互作用とヨウ素とカルボニル基との間のハロゲン結合によって、仲介されていると述べている。結晶構造(図-下)は三角形配列をしており、2はほぼ対照的だった。加えて、全てのハロゲン結合相互作用の組は同一ではなく、ハロゲンとハロゲン結合アクセプターとの間の全ての分子間相互作用はファンデルワールス半径の和よりもわずかに越えていた。これはわずかに弱いハロゲン結合であることを示しており、この構造により柔軟性を与えている。二次元レイヤーは、それぞれ平行に積み上がり溶媒で満たされるチャネルを作り出している。
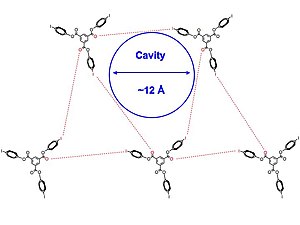
溶媒相互作用、特にピリジンとクロロホルム、もまた六角形構造の形成において言及されている。始めに、これらの溶媒によって形成される結晶がチャネル構造を形成する。長い時間をかけて、新しい針状の溶媒を含まない構造が密にパッキングされる。この針は実際に熱力学的に安定な結晶である。著者らは、この情報が、水素結合とハロゲン結合の相補的性質をより理解し、新たな低分子を設計するのに活用されることを望んでいる。
生体高分子におけるハロゲン結合
[編集]時折、生体高分子構造におけるハロゲン結合の重要性は見過ごされてきた。蛋白質構造データバンク(protein data bank, PDB: 2004年7月版)中の単結晶構造に基づいた、PDBに登録されている解像度3 Å以下の単結晶構造を対象としたAuffingerらの研究で、100以上のハロゲン-酸素相互作用ハロゲン結合が、ハロゲン化塩基を持つ6つの核酸構造ならびに66のタンパク質-基質複合体に見いだされた。ハロゲン-酸素相互作用ほど頻繁ではないが、ハロゲン-窒素およびハロゲン-硫黄接触も同様に同定されている[27]。これらの科学的発見は、生物システムにおけるハロゲン結合の役割を明らかにするためのユニークな基礎を提供する。
生体分子レベルでは、ハロゲン結合は基質特異性や、結合、分子折り畳みで重要である[28]。タンパク質-リガンド相互作用の場合は、最も一般的な分極したハロゲンとの電荷移動結合は、主鎖のカルボニル基および/あるいはアミノ酸残基のヒドロキシ基ならびにカルボキシ基が関与している。DNAおよびタンパク質-リガンド複合体では通常は、ルイス塩基ドナー原子(例: O, S, N)とルイス酸(ハロゲン)との間の結合距離は、これらのファンデルワールス半径の和よりも短い。構造的ならびに化学的環境に依存して、ハロゲン結合相互作用は弱くも強くもなる。いくつかのタンパク質-リガンド複合体の場合は、ドナー-アクセプターの方向性が一致しているならば、ハロゲン結合はエネルギー的にも幾何学的にも水素結合に匹敵している。この分子間相互作用はタンパク質-リガンドやDNA構造を安定化しコンホメーション(配座)の決定因子であることが示されている。
分子認識および結合でも、ハロゲン結合は重要であろう。この主張の薬剤設計における一例は、IDD 594のヒトアルドースレダクターゼへの結合での基質特異性である[29]。E. I. Howardはこの単量体酵素について最も優れた解像度 (0.66 Å) の構造を報告している。この生体高分子は316アミノ酸残基からなり、アルドースやコルチコステロイド、アルデヒドを還元する。本酵素によってD-グルコースから得られるD-ソルビトールは、糖尿病の病状の下流効果に寄与していると考えられている[30]。したがって、本酵素の阻害は治療においてメリットがある。
アルデヒドやカルボン酸を有する阻害剤は効果的であるが、アルデヒドレダクターゼの機能を損うため毒性を示す。カルボン酸およびアルデヒド阻害剤は、Trp 111、Tyr 48、His 110と水素結合している。阻害剤の結合の結果作られる特異性ポケットはLeu 300、Ala 299、Phe 122、Thr 113、Trp 11から構成される。阻害剤が有効であるため相互作用する、鍵残基はThr 113とTrp 111であることが同定された。IDD 594は、ハロゲンが選択性と活性が向上させるように設計された。結合する時、本化合物はコンホメーション変化を誘導し、Thrの酸素原子と阻害剤の臭素とのハロゲン結合を引き起こす。このハロゲン結合の距離は2.973(4) Åだった。このO-Brハロゲン結合が、本阻害剤がアルデヒドレダクターゼではなくヒトアルドースレダクターゼに対して高い活性を示すことに寄与している。

脚注
[編集]- ^ a b Metrangolo, P.; Resnati, G. (2001), “Halogen Bonding: A Paradigm in Supramolecular Chemistry”, Chem. Eur. J. 7 (12): 2511–2519, doi:10.1002/1521-3765(20010618)7:12<2511::AID-CHEM25110>3.0.CO;2-T
- ^ Politzer, P.; Lane, P.; Concha, M. C.; Ma, Y.; Murray, J. S. (2007), “An Overview of Halogen Bonding”, J. Mol. Model. 13 (2): 305–311, doi:10.1007/s00894-006-0154-7, PMID 17013631
- ^ Metrangolo, P.; Neukirch, H.; Pilati, T.; Resnati, G. (2005), “Halogen Bonding Based Recognition Processes: A World Parallel to Hydrogen Bonding†”, Acc. Chem. Res. 38 (5): 386–395, doi:10.1021/ar0400995, PMID 15895976
- ^ a b Hassel, O.; Hvoslef, J. (1954). “The Structure of Bromine 1,4-Dioxanate”. Acta Chem. Scand. 8: 873. doi:10.3891/acta.chem.scand.08-0873.
- ^ Guthrie, F. (1863), “Xxviii.—On the Iodide of Iodammonium”, J. Chem. Soc. 16: 239–244, doi:10.1039/js8631600239
- ^ Mulliken, R. S. (1950), J. Am. Chem. Soc. 72 (1): 600, doi:10.1021/ja01157a151
- ^ Mulliken, R. S. (1952), J. Am. Chem. Soc. 74 (3): 811–824, doi:10.1021/ja01123a067
- ^ Mulliken, R. S. (1952), J. Phys. Chem. Soc. 56 (7): 801–822, doi:10.1021/j150499a001
- ^ Hassel, O. (1970), “Structural Aspects of Interatomic Charge-Transfer Bonding”, Science 170 (3957): 497–502, doi:10.1126/science.170.3957.497, PMID 17799698
- ^ Hassel, O. (1972). “Structural Aspects of Interatomic Charge-Transfer Bonding”. In Nobel Lectures, Chemistry 1963-1970: 314–329.
- ^ Bent, H. A. (1968). “Structural Chemistry of Donor-Acceptor Interactions”. Chem. Rev. 68 (5): 587–648. doi:10.1021/cr60255a003.
- ^ Dumas, J.-M.; Peurichard, H.; Gomel, M. (1978). “CX4...Base Interactions as Models of Weak Charge-transfer Interactions: Comparison with Strong Charge-transfer and Hydrogen-bond Interactions”. J. Chem. Res.(S) 2: 54–57.
- ^ Legon, A. C. (1999). “Prereactive Complexes of Dihalogens XY with Lewis Bases B in the Gas Phase: A Systematic Case for the Halogen Analogue B···XY of the Hydrogen Bond B···HX”. Angew. Chem. Int. Ed. 38 (18): 2686–2714. doi:10.1002/(sici)1521-3773(19990917)38:18<2686::aid-anie2686>3.0.co;2-6.
- ^ Politzer, P.; Murray, J. S.; Clark, T. (2010). “Halogen Bonding: An Electrostatically-driven Higly Directional Noncovalent Interaction”. Phys. Chem. Chem. Phys. 101: 16789–16794.
- ^ Clark, T.; Hennemann, M.; Murray, J. S.; Politzer, P. (2007). “Halogen Bonding: The σ-Hole”. J. Mol. Model 13 (2): 291–296. doi:10.1007/s00894-006-0130-2. PMID 16927107.
- ^ Gilday, L. C.; Robinson, S. W.; Barendt, T. A.; Langton, M. J.; Mullaney, B. R.; Beer, P. D. (2015). “Halogen Bonding in Supramolecular Chemistry”. Chem. Rev. 115 (15): 7118–7195. doi:10.1021/cr500674c. PMID 26165273.
- ^ Cavallo, G.; Metrangolo, P.; Milani, R.; Pilati, T.; Priimagi, A.; Resnati, G.; Terraneo, G. (2016). “The Halogen Bond”. Chem. Rev. 116 (4): 2478–2601. doi:10.1021/acs.chemrev.5b00484. PMC 4768247. PMID 26812185.
- ^ Braga, D.; Desiraju, G. R.; Miller, J. S.; Orpen, A. G.; Price, S. L. (2002), “Innovation in Crystal Engineering”, CrystEngComm 4 (83): 500–509, doi:10.1039/b207466b
- ^ Schmidt, G. M. J. (1971), “Photodimerization in the solid state”, Pure Appl. Chem. 27 (4): 647–678, doi:10.1351/pac197127040647
- ^ Metrangolo, P.; Resnati, G.; Pilati, T.; Liantonio, R.; Meyer, F. (2007), “Engineering Functional Materials by Halogen Bonding”, J. Polym. Sci. Part A: Polym. Chem 45 (1): 1–14, doi:10.1002/pola.21725
- ^ Metrangolo, P.; Pilati, T.; Terraneo, G.; Biella, S.; Resnati, G. (2009), “Anion coordination and anion-templated assembly under halogen bonding control”, CrystEngComm 11 (7): 1187–1196, doi:10.1039/B821300C
- ^ Nguyen, H. L.; Horton, P. N.; Hursthouse, M. B.; Legon, A. C.; Bruce, D. W. (2004), “Halogen Bonding: A New Interaction for Liquid Crystal Formation”, J. Am. Chem. Soc. 126 (1): 16–17, doi:10.1021/ja036994l, PMID 14709037
- ^ Bruce, D. W. (2001), “The Materials Chemistry of Alkoxystilbazoles and Their Metal Complexes”, Adv. Inorg. Chem. 52: 151–204, doi:10.1016/S0898-8838(05)52003-8
- ^ Weingarth, M.; Raouafi, N.; Jouvelet, B.; Duma, L.; Bodenhausen, G.; Boujlel, K.; Schöllhorn, N.; Tekely, P. (2008). “Revealing molecular self-assembly and geometry of non-covalent halogen bonding by solid-state NMR spectroscopy”. Chem. Commun. 45: 5981-5983. doi:10.1039/B813237B.
- ^ Sun, A.; Lauher, J. W.; Goroff, N. S. (2006), “Preparation of Poly(Diiododiacetylene), an Ordered Conjugated Polymer of Carbon and Iodine”, Science 312 (5776): 1030–1034, doi:10.1126/science.1124621, PMID 16709780
- ^ Pigge FC, Vangala VR, Kapadia PP, Swenson DC, Rath NP (2008). “Hexagonal Crystalline Inclusion Complexes of 4-Iodophenoxy Trimesoate”. Chem. Commun. (39): 4726–8. doi:10.1039/B809592B. PMID 18830473.
- ^ Auffinger P, Hays FA, Westhof E, Ho PS, “Halogen Bonds in Biological Molecules”, Proc. Natl. Acad. Sci. U.S.A 101 (48): 16789–16794, doi:10.1073/pnas.0407607101, PMC 529416, PMID 15557000
- ^ Steinrauf LK, Hamilton JA, Braden BC, Murrell JR, Benson MD (1993), “X-ray crystal structure of the Ala-109-->Thr variant of human transthyretin which produces euthyroid hyperthyroxinemia.”, J. Biol. Chem 268 (4): 2425–2430, PMID 8428916
- ^ a b Howard EI, Sanishvili R, Cachau RE, Mitschler A, Chevrier B, Barth P, Lamour V, Van Zandt M, Sibley E, Bon C, Moras D, Schneider TR, Joachimiak A, Podjarny A (2004), “Ultrahigh Resolution Drug Design I: Details of Interactions in Human Aldose Reductase-Inhibitor Complex at 0.66 Å”, Proteins: Struct., Funct., Bioinf 55 (4): 792–804, doi:10.1002/prot.20015, PMID 15146478
- ^ Yabe-nishimura, C. (1998), “Aldose reductase in glucose toxicity: a potential target for the prevention of diabetic complications”, Pharmacol Rev 50 (1): 21–33, PMID 9549756
参考文献
[編集]- Stephen K. Ritter (2009-09-21). “Halogen Bonding Begins To Fly - ACS Meeting News: Noncovalent interaction akin to hydrogen bonding is becoming an important tool for chemists”. Chem. Eng. News 87 (38): 39 - 42. doi:10.1021/cen-v087n038.p039.


