放射線療法
| 放射線療法 | |
|---|---|
| 治療法 | |
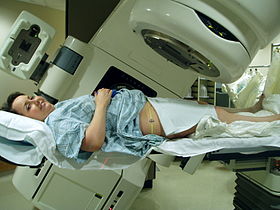 骨盤への照射 | |
| 診療科 | 放射線腫瘍学 |
| ICD-10-PCS | D |
| ICD-9-CM | 92.2-92.3 |
| MeSH | D011878 |
| OPS-301 code | 8–52 |
| MedlinePlus | 001918 |

放射線療法(ほうしゃせんりょうほう、英語: radiation therapy / radiotherapy[2])は、放射線を患部に体外および体内から照射する治療法である[3]。手術、抗がん剤治療とともに、癌(がん)に対する主要な治療法の一つである[4]。放射線腫瘍学はこの放射線処方に対しての専門分野であり、撮影を主とする放射線診断学とは区別される。
放射線治療は、エックス線、電子線、ガンマ線といった放射線を照射することで細胞内の遺伝子 (DNA) にダメージを加え、がん細胞を破壊する。放射線の照射により正常細胞にもダメージを与えてしまうが、その感受性はがん細胞より低い[5]。与えられる放射線の線量に応じて双方が受けるダメージは上記の「腫瘍と正常組織に対する放射線照射の効果」の図にあるように一定の線量以下においては腫瘍および正常組織にもダメージがなく、ある線量を超えると線量の増加とともにダメージが増加する。その様子はS字状の曲線で示される[1]。同じく固形腫瘍の根治療法である外科療法と比較し、放射線治療では、がんが発生した臓器の機能と形態をある程度維持することが可能である[注 1][6]。日本では癌患者がその生涯で放射線治療を受けるのは4人に1人であり、アメリカでの3人に2人と比べると少ない[7]。
放射線療法の歴史は19世紀末のエックス線、ラジウムの発見を始まりとし、抗生物質、抗がん剤の開発および外科手術や麻酔法の確立がなされていなかった当時の癌治療はほとんど放射線療法のみであった[8][注 2]。癌治療の目標には根治(完治)、延命、緩和があるが[9]、放射線療法はこの全てに利用される[10]。固形がんを根治させる可能性があるのは手術のほかは放射線療法だけであり、さらに放射線療法は患者の負担が少ない優しい治療法で[11]、耐術能に乏しい高齢者にも適用できる[6]。局所療法のため副作用は比較的少なく、それも大部分は治療後1か月から2か月で自然に治まる[12]。これは、上述のごとく、有害事象を考慮した線量で治療していることと関連が深く、予定調和的な軽度の有害事象とその快癒である。使用される放射線のエネルギーが、正常組織に対して無視できない影響を与えると[注 3]、後述するように放射線障害と呼ばれる有害事象を起こし、その内容は部位により多彩であるものの、この影響は放射線治療のメリットに比べて十分小さい[13]。繰り返しにあるが、そうなるように放射線治療医が、適切に線量を選択しているのである。
適用
[編集]通常、放射線治療(放射線療法)の適用となる疾患はケロイド、甲状腺眼症、髄膜腫、聴神経腫瘍、下垂体腺腫など一部の良性疾患[14]と、ほぼ全ての悪性腫瘍である。また、放射線治療(放射線療法)は外科手術、化学療法、ホルモン療法などと組み合わされ、集学的治療の一環として利用される場合もある。治療の対象となる代表的な癌を次に挙げる。
- 乳癌 (breast cancer) - 乳房温存療法の一環として温存術後の接線照射や乳房切除後多数リンパ節転移例で、接線照射+鎖骨上照射などが 50 Gy / 25 fr(2 Gy ✕ 25回照射。計50 Gy)程度で施行される。
- 前立腺癌 (prostate cancer)[2] - 局所症例の根治照射として強度変調放射線治療で 78 Gy 39 fr 前後が照射される。
- 肺癌 (lung cancer) - 定位放射線治療や同時化学放射線療法が行われる。
- 結腸直腸癌 (colorectal cancer) - 海外では術前照射や緩和照射として行なわれることが多いが、日本では施設間格差が大きい。
- 脳腫瘍 (brain tumour)
- 頭頸部癌 (head & neck cancer): 喉頭癌および咽頭癌、副鼻腔癌、口腔癌(舌癌、歯肉癌、頬粘膜癌など)
- 食道癌 (oesophagus cancer)
- 肝臓癌 (hepatic cancer)
- 子宮頸癌などの婦人科の癌
- 膀胱癌 (bladder cancer)
- 前立腺癌 (prostate cancer)
- 悪性リンパ腫 (malignant lymphoma)
- 膵臓癌 (pancreatic cancer)
放射線治療(非密封小線源療法を除いて)は局所療法であり、普通は腫瘍のある部分のみを狙って適用されるが、手術の領域リンパ節郭清と同様に領域リンパ節やその近傍近傍を含めることもある。また、特殊な照射としては、白血病などの骨髄移植前処置として全身に照射される(全身照射)治療法もある。放射線治療の特徴は、「切らずに治すこと」であり、外科手術と異なり臓器温存(形態や機能)を可能とする。このため頭頸部腫瘍など切除術により著しく生活の質 (Quality of Life: QOL) の低下を生じるものに、第一選択の治療とされる場合が多い。
放射線治療は他の手術療法などと同じく治癒可能な病期・病勢では「根治治療 (radical therapy)」の重要な選択肢として施行される。その他、癌が治癒不能な病期・病勢、再発・転移癌の場合でも、部分的な腫瘍縮小効果により症状の緩和を目指す「緩和治療・姑息治療 (palliative therapy)」として広く用いられる。局所的な放射線治療の特徴として、全身への侵襲が小さいため、高齢者や全身状態が悪化した患者に対しても負担が少なく、緩和医療の重要な手段として治療が行える利点がある。代表的な緩和治療の対象病態は、骨転移の疼痛・骨折予防、脳転移による神経症状、縦隔腫瘍による上大静脈症候群などである。
副作用
[編集]使用される放射線のエネルギーが、正常組織に対して無視できない影響を与えた場合には、放射線障害と呼ばれる副作用を生ずる[13]。放射線の副作用には照射中もしくは照射後早期に起こる早期反応と、照射後数か月以上へて起こる晩期反応がある[13]。
早期反応の主なものには皮膚・粘膜の炎症と、骨髄への障害がある。炎症はどれも照射を終了あるいは中断することで1週間ないし2週間のうちに大部分が治まる[13]。その程度が重症であれば致死的ともなるものの、現在の放射線治療で高度の早期反応が問題となることはまずない[13]。一方、放射線感受性が非常に高い骨髄は、低い照射量においても白血球の減少などを起こすが[15]、照射がかなりの広範囲に及ばない限り、実際の問題になることはまれである[13]。
晩期反応は、照射後数か月から十数年たってから起き、その本質は微小血管障害と見られている[13]。ほとんどの臓器・組織で問題となりうるもので、主なものには皮膚や皮下組織の萎縮・線維化や潰瘍、肺の線維化による呼吸障害、消化管の潰瘍や穿孔、中枢神経の麻痺などがあり、すべてを考慮すると放射線治療後の長期生存例の数%において何らかの晩期反応が問題になっているといわれる[13]。さらに現在も極めて少数ながら致死的晩期障害の報告があり、また治療に使用する放射線が将来2次がんを誘発する可能性も指摘されてはいる。これらの影響は放射線治療のメリットに比べて十分小さく[13]、また重粒子線治療では2次がんのリスクが極めて小さいことが示唆されている[16]。
肺における合併症
[編集]肺は体の中で最も放射線に敏感な器官の一つで、放射線治療によって高度の線量で照射された肺細胞の体積に依存してダメージを受け、暴露後、2〜6ヶ月後に早期の合併症として放射線肺臓炎などの放射線による肺障害 (Radiation-induced lung injury) を引き起こすことがある[17]。晩発性の合併症としては、胸部放射線治療における放射線肺線維症などがある[18]。これらの放射線による肺毒性 (Pulmonary toxicity due to radiation) がもたらす合併症を抑えるために、装置の改良などによって治療時における正常細胞へのダメージを減らすための努力がなされている[19]。
作用原理
[編集]放射線療法は、放射線により生物の細胞が死滅する効果を利用しているが、この作用は細胞分裂の盛んな細胞に対して効果が大きく、分裂の盛んながん細胞により大きな影響を与えると経験的に知られ、例外はあるもののベルゴニエー・トリボンドウの法則として知られている[20]。放射線は、がん細胞のみならず正常細胞にも障害を与えるが、がん細胞は放射線による障害からの回復能力が乏しいため[21]放射線療法は分割照射という形式を取ることが多いが、これはある照射から次の照射までに、正常細胞がダメージから回復する時間を与え、ダメージから回復できないがん細胞だけが効果的に死滅させるようにする照射技術である[22]。がん細胞の数が減少すると免疫細胞側が優勢となり、残ったがん細胞すべてを処分することができるようになる[23]。また、ふだんは免疫細胞が見逃しているがん細胞も放射線照射によってその存在が知られ、免疫細胞はがん細胞の場所に移動し、ただちにこれを処分する[24]。照射されているがん細胞ばかりか、遠隔転移しているがん細胞への免疫細胞の攻撃力が高まり、転移巣が治癒することもあり、アブスコパル効果と呼ばれている。
用量
[編集]放射線利用法はいくつかの点で、薬剤投与と同じように扱われているが、根本的に異なるのは照射体積の大きさや、同じ照射線量でも照射部位や照射方法により生体反応(耐容線量)が全く異なる点である。放射線療法が単独で実施されるか、化学療法と併用されるか、手術の前か後か、郭清手術が成功したかどうかなどの要素が治療医(放射線治療医)の判断によって調節される。腫瘍制御に必要な線量は、腫瘍の感受性により異なり、一般的な固形がん(扁平上皮癌、腺癌など)への線量は通常50Gy(グレイ Gray; 放射線の項を参照)程度、それ以上が必要との見解もあるが正常組織への耐容線量を考慮すると照射が難しい場合が多い[25]。高感受性のリンパ腫(白血病)などは総線量で20〜40Gyで腫瘍制御が充分可能とされる。現在、定位手術的放射線治療 (Radiosurgery) を除いて1回照射法は少なく、小線量を1日1回、週4〜5回照射する分割照射が多く行われる。分割照射の場合、一回線量は1.8〜2.0Gyが経験的に多く用いられる。1回の用量を小さくして繰り返し実施することは、正常細胞が成長し直す時間を与え、照射で与えた障害を回復させる。生物学的効果線量 (biological effective dose) は同じ総線量でも一回線量の大きさ(分割回数)、照射期間により左右される。また、正常組織の耐容線量が照射容積に影響されるのは前述の通りである。小線源治療法(放射性同位元素を直接体内に挿入する治療法)において、古典的には挿入したラジウムの量と体内に留置した時間の積 (mgh) で線量を表現した時代があった。現代では、外照射と同じく吸収線量Gyが用いられるが、外照射と生物学的効果を比較、換算するのには注意が必要である。小線源治療では生物学的効果線量に影響を及ぼすものとして線量率 (dose rate) が加わる。
分割照射スケジュール
[編集]前述したように、通常の1日当り照射量のスケジュールは成人患者で1回当り2.0Gyで、1日1回照射であるが、場合によっては違うスケジュールのことがある。1つの方法として、肺癌での投与法であるCHART法 (Countinoys Hyperfractionated Accelerated RadioTherapy) がある。これは肺癌に適用されることが多く、1日当たり2〜3回の少量分割照射を行う。成功例が多いとはいえ、週末も含めて毎日複数回の照射を実施することにより大きな負担が患者にかかってくる。小児癌では、分割照射スケジュールは1回当り1.5〜1.8Gyとなる。原理的には分割のやり方は治療効果と急性あるいは遅発障害との兼ね合いになり、1回当たりの照射量が小さいほど、効果発現に時間がかかる(小児は正常組織の感受性が高いので成人の標準分割線量より低い線量が設定されている)。
種別
[編集]周囲の正常組織へのダメージを最小限に抑えつつ、がんに十分な放射線を照射するため、がんの場所や大きさ、種類に応じて、最適な治療法が選ばれるが、治療法は外照射と小線源治療に分類できる[26]。外照射ではリニアックを利用して体外から体内の病巣部に向けて放射線照射を行い、小線源治療では病巣の内部あるいは近くに放射性物質を置いて、体内から放射線を照射させる[26]。
外照射
[編集]

外照射療法に使用される代表的な装置を次に挙げる
- リニアック - X線、電子線:最も多く用いられる放射線治療機器
- コバルト照射装置 - γ線:リニアックへの置換が進んだため日本国内ではあまり使用されない
- ガンマナイフ - γ線:定位照射に用いられる特殊なコバルト装置
- ガンマナイフは頭蓋内の治療に広く用いられ、脳腫瘍以外にも脳血管障害(脳動静脈奇形)などの治療にも用いられてきた。最近ではリニアックを用いた定位放射線治療でも同等の治療効果が得られるため、多くの放射線治療施設で同疾患の治療が可能となっている。またガンマナイフは三叉神経痛や顔面痙攣といった機能的脳神経外科疾患の治療にも一定の治療成績を得ているが、現在のところ頸椎の7番目から頭部以外の疾患は医療保険外の診療となっている。
- 医療用加速器 加速器としてはシンクロトロンあるいはサイクロトロンが使用される。シンクロトロンは陽子線あるいは重粒子線用、サイクロトロンは陽子線用として用いられている。
- ホウ素中性子捕捉療法 (BNCT) 装置(医療用原子炉) - 中性子線
- 京都大学の京大複合 (KUR)、武蔵工業大学(現東京都市大学)の武蔵工大炉 (MITRR)、日本原子力研究開発機構の研究炉 (JRR-4) で研究が行われているが、MITRRが廃炉となったため、現在はKURとJRR-4で実験的治療を行っている。一方、原子炉に頼らず一般病院でも施設可能な、100m2程度の部屋の大きさの小型の中性子発生装置が、NEDOプロジェクトや、三菱重工、京都大学などにより開発中である。京都大学原子炉実験所と住友重機械工業株式会社は共同で30MeVサイクロトロン加速器を用いた加速器中性子源を開発しており、2009年にはBNCTの動物実験が開始された[27]。2012年からはステラファーマ、住友重機械工業株式会社、京都大学原子炉実験所の共同により、京都大学原子炉実験所の加速器中性子源を用いて、世界初となる加速器中性子源によるBNCTの治験が開始された[28][29]。当初、再発悪性神経膠腫を対象として始まった治験は、2014年に再発頭頸部がんも対象に加わり[30]、実用化へ向けた研究が進められている。福島県の一般財団法人脳神経疾患研究所は、2013年に住友重機械工業株式会社にホウ素中性子捕捉療法システムを発注しており、世界初の病院設置型加速器BNCTシステムとして、2015年の治験開始、2018年の治療開始を目指している[31]。その他、臨床応用可能機器として、国立がん研究センター、江戸川病院に株式会社リライズメディカルシステムズが加速器BNCTシステムの導入を検討している。
密封小線源治療
[編集]密封小線源治療では、放射線源が患部の近傍に導入されて照射される。
RI内用療法
[編集]非密封小線源治療に分類され、放射性同位元素 (Radio Isotope; RI) を組み込んだ薬剤を、経口的あるいは経静脈的に投与して悪性腫瘍や一部の良性疾患に対する効果を発現させる[32]。
薬剤は経口的あるいは経静脈的に全身投与されるが、ベータ線やアルファ線の飛程が短いことから、標的に選択的に薬剤を集積させることによって、標的近傍でのみ効果を発揮させることが実現できる[32]。
高精度放射線治療
[編集]放射線治療の成績を向上させるために治療方法の工夫が試みられてきたが、その工夫は大きく2種類に分けることができる[33]。1つはがん細胞と正常細胞との放射線に対する感受性の差を広げることで生物学的な意味での高線量を投与して治療効果の向上を求める生物学的な試みであり、これらには放射線増感剤・防護剤の利用、放射線照射の分割方法の工夫、抗がん剤の併用が含まれ、その効果は細胞実験などを含めた多角的な検証が容易であり、放射線治療の歴史にわたり研究されているが、臨床的な有用性が示されずに使用されなくなったものも少なくない[33]。もう1つは物理的に放射線を腫瘍に集中させる手段の追求であり、照射を必要かつ十分な範囲に限定しながら多門放射を行うことで腫瘍周囲の正常組織の被曝線量を減少させて副作用の低減を得るほど腫瘍への高線量投与を可能とするもので、最近の放射線治療成績向上に貢献しているCTシミュレーターによる三次元放射線治療計画における考え方であるが、高精度放射線治療はこの方向において、さらに進化したものである[33]。
高精度放射線治療は、放射線治療時に専用の装置・器具を用いることで目標の領域に高精度な正確さをもって放射線を集中させて行われる治療方法の総称である[33]。これには特殊な固定具によるセットアップ誤差の低減、患者体内における腫瘍あるいは正常臓器の移動制御による放射線照射範囲の最小限化、コンピューターの行う計算による最適化を根拠とした腫瘍に近接する正常構造の線量のみを下げて放射線を投与する方法(強度変調放射線治療 intensity-modulated radiotherapy ; IMRT)といったものがあり、これらを複数組み合わせて一層高精度の治療を行う装置・施設も増加している[33]。特に普及している高精度放射線治療としては定位的放射線治療(ピンポイント照射)があり、脳転移症例に対するガンマナイフ治療、手術適応のない早期肺癌症例に対する体幹部定位放射線治療というように非侵襲的かつ治療効果の高い手段として治療の選択肢になっている[33]。近年はセットアップされた治療寝台上の患者の照射部位の画像を取得して治療計画時の画像との位置のずれを検出してはセットアップ位置を修正するという手順を分割して実施される放射線治療のたびに行うことでセットアップの誤差の最小化を実現する治療法(画像誘導放射線治療 image-guided radiotherapy ; IGRT)が急速に広まり、透視・撮影装置が装備されたIGRT対応リニアックを利用して、治療寝台上でセットアップ誤差や腫瘍の呼吸性移動をリアルタイムに確認し、照射位置を修正しながら精確な放射線治療を行うことができる装置も徐々に増えている[33]。
これまでの放射線治療では照射範囲におけるX線強度は均一であったが、IMRTは照射範囲内のX線強度を場所ごとに設定して照射することで、任意の線量分布を作る技法であり、リスク臓器が腫瘍の近くに存在する、前立腺がんや頭頸部がんで主に使用されている治療法であり、照射範囲内のX線強度差はコンピューターによる最適化による[33]。頭頸部がんに対しては、多くの場合、原発巣とともに頸部リンパ節も系統的に放射線照射を行うが、従来法では唾液腺、特に耳下腺が被曝することで唾液量が極端に減少し、治療後も唾液量の回復はほとんどなかったが、耳下腺の線量を落としながらIMRTを実施することで唾液量は一時的に減少するものの治療後数カ月程でほぼ治療前の唾液量まで回復する[33]。
脚注
[編集]注釈
[編集]- ^ 放射線治療は、治療後にも臓器機能を温存し、生活する上で支障となるような合併症をもたらさないことを目指すのが原則であり、合併症が当然とされる手術と対照的である。しかし、一般に有害事象は完全に避けることはできず、同一部位への再度の照射では合併症が生じる危険性が増す(近藤 1999 pp.15,99)。
- ^ 人類初の放射線治療は1896年11月24日から12月3日まで、1日1回の照射に分割された形式で行われた局所進行鼻腔癌の治療である。分割されたのは機械の性能が不足していたためであり、その後は治療機器が改良され高線量を1回で照射することも行われたが、20年後には、1回で照射する方式の効果が極めて低いと結論付けられている。現在、経験的知見から推奨される治療計画はどれも同じように分割化されている(アリソン 2011 p.156)。
- ^ 近藤誠によれば、治癒率を上げようと線量を多くしたり、照射する範囲を広げたりすることが原因として多いとされている(近藤 1999 p.99)。
出典
[編集]- ^ a b 西村恭昌 『肺がん』 p.92
- ^ a b CG175: Prostate cancer: diagnosis and management (Report). 英国国立医療技術評価機構. January 2015.
- ^ 青山喬(編著)「放射線基礎医学」第9版 金芳堂(2000.3)
- ^ 鎌田中川 2007, p.115
- ^ “放医研ニュース No.41”. www.nirs.qst.go.jp. 2021年8月19日閲覧。
- ^ a b 西村恭昌 近畿大学医学部放射線腫瘍学部門
- ^ 唐澤 2009, p.14
- ^ 井上手島 2010, p.14
- ^ 鎌田中川 2007, pp.115-116
- ^ 中川 2007, p.42
- ^ 唐澤 2009, p.12
- ^ 唐澤 2009, p.15
- ^ a b c d e f g h i 「3.放射線治療の副作用」『放射線によるがんの治療(特徴と利点) (08-02-02-03)』原子力百科事典ATOMICA
- ^ 晴山雅人 良性疾患の放射線治療 臨床放射線 第47巻 別冊 2002/11/30 発行
- ^ Jeong, Youn Kyoung; Oh, Ju Yeon; Yoo, Jae Kuk; Lim, Sun Ha; Kim, Eun Ho (2020-01-29). “The Biofunctional Effects of Mesima as a Radiosensitizer for Hepatocellular Carcinoma”. International Journal of Molecular Sciences 21 (3): 871. doi:10.3390/ijms21030871. ISSN 1422-0067. PMC 7036851. PMID 32013255.
- ^ Mohamad, Osama; Tabuchi, Takahiro; Nitta, Yuki; Nomoto, Akihiro; Sato, Akira; Kasuya, Goro; Makishima, Hirokazu; Choy, Hak et al. (2019-5). “Risk of subsequent primary cancers after carbon ion radiotherapy, photon radiotherapy, or surgery for localised prostate cancer: a propensity score-weighted, retrospective, cohort study”. The Lancet. Oncology 20 (5): 674–685. doi:10.1016/S1470-2045(18)30931-8. ISSN 1474-5488. PMID 30885458.
- ^ Ann C. Mertens et al. (2002). “Pulmonary complications in survivors of childhood and adolescent cancer”. Cancer 95 (11): 2431–2441. doi:10.1002/cncr.10978. "The lung is one of the most radiation-sensitive structures in the body. Therapy-related radiation damage to the lung depends on the volume of lung tissue irradiated, the total dose received, and fractionation scheduling.2 Radiation-induced lung disease includes an acute phase of radiation pneumonitis that occurs 2–6 months after exposure."
- ^ Ann C. Mertens et al. (2002). “Pulmonary complications in survivors of childhood and adolescent cancer”. Cancer 95 (11): 2431–2441. doi:10.1002/cncr.10978. "Chest radiation was associated with a 3.5% cumulative incidence of lung fibrosis at 20 years after diagnosis."
- ^ Ericka Wiebe al. (2006), “RADIATION-INDUCED LUNG INJURY” (PDF), Oncology Exchange 5 (2): 29–32
- ^ 中川 2007, p.66
- ^ 中川 2007, pp.66-68
- ^ 唐澤 2009, p.25
- ^ 中川 2007, pp.68-70
- ^ 中川 2007, p.70
- ^ 「放射線治療計画ガイドライン」の付表1:通常分割照射における正常組織の耐容線量 日本放射線科専門医会・医会放射線診療ガイドライン策定事業
- ^ a b 放射線治療|治療法について|がん研有明病院「Chapter.3: 放射線治療法の種類」
- ^ 世界初の加速器によるホウ素中性子捕捉療法の動物実験を開始しました。(2009年8月5日) — 京都大学
- ^ 世界初の加速器BNCTによる治験開始について (PDF)
- ^ 世界初の加速器BNCT(ホウ素中性子捕捉療法)による治験開始について (PDF)
- ^ http://www.yomidr.yomiuri.co.jp/page.jsp?id=96938 頭頸部がんで世界初の治験…京大など中性子治療
- ^ 世界初 病院設置型加速器によるホウ素中性子捕捉療法システム(BNCT)を受注 | お知らせ 2012年度 | 住友重機械工業株式会社
- ^ a b 2011年2月17日の朝日新聞朝刊33面
- ^ a b c d e f g h i 井垣 2011 p.516
参考文献
[編集]- 井垣浩、中川恵一「放射線治療の現状と展望--高精度放射線治療を中心に」『成人病と生活習慣病』東京医学社、2011年。ISSN 1347-0418。
- 井上俊彦、井上武宏、手島昭樹『放射線治療学』南山堂、2010年。ISBN 978-4-525-27094-0。
- 鎌田實、中川恵一『がん生きたい患者と救いたい医者』三省堂、2007年。ISBN 978-4-385-36323-3。
- 唐澤克之『がんの放射線治療がよくわかる本』主婦と生活社、2009年。ISBN 978-4-391-13702-6。
- 近藤誠『ぼくがすすめるがん治療』文芸春秋、1999年。ISBN 978-4-16-3548005。
- 西條長宏、加藤治文(編)、2011年、『肺がん』、医薬ジャーナル社 ISBN 978-4753225231
- 中川恵一『切らずに治すがん治療』法研、2007年。ISBN 978-4-87954-652-4。
- ウェード・アリソン『放射能と理性-なぜ「100ミリシーベルト」なのか』徳間書店、2011年。ISBN 978-4-19-863218-2。
