ドブニウム
原文と比べた結果、この記事には多数の(または内容の大部分に影響ある)誤訳があることが判明しています。情報の利用には注意してください。 (2023年1月) |
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 外見 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 不明 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 一般特性 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 名称, 記号, 番号 | ドブニウム, Db, 105 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 分類 | 遷移金属 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 族, 周期, ブロック | 5, 7, d | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子量 | [268] | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 電子配置 | [Rn] 5f14 6d3 7s2(推定) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 電子殻 | 2, 8, 18, 32, 32, 11, 2(推定)(画像) | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 物理特性 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 相 | 不明 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 密度(室温付近) | 29 (推定) g/cm3 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子特性 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 酸化数 | 5 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 共有結合半径 | 149 pm | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| その他 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS登録番号 | 53850-35-4 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 主な同位体 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細はドブニウムの同位体を参照 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ドブニウム (Dubnium)は、元素記号Db、原子番号105の化学元素である。高い放射性を持ち、最も安定な既知の同位体であるドブニウム268の半減期は約16時間である。このため、この元素に関する実験は非常に制限されている。
ドブニウムは地球上では天然に生成せず、人工的に作られる。ソビエト連邦のドゥブナ合同原子核研究所は、1968年にこの元素の発見を主張し、1970年にはアメリカ合衆国のローレンス・バークレー国立研究所が続いた。両チームが各々新元素への命名を提案し、公式な承認なしで用いた。長い議論は、1993年にIUPAC/IUPAP超フェルミウム元素作業部会が発見に関する主張を公式に調査し発見は両チームによるものだと公式に認定するまで続いた。1997年に、ドゥブナ合同原子核研究所の所在地であるドゥブナの町に因んで、ドブニウムと公式に命名された。
6dブロックの第5族元素であり、周期表上では、バナジウム、ニオブ、タンタルの下に位置する。相対論効果により若干の違いはあるものの、価電子の電子配置や+5の酸化状態が支配的であること等、多くの性質が第5族元素と共通であると考えられており、ドブニウムの化学的性質に関する限られた実験によりこれが確かめられている。
導入
[編集]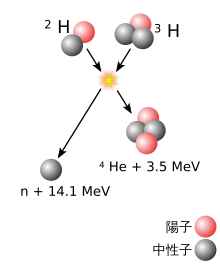
重い[注釈 1]原子核は、2つの異なる原子核[注釈 2]の核融合反応により形成され、おおまかに、2つの原子核の質量の差が大きいほど、反応の可能性は高くなる[9]。重い方の原子核を持つ物質を標的とし、軽い原子核の粒子線を照射することで、2つの原子核が十分に接近すると、1つの原子核への融合が起こりうる。通常、陽電荷を持つ2つの原子核は、クーロンの法則により互いに反発する。原子核同士が非常に近づくときのみ、強い相互作用がこの反発力に打ち克つ。そのため、粒子線となる原子核の速度を、この反発力が無視できる程度まで、加速器で加速する必要がある。ただし、2つの原子核が融合するためには、2つの原子核が単に近づくだけでは不十分である。2つの原子核が近づいただけでは、通常、1つの原子核に融合するのではなく、10-20秒間だけ一緒に留まった後、離れていく(この時、反応前と同じ構成とは限らない)[10][11]。核融合が起こる場合、複合核と呼ばれる一時的な融合状態が励起状態となる。励起エネルギーを失い、より安定な状態に達すると、複合核は核分裂反応を起こすか、1つまたはいくつかの原子核の核破砕反応を起こして、エネルギーを持ち去る[注釈 3]。この事象は、最初の衝突の約10-16秒後に起こる[12][注釈 4]
粒子線が標的を通り過ぎると、次のチェンバーであるセパレーターに移送される。新しい原子核ができていると、この粒子線により運ばれる[15]。セパレーターでは、生成した原子核は他の原子核(粒子線の原子核やその他の反応生成物)から分離され[注釈 5]、表面障壁型半導体検出器に運ばれる。粒子はそこで停止し、検出器上での正確な衝突位置とそのエネルギー、到達時間が記録される[15]。移送には約10-6秒を必要とし、検出までに原子核はこの長時間を生き残る必要がある[18]。崩壊が起こると、原子核の位置、エネルギー、崩壊時間が再度記録される[15]。
原子核の安定性は、強い相互作用によってもたらされる。しかしそれが及ぶ範囲は非常に短く、原子核が大きくなるほど、最外殻の核子(陽子と中性子)が強い相互作用から受ける影響は小さくなっていく。同時に、陽子間の静電反発により原子核は引き裂かれ、これは範囲の制約がない[19]。そのため、重元素の原子核は、このような反発によるアルファ崩壊や自発核分裂[注釈 6]のようなモードが主要な崩壊過程になると理論的に予測されており[21]、これまで実際の観測もそれを裏付けてきた[22]。このような崩壊モードは、超重元素の原子核には支配的なものである。アルファ崩壊は、放出されたアルファ粒子により記録され、崩壊生成物は実際の崩壊前に容易に決定できる。一度の崩壊や連続した崩壊により既知の原子核が生成されると、計算により反応の出発点となる原子核が決定できる[注釈 7]。しかし、自発核分裂では生成物として様々な原子核が生じ、そのため、娘核からは、出発点となる原子核が決定できない[注釈 8]。
重い元素を合成しようとする物理学者が得られる情報は、このように検出器により収集される、粒子が検出器に衝突した距離、エネルギー、時間と、崩壊の際の同様の情報となる。物理学者はこのデータを分析し、これが新元素によって引き起こされたものであり、他の核種により引き起こされたものではないと結論付けようとする。しばしば、得られたデータは、新元素の生成を確定するには不十分なものであったり、解釈の誤りの元となりうる[注釈 9]。
発見
[編集]背景
[編集]天然である程度の量が生成する最も重い元素は原子番号92のウランである。これより重い元素は人工合成により作られる。新元素の最初の合成は、原子番号93のネプツニウムで、1940年にアメリカ合衆国の科学者チームにより達成された[32]。これに続き、1955年までに、原子番号101番のメンデレビウムまでが人工合成された。102番元素以降は、アメリカ合衆国とソビエト連邦の物理学者の間で、発見の優先権が争われた[33]。新しい元素とその発見を巡るこの争いは、後にw:Transfermium Warsと名付けられた[34]。
報告
[編集]105番元素の発見に関する最初の報告は、1968年4月にドゥブナ合同原子核研究所から出された。243Am原子核を標的として22Neイオンのビームを照射した。9.4 MeV(半減期0.1-3秒)及び9.7 eV(半減期0.05秒以上)のアルファ崩壊の後に、256103または257103のものと似たアルファ崩壊が続いたと報告した。以前の理論予測に基づき、2つの崩壊系列は、261105と260105に割り当てられた[35]。
- 243
95Am + 22
10Ne → 265-x
105 + x n (x=4, 5)
105番元素のアルファ崩壊の観測の後、この元素の自発核分裂を観測し、結果として生じる分裂断片を研究することが目指された。彼らは1970年2月に論文を発表し、半減期が14ミリ秒と2.2±0.5秒の複数の崩壊の事例を報告し、前者を242mfAm[注釈 10]、後者を105番元素の同位体に起因するとした。この反応の収率は242mfAmを生成する移行反応よりもかなり低く、理論予測と一致しているため、この崩壊が105番元素によるものではなく移行反応に起因する可能性は低いことが示唆された。
この崩壊が(22Ne,xn)反応に起因するものではないことを立証するために、243Am原子核を標的として18Oイオンを照射する実験が行われた。256103及び257103を生成する反応は自発核分裂をほとんど起こさず、より重い258103及び259103を生成する反応は自発核分裂を全く起こさなかった。これは理論データと一致した。その結果、観測された崩壊は、105番元素の自発核分裂に起因するものと結論付けられた[35]。
1970年4月、ローレンス・バークレー国立研究所のチームは、249Cf原子核に15Nイオンのビームを照射して9.1 MeVの崩壊を観測し、105番元素を合成したと主張した。この崩壊が別の反応に起因するものではないことを示すため、249Cfと14N、Pbと15N、Hgと15Nを用いた別の反応も試した。これらの反応では崩壊は観測されず、娘核の性質は256103とよく一致するものであったことから、親核は260105であることが示唆された[35]。
- 249
98Cf + 15
7N → 260
105 + 4 n
これらの結果は、9.4 MeVまたは9.7 MeVのエネルギーを持つ260105のアルファ崩壊を観測したドゥブナの発見と一致せず、合成された同位体の可能性は261105だけに絞られた[35]。
ドゥブナのチームは、その後、105番元素を生成する別の実験を行い、1970年5月に報告を公表した。彼らは、さらに多くの105番元素の原子核を合成し、この実験により以前の研究が裏付けられたと主張した。論文によると、彼らが作成した同位体は恐らく261105か260105であった[35]。この報告は、温度勾配ガスクロマトグラフィーによって、自発核分裂により形成されたものの塩化物が、四塩化ハフニウムではなく五塩化ニオブとほぼ一致することを初めて実証した。またチームは、エカタンタルの特性を示す揮発性塩化物の半減期2.2秒の自発核分裂を特定し、自発核分裂を起こした核種が105番元素に間違いないと推測した[35]。
1970年6月、ドゥブナのチームは、彼らの最初の実験を改良した。より純粋な標的を用い、またキャッチャーの前にコリメーターを設置することで移行反応の可能性を減らした。今回は、 娘核が256103または257103であることを示す9.1 MeVのアルファ崩壊が観測され、親核が260105か261105であることが示唆された[35]。
命名を巡る論争
[編集]ドゥブナのチームは、105番元素の合成を主張する最初の報告で、慣例として行われていた命名の提案をしなかった。そのため、バークレーのチームは、彼らが合成の主張を裏付ける十分な実験データを得られていないと信じた[36]。より多くのデータを集めた後、ドゥブナは、デンマークの核物理学者で原子構造理論及び量子理論の創設者であるニールス・ボーアの名前に因んだボーリウム(Bo)という名前を提案したが[37]、その後すぐに、ホウ素(boron)との混同を避けるため、ニールスボーリウム(Ns)に提案を変えた[38]。他に提案された名前には、ドブニウムがあった[39][40]。バークレーのチームは、105番元素の合成を最初に公表した際、ドイツの化学者で「核化学の父」と呼ばれるオットー・ハーンに因んだハーニウム(Ha)という名前を提案し、元素の命名を巡る論争が生じた[41]。
1970年代初期には、両チームは次の元素である106番元素の合成を報告したが、やはり名前を提案しなかった[42]。ドゥブナのチームは、発見の基準を明確にするための国際委員会の設立を提案した。この提案は1974年に受け入れられ、中立の合同グループが設立された[43]。どちらのチームも第三者に論争の解決を任せることを望まず、合同中立グループの設立を不要とし論争を内部で解決するために、バークレーのチームを率いるアルバート・ギオルソとグレン・シーボーグが1975年にドゥブナを訪問し、ドゥブナのチームを率いるゲオルギー・フリョロフ、ユーリイ・オガネシアンらと面会した。2時間の議論の後、これは失敗に終わった[44]。合同の中立グループは主張を評価するために集まることはなく、紛争は未解決のままとなった[43]。1979年、国際純正・応用化学連合(IUPAC)は、恒久的な名前が決定する前に仮名として用いられる、元素の系統名を提案した。これに基づき、105番元素はウンニルペンチウムとされたが、どちらのチームも彼らの主張を弱めることを望まず、これを無視した[45]。
1981年、西ドイツの重イオン研究所が107番元素の合成を主張した。この報告はドゥブナによる最初の報告より5年遅れていたが、より正確で発見に関するより強固な主張であった[35]。重イオン研究所は、この新元素にニールスボーリウムという名前を提案することで、ドゥブナの貢献に報いた[43]。ドゥブナは、105番元素に新しい名前を提案せず、まず発見者を確定することがより重要であると述べた[43]。
1985年、IUPACと国際純粋・応用物理学連合(IUPAP)は、議論のある元素について発見者を評価し、正式な名前を確定するために、超フェルミウム作業部会(TWG)を創設した[35]。競合する3つの機関から代表団を招いて会議を開催し、1990年に元素の認識の基準を策定し、1991年には発見を評価する作業を終了し、解散した。これらの結果は1993年に公表された。報告書によると、成功が確実な最初の実験は、1970年4月のバークレーでのもので、その直後6月のドゥブナでの実験が続いた。そのため、この元素の発見は、2つのチームが分け合うべきとされた[35]。
バークレーのチームは、レビューの中で、ドゥブナのチームは彼らの1年後にようやく105番元素を疑いなく合成できたに過ぎず、その成果が過大評価されていると主張したが、ドゥブナと重イオン研究所のチームはこの報告を支持した[43]。
1994年、IUPACは、議論のある元素の命名に関する勧告を公表し、105番元素については、フランスの物理学者で核物理学及び核化学の発展に貢献したフレデリック・ジョリオ=キュリーの名前に因むジョリオチウム(Jl)という名前を提案した。この名前は、もともとソビエト連邦のチームが、それまで長い間ノーベリウムと呼ばれていた102番元素に提案していたものだった[46]。この勧告は、いくつかの理由からアメリカの科学者に批判された。第一に、この提案はそれまでの提案をごちゃ混ぜにしたもので、もともとバークレーが104番元素と105番元素に提案していたラザホージウム、ハッシウムという名前を各々106番元素、108番元素に割り当てていた。第二に、バークレーが共同発見者と認識されていた104番元素と105番元素にはドゥブナの支持する名前が与えられた。第三に、そして最も重要なことには、1993年の報告で106番元素はバークレーの単独の発見であると認定されていたにもかかわらず、存命人物に因む元素名は認めないという新しい規則を元に、IUPACはこの元素に対するシーボーギウムという命名の提案を拒絶した[47]。
1995年、IUPACは議論を呼んだ規則を廃止し、妥協点を探し出すために、国家の代表による委員会を設立した。彼らは、106番元素をシーボーギウムと命名する代わりに、103番元素に対するローレンシウムという確立していた命名を除いて、他の全てのアメリカの提案を撤回するという提案をした。
102番元素に対して等しく定着していたノーベリウムという名前は、1993年の報告でこの元素の最初の合成がドゥブナによるものであると認定された後、ゲオルギー・フリョロフに因むフレロビウムという名前に置き換えられた。この決定はアメリカの科学者に拒絶され、撤回された[48][49]。フレロビウムという名前は、後に114番元素に用いられた[50]。
1996年、IUPACは別の会議を開催し、提案されていた全ての命名案を再検討し、一連の別の勧告を提案した。これは1997年に承認されて公表された[51]。105番元素はドゥブナという地名に因んでドブニウムと命名され、アメリカの提案は、102番、103番、104番、106番元素に使われた。ドブニウムという名前は、以前のIUPACの勧告では104番元素に用いられていた。アメリカの科学者は「しぶしぶ」この決定を受け入れた[52]。IUPACは、バークレーの提案は、既にバークリウム、カリホルニウム、アメリシウムの命名において複数認めれており、104番元素へのラザホージウム、106番元素へのシーボーギウムという命名は、104-106番元素の発見に対するドゥブナの貢献に報いることで相殺されるべきであると指摘した[53]。
1997年以降になっても、ローレンス・バークレー国立研究所は、自身の発行する論文誌等において105番元素に対するハーニウムという名前を用いることがあり、これは2014年まで続いた[54][55][56][57]。しかし、Radiochimica Acta誌のエディタであるJens Volker Kratzが、1997 年のIUPAC勧告を使用していない論文の受理を拒否したことで、この問題は解決された[58]。
同位体
[編集]
原子番号105のドブニウムは超重元素であり、このような大きな原子番号を持つ他の元素と同様に、非常に不安定である。半減期が最も長い既知の同位体は286Dbであり、半減期は約1日である[60]。安定同位体は知られておらず、2012年にドゥブナで行われた計算では、全てのドブニウム同位体の半減期は1日を大きく超えないことが示された[59][注釈 11]。ドブニウムは人工合成のみで得られる[注釈 12]。
短い半減期のため、ドブニウムの実験は難しい。さらに悪いことに、最も安定な同位体は、合成が最も難しい[63]。原子番号が小さい元素は、原子番号が大きい元素よりも中性子:陽子比が低い安定同位体を持っている。つまり、超重元素を合成するために使用する標的とビーム核は、これらの最も安定な同位体を形成するのに必要な量よりも少ない中性子を持つ(2010年代時点で、r過程と核子移行反応に基づく様々な技術が検討されているが、この分野では未だ大小の原子核の衝突に基づく技術が支配的である)[64][65]。
各々の実験で合成される268Dbは数原子のみであり、そのため、測定された寿命は過程によって大きく変わりうる。2022年時点で、ドゥブナで追加的に行われた実験では、268Dbの半減期は、16+6-4時間と測定されている[66]。 268Dbの次に安定な同位体である270Dbは、さらに合成例が少ない。合計3原子が報告されており、それぞれ33.4時間[67]、1.3時間、1.6時間で崩壊している[68]。これら2つは、ドブニウムの既知の最も重い同位体であり、これらを合成した実験はもともとドゥブナで、48Caビームのために設計されたものであったため、どちらも直接合成ではなく、より重い原子核である288Mc、294Tsの崩壊により生成される[69]。48Caは、実用可能な全ての安定原子核の中で、その質量に対して定量的及び相対的に中性子過剰が圧倒的に大きいものであるため[60]、より多くの中性子を含む超重原子核を合成するのに役立つが、この利点は、原子番号が高いほど核融合の可能性が低下することによって相殺される[70]。
予測される性質
[編集]周期表上では、ドブニウムは、バナジウム、ニオブ、タンタルとともに、第5族元素に分類される。105番元素の性質に関するいくつかの実験が行われ、周期律により予測される性質と一般的には一致することが確かめられた。しかし、原子的及び巨視的な物理的性質を大きく変える相対論効果により、大きく差が出る部分もある[注釈 13]。これらの性質は、超重元素の合成の難しさや収率の低さ、放射線対策の必要性、短い半減期等の様々な理由により、測定が難しくなっており、これまでのところ、単原子に対する実験のみが行われている[49]。
物理学的性質
[編集]
直接の相対論効果は、元素の原子番号が増えるにつれ、電子と原子核の間の静電引力が増加する結果、最内殻の電子が原子核の周りをより高速に回り始めることである。同様の効果は最外殻のs軌道(及びドブニウムでは空であるがp1/2軌道)でも見られ、例えば、7s軌道の大きさは25%収縮し、2.6 eV安定化する[49]。
より間接的な効果には、s軌道及びp1/2軌道による核子の電荷の遮蔽効果がより有効になり、外殻のd電子及びf電子に与えられる電荷が減少することで、より大きな軌道に移動する。ドブニウムはこの効果を大きく受け、他の第5族元素とは異なり、7s電子は6d電子よりも引き抜かれにくくなる[49]。

他の効果には、スピン軌道相互作用、特にスピン軌道分裂があり、6d小軌道(d殻の軌道角運動量lは2)が2つの小軌道に分裂する。10個の軌道のうち4つはlが3/2に下がり、一方6つはlが5/2に上がる。10個全てのエネルギー準位は上がり、そのうち4つは他の6つより低くなる(3つの6d電子は通常、最低のエネルギー準位6d3/2を占める)[49]。
1価のイオン化したドブニウム原子(Db+)は、中性原子と比べて6d電子を失いやすい。2価(Db2+)及び3価(Db3+)のイオン化原子は、より軽い同族元素と異なり、7s電子を失う。この変化に関わらず、ドブニウムはやはり5つの価電子を持つと推測され、7pエネルギー準位はドブニウム及びその性質に影響を与えていないように見える。ドブニウムの6d軌道はタンタルのの5d軌道よりも不安定化するため、Db3+は7s電子ではなく、2つの6d電子が残ると推測される。結果として生じる+3の酸化状態は不安定で、タンタルのものよりも生じにくいと推測される。最大の+5の酸化状態のドブニウムのイオン化エネルギーは、タンタルのものよりも若干低く、イオン半径はタンタルと比べて大きくなる。これは、ドブニウムの化学的性質に大きく影響している[49]。
固体状態のドブニウム原子は、他の第5族元素と同様、体心立方格子に配列する[71]。予想される密度は、21.6 g/cm3である[72]。
化学的性質
[編集]
分子間相互作用が取るに足りないものとして無視できるため、計算化学は、気相において最も単純化される。複数の研究者[49]が五フッ化ドブニウムの研究を行っており、計算によると、周期律に従って他の第5族元素と同様の性質を示す。例えば、分子軌道準位は、ドブニウムが推測どおり3つの6d電子準位を用いていることを示す。タンタルのアナログと比較すると、五フッ化ドブニウムは共有結合性が増加し、原子の有効電荷が減少し、ドブニウムと塩素の軌道間の重なりが大きくなることが推測される[49]。
溶液の化学的性質の計算では、最大の酸化状態である+5の状態がニオブやタンタルよりも安定化し、+3や+4の状態がより不安定化することが示される。最大酸化状態の陽イオンの加水分解の傾向は、第5族元素内で減少するはずであるが、それでも非常に急速であると予測される。ドブニウムの錯化は、その豊富さにおいて第5族元素の傾向を踏襲すると予測される。水酸化物錯体、塩化物錯体の計算では、第5族元素の錯体の形成や抽出の傾向と逆行し、タンタルと比べてより逆行しやすいことが示される[49]。
ドブニウムに関する実験
[編集]ドブニウムの化学的性質に関する実験は、1974年から1976年まで遡る。ドゥブナの研究者は、サーモクロマトグラフィーを用いて臭化ドブニウムは臭化ニオブよりも揮発性が低く、臭化ハフニウムと同程度であると結論付けた。検出された分裂生成物は確定しておらず、親核が本当に105番元素であったかどうかははっきり分かっていない。これらの結果は、ドブニウムがニオブよりもタンタルと似た挙動を示すことを示唆する[49]。
ドブニウムの化学的性質に関する次の実験は、1988年にバークレーで行われ、水溶液中でドブニウムの最も安定な酸化状態が+5であるかどうかが確かめられた。2度燻蒸し、濃硝酸で洗って、スライドガラス上に吸着したドブニウムを、同様の処理を行った第5族元素のニオブ、タンタル、第4族元素のジルコニウム、ハフニウムと比較した。第5族元素はガラス表面に吸着することが知られているが、第4族元素はそうではなく、ドブニウムは第5族であることが確認された。驚いたことに、硝酸/フッ化水素酸混合物溶液からメチルイソブチルケトンへの抽出物の挙動は、ドブニウム、タンタル、ニオブの間で異なった。ドブニウムは抽出されず、その挙動はタンタルよりもニオブと似ており、錯化挙動は周期表の族の中での傾向を単に外挿するだけでは予測できないことが示された[49]。
これにより、ドブニウム錯体の化学的挙動のさらなる研究が促されることとなった。1988年から1993年まで、いくつかの研究所が共同で数千回に及ぶクロマトグラフィー実験を繰り返した。第5族の全ての元素とプロトアクチニウムを濃塩酸から抽出し、低濃度の塩化水素と混合した後、少量のフッ化水素を添加して、選択的再抽出が開始された。ドブニウムは、塩化水素濃度が12 M以下の範囲で、タンタルとは異なるがニオブや擬同族体であるプロトアクチニウムと似た挙動を示した。2つの元素のこの類似性は、形成された錯体がDbOX4-または[Db(OH)2X4]-であることを示す。臭化水素からプロトアクチニウム用の抽出剤であるジイソブチルカルビオール(2,6-ジメチルヘプタン-4-オール)でドブニウムを抽出した後、続いて塩化水素/臭化水素の混合物と塩化水素で溶出し、ドブニウムはプロトアクチニウムやニオブと比べて抽出されにくい傾向があることが示された。これは、複数負電荷を持った抽出できない錯体の形成が増える傾向から説明される。1992年に行われた追加の実験で、+5状態の安定化が確認された。Db(V)は、他の第5族元素やプロトアクチニウムと同様にα-ヒドロキシイソ酪酸を用いて陽イオン交換樹脂から抽出可能であることが示されたが、Db(III)とDb(IV)はそうではない。1998年と1999年には、新しい予測により、ハロゲン化溶液から、ニオブとほぼ同程度、タンタルよりもよく抽出されることが示され、後に確認された[49]。
半減期35秒の262Dbを用いて、等温ガスクロマトグラフィーの実験が1992年に初めて行われた。ニオブとタンタルの揮発性は誤差の範囲内で類似していたが、ドブニウムは揮発性が若干低かった。これは、系の中の痕跡量の酸素が、DbBr5よりも揮発性が低いと予測されるDbOBr3の形成を促進していたためと推測された。1996年の実験で、タンタルを除く第5族元素の塩化物は、対応する臭化物と比べて揮発性が高いことが示され、これは恐らくTaOCl3の形成のためであると考えられた。後に行われた実験では、ドブニウムとニオブを制御された酸素分圧の関数とし、生成した酸塩化物の揮発性は、一般的に酸素の濃度に依存することが示された。また酸塩化物は塩化物よりも揮発しにくいことが示された[49]。
2004-05年、ドゥブナとリバモアの研究者は、新しく合成された115番元素(モスコビウム)の5回目のアルファ崩壊の生成物として、ドブニウムの新しい同位体268Dbを同定した。この新しい同位体は、約1日の半減期で、化学実験を行うのに十分な寿命を持つことが明らかとなり、2004年、標的の表面からドブニウムを含む薄層を除去し、トレーサー、ランタンキャリアとともに王水に溶解し、水酸化アンモニウムを加えると、そこから、+3、+4、+5の様々な化学種が沈殿した。沈殿を洗って塩酸に溶かすと硝酸塩に変化し、その後薄層上で乾燥させ、計数した。大部分は+5の化学種であり、すぐにドブニウムに由来するものと判断されたが、+4の化学種も存在し、この結果から、チームはさらなる化学分離が必要であると決定した。2005年にこの実験が繰り返され、最終生成物は硝酸塩の沈殿ではなく水酸化物であることが分かり、リバモアでは逆相クロマトグラフィー、ドゥブナでは陰イオン交換クロマトグラフィーにより、さらなる処理が行われた。+5の化学種は効率的に分離された。ドブニウムは、タンタルのみの画分に3回現れ、ニオブのみの画分には全く現れなかった。これらの実験は、ドブニウムの一般的な化学プロファイルを描くには不十分なものであったことには留意が必要である[73]。
2009年、日本原子力研究開発機構のタンデム加速器内で、ニオブがNbOF4-、タンタルがTaF6-を形成する程度の濃度で、硝酸とフッ化水素酸によるドブニウムの処理が行われた。ドブニウムの挙動は、ニオブの挙動と似ているがタンタルの挙動とは似ておらず、ドブニウムがDbOF4-を形成していることが示唆された。入手可能な情報から、ドブニウムはしばしばニオブと、また時にプロトアクチニウムと似た挙動を示すが、タンタルと似た挙動は滅多に示さないと結論付けられた[74]。
2021年、日本原子力研究開発機構のタンデム加速器を用いて第5族元素の揮発性の酸塩化物MOCl3 (M = Nb, Ta, Db)の実験が行われた。揮発性の傾向は、NbOCl3 > TaOCl3 > DbOCl3であり、周期律に従った傾向を示した[75]。
脚注
[編集]- ^ 核物理学では、原子番号の大きい元素は、「重い」元素と呼ばれる。原子番号82の鉛は、重い元素の一例である。「超重元素」という用語は、通常、原子番号103番以降の元素を指す(ただし、原子番号100[4]以降とするものや112以降[5]とするもの等、いくつかの定義がある。超アクチノイド元素と同義の言葉として使われることもある[6])。ある元素における「重い同位体」や「重い核」という言葉は、各々、質量の大きい同位体、質量の大きい核を指す。
- ^ 2009年、ユーリイ・オガネシアン率いるドゥブナ合同原子核研究所のチームは、対称の136Xe + 136Xe反応におるハッシウム合成の試みの結果について公表した。彼らはこの反応で単原子を観測できず、反応断面積の上限を2.5 pbとした[7]。対称的に、ハッシウムの発見に繋がった反応である208Pb + 58Feの反応断面積は、発見者らにより19+19-11pbと推定された[8]。
- ^ 励起エネルギーが大きくなるほど、より多くの中性子が放出される。励起エネルギーが、各々の中性子を残りの核子に結び付けるエネルギーより低い場合、中性子は放出されない。その代わり、複合核はガンマ線を放出して脱励起する[12]。
- ^ 共同作業部会による定義では、その核が10-14秒にわたり崩壊しない場合にのみ、発見として認定される。この値は、原子核が外側の電子を獲得して化学的性質を示すのにかかる時間の推定値として選択された[13]。また、一般的に考えられる複合核の寿命の上限値を示すものでもある[14]。
- ^ この分離は、生成した原子核が未反応の粒子線の原子核よりも、標的の上をよりゆっくり通り過ぎることに基づく。セパレーター内には、特定の粒子速度で移動する粒子への影響が相殺される電磁場がある[16]。このような分離は、飛行時間型質量分析計や反跳エネルギー測定でも用いられ、この2つを組み合わせて、原子核の質量を推定することが可能となる[17]。
- ^ 全ての崩壊モードが静電反発を原因とするのではなく、例えば、ベータ崩壊の原因は弱い相互作用である[20]。
- ^ 原子核の質量は直接測定されず、ほかの原子核の値から計算され、このような方法を間接的と呼ぶ。直接測定も可能であるが、もっとも重い原子核についてはほとんどの場合可能ではない[23]。超重元素の質量の直接測定は、2018年にローレンス・バークレー国立研究所により初めて報告された[24]。
- ^ 自発核分裂は、ドゥブナ合同原子核研究所を率いていたゲオルギー・フリョロフにより発見され[25]、この研究所の得意分野となった[26]。対称的に、ローレンス・バークレー国立研究所の科学者は、自発核分裂から得られる情報は新元素の合成を裏付けるのに不十分であると信じていた。これは、複合核が中性子だけを放出し、陽子やアルファ粒子のような荷電粒子を放出しないことを立証するのは困難なためである[14]。そのため彼らは、連続的なアルファ崩壊により、新しい同位体を既知の同位体と結び付ける方法を好んだ[25]。
- ^ 例えば、1957年にスウェーデンのノーベル物理学研究所は、102番元素を誤同定した[27]。これ以前にこの元素の合成に関する決定的な主張はなく、発見者により、ノーベリウムと命名されたが、後に、この同定は誤りであったことが分かった[28]。翌年、ローレンス・バークレー国立研究所は、ノーベル物理学研究所による結果は再現性がなく、代わりに彼ら自身がこの元素を合成したと発表したが、この主張も後に誤りであったことが判明した[28]。ドゥブナ合同原子核研究所は、彼らこそがこの元素を最初に合成したと主張し、ジョリオチウムと命名したが[29]、この名前も認定されなかった(ドゥブナ合同原子核研究所は、のちに、102番元素の命名は「性急」であったと述べた)[30]。「ノーベリウム」という名前は、広く使われていたため、変更されなかった[31]。
- ^ この表記は、核が自然分裂によって崩壊する核異性体であることを意味している。
- ^ 268Dbの半減期の現在の実験値は28+11
-4時間であるが、実験 (崩壊) の数が非常に限られているため、半減期の決定が依存する大数の法則を直接適用することはできない。不確実性の範囲は、95%の確からしさで半減期がこの範囲内にあることを示す。 - ^ 原子核に関する現代の理論は、ドブニウムの長寿命同位体が存在することを示唆していないが、かつては、超重元素の未知の同位体が原始地球上に存在していたという主張がなされていた。例えば、1963 年には、4億年から5億年の半減期を持つ267108[61]、2009年には1億年以上の半減期を持つ292122[62]が存在するという主張がなされたが、どちらの主張も合意が得られていない。
- ^ 相対論効果は、物体が光速に近い速度で移動する時に生じる。原子の場合、高速に移動する物体は電子である。
出典
[編集]- ^ Münzenberg, G.; Gupta, M. (2011). Production and Identification of Transactinide Elements. pp. 877. doi:10.1007/978-1-4419-0720-2_19.
- ^ a b c d e http://newscenter.lbl.gov/news-releases/2010/10/26/six-new-isotopes/
- ^ Oganessian, Yu. Ts.; Abdullin, F. Sh.; Bailey, P. D.; Benker, D. E.; Bennett, M. E.; Dmitriev, S. N.; Ezold, J. G.; Hamilton, J. H. et al. (2010). “Synthesis of a New Element with Atomic Number Z=117”. Physical Review Letters 104. doi:10.1103/PhysRevLett.104.142502. PMID 20481935.
- ^ Kramer, K. (2016年). “Explainer: superheavy elements”. Chemistry World. 2020年3月15日閲覧。
- ^ “Discovery of Elements 113 and 115”. Lawrence Livermore National Laboratory. 2015年9月11日時点のオリジナルよりアーカイブ。2020年3月15日閲覧。
- ^ Eliav, E.; Kaldor, U.; Borschevsky, A. (2018). "Electronic Structure of the Transactinide Atoms". In Scott, R. A. (ed.). Encyclopedia of Inorganic and Bioinorganic Chemistry. John Wiley & Sons. pp. 1–16. doi:10.1002/9781119951438.eibc2632. ISBN 978-1-119-95143-8. S2CID 127060181。
- ^ Oganessian, Yu. Ts.; Dmitriev, S. N.; Yeremin, A. V. et al. (2009). “Attempt to produce the isotopes of element 108 in the fusion reaction 136Xe + 136Xe”. Physical Review C 79 (2): 024608. doi:10.1103/PhysRevC.79.024608. ISSN 0556-2813.
- ^ Munzenberg, G.; Armbruster, P.; Folger, H. et al. (1984). “The identification of element 108”. Zeitschrift fur Physik A 317 (2): 235-236. Bibcode: 1984ZPhyA.317..235M. doi:10.1007/BF01421260 20 June 2024閲覧。.
- ^ Subramanian, S. (2019年). “Making New Elements Doesn't Pay. Just Ask This Berkeley Scientist”. Bloomberg Businessweek. November 14, 2020時点のオリジナルよりアーカイブ。2020年1月18日閲覧。
- ^ Ivanov, D. (2019年). “Сверхтяжелые шаги в неизвестное” [Superheavy steps into the unknown] (ロシア語). N+1. 2020年2月2日閲覧。
- ^ Hinde, D. (2014年). “Something new and superheavy at the periodic table”. The Conversation. 2020年1月30日閲覧。
- ^ a b Krasa, A. (2010年). “Neutron Sources for ADS”. Czech Technical University in Prague. pp. 4-8. 2019年3月3日時点のオリジナルよりアーカイブ。October 20, 2019閲覧。
- ^ Wapstra, A. H. (1991). “Criteria that must be satisfied for the discovery of a new chemical element to be recognized”. Pure and Applied Chemistry 63 (6): 883. doi:10.1351/pac199163060879. ISSN 1365-3075 2020年8月28日閲覧。.
- ^ a b Hyde, E. K.; Hoffman, D. C.; Keller, O. L. (1987). “A History and Analysis of the Discovery of Elements 104 and 105”. Radiochimica Acta 42 (2): 67-68. doi:10.1524/ract.1987.42.2.57. ISSN 2193-3405.
- ^ a b c Chemistry World (2016年). “How to Make Superheavy Elements and Finish the Periodic Table [Video]”. Scientific American. 2020年1月27日閲覧。
- ^ Hoffman, Ghiorso & Seaborg 2000, p. 334.
- ^ Hoffman, Ghiorso & Seaborg 2000, p. 335.
- ^ Zagrebaev, Karpov & Greiner 2013, p. 3.
- ^ Beiser 2003, p. 432.
- ^ Beiser 2003, p. 439.
- ^ Staszczak, A.; Baran, A.; Nazarewicz, W. (2013). “Spontaneous fission modes and lifetimes of superheavy elements in the nuclear density functional theory”. Physical Review C 87 (2): 024320-1. arXiv:1208.1215. Bibcode: 2013PhRvC..87b4320S. doi:10.1103/physrevc.87.024320. ISSN 0556-2813.
- ^ Audi et al. 2017, pp. 030001-128–030001-138.
- ^ Oganessian, Yu. Ts.; Rykaczewski, K. P. (2015). “A beachhead on the island of stability”. Physics Today 68 (8): 32-38. Bibcode: 2015PhT....68h..32O. doi:10.1063/PT.3.2880. ISSN 0031-9228. OSTI 1337838.
- ^ Grant, A. (2018). “Weighing the heaviest elements”. Physics Today. doi:10.1063/PT.6.1.20181113a.
- ^ a b Robinson, A. E. (2019). “The Transfermium Wars: Scientific Brawling and Name-Calling during the Cold War”. Distillations 2020年2月22日閲覧。.
- ^ “Популярная библиотека химических элементов. Сиборгий (экавольфрам)” [Popular library of chemical elements. Seaborgium (eka-tungsten)] (ロシア語). n-t.ru. 2020年1月7日閲覧。 Reprinted from “Экавольфрам [Eka-tungsten]” (ロシア語). Популярная библиотека химических элементов. Серебро - Нильсборий и далее [Popular library of chemical elements. Silver through nielsbohrium and beyond]. Nauka. (1977)
- ^ “Nobelium - Element information, properties and uses | Periodic Table”. Royal Society of Chemistry. 2020年3月1日閲覧。
- ^ a b Kragh 2018, pp. 38–39.
- ^ Kragh 2018, p. 40.
- ^ Ghiorso, A.; Seaborg, G. T.; Oganessian, Yu. Ts. et al. (1993). “Responses on the report 'Discovery of the Transfermium elements' followed by reply to the responses by Transfermium Working Group”. Pure and Applied Chemistry 65 (8): 1815-1824. doi:10.1351/pac199365081815. オリジナルの25 November 2013時点におけるアーカイブ。 7 September 2016閲覧。.
- ^ Commission on Nomenclature of Inorganic Chemistry (1997). “Names and symbols of transfermium elements (IUPAC Recommendations 1997)”. Pure and Applied Chemistry 69 (12): 2471-2474. doi:10.1351/pac199769122471.
- ^ Choppin, G. R.; Liljenzin, J.-O.; Rydberg, J. (2002). Radiochemistry and Nuclear Chemistry. Elsevier. p. 416. ISBN 978-0-7506-7463-8
- ^ Hoffman, D. C. (1996). The Transuranium Elements: From Neptunium and Plutonium to Element 112 (PDF) (Report). Lawrence Livermore National Laboratory. 2017年10月9日時点のオリジナルよりアーカイブ (PDF)。2017年10月10日閲覧。
- ^ Karol, P. (1994). “The Transfermium Wars”. Chemical & Engineering News 74 (22): 2-3. doi:10.1021/cen-v072n044.p002.
- ^ a b c d e f g h i j Barber, R. C.; Greenwood, N. N.; Hrynkiewicz, A. Z. et al. (1993). “Discovery of the Transfermium elements”. Pure and Applied Chemistry 65 (8): 1757. doi:10.1351/pac199365081757 September 7, 2016閲覧。.
- ^ "Dubnium | chemical element". Encyclopedia Britannica (英語). 2018年3月25日閲覧。
- ^ Stadtler, Ingrid; Niemann, Hans (1971) (ドイツ語). Symbolik und Fachausdruecke. Mathematik, Physik, Chemie. Germany: Verlag Enzyklopadie. p. 83
- ^ (フランス語) Industries atomiques et spatiales, Volume 16. Switzerland. (1972). pp. 30-31
- ^ Radiochemistry. Royal Society of Chemistry. (1972). ISBN 9780851862545
- ^ Suomen kemistilehti. Suomalaisten Kemistien Seura.. (1971)
- ^ Fontani, M.; Costa, M.; Orna, M. V. (2014). The Lost Elements: The Periodic Table's Shadow Side. Oxford University Press. p. 386. ISBN 978-0-19-938335-1. オリジナルのFebruary 27, 2018時点におけるアーカイブ。
- ^ Hoffmann, K. (1987) (ロシア語). Можно ли сделать золото? Мошенники, обманщики и ученые в истории химических элементов [Can one make gold? Swindlers, deceivers and scientists from the history of the chemical elements]. Nauka. pp. 180-181 Translation from Hoffmann, K. (1979) (ドイツ語). Kann man Gold machen? Gauner, Gaukler und Gelehrte. Aus der Geschichte der chemischen Elemente [Can one make gold? Swindlers, deceivers and scientists. From the history of the chemical elements]. Urania
- ^ a b c d e Ghiorso, A.; Seaborg, G. T.; Oganessian, Yu. Ts. et al. (1993). “Responses on the report 'Discovery of the Transfermium elements' followed by reply to the responses by Transfermium Working Group”. Pure and Applied Chemistry 65 (8): 1815-1824. doi:10.1351/pac199365081815. オリジナルの25 November 2013時点におけるアーカイブ。 7 September 2016閲覧。.
- ^ Robinson, A. (2017). “An Attempt to Solve the Controversies Over Elements 104 and 105: A Meeting in Russia, 23 September 1975”. Bulletin of the American Physical Society 62 (1): B10.003. Bibcode: 2017APS..APRB10003R October 14, 2017閲覧。.
- ^ Ohrstrom, L.; Holden, N. E. (2016). “The Three-letter Element Symbols”. Chemistry International 38 (2). doi:10.1515/ci-2016-0204.
- ^ “Names and symbols of transfermium elements (IUPAC Recommendations 1994)”. Pure and Applied Chemistry 66 (12): 2419-2421. (1994). doi:10.1351/pac199466122419 June 20, 2024閲覧。.
- ^ Yarris, L. (1994年). “Naming of element 106 disputed by international committee”. September 7, 2016閲覧。
- ^ Hoffman, Ghiorso & Seaborg 2000, pp. 389–394
- ^ a b c d e f g h i j k l m Hoffman, D. C.; Lee, D. M.; Pershina, V. (2006). “Transactinides and the future elements”. In Morss, L.R.; Edelstein, N. M.; Fuger, Jean. The Chemistry of the Actinide and Transactinide Elements (3rd ed.). Springer Science+Business Media. pp. 1652–1752. ISBN 978-1-4020-3555-5
- ^ Loss, R. D.; Corish, J. (2012). “Names and symbols of the elements with atomic numbers 114 and 116 (IUPAC Recommendations 2012)”. Pure and Applied Chemistry 84 (7): 1669-1672. doi:10.1351/PAC-REC-11-12-03 21 April 2018閲覧。.
- ^ Bera, J. K. (1999). “Names of the Heavier Elements”. Resonance 4 (3): 53-61. doi:10.1007/BF02838724.
- ^ Hoffman, Ghiorso & Seaborg 2000, pp. 369–399
- ^ “Names and symbols of transfermium elements (IUPAC Recommendations 1997)”. Pure and Applied Chemistry 69 (12): 2471-2474. (1997). doi:10.1351/pac199769122471.
- ^ “Periodic Table of the Elements”. lbl.gov. Lawrence Berkeley National Laboratory (1999年). 6 December 2022閲覧。
- ^ Wilk, P. A. (2001). Properties of Group Five and Group Seven transactinium elements (PhD). University of California, Berkeley. doi:10.2172/785268. 2022年12月6日閲覧。
- ^ Buhler, Brendan (2014年). “Branding the Elements: Berkeley Stakes its Claims on the Periodic Table”. alumni.berkeley.edu. Cal Alumni Association. 6 December 2022閲覧。 “Poor element 105 has had five different names-Berkeley partisans still call it hahnium.”
- ^ @BerkeleyLab (2014年1月8日). "#16elements from Berkeley Lab: mendelevium, nobelium, lawrencium, rutherfordium, hahnium, seaborgium". X(旧Twitter)より2022年12月23日閲覧。
- ^ Armbruster, Peter; Munzenberg, Gottfried (2012). “An experimental paradigm opening the world of superheavy elements”. The European Physical Journal H 37: 237-309. doi:10.1140/epjh/e2012-20046-7 6 December 2022閲覧。.
- ^ a b Karpov, A. V.; Zagrebaev, V. I.; Palenzuela, Y. M.; Greiner, W. (2013). Greiner, W.. ed (英語). Exciting Interdisciplinary Physics. FIAS Interdisciplinary Science Series. Springer International Publishing. pp. 69-79. doi:10.1007/978-3-319-00047-3_6. ISBN 978-3-319-00046-6
- ^ a b Audi, G.; Kondev, F. G.; Wang, M. et al. (2012). “The NUBASE2012 evaluation of nuclear properties”. Chinese Physics C 36 (12): 1157-1286. Bibcode: 2012ChPhC..36....1A. doi:10.1088/1674-1137/36/12/001.
- ^ Emsley, J. (2011). Nature's Building Blocks: An A-Z Guide to the Elements (New ed.). New York: Oxford University Press. pp. 215-217. ISBN 978-0-19-960563-7
- ^ Marinov, A.; Rodushkin, I.; Kolb, D. et al. (2010). “Evidence for a long-lived superheavy nucleus with atomic mass number A=292 and atomic number Z=~122 in natural Th”. International Journal of Modern Physics E 19 (1): 131-140. arXiv:0804.3869. Bibcode: 2010IJMPE..19..131M. doi:10.1142/S0218301310014662.
- ^ Karpov, A. V.; Zagrebaev, V. I.; Palenzuela, Y. M. et al. (2013). “Superheavy Nuclei: Decay and Stability”. Exciting Interdisciplinary Physics. FIAS Interdisciplinary Science Series. p. 69. doi:10.1007/978-3-319-00047-3_6. ISBN 978-3-319-00046-6
- ^ Botvina, Al.; Mishustin, I.; Zagrebaev, V. et al. (2010). “Possibility of synthesizing superheavy elements in nuclear explosions”. International Journal of Modern Physics E 19 (10): 2063-2075. arXiv:1006.4738. Bibcode: 2010IJMPE..19.2063B. doi:10.1142/S0218301310016521.
- ^ Wuenschel, S.; Hagel, K.; Barbui, M. et al. (2018). “An experimental survey of the production of alpha decaying heavy elements in the reactions of 238U +232Th at 7.5-6.1 MeV/nucleon”. Physical Review C 97 (6): 064602. arXiv:1802.03091. Bibcode: 2018PhRvC..97f4602W. doi:10.1103/PhysRevC.97.064602.
- ^ Oganessian, Yu. Ts.; Utyonkov, V. K.; Kovrizhnykh, N. D. et al. (29 September 2022). “First experiment at the Super Heavy Element Factory: High cross section of 288Mc in the243Am+48Ca reaction and identification of the new isotope 264Lr”. Physical Review C 106 (3): L031301. doi:10.1103/PhysRevC.106.L031301.
- ^ Oganessian, Yu. Ts.; Abdullin, F. Sh.; Bailey, P. D. et al. (2010). “Synthesis of a New Element with Atomic Number Z=117”. Physical Review Letters 104 (14): 142502. Bibcode: 2010PhRvL.104n2502O. doi:10.1103/PhysRevLett.104.142502. PMID 20481935.
- ^ Khuyagbaatar, J.; Yakushev, A.; Dullmann, Ch. E. et al. (2014). “48Ca + 249Bk Fusion Reaction Leading to Element Z = 117: Long-Lived α-Decaying 270Db and Discovery of 266Lr”. Physical Review Letters 112 (17): 172501. Bibcode: 2014PhRvL.112q2501K. doi:10.1103/PhysRevLett.112.172501. hdl:1885/148814. PMID 24836239.
- ^ Wills, S.; Berger, L. (2011). “Science Magazine Podcast. Transcript, 9 September 2011”. Science. オリジナルのOctober 18, 2016時点におけるアーカイブ。 October 12, 2016閲覧。.
- ^ Oganessian, Yu. Ts.; Sobiczewski, A.; Ter-Akopian, G. M. (2017). “Superheavy nuclei: from prediction to discovery”. Physica Scripta 92 (2): 023003. Bibcode: 2017PhyS...92b3003O. doi:10.1088/1402-4896/aa53c1.
- ^ Östlin, A.; Vitos, L. (2011). “First-principles calculation of the structural stability of 6d transition metals”. Physical Review B 84 (11). Bibcode: 2011PhRvB..84k3104O. doi:10.1103/PhysRevB.84.113104.
- ^ Gyanchandani, Jyoti; Sikka, S. K. (10 May 2011). “Physical properties of the 6 d -series elements from density functional theory: Close similarity to lighter transition metals”. Physical Review B 83 (17): 172101. doi:10.1103/PhysRevB.83.172101.
- ^ Stoyer, N. J.; Landrum, J. H.; Wilk, P. A. (2006年). Chemical Identification of a Long-Lived Isotope of Dubnium, a Descendant of Element 115 (Report). IX International Conference on Nucleus Nucleus Collisions. doi:10.1016/j.nuclphysa.2006.12.060. 2024年6月20日閲覧。
- ^ Nagame, Y.; Kratz, J. V.; Schadel, M. (2016). “Chemical properties of rutherfordium (Rf) and dubnium (Db) in the aqueous phase” (英語). EPJ Web of Conferences 131: 07007. Bibcode: 2016EPJWC.13107007N. doi:10.1051/epjconf/201613107007.
- ^ Chiera, Nadine M.; Sato, Tetsuya K.; Eichler, Robert et al. (2021). “Chemical Characterization of a Volatile Dubnium Compound, DbOCl3”. Angewandte Chemie International Edition 60 (33): 17871-17874. doi:10.1002/anie.202102808.
関連文献
[編集]- Audi, G.; Kondev, F. G.; Wang, M. et al. (2017). “The NUBASE2016 evaluation of nuclear properties”. Chinese Physics C 41 (3): 030001. Bibcode: 2017ChPhC..41c0001A. doi:10.1088/1674-1137/41/3/030001.
- Beiser, A. (2003). Concepts of modern physics (6th ed.). McGraw-Hill. ISBN 978-0-07-244848-1. OCLC 48965418
- Hoffman, D. C.; Ghiorso, A.; Seaborg, G. T. (2000). The Transuranium People: The Inside Story. World Scientific. ISBN 978-1-78-326244-1
- Kragh, H. (2018). From Transuranic to Superheavy Elements: A Story of Dispute and Creation. Springer Science+Business Media. ISBN 978-3-319-75813-8
- Zagrebaev, V.; Karpov, A.; Greiner, W. (2013). “Future of superheavy element research: Which nuclei could be synthesized within the next few years?”. Journal of Physics: Conference Series 420 (1): 012001. arXiv:1207.5700. Bibcode: 2013JPhCS.420a2001Z. doi:10.1088/1742-6596/420/1/012001. ISSN 1742-6588.
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| |||||||||||||||||||||||||||||||||




