塩化アルミニウム
| 塩化アルミニウム | |
|---|---|
| |
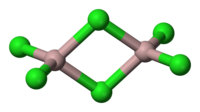
三塩化アルミニウム | |
| 識別情報 | |
| CAS登録番号 | 7446-70-0 10124-27-3 (六水和物) |
| PubChem | 24012 |
| ChemSpider | 22445 |
| UNII | LIF1N9568Y |
| RTECS番号 | BD0530000 |
| ATC分類 | D10AX01 |
| |
| |
| 特性 | |
| 化学式 | AlCl3 |
| モル質量 | 133.34 g/mol(無水物) 241.43 g/mol(六水和物) |
| 外観 | 白色、または淡黄色固体 潮解性 |
| 密度 | 2.48 g/cm3(無水物) 1.3 g/cm3(六水和物) |
| 融点 |
192.4 ℃(無水物) |
| 沸点 |
120 ℃(六水和物) |
| 水への溶解度 | 43.9 g/100 ml (0 ℃) 44.9 g/100 ml (10 ℃) 45.8 g/100 ml (20 ℃) 46.6 g/100 ml (30 ℃) 47.3 g/100 ml (40 ℃) 48.1 g/100 ml (60 ℃) 48.6 g/100 ml (80 ℃) 49 g/100 ml (100 ℃) |
| 溶解度 | 塩化水素、エタノール、クロロホルム、四塩化炭素に可溶。ベンゼンに微溶。 |
| 構造 | |
| 結晶構造 | 単斜晶、mS16 |
| 空間群 | C12/m1, No. 12 |
| 配位構造 | 八面体(固体) 四面体(液体) |
| 分子の形 | 平面三角形(気体モノマー) |
| 危険性 | |
| EU分類 | 腐食性 (C) |
| Rフレーズ | R34 |
| Sフレーズ | (S1/2), S7/8, S28, S45 |
| 半数致死量 LD50 | 無水物: 380 mg/kg, ラット(経口) 六水和物: 3311 mg/kg, ラット(経口) |
| 関連する物質 | |
| その他の陰イオン | フッ化アルミニウム 臭化アルミニウム ヨウ化アルミニウム |
| その他の陽イオン | 三塩化ホウ素 三塩化ガリウム 三塩化インジウム 塩化マグネシウム |
| 関連するルイス酸 | 塩化鉄(III) 三フッ化ホウ素 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
塩化アルミニウム(えんかあるみにうむ、英語: Aluminium chloride)はアルミニウムの塩化物で、無水物と6水和物が知られている。組成式AlCl3で表される物質である。塩基性塩化アルミニウムの重合体を指して塩化アルミニウムと呼ぶ場合もある。塩化アルミニウム(ポリ塩化アルミニウム・アルミナ10%換算値)2008年度日本国内生産量は582,542t、工業消費量は9,036tである[1]。
生成
[編集]金属アルミニウムと塩素、または塩化水素との反応で無水塩化アルミニウムは生成される。
塩化アルミニウムの水和物は無水塩化アルミニウムを塩酸に溶かし生成する。また、水酸化アルミニウムと塩酸の反応、
塩酸と金属アルミニウムの直接反応でも得られる。[2]
無水塩化アルミニウム
[編集]
融点 170.9 ℃の白色固体で重合体を形成している。不純物を含むものは淡黄色を帯びる。液体状態では二量体を形成することが知られ、電気伝導度が低い等アルミニウムと塩素との結合は共有結合性である。
160 ℃より昇華性を示し、気体は二量体 Al2Cl6 を形成しており、800 ℃以上で単量体となることが知られている。
金属アルミニウムに直接塩素や塩化水素を作用させて製造する。フリーデル・クラフツ反応などルイス酸触媒として有機化学反応等に用いられる。 アルミニウムイオンは水との親和性が強く、激しく加水分解して塩化水素を発生する。
その為、湿気を含む空気中では白煙を発する。エンタルピーの値から分かるように、逆に6水和物から無水物を得る場合は厳しい反応条件を要する。
塩化アルミニウム6水和物
[編集]
で示される化合物で、アルミニウムに水分子が6つ配位した錯イオンと塩化物イオンとから構成されるイオン性物質。水に溶解すると部分的に水酸化アルミニウムと塩酸とに加水分解する。水溶液を加熱しても再結晶はされず、水酸化アルミニウムが析出する[2]。
6水和物は水酸化アルミニウムを塩酸に溶かし、さらに塩化水素ガスを導入して飽和させると得られる。塩析剤や木材の防腐剤、染色剤、写真の定着、防臭あるいは医療用の防汗剤として利用される。
ポリ塩化アルミニウム
[編集]水酸化アルミニウムを塩酸に溶解すると塩基性塩化アルミニウムの重合体 が生成し、これをポリ塩化アルミニウムと呼ぶ。主に、上下水道の凝集剤として用いられる。
排出基準
[編集]アルミニウムイオンは有害で魚毒性や植物の生育阻害要因となり得るため、水道法の水質基準ではアルミニウム濃度を0.1ppm未満に抑えることが求められる。[4]
このため過度の使用は避け適正な利用が必要である。
空気酸化
[編集]長時間空気中に放置すると酸化され酸化アルミニウムの白色結晶が析出するので注意が必要。[5]
安全性
[編集]神経毒性
[編集]塩化アルミニウムは神経毒として確立されている。ミクログリアの活性化を抑制する作用、血液脳関門(BBB)における膜機能の変化などが示唆されている[6][7][8][9]。
医療用途
[編集]アジュバント(抗原性補強剤)
[編集]- ワクチンの効果を強める目的で添加されている。ジフテリアワクチン、二種混合ワクチン(DTワクチン, ジフテリア・破傷風混合)、三種混合ワクチンなどに塩化アルミニウムがアジュバントとして添加されている。他のワクチンにもアルミニウム化合物が添加されていることが多い。アルミニウム化合物は、世界初のアジュバントとして1926年に認可され90年以上の歴史がある[10]。
ニキビ(尋常性痤瘡)治療
[編集]局所多汗症治療
[編集]- 局所多汗症治療の第一選択肢として、塩化アルミニウム水溶液の外用が適用となる。塩化アルミニウムが角層内の汗管と結合し、発汗の出口をふさぐことによる制汗作用と考えられている[12]。塩化アルミニウム溶液は病院での院内製剤として、10〜50%溶液が処方されている[13]。
脚注
[編集]- ^ 統計表一覧(経済産業省生産動態統計) - 経済産業省
- ^ a b 『日本大百科全書(ニッポニカ)』小学館、2014年。
- ^ 村上雅彦「アルミニウムの化学 : 有機合成反応における利用(身近な元素の世界)」『化学と教育』第61巻第11号、日本化学会、2013年、548-553頁、doi:10.20665/kakyoshi.61.11_548、ISSN 03862151。
- ^ “水道水の浄化に使われたアルミニウムの挙動を追う”. Research at Kobe. 2022年3月15日閲覧。
- ^ “アルミ系凝集剤(PAC・硫酸バンド)”. 株式会社日吉. 2024年8月5日閲覧。
- ^ Banks WA, Kastin AJ. (1989-4). “Aluminum-induced neurotoxicity: alterations in membrane function at the blood–brain barrier.”. en:Neuroscience & Biobehavioral Reviews. 13 (1): 47-53. doi:10.1016/S0149-7634(89)80051-X. PMID 2671833.
- ^ Zubenko GS, Hanin I. (1989-10). “Cholinergic and noradrenergic toxicity of intraventricular aluminum chloride in the rat hippocampus.”. en:Brain Research. 498 (2): 381-4. doi:10.1016/0006-8993(89)91121-9. PMID 2790490.
- ^ Peng JH, Xu ZC, Xu ZX. (1992-8). “Aluminum-induced acute cholinergic neurotoxicity in rat.”. en:Molecular and chemical neuropathology. 17 (1): 79-89. doi:10.1007/BF03159983. PMID 1388451.
- ^ He BP, Strong MJ. (2000-1). “A morphological analysis of the motor neuron degeneration and microglial reaction in acute and chronic in vivo aluminum chloride neurotoxicity.”. en:Journal of Chemical Neuroanatomy. 17 (4): 207-15. doi:10.1016/S0891-0618(99)00038-1. PMID 10697247.
- ^ 安全かつ有効なアジュバントの研究開発と将来の応用分野 メディカル日経BP 2016年9月11日閲覧
- ^ Zaenglein AL, Pathy AL, Schlosser BJ, Alikhan A, Baldwin HE, Berson DS, Bowe WP, Graber EM, Harper JC, Kang S, Keri JE, Leyden JJ, Reynolds RV, Silverberg NB, Stein Gold LF, Tollefson MM, Weiss JS, Dolan NC, Sagan AA, Stern M, Boyer KM, Bhushan R. (2016-5). “Guidelines of care for the management of acne vulgaris.”. en:Journal of the American Academy of Dermatology.(JAAD) 74 (5): 945-973.e33. doi:10.1016/j.jaad.2015.12.037. PMID 26897386.
- ^ マルホ皮膚科セミナー(2017年11月16日放送) (PDF) ラジオ日経
- ^ 原発性局所多汗症診療ガイドライン 2015 年改訂版 (PDF) 日本皮膚科学会ガイドライン





![{\displaystyle {\ce {{Al^{3}+}+6H2O->{[Al(H2O)6]^{3}+}}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/79d6c4b7c1fe6b96cc6c30185fc22c99149590b8)



![{\displaystyle {\ce {[Al2(OH)_{n}Cl_{6-n}]_m}}}](https://wikimedia.org/api/rest_v1/media/math/render/svg/e92311636af4646a691f665bc35cf9ecc07f6dca)