基準電極
基準電極(きじゅんでんきょく、英: reference electrode)とは、電極電位の測定時に電位の基準点を与える電極のこと。 参照電極(さんしょうでんきょく)、照合電極(しょうごうでんきょく)ともいう。
電位の基準点を与えるという性質上、基準電極にはその電極電位の安定性と再現性が要求される。
すなわち、
などが要求される。
本項では、一般的によく用いられる基準電極について簡単に解説する。
標準水素電極
[編集]標準水素電極(ひょうじゅんすいそでんきょく、英: standard hydrogen electrode、SHE)とは、水素ガスおよび水素イオンの活量が全て1である水素電極である[1]。
水素電極の構造と電極反応
[編集]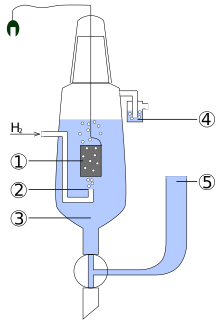
水素電極は水素イオン(H+)と水素ガスとの電気化学的酸化還元反応に基づく電極であり、次のような電極反応がおこっている。
また、水素電極の電極電位は、ネルンストの式により次式で表される。
ここで、
- は水素電極の電極電位(単位 V)
- は水素電極の標準電極電位(単位 V)
- は気体定数(=8.31447 J K−1 mol−1)
- は絶対温度(単位 K)
- はファラデー定数(=9.64853×104 C mol−1)
- は電解質溶液中の水素イオンの活量
- は水素ガスの分圧(単位 Pa)
- は標準圧力(=101.3×103 Pa)
である。
標準水素電極の電極電位
[編集]ヴァルター・ネルンストの提案により、標準水素電極を全ての電位測定の基準とし、その電極電位は全ての温度範囲において0であるとされた。
標準水素電極を基準にして測定されたことを表すために、測定された電位の後ろに(vs. SHE)と付記されることがある。
可逆水素電極
[編集]可逆水素電極(かぎゃくすいそでんきょく、英: reversible hydrogen electrode、RHE)は、測定対象の電極が入っている溶液のpHと同じpHの電解質溶液を用いた水素電極である。
上記の標準水素電極の電極電位の式からわかるように、電解質溶液の水素イオン活量(言い換えればpH)が変わると水素電極の電位も変化してしまう。 このため可逆水素電極と標準水素電極の電極電位は一致しないが、測定対象の電解槽で用いているのと同じ電解質が使えるので液間電位差を考える必要が無いので実験上便利である。
可逆水素電極を基準にして測定されたことを表すために、測定された電位の後ろに(vs. RHE)と付記されることがある。
銀-塩化銀電極
[編集]
銀-塩化銀電極(ぎんえんかぎんでんきょく、英: silver-silver chloride electrode)は、電極として銀と塩化銀を用いる基準電極である。一般的な構造は、銀の表面を塩化銀で覆い、それを塩化物水溶液中に浸したものである。塩化物水溶液としては一般的に飽和塩化カリウム水溶液が用いられる。構造が単純で取扱が容易であり、電位の再現性も良いため、近年最も広く利用されている基準電極である。
銀-塩化銀電極の電極反応は
その電極電位はネルンストの式により次式で表される。
ここで、
- は銀-塩化銀電極の電極電位
- は銀-塩化銀電極の標準電極電位
- は気体定数
- は絶対温度
- はファラデー定数
- は塩化物イオンの活量
である。
上記より、銀-塩化銀電極の電極電位は温度やCl−の濃度に依存することがわかる。
銀-塩化銀電極(飽和KCl)の電極電位は+0.199 V (vs. SHE、25℃)である。
銀-塩化銀電極を基準にして測定されたことを表すために、測定された電位の後ろに(vs. Ag/AgCl)等と付記されることがある。
カロメル電極
[編集]カロメル電極(かろめるでんきょく、英: calomel electrode)は、水銀と塩化水銀(I)を用いる基準電極である。甘汞電極(かんこうでんきょく)とも言われる。一般的には、電解液として飽和塩化カリウム水溶液を用いた飽和カロメル電極(ほうわ-でんきょく、英: saturated calomel electrode、SCE)が使われる。構造が単純で取り扱いが容易であるため過去には広く使用されていたが、近年では水銀を用いているため使われない傾向にある。
飽和カロメル電極の電極反応は
その電極電位はネルンストの式により次式で表される。
ここで、
- はカロメル電極の電極電位
- はカロメル電極の標準電極電位
- は気体定数
- は絶対温度
- はファラデー定数
- は塩化物イオンの活量
である。
上記より、カロメル電極の電極電位は温度やCl−の濃度に依存することがわかる。
飽和カロメル電極の電極電位は、およそ+0.244 V(vs. SHE、25℃)である。
飽和カロメル電極を基準にして測定されたことを表すために、測定された電位の後ろに(vs. SCE)と付記されることがある。
パラジウム・水素電極
[編集]パラジウム・水素電極 (略称: Pd/H2) は電気化学での電位測定に用いられる基準電極の一種である。[2]機能は大半の基準電極と似ており、白金電極との重要な違いは電極自体に溶解する吸収された水素分子である。[3][4].
電極の動作
[編集]パラジウム内に二相(アルファ相およびベータ相)が共存する時に水素は吸収される。:
- アルファ相は1アトムあたりの水素濃度が0.025 アトム以下の場合
- ベータ相は1アトムあたりの水素濃度が非化学量論的にPdH0.6の場合
に対応する。 H3O+イオンが類似の溶存のパラジウムと水素分子の振る舞いは平衡状態のパラジウム電極の電気化学的な振る舞いである。
したがって、平衡状態は水素分子と他の溶存した活性水素イオンによって制御される。
パラジウムが電気化学的に水素をためた場合、二相の存在は可逆水素電極と比較してポテンシャル定数がおよそ+50 mVであることが明らかになる。 このポテンシャルは広範囲にわたって吸収された水素の量と独立している。パラジウム・水素基準電極はこれを利用することで成り立っている。この電極には気体の水素分子が発生し続けないという特徴があり、これは基準電極として必須の性質である。
脚注
[編集]- ^ IUPAC Gold Book - standard hydrogen electrode
- ^ Operation principle of Pd/H2 reference electrode
- ^ 微小基準電極として使用するパラジウム・水素電極
- ^ 電量滴定法へのパラジウム・水素電極

















