重水素化アセトン
表示
| 重水素化アセトン | |
|---|---|

|
|

| |
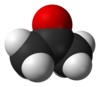
(1,1,1,3,3,3-2H6)Propan-2-one | |
| 識別情報 | |
| CAS登録番号 | 666-52-4 |
| PubChem | 522220 |
| ChemSpider | 455535 |
| UNII | B0N19B53H8 |
| EC番号 | 211-563-9 |
| 国連/北米番号 | 1090 |
| ChEBI | |
| バイルシュタイン | 1702935 |
| |
| 特性 | |
| 化学式 | C32H6O or C3D6O |
| モル質量 | 64.1161 g mol−1 |
| 密度 | 0.872 g cm−3 |
| 融点 |
-94 °C, 179 K, -137 °F |
| 沸点 |
56 °C, 329 K, 133 °F |
| 蒸気圧 | 24.5-25.3 kPa (at 20°C) |
| 危険性 | |
| GHSピクトグラム |  
|
| GHSシグナルワード | 危険(DANGER) |
| Hフレーズ | H225, H319, H336 |
| Pフレーズ | P210, P233, P240, P241, P242, P243, P261, P264, P271, P280, P303+361+353, P304+340, P305+351+338, P312 |
| NFPA 704 | |
| 引火点 | −19 °C (−2 °F; 254 K) |
| 関連する物質 | |
| 関連物質 | アセトン |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
重水素化アセトン(じゅうすいそかアセトン、重アセトン、英: Deuterated acetone)は、アセトンの同位体置換体(英: isotopologue)である。アセトン中の水素原子(H)が同位体である重水素(D)に置換されている。重水素化アセトンは核磁気共鳴分光法で用いられる一般的な溶媒である[1]。
製造
[編集]重水素化アセトンは塩基存在下でアセトンと重水との反応によって調製される。塩基には重水素化水酸化リチウムが用いられる[1]。

アセトンを完全に重水素化するには、重水をアセトンから留去し、新しい重水でまた反応を再開するというプロセスを数回繰り返す。
脚注
[編集]出典
[編集]- ^ a b Paulsen, P. J.; Cooke, W. D. (1963-09-01). “Preparation of Deuterated Solvents for Nuclear Magnetic Resonance Spectrometry.” (英語). Analytical Chemistry 35 (10): 1560–1560. doi:10.1021/ac60203a072. ISSN 0003-2700.

