白血球分画



白血球分画(はっけっきゅうぶんかく、英語: White blood cell differential)とは、血液中の白血球を分類しそれぞれの分画の比率を求める血液学的検査である。白血球分類、血液像、末梢血液像、白血球像、ヘモグラム、ともいう。 白血球は、主に生体防御・免疫に関与する血液細胞であり、自動血球計数機では、通常、好中球、リンパ球、単球、好酸球、好塩基球の5種類に分画(分類)される。末梢血塗抹検査に際しては、好中球をさらに桿状核球と分葉核球に分類することも多い。 白血球分画は、基本的な臨床検査の一つであり、通常、全血球計算(血算、CBC)と同時に実施される。血液疾患のみならず、感染症、炎症、アレルギー・免疫疾患、をはじめとする多くの疾患の診断や経過観察、全身状態の評価などに関する重要な情報を得ることができ、医療において広く用いられている[1]。
検査法
[編集]通常、自動血球計数機を用いるが、自動血球計数機による白血球分画で異常が疑われたとき、および、病歴から血液疾患などが疑われた場合には末梢血塗抹検査による白血球分類がおこなわれる(なお、白血球分画と白血球分類は同義語としても用いられるが、自動血球計数機の場合は白血球分画、塗抹標本で視算する場合は白血球分類、と使い分けることもある)[2]。
検査材料
[編集]白血球分画の検査は、通常、EDTAで抗凝固[※ 1]した静脈血、または、毛細管血を用いる。なお、ヘパリンで抗凝固した検体(動脈血など)は血液像の検査には不適切である[3]。 また、採取後、迅速に検査ないし塗抹標本の作成を行なう必要がある。
自動血球計数機による白血球分画
[編集]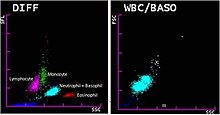
保険診療では「血液像(自動機械法)」とよばれる。 通常、全血球計算(血算、CBC)と同時に自動血球計数機を用いて、実施する。およそ100 μL程度の血液を使用して1分程度で全血球計算と白血球分画を報告可能である[4]。 通常、好中球、リンパ球、単球、好酸球、好塩基球の5種類に分画(分類)され、それぞれの絶対数と相対的比率が得られる。 なお、5分画に加え、幼若顆粒球などの分画を報告可能な機種も存在する[5]。一方、診療現場検査(POCT)向けの小型機種では、顆粒球(好中球+好酸球+好塩基球)[※ 2]、単球、リンパ球の3分画を行なうものも存在する[6]。
自動機械法の長所としては、全血球計算と同時に実施可能で高速であり、客観的で、かつ、一度に多数の細胞(10,000個程度)を対象とするため結果の精度が高いことがあげられる。
短所としては、古典的な左方移動の基準である分葉核球・桿状核球の区別はできないほか、一般に、病的細胞(特にリンパ系悪性腫瘍や病的細胞が少ない場合)の同定は視算に比べ劣る[7][8][9][10][11]。 また、好塩基球など数が少ない細胞については機種間差がみられることがある[11]。
測定原理
[編集]一般に、血球細胞を一個ずつ細いチャンネルを通過させ、電気抵抗、レーザー散乱光、染色、などの組み合わせ(機種により異なる)で 細胞種の判別を行っている [12] [13] [14] 。
電気抵抗
[編集]電気抵抗法(コールター原理)では、血球(周囲の液に比べ電気抵抗が大きい)が通過する際の電気抵抗の変化が細胞の容積に相関することにより、細胞容積を計測する。 また、高周波電気インピーダンスは同じ容積の細胞であっても内部構造の違いにより異なるので、直流電気抵抗と高周波電気インピーダンスの組み合わせにより、血球の種類を判別することができる [15]:3[12][13]。
レーザー散乱光
[編集]フローサイトメトリーでよく使われている方法であり、前方散乱光(細胞容積を反映)と側方散乱光(細胞の表面や内部の構造を反映)の組み合わせで細胞分類を行う。 [10][9][12][13][14]。
染色
[編集]核酸を染色する蛍光色素がよく使用される[14]。その他、ペルオキシダーゼ染色(骨髄系の白血球細胞を染める)を利用する機種もある[16]。
その他の方法
[編集]いずれも、自動血球計数機による白血球分画で異常を検知した際に鏡検が必要かどうかスクリーニングする目的で使用するのが通常である。
- 細胞表面マーカー:モノクローナル抗体を使用して専用のフローサイトメーターで白血球分類を行なうシステムも開発されており、高精度で、かつ、リンパ球のサブセットや幼弱細胞など、従来の白血球分類の枠組みを超えた情報を得ることができるが、まだ一般的ではない[17]。
- パターン認識:末梢血塗抹標本を機械でスキャンして視算と同様にパターン認識により白血球分類をおこなう装置も市販されているが、一般的ではない[18][19]。
視算(鏡検法)による白血球分類
[編集]保険診療では「血液像(鏡検法)」とよばれる。 視算による白血球分類は末梢血塗抹検査の際に行われる。通常、好中球をさらに桿状核球と分葉核球に分けて、(好中球)桿状核球、(好中球)分葉核球、リンパ球、単球、好酸球、好塩基球の6分画で報告することが多いが、その他の細胞(後骨髄球、骨髄球、前骨髄球、芽球など)がみられた場合は、追加して報告する。
鏡検法の長所としては、一般に病的細胞の同定に優れている。また、形態学的な重要な情報(たとえば、桿状核球と分葉核球の分別、反応性リンパ球(異型リンパ球)、アウエル小体・中毒性顆粒・デーレ小体などの細胞質内構造物、過分葉・ペルゲル・フェット核異常などの核形態異常)が得られることがあげられる[10]。
短所としては、まず塗抹標本を作成してから臨床検査技師が顕微鏡を用いて計数するので時間と労力がかかり、分類は主観的で個人差・力量差が存在すること、サンプル数が少ないため精度が低く[※ 3]、各分画の絶対数は、別途、白血球数に比率を乗じて求める必要があること、などがあげられる[7]。
基準値
[編集]白血球分画の基準値(基準範囲)は施設により異なることが多いが、以下、日本人成人の基準値例を示す。なお、白血球分画には年齢差があり、出生直後を除き、生後1ヶ月から2歳ごろはリンパ球の方が多い。5、6歳で好中球優位となる。小児の白血球分画の基準値については、文献[20][21]を参照されたい。
自動血球計数機による白血球分画の基準値
[編集]基準値は機種や施設により異なるが、ここでは、日本検査血液学会が、次項の視算による白血球分画基準値とともに発表しているものを示す[22]。
| 自動血球計数機による 白血球分画(略称) |
比率の基準値(%) [下限値 - (メジアン) - 上限値] |
絶対数の基準値( ×103/μL )[※ 4] [下限値 - (メジアン) - 上限値] |
|---|---|---|
| 好中球(NEUT:neutrophil) | 42.0 -(57.8)- 75.6 | 1.78 -(3.29)- 6.33 |
| リンパ球(LYMPH:lymphocyte) | 17.4 -(32.8)- 48.2 | 1.06 -(1.81)- 3.03 |
| 単球(MONO:monocyte) | 3.4 -(5.4)- 9.0 | 0.17 -(0.30)- 0.55 |
| 好酸球(EO:eosinophil) | 0.4 -(2.0)- 8.6 | 0.02 -(0.11)- 0.54 |
| 好塩基球(BASO:basophil) | 0.2 -(0.5)- 1.4 | 0.01 -(0.03)- 0.08 |
視算による白血球分画の基準値
[編集]視算(末梢血塗抹検査)では、白血球は、通常、下表の6分画に分類して報告される。基準値は各施設で独自に設定している場合も多いが、ここでは、日本臨床衛生検査技師会と日本検査血液学会の提唱する共用基準範囲[23]を示す。
| 視算による 白血球分画(略称) |
基準値(%) [下限値 - (メジアン) - 上限値] |
|---|---|
| (好中球)桿状核球(BAND、STAB) | 0.5 -( 2.0)- 6.5 |
| (好中球)分葉核球(SEG) | 38.0 -(57.0)- 74.0 |
| リンパ球(LYMPH) | 16.5 -(32.0)- 49.5 |
| 単球(MONO) | 2.0 -(5.0)- 10.0 |
| 好酸球(EO) | 0.0 -(2.0)- 8.5 |
| 好塩基球(BASO) | 0.0 -(1.0)- 2.5 |
検査の意義
[編集]白血球分画は、血液疾患のみならず、感染症、炎症、免疫・アレルギー関連疾患、内分泌疾患、など、非常に広範な病態を反映して変化する情報量の多い検査であり、全血球計算で異常を認めた際は最初に選択される検査である。
白血球分画の解釈は、主に各分画の増加・減少の有無と原因となる病態の推定となる。この際、相対的比率のみではなく、各分画の絶対数を考慮する必要がある。たとえば、リンパ球の比率が10 %だったとして、もし白血球数が5000 /μLならリンパ球の絶対数は500 /μLでリンパ球減少症といえるが、好中球が増加して白血球数が15000 /μLならリンパ球の絶対数は1500 /μLで基準範囲内であり、好中球増多症により相対的にリンパ球の比率が減少したのみと推定できる[4]。
好中球
[編集]

好中球は生体防御の中心的な役割を果たす細胞であり、細菌・真菌などの病原微生物や異物を貪食し破壊するほか、自らのDNAを放出して好中球細胞外トラップを形成し、病原体を捕捉する[15]:3-4。 好中球は骨髄で産生されて血中に移行し、半減期7時間程度で組織に移行する[15]:119-124。
塗抹標本鏡検では、好中球は径10 - 15 μm程度(赤血球の2倍程度)で、淡褐色の細胞質に橙褐色の微細な顆粒が多数ある。核のクロマチンは粗大で結節状であり、大部分は核が3(2-5)葉程度に分葉(分葉核球)している。核がまだ分葉していない未熟な好中球を桿状核球という[24][1]。
好中球増多症
[編集]増多症の厳密な基準はないが、好中球絶対数が 7000[25][26]、7500[8]、ないし、8000[1] /μL以上が好中球増多症(neutrophilia)とみなされている。(小児の場合は8500[25] /μL 以上とされる。) 通常、好中球増多それ自体よりは、その原因となる病態の方が問題となる[※ 5]。以下、好中球増多の主要な原因をあげる[8][1][25]。
- 生理的:妊娠、出産、新生児、喫煙
- 反応性[※ 6]:各種のストレス状態(激しい運動後、急性出血、出生後、手術後、痙攣後、など)、アドレナリン投与。糖質コルチコイド投与。
- 感染症:特に、各種の細菌性感染症(ただし腸チフスなど例外あり)。ウイルス感染でもウイルス種などによっては増加することがある。
- 炎症:急性虫垂炎など臓器の炎症、自己免疫疾患(リウマチ熱、血管炎症候群など)、慢性炎症性疾患、悪性腫瘍、など
- 組織壊死:心筋梗塞、熱傷、急性膵炎、外傷、腫瘍壊死、など
- 内分泌代謝疾患:クッシング症候群、糖尿病性ケトアシドーシス、痛風
- 産生増加:G-CSFの投与やG-CSF産生腫瘍、骨髄抑制の回復期
- 骨髄増殖性疾患:慢性骨髄性白血病など
- 左方移動(桿状核球増多)
細菌感染や身体への重度の侵襲(重度の感染症、外傷、手術、など)の際には、しばしば、左方移動、すなわち、桿状核球などの幼若な好中球の増加がみられる。鏡検で桿状核球と分葉核球を別々にカウントしたり、一部の自動血球計数装置で幼若顆粒球数を計数するのは左方移動を検出するのが目的である。
- 類白血病反応
類白血病反応とは、感染症、悪性腫瘍、などに伴い著明な好中球増多(と左方移動)により、白血球数が50,000 /μLを超えた状態を指す。慢性骨髄性白血病と鑑別する必要があるが、類白血病反応では、好塩基球や好酸球の増多を伴わず、鏡検で中毒性変化(好中球細胞質に中毒性顆粒、デーレ小体、空胞変性などが出現)がみられることが参考になる。
好中球減少症
[編集]好中球絶対数 1500 /μL以下[8]、ないし、1000 /μL以下[1]が好中球減少症(neutropenia)とされる。(人種差があり、白人成人では2000 /μL未満、黒人成人では1300 /μL未満とする文献もある[25]。)なお、好中球減少症においては、通常、桿状核球と分葉核球は区別せず、一括して好中球として扱う。
好中球減少症は、それ自体が細菌や真菌に対する防御能の低下を意味し、1000 /μL未満では感染症のリスクが上昇し、500 /μL未満ではさらにリスクが大きくなるとされる[25]。500 /μL以下[8]、ないし、100 /μL未満[25]は無顆粒球症と呼ぶ。主要な原因をあげる[8]。
- 感染症:重篤な細菌感染症[※ 7]、腸チフス、ウイルス感染症、リケッチア症、など。
- 産生低下:血液疾患(巨赤芽球性貧血、再生不良性貧血、急性白血病、骨髄異形成症候群、癌の骨髄転移、骨髄線維症、など)、化学療法、放射線など。
- 破壊亢進:肝硬変などの脾機能亢進、血球貪食症候群、自己免疫疾患、など。
- 内分泌疾患:アジソン病、バセドウ病。
- 薬剤アレルギー:抗痙攣剤、抗精神病薬、抗甲状腺剤、抗菌薬、その他、多数の薬剤で無顆粒球症が重篤な副作用として知られている。
- 免疫性:自己免疫性好中球減少症、新生児同種免疫性好中球減少症(父親由来の抗原に対する母のIgG抗体移行による)
- 体内分布異常:偽性好中球減少症[※ 8]
リンパ球
[編集]

リンパ球は免疫系の中心的機能をもつ白血球である。外来性の抗原を認識し、液性免疫(抗体産生)や細胞性免疫の機能を発揮する。T細胞、B細胞、NK細胞などのサブセットがあるが、通常の機械分類や鏡検ではサブセットの区別は困難であり、フローサイトメーターで細胞表面抗原により分類するのが通常である。 リンパ球は骨髄で産生され、サブセットにより、胸腺(T細胞)、骨髄・リンパ組織などで成熟した後に、血液やリンパ組織に移行する[15]:3-4。
塗抹標本鏡検では、リンパ球は径6 - 15 μm程度、核は円形ないし腎形で核クロマチンは粗大で結節状、細胞質は淡青色で、一部、少数のアズール顆粒をもつものがある[24][1]。
リンパ球増多症
[編集]成人では、リンパ球 4000 /μL以上[8][26][1][27]ないし5000 /μL超[25]をリンパ球増多症(lymphocytosis)とみなす。 小児では生理的にリンパ球が多く、10,000 /μL超[25]をリンパ球増多症(lymphocytosis)とみなす。以下、リンパ球が増多する病態の例をあげる[27]。
- ウイルス感染症:しばしば反応性リンパ球(異型リンパ球)が増加(EBウイルス、サイトメガロウイルス、急性HIV感染症、をはじめとする各種のウイルス感染症)
- 細菌感染症の一部:百日咳(著明なリンパ球増多が特徴的であるが、反応性リンパ球(異型リンパ球)ではなく、成熟リンパ球(核に切れ込みをもつ)が増加する[25][27])、猫ひっかき病、など。
- 寄生虫感染症:トキソプラズマなど。
- リンパ系の血液腫瘍:悪性リンパ腫をはじめとするリンパ系の腫瘍ではリンパ腫細胞の末梢血出現がよくみられる(20-80 %)[27]。慢性リンパ性白血病、ワルデンシュトレームマクログロブリン血症などでは成熟型のリンパ球が増加する。通常の白血球分画では正常リンパ球と腫瘍細胞の区別が困難なことがある。
- 薬剤:薬剤性過敏症症候群(DIHS/DRESS症候群)の30-70 %でリンパ球増多がみられる。
- 内分泌疾患:アジソン病、甲状腺機能亢進症
- 各種のストレス状態(痙攣発作、外傷、など)で好中球の増加に先行して一過性のリンパ球増多がみられることがある。
なお、好中球が減少する病態では、リンパ球の比率が相対的に高くなることが多い[1]。
リンパ球減少症
[編集]成人:1000 /μL未満、小児:2000 /μL未満をリンパ球減少症(lymphopenia)とよぶ[8][25]。 なお、好中球が増加する病態では相対的にリンパ球比率が減少するが、絶対数を確認しないとリンパ球減少症とはいえない。 リンパ球が減少する病態は多数あるが、代表的なものをあげる[8][1]。
- 感染症:ウイルス感染症、結核、急性感染症初期、など。
- 副腎皮質ステロイド:糖質コルチコイド投与、内因性の糖質コルチコイドが増加している状態(クッシング症候群、ストレス、大手術、など)。
- 産生低下:栄養不良状態・悪液質、腎不全、心不全、悪性リンパ腫、骨髄障害(再生不良性貧血、化学療法、放射線、など)。
- 免疫不全症:原発性免疫不全症候群、後天性免疫不全症候群など。
- リンパ球破壊亢進:AIDS、抗リンパ球グロブリン投与、など。
- 自己免疫疾患:全身性エリテマトーデス(SLE)
- 漏出:胸管・リンパ管癆、胸管ドレナージ。
なお、低栄養でリンパ球が減少することを応用して、栄養状態の評価にリンパ球数が用いられる[28]。
単球
[編集]
単球は好中球と同じく食細胞であり病原体(特に真菌、原虫など大型ないし複雑なもの)や異物、壊死組織などを貪食する。また、自然免疫や抗原提示の担い手として重要な細胞である。単球は骨髄で産生され、血中では半減期1から3日程度で組織に移行してマクロファージや樹状細胞に分化していく[29][15]:3-4。
塗抹標本鏡検では、単球は径13 - 21 μm程度で最も大きい白血球である。灰色がかった青色の細胞質が豊富であり細胞質は微細な顆粒ですりガラス状にみえる。核は円形から腎臓形で、複雑にくびれ、核クロマチンは繊細で網状である[24][1]。
単球増多症
[編集]単球 700 /μL以上[8]ないし 1000 /μL以上[1]を単球増多症(monocytosis)とよぶ。 感染症、外傷、薬剤、自己免疫疾患、一部の悪性腫瘍、など、さまざまな病態でみられる。 なお、化学療法後など骨髄抑制からの回復期には単球が最初に増加してくるため、比率では増加しているようにみえる[1][8][25]。
- 各種感染症:特に、結核、感染性心内膜炎など亜急性から慢性の感染症や、水痘、麻疹、風疹など発疹性感染症。
- 自己免疫・炎症性疾患: 膠原病(全身性エリテマトーデス、関節リウマチ)、炎症性腸疾患、サルコイドーシス、など。
- 悪性腫瘍:肺癌、ホジキン病、など。
- 組織壊死:心筋梗塞、など。
- 骨髄増殖性疾患:慢性骨髄単球性白血病など。
- 産生増加:G-CSFの投与、骨髄抑制の回復期
単球減少症
[編集]単球200/μL以下[8]を単球減少症(monocytopenia)とよぶ。単球減少症は骨髄異形成症候群でよくみられる所見である[29]。また、有毛細胞白血病(HCL、慢性のBリンパ球性の白血病)の所見として知られる [30]。 その他、重症敗血症や骨髄での造血障害(再生不良性貧血、悪性貧血、化学療法後など)、ウイルス感染症(特にEBウイルス)、糖質コルチコイド(ステロイド)投与、などでも単球減少症はみられるが、診断的意義は低い[1][8][25]。
好酸球
[編集]
好酸球は、酸性色素エオシンで赤く染まる顆粒(好酸性顆粒)をもつ白血球(顆粒球)である。 骨髄で産生される。好酸球の分化にはインターロイキン-5(IL-5)が重要とされる。骨髄から血液に出た後の半減期は4.5 - 8時間程度で、気道系や消化管など組織に移行したあとの寿命は8 - 12 日程度である。好酸球は寄生虫に対する生体防御に重要な役割をもつ[31]。
塗抹標本鏡検では、好酸球は径13 - 21 μm程度で好中球よりやや大きく、淡褐色の細胞質には大きな橙赤色の顆粒がある。核は通常2分葉しており、核クロマチンは粗大で結節状である[24][1]。
好酸球増多症
[編集]好酸球絶対数500 /μL以上が好酸球増多症(eosinophilia)であり、さらに、500 - 1500 /μL を軽度増加、1500-5000 /μL を中等度増加、5000 /μL 以上を高度増加とする。中等度以上(1500 /μL以上)の好酸球増加が一ヶ月以上持続、または、組織で好酸球の著明な浸潤がみられるものを好酸球増多症候群という。好酸球は活性化すると好酸球カチオン性タンパク質 (ECP) や主要塩基性タンパク質 (MBP)といった寄生虫障害作用をもつ蛋白を放出するが、これらは人体組織にも有害であるため、好酸球増多症では、心臓、肺などの臓器障害がおきることがある[31][26]。 好酸球増多がみられる病態は非常に多岐にわたるが、代表的なものをあげる[8][1][25]。
- アレルギー疾患:よくみられる好酸球増多の原因。気管支喘息、花粉症、蕁麻疹、アトピー性皮膚炎、薬物過敏症、アレルギー性気管支肺アスペルギルス症、など
- 寄生虫感染:世界的にもっともよくみられる好酸球増加の原因。また、一部の原虫でも増加することがある。
- 皮膚疾患:天疱瘡、多形滲出性紅斑、痒疹、好酸球性血管浮腫、など
- 膠原病・血管炎:好酸球性多発血管炎性肉芽腫症(チャーグ・ストラウス症候群)、結節性多発動脈炎、好酸球性筋膜炎、軟部好酸球性肉芽腫(木村病)、など
- 血液腫瘍:慢性骨髄性白血病、好酸球増加症候群、慢性好酸球性白血病、悪性リンパ腫、など
- 悪性腫瘍:特に、転移、壊死を伴うもの
- 肺疾患:レフラー症候群(単純性肺好酸球増多症)、好酸球性肺炎(PIE症候群)、過敏性肺臓炎
- 内分泌疾患:アジソン病(副腎皮質機能低下)
- 免疫不全症の一部:ウィスコット・アルドリッチ症候群、高IgE症候群、など
- その他:コレステロール塞栓症候群、放射線照射後、など
好酸球減少
[編集]好酸球 100 /μL以下[8]ないし90 /μL以下[25]は好酸球減少(eosinopenia)とされる[※ 9]。 もともと数がすくない白血球であるので減少の判断が難しく、また、 診断的意義は乏しいが[15]、文献に記載されている原因をあげる[8][1][25]。
- 急性感染症:腸チフスで特徴的とされる
- 骨髄での造血能の障害:悪性貧血、再生不良性貧血、顆粒球減少症、など
- ステロイド:糖質コルチコイド投与、クッシング症候群
- その他:ストレス(外傷・熱傷など)、各種の急性炎症、自己免疫疾患
好塩基球
[編集]
好塩基球は好塩基性(ロマノフスキー染色で青に染まる)の顆粒を多数持つのが特徴であり、健常人の末梢血液中でもっとも少ない白血球分画である[32]。骨髄で産生され、血中の半減期は6時間程度で急速に組織に移行し、組織中では2週間程度まで生存しうる[33]。自動血球計数装置では好塩基球数は過小評価されることがあり、正確な評価が必要な場合にはフローサイトメーターの方がすぐれている[33]。
塗抹標本鏡検では、好塩基球は径10 - 16 μm程度、淡褐色の細胞質には大きな暗青紫色の顆粒が多数ある。核は顆粒のために観察しにくいことが多い[24][1]。
好塩基球増多症
[編集]好塩基球数が 150/μL以上[1][8]、ないし、200/μL以上[32]は好塩基球増多症(basophilia)とされる。まれな病態である。アレルギー疾患で軽度の増多がみられることがある[26][15]。慢性骨髄性白血病などの骨髄増殖性疾患では好塩基球増多症(絶対数・比率とも)がみられることがあり、原因不明の好塩基球増多症は骨髄増殖性疾患の精査が必要である。 以下、主要な好塩基球増多の原因をあげる[32][1][33]。
- 血液腫瘍:慢性骨髄性白血病 をはじめとする骨髄増殖性疾患。
- 慢性炎症:潰瘍性大腸炎、全身型若年性関節リウマチ、など。
- アレルギー疾患:薬剤過敏症、食物過敏症など。(好酸球の増多を伴うアレルギー疾患では通常増加するが、I型過敏症では減少する。)
- 内分泌疾患:粘液水腫
- 寄生虫疾患:通常、好酸球の増加も伴っている。
- その他の感染症:ウイルス感染症(インフルエンザ、水痘)、細菌感染症(結核、ヘリコバクター・ピロリ)
好塩基球減少
[編集]好塩基球は本来数がすくない白血球であり、減少の判断は難しく、好塩基球減少(basopenia)が問題にされることはまれである[15]:3-4[※ 9]。好塩基球減少の原因としては、糖質コルチコイド、骨髄抑制、I型過敏症、甲状腺機能亢進症、などがあげられている[33]。
その他の細胞
[編集]- 幼若顆粒球
自動血球計算装置によっては、幼弱な顆粒球(視算での前骨髄球、骨髄球、後骨髄球に相当)の数を計測できるものがあり、細菌感染症、慢性骨髄性白血病、など左方移動がみられる病態の評価に有用とされる[5]。
- 反応性リンパ球(異型リンパ球)
反応性リンパ球(異型リンパ球)とは、ウイルス感染(特に伝染性単核球症、サイトメガロウイルス初感染、急性HIV感染)、アレルギー、など免疫系が刺激されて活性化したリンパ球である。免疫を刺激する病態の存在を示唆するが、それ自体が治療の対象になるわけではない。 主に鏡検で確認する。
- 腫瘍細胞
各種の白血病やリンパ系の悪性腫瘍では腫瘍細胞が末梢血に出現するが、自動血球計数装置では適切に認識されないことも多く、鏡検が必要である[34](まれに乳癌や肺癌でも癌細胞が末梢血に出現することがある[35])。
- 微量成分
健常人の末梢血には、正常成熟白血球5分類以外にも、ごく微量ながら、芽球(白血球の0.05-0.75 %)[17]、樹状細胞(末梢血単核球の0.16-0.68 %)[36]や造血幹細胞(CD34陽性細胞、末梢血単核球の0.16-0.68 %)[36]などが存在するが、鏡検や一般的な自動血球計数装置では分類できない。ただし、自動血球計数装置の機種によっては、造血幹細胞数を計数しうるものも存在する[36]。
歴史
[編集]1674年にオランダのアントニ・ファン・レーウェンフック(Antonie van Leeuwenhoek)が顕微鏡による赤血球の詳細な観察を報告した[19]。 1770年に英国のウイリアム・ヒューソン(William Hewson)が白血球を発見した[37][38]。19世紀前半には顆粒をもつ白血球(顆粒球)の存在が知られていた[39]。
1879年に、ドイツの化学者・細菌学者、パウル・エールリヒ(Paul Ehrlich)が、血液塗抹標本を複数の染料で染色して白血球を分画する方法を発表し、好中球、好酸球、好塩基球、単球、リンパ球の白血球5分画を確立した[39][40][38]。
1890年に、ロシアの内科医ドミトリー・レオニドビッチ・ロマノフスキー(Dmitri Leonidovich Romanowsky)が細胞質と核を染め分けることができる染色法を発表した(ロマノフスキー染色)。以後、ロマノフスキー染色の改良法として、ライト染色(1902年)、ギムザ染色(1904年)、メイ・グリュンワルド・ギムザ染色(1908年)など多数の染色法が開発され、視算による白血球分画が普及した[40]。
1940年代に米国のウォレス・コールター(Wallace H. Coulter)は、血球細胞は電気伝導性が低いため、電流が流れている細い流路を細胞が通過すると細胞の容積に比例した電流の変化が生じること(コールター原理)を見出して1953年に特許を取得し1956年に最初の自動血球計数機を発表した[41]。自動血球計数機は、当初は赤血球しか計数できなかったが、その後、赤血球を溶血して白血球を計数できるようになり、1960年代には多くの検査室に導入された[38]。国産の半自動血球計数機は1963年に東亜特殊電機(シスメックス社の前身)から発売されている[38]。なお、血小板が計数可能な機種が発表されたのは1970年のことである[42]。
1970年代には白血球分類の自動化の開発が進められた。1960年代から進歩してきたフローサイトメーターの技術も取り入れ、1974年には細胞染色に基づく最初の自動白血球分類装置がテクニコン社から発売された[43]。1980年代には自動血球計数機と自動白血球分類装置の統合が進み、自動白血球分類が医療機関に普及していった[13][38]。
「ロマノフスキー染色」、「英語版の白血球分画(White blood cell differential)」も参照されたい。
獣医学領域
[編集]獣医学領域でも、ヒトと同様に、白血球分画は活用されているが、白血球数および白血球分画、白血球の形態は動物種により差がある。たとえば、ウサギ、鳥類、爬虫類などにおいては、ヒトの好中球に相当する白血球は好酸性の顆粒をもち、偽好酸球(heterophil)とよばれる。詳細は、文献[44]:122,132[45][46]を参照されたい。
脚注
[編集]- ^ 血液は放置すると凝固して細胞を個別に検査できなくなるため、フィブリンの形成を抑止する抗凝固剤のはいった採血管に採取して検査を行なう。
- ^ 好中球・好酸球・好塩基球はいずれも細胞質に特異顆粒をもつのであわせて顆粒球(granulocyte)とよぶ。また、顆粒球はいずれも核が分葉するため、多形核球(polymorphonuclear leukocytes)とよばれることがある。一方で、リンパ球・単球は、特異顆粒をもたないので無顆粒白血球(agranulocyte)、また、核が分葉しないので単核球(mononuclear leukocytes)とよばれることがある。
- ^ 視算では、通常は100個(場合により200個)の白血球をカウントした結果で白血球分画を報告する。
- ^ 白血球数の単位は ×109/L が国際標準であるが、ここでは慣用単位 ×103/μL で表記している。
- ^ 好中球増多自体は通常無害であるが、慢性骨髄性白血病で白血球数が20万 /μLを超えるような場合は、白血球が血管内に滞留して虚血による臓器障害を起こす場合がありうる(leukostasis)。
- ^ 各種のストレス状態でカテコールアミン分泌が増加したり、アドレナリンなどのカテコールアミンを投与すると、好中球は血管壁付近(辺縁プール)から血中(循環プール)に移動するため、好中球数は急に増加する。
- ^ 重篤な細菌感染症では、組織での好中球の大量の消費に骨髄での産生が追いつかないため、血中の好中球数は減少することがあり、重篤な状態であることを意味する。
- ^ 偽性好中球減少症とは、好中球の体内分布の異常で、辺縁プール(血管壁付近にとどまっているもの)の増大により循環プール(血液)の好中球数が少なくなっているが、生体防御能は正常である。
- ^ a b 好酸球や好塩基球のような絶対的にも相対的にも数が少ない白血球種については、減少の判断が難しく、また減少していたとしてもその臨床的意義に乏しく、「減少症」という言葉はあまり使われない。
出典
[編集]- ^ a b c d e f g h i j k l m n o p q r s 高久史麿 編『臨床検査データブック2023-2024』医学書院、2023年1月15日、350-352頁。ISBN 978-4-260-05009-8。
- ^ 吉冨一恵, 上硲俊法「〈臨床検査シリーズ〉血液検査室の流れ:血球算定から骨髄像検査まで」『近畿大学医学雑誌』第34巻第4号、近畿大学医学会、2009年12月、275-284頁、CRID 1050282677516207616、ISSN 03858367。
- ^ “末梢血液検査|検体検査(血液検査)”. 看護roo!. 2023年7月28日閲覧。
- ^ a b Tulin Tiraje Celkan (2020). “What does a hemogram say to us?”. Turk Pediatri Ars 55: 103-116.
- ^ a b 鯉田祐佳里, 岡崎葉子, 菊間知恵, 山 智江, 湊由理, 野原圭一郎, 仲井里枝, 三枝淳「多項目自動血球分析装置XRシリーズの基礎的検討」『医学検査』第71巻第4号、2022年、657-666頁、doi:10.14932/jamt.22-36。
- ^ “自動血球計数装置 Microsemi LC-661”. 日本臨床検査機器・試薬・システム振興協会. 2023年8月4日閲覧。
- ^ a b “血球計数における自動白血球分類(3)”. BECKMAN COULTER 臨床検査分野. BECKMAN COULTER. 2023年7月31日閲覧。
- ^ a b c d e f g h i j k l m n o p q 櫻林郁之介 編『今日の臨床検査2021-2022』南江堂、2021年5月15日、65-66頁。ISBN 978-4-524-22803-4。
- ^ a b 田窪孝行「4.血液疾患 1)血球検査」『日本内科学会雑誌』第100巻第11号、2011年、3230-3239頁、doi:10.2169/naika.100.3230。
竹中克斗「IV.骨髄増殖性腫瘍の初期診断と外来治療」『日本内科学会雑誌』第111巻第7号、2022年、1364-1370頁、doi:10.2169/naika.111.1364。 - ^ a b c 宮地 勇人「5.血液疾患 1)血球検査」『日本内科学会雑誌』第97巻第12号、2008年、2966-2973頁、doi:10.2169/naika.97.2966。
- ^ a b 大西宏明, Medical Practice編集委員会 編『臨床検査ガイド 2020年改訂版』文光堂、2020年6月17日、481-484頁。ISBN 978-4-8306-8037-3。
- ^ a b c “血球計数装置の測定原理”. HORIBA Medical. HORIBA. 2023年7月31日閲覧。
- ^ a b c d “血球計数における自動白血球分類(1)”. https://www.beckmancoulter.co.jp/. BECKMAN COULTER. 2023年7月31日閲覧。
- ^ a b c “多項目自動血球分析装置XNシリーズの測定原理および特長 2021” (PDF). 日本医療検査科学会. 日本医療検査科学会. 2023年7月31日閲覧。
- ^ a b c d e f g h Keohane, Elaine M.; Otto, Catherine N.; Walenga, Jeanine M. (2019-02-22) (英語). Rodak's Hematology - E-Book: Rodak's Hematology - E-Book. Elsevier Health Sciences. ISBN 978-0-323-54963-9
- ^ 山田巻弘,秋葉俊一「光学的白血球自動分類法の精確さの保障」(PDF)『生物試料分析』第31巻第5号、2008年、339-344頁。
- ^ a b Marion Magierowicz, et al. (2019). “Reference Values for WBC Differential by Hematoflow Analysis”. Am J Clin Pathol 151: 324-327. doi:10.1093/AJCP/AQY147.
- ^ Ben-Zion Katz, et al. (2021). “Evaluation of Scopio Labs X100 Full Field PBS: The first high-resolution full field viewing of peripheral blood specimens combined with artificial intelligence-based morphological analysis”. International Journal of Laboratory Hematology 43: 1408-1416. doi:10.1111/ijlh.13681.
- ^ a b Barry S. Coller (2015). “Blood at 70: its roots in the history of hematology and its birth”. Blood 126: 2548-2560. doi:10.1182/blood-2015-09-659581.
- ^ “小児臨床検査基準値(国立成育医療研究センター)”. 総合医学社. 2023年6月21日閲覧。
- ^ 田中敏章, 山下敦, 市原清志「潜在基準値抽出法による小児臨床検査基準範囲の設定」『日本小児科学会雑誌』第112巻第7号、日本小児科学会、2008年7月、1117-1132頁、CRID 1520853833314424832、ISSN 00016543。「https://www.jpeds.or.jp/journal/abstract/112-07.html#112071117」 (
 要購読契約)
要購読契約)
- ^ Takami, Akiyoshi; Watanabe, Shinichiro; Yamamoto, Yoshikazu; Miyachi, Hayato; Bamba, Yukiharu; Ohata, Masahiko; Mishima, Seiji; Kubota, Hiroshi et al. (2021-10). “Reference intervals of white blood cell parameters for healthy adults in japan” (英語). International Journal of Laboratory Hematology 43 (5): 948?958. doi:10.1111/ijlh.13486. ISSN 1751-5521.
- ^ 血液形態検査における標準化の普及に向けて 日本臨床衛生検査技師会・日本検査血液学会 血球形態標準化ワーキンググループ
- ^ a b c d e 金井正光 編『臨床検査法提要』(改定第31版)金原出版株式会社、1998年9月20日、298-309頁。ISBN 4-307-05033-9。
- ^ a b c d e f g h i j k l m n o Marionneaux, Steven (2020). “Nonmalignant leukocyte disorders”. Rodak's Hematology (Elsevier): 445. doi:10.1016/B978-0-323-53045-3.00035-0. PMC 7151933.
- ^ a b c d 日本臨床検査医学会ガイドライン作成委員会(編)「臨床検査のガイドライン:JSLM2018」、日本臨床検査医学会、2018年、2023年7月19日閲覧。
- ^ a b c d Hamad, Hussein; Mangla, Ankit (2023), Lymphocytosis, StatPearls Publishing, PMID 31747226 2023年7月27日閲覧。
- ^ 板東 浩 (2007). “栄養サポートチーム(NST)”. 日本内科学会雑誌 96: 1515-1520. doi:10.2169/naika.96.1515.
- ^ a b Espinoza, Valerie E.; Emmady, Prabhu D. (2023), Histology, Monocytes, StatPearls Publishing, PMID 32491550 2023年7月27日閲覧。
- ^ Phyu Thin Naing; Utkarsh Acharya; Abhishek Kumar (2023-5). Hairy Cell Leukemia. StatPearls [Internet]. Treasure Island (FL): StatPearls Publishing 2023年8月5日閲覧。
- ^ a b Kanuru, Sruthi; Sapra, Amit (2023), Eosinophilia, StatPearls Publishing, PMID 32809764 2023年7月27日閲覧。
- ^ a b c Sticco, Kristin L.; Pandya, Nirzari K.; Lynch, David T. (2023), Basophilia, StatPearls Publishing, PMID 30570986 2023年7月27日閲覧。
- ^ a b c d C.M. Carter (2018). Charlene A. McQueen. ed. Comprehensive Toxicology (Third Edition). Elsevier. pp. 249-293. doi:10.1016/B978-0-12-801238-3.64251-4 2023年8月9日閲覧。
- ^ 平成24年度血液検査機器技術委員会. “自動血球分析装置におけるスキャッタ-から判る異常細胞”. 日本医療検査科学会. 2023年8月4日閲覧。
- ^ Shira Ronen, et al. (2019). “Carcinocythemia: A rare entity becoming more common? A 3-year, single institution series of seven cases and literature review”. Int J Lab Hematol. 41: 69-79. doi:10.1111/ijlh.12924.
- ^ a b c “フローサイトメトリー法による白血球5分類算定法(JSLH-Diff法)手順書”. 日本検査血液学会. 2023年7月31日閲覧。
- ^ Derek Doyle (2006). “William Hewson (1739?74): the father of haematology”. British Journal of Haematology 133: 375-381. doi:10.1111/j.1365-2141.2006.06037.x.
- ^ a b c d e 伊藤 道雄. “臨床検査技術の系統化調査”. 国立科学博物館. 2023年8月1日閲覧。
- ^ a b A. B. Kay (2015). “The early history of the eosinophil”. Clinical & Experimental Allergy 45: 575-582. doi:10.1111/cea.12480.
- ^ a b KP Krafts, E Hempelmann; BJ Oleksyn (2011). “The color purple: from royalty to laboratory, with apologies to Malachowski”. Biotechnic & Histochemistry (Taylor & Francis) 86 (1): 7-35. doi:10.3109/10520295.2010.515490. PMID 21235291.
- ^ Marshall Don. Graham (2022). “The Coulter Principle: A history”. Cytometry 101: 45149. doi:10.1002/cyto.a.24505.
- ^ Ralph Green, Sebastian Wachsmann-Hogiu (2015). “Development, History, and Future of Automated Cell Counters”. Clin Lab Med 35: 44936. doi:10.1016/j.cll.2014.11.003.
- ^ Julien Picot, et al. (2015). “Flow cytometry: retrospective, fundamentals and recent instrumentation”. Cytotechnology 64: 109-130. doi:10.1007/s10616-011-9415-0.
- ^ Harvey, John W. (2011-10-31) (英語). Veterinary Hematology: A Diagnostic Guide and Color Atlas. Elsevier Health Sciences. ISBN 978-1-4377-2360-1
- ^ “MSD MANUAL Veterinary / Circulatory System / Leukocyte Disorders / Leukogram Abnormalities in Animals”. MSD MANUAL Veterinary Manual. 2023年7月31日閲覧。
- ^ 佐藤昭夫「白血球の鑑別」『日本獣医師会雑誌』第15巻第11号、1962年、461-465頁、doi:10.12935/jvma1951.15.461。
関連項目
[編集]- 全血球計算
- 末梢血塗抹検査
- 白血球・多形核白血球・顆粒球
- 好中球・好中球増多症・好中球減少症
- 好酸球・好酸球増多症・好酸球減少症
- 好塩基球・好塩基球増多症・好塩基球減少症
- 単球・単球増多症・単球減少症
- リンパ球・リンパ球増多症・リンパ球減少症・異型リンパ球
- 血液・末梢血・血液学・臨床検査
- 英語版の白血球分画(White blood cell differential)
外部リンク
[編集]- MSDマニュアル 家庭版 / 13. 血液の病気 / 白血球の病気 / 好中球増多症
- MSDマニュアル 家庭版 / 13. 血液の病気 / 白血球の病気 / 好中球減少症
- MSDマニュアル プロフェッショナル版 / 11. 血液学および腫瘍学 / 白血球減少症 / 好中球減少症
