「モノクローナル抗体の命名法」の版間の差分
Karasunoko (会話 | 投稿記録) →起源を表すサブステム: 翻訳 |
m こう書いた方が良いかと。 |
||
| 64行目: | 64行目: | ||
|} |
|} |
||
'''モノクローナル抗体の命名法'''は商標登録されていない名称である一般名を[[モノクローナル抗体]]に割り当てるための命名体系 |
'''モノクローナル抗体の命名法'''では、商標登録されていない名称である一般名を[[モノクローナル抗体]]に割り当てるための命名体系について解説する。 |
||
[[抗体]]はB細胞が分化してできる[[形質細胞]]によって産生される[[タンパク質]]で、ヒトやその他の[[脊椎動物]]の[[免疫系]]において[[真正細菌|細菌]]や[[ウイルス]]などの外来物質を識別する役割を持つ。"モノクローナル"抗体は特に[[クローン (細胞生物学)|同一の細胞]]によって、しばしば人工的に産生される抗体であり、標的が単一である。モノクローナル抗体は医学用途を含め様々な方法で応用される<ref name="Janeway" />。 |
|||
医薬品の命名のために[[世界保健機関|世界保健機構]]の定める[[国際一般名]] (INN)<ref name="WHO_1997" />と[[米国一般名]] (USAN)<ref name="AMA_2007" />の両者がこの命名体系を用いている。一般に[[語幹]](ステム)は医薬品のクラスを明らかにするために用いられ、多くの場合単語の終わりに置かれる。全てのモノクローナル抗体の名称は接尾辞である''-マブ'' (''-mab'') で終わる。他の医薬品と異なるのは、モノクローナル抗体の命名がその形状や機能に合わせて接尾辞以外の単語の部品([[形態素]])を接尾辞に先行して用いる点にある。この形態素は公式にはサブステムと呼ばれるが、USAN会議自身が誤って[[接中辞]]と呼ぶ事もある<ref name="AMA_2007" />。 |
医薬品の命名のために[[世界保健機関|世界保健機構]]の定める[[国際一般名]] (INN)<ref name="WHO_1997" />と[[米国一般名]] (USAN)<ref name="AMA_2007" />の両者がこの命名体系を用いている。一般に[[語幹]](ステム)は医薬品のクラスを明らかにするために用いられ、多くの場合単語の終わりに置かれる。全てのモノクローナル抗体の名称は接尾辞である''-マブ'' (''-mab'') で終わる。他の医薬品と異なるのは、モノクローナル抗体の命名がその形状や機能に合わせて接尾辞以外の単語の部品([[形態素]])を接尾辞に先行して用いる点にある。この形態素は公式にはサブステムと呼ばれるが、USAN会議自身が誤って[[接中辞]]と呼ぶ事もある<ref name="AMA_2007" />。 |
||
==構成成分== |
== 構成成分 == |
||
[[File:Antibody IgG2.png|thumb|left|抗体の構造。4つの[[抗体#定常領域と可変領域|可変領域]]は右上と左上の末端の塊である。]] |
[[File:Antibody IgG2.png|thumb|left|抗体の構造。4つの[[抗体#定常領域と可変領域|可変領域]]は右上と左上の末端の塊である。]] |
||
===語幹=== |
=== 語幹 === |
||
語幹である''-マブ (-mab) ''はモノクローナル抗体と同様に、1つでも[[抗体#定常領域と可変領域|可変領域]](標的と結合する構造を含んだドメイン)を含んでいれば、モノクローナル抗体の部位にも使われる<ref name="WHO-INN" />。人工タンパク質の中でも[[:en:Fragment antigen-binding|Fab領域]]<ref name="Ranibizumab" />と[[:en:Single-chain variable fragment|一本鎖抗体]] (scFv) <ref name="Pexelizumab" />がこれにあたる。一方で[[Fc領域]]のような抗体の標的認識に関わらない部分や、他の抗体に類似した構造を持つ分子には別の命名系が用いられる。 |
語幹である''-マブ (-mab) ''はモノクローナル抗体と同様に、1つでも[[抗体#定常領域と可変領域|可変領域]](標的と結合する構造を含んだドメイン)を含んでいれば、モノクローナル抗体の部位にも使われる<ref name="WHO-INN" />。人工タンパク質の中でも[[:en:Fragment antigen-binding|Fab領域]]<ref name="Ranibizumab" />と[[:en:Single-chain variable fragment|一本鎖抗体]] (scFv) <ref name="Pexelizumab" />がこれにあたる。一方で[[Fc領域]]のような抗体の標的認識に関わらない部分や、他の抗体に類似した構造を持つ分子には別の命名系が用いられる。 |
||
===起源を表すサブステム=== |
=== 起源を表すサブステム === |
||
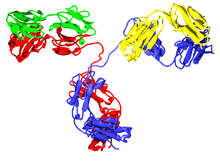
[[File:Chimeric and humanized antibodies with CDRs.svg|thumb|'''起源を表すサブステム''': [[マウス]](左上)、[[キメラ抗体|キメラ]](右上)、[[ヒト化]](左下)、キメラ/ヒト化(下段中央)、および[[ヒト]](右下)モノクローナル抗体。<br />ヒトの配列を茶色で、ヒト以外の動物に由来する配列を青色で示す。可変領域は各抗体の頂上部の箱、CDRはその上部の3本のループ。]] |
[[File:Chimeric and humanized antibodies with CDRs.svg|thumb|'''起源を表すサブステム''': [[マウス]](左上)、[[キメラ抗体|キメラ]](右上)、[[ヒト化]](左下)、キメラ/ヒト化(下段中央)、および[[ヒト]](右下)モノクローナル抗体。<br />ヒトの配列を茶色で、ヒト以外の動物に由来する配列を青色で示す。可変領域は各抗体の頂上部の箱、CDRはその上部の3本のループ。]] |
||
| 83行目: | 85行目: | ||
ラット/マウスハイブリッド抗体は2つの異なる抗原と結合できる。このような薬品はトリファンクショナル抗体と呼ばれ、サブステム ''-アクソ- (-axo-)'' が用いられる<ref name="Lordick" />。 |
ラット/マウスハイブリッド抗体は2つの異なる抗原と結合できる。このような薬品はトリファンクショナル抗体と呼ばれ、サブステム ''-アクソ- (-axo-)'' が用いられる<ref name="Lordick" />。 |
||
===標的を表すサブステム=== |
=== 標的を表すサブステム === |
||
抗体の起源を表すサブステムの前に |
抗体の起源を表すサブステムの前に付くもう1つのサブステムは薬の標的を示す。標的の例として、[[腫瘍]]や、[[循環系]]のような[[器官]]、[[真正細菌|細菌]]や[[ウイルス]]のような[[病原体]]が挙げられる。''標的''という語は抗体の使用目的を意味しない。つまり、[[治療]]目的か、[[予防医学|予防]]目的か、あるいは[[診断]]用かといった区別はこの命名系ではなされない。 |
||
命名系が制定された当初、標的用のサブステムは子音-母音-子音という構成であった。ただし最後の子音は発音が困難になる場合欠落する事がある。例として循環系を示す''-シ(ル)- (-ci(r)-)''、[[免疫系]]を示す''-リ(ム)- (-li(m)-)''(limは[[リンパ球]]を意味する)、神経系を示す''-ネ(ル)- (-ne(r)-)'' が例として挙げられる。最後の子音は続くサブステムが子音で始まる(例えば''-ズ-(-zu-)'' や''-キシ-(-xi-)'')場合、通常除かれるが、常に標的用サブステムが短い形でも用いられるとは限らない。例えば''-ムル- (-mul-)'' は、キメラないしヒト化された[[運動器|筋骨格系]]を標的とする抗体がINNに登録されていないため、短縮形である''-ム- (-mu-)'' が用いられた事は無い。標的用サブステムと起源用サブステムの組み合わせによって、免疫系を標的とするヒト抗体を意味する''-リムマブ (-limumab)'' や、循環系を標的とするキメラ抗体で子音rが脱落した''-シキシマブ (-ciximab)'' などで終わる名称が生じる<ref name="AMA_2007" />。 |
命名系が制定された当初、標的用のサブステムは子音-母音-子音という構成であった。ただし最後の子音は発音が困難になる場合欠落する事がある。例として循環系を示す''-シ(ル)- (-ci(r)-)''、[[免疫系]]を示す''-リ(ム)- (-li(m)-)''(limは[[リンパ球]]を意味する)、神経系を示す''-ネ(ル)- (-ne(r)-)'' が例として挙げられる。最後の子音は続くサブステムが子音で始まる(例えば''-ズ-(-zu-)'' や''-キシ-(-xi-)'')場合、通常除かれるが、常に標的用サブステムが短い形でも用いられるとは限らない。例えば''-ムル- (-mul-)'' は、キメラないしヒト化された[[運動器|筋骨格系]]を標的とする抗体がINNに登録されていないため、短縮形である''-ム- (-mu-)'' が用いられた事は無い。標的用サブステムと起源用サブステムの組み合わせによって、免疫系を標的とするヒト抗体を意味する''-リムマブ (-limumab)'' や、循環系を標的とするキメラ抗体で子音rが脱落した''-シキシマブ (-ciximab)'' などで終わる名称が生じる<ref name="AMA_2007" />。 |
||
| 90行目: | 92行目: | ||
2009年には新しい短縮されたサブステムが採用された。新しいサブステムのほとんどは1つの子音のみからなるが、母音を伴う事もある。しかし、この母音は起源用サブステムが母音で始まる場合には省略される。例えば免疫系を標的としたヒト抗体は旧命名系における''-リムマブ (-limumab)'' の代わりに''-ルマブ (-lumab)'' で終わる名称が付けられる。''-シキシマブ (-ciximab)'' のような一部の命名は変化しない<ref name="WHO_2009" />。旧体系においては腫瘍のタイプに応じて腫瘍を標的とするサブステムが7つ用いられていた。多くの抗体は複数の腫瘍を標的として開発されるため、新しい体系は''-ト(ゥ)- (-t(u)-)'' のみが使用される<ref name="AMA_2007" />。 |
2009年には新しい短縮されたサブステムが採用された。新しいサブステムのほとんどは1つの子音のみからなるが、母音を伴う事もある。しかし、この母音は起源用サブステムが母音で始まる場合には省略される。例えば免疫系を標的としたヒト抗体は旧命名系における''-リムマブ (-limumab)'' の代わりに''-ルマブ (-lumab)'' で終わる名称が付けられる。''-シキシマブ (-ciximab)'' のような一部の命名は変化しない<ref name="WHO_2009" />。旧体系においては腫瘍のタイプに応じて腫瘍を標的とするサブステムが7つ用いられていた。多くの抗体は複数の腫瘍を標的として開発されるため、新しい体系は''-ト(ゥ)- (-t(u)-)'' のみが使用される<ref name="AMA_2007" />。 |
||
===接頭辞=== |
=== 接頭辞 === |
||
接頭辞は特別な意味を持たない。<!--It should be unique for each medicine and contribute to a well sounding name.<ref name="WHO_2009" /> This means that antibodies with the same source and target substems are only distinguished by their prefix. Even antibodies targeting exactly the same structure are differently prefixed, such as the [[adalimumab|''ada''limumab]] and [[golimumab|''go''limumab]], both of which are [[TNF inhibitor]]s but differ in their chemical structure.<ref name="Adalimumab" /><ref name="Golimumab" /> |
接頭辞は特別な意味を持たない。<!--It should be unique for each medicine and contribute to a well sounding name.<ref name="WHO_2009" /> This means that antibodies with the same source and target substems are only distinguished by their prefix. Even antibodies targeting exactly the same structure are differently prefixed, such as the [[adalimumab|''ada''limumab]] and [[golimumab|''go''limumab]], both of which are [[TNF inhibitor]]s but differ in their chemical structure.<ref name="Adalimumab" /><ref name="Golimumab" /> |
||
===Additional words=== |
=== Additional words === |
||
A second word following the name of the antibody indicates that another substance is attached,<ref name="WHO_2009" /> which is done for several reasons. |
A second word following the name of the antibody indicates that another substance is attached,<ref name="WHO_2009" /> which is done for several reasons. |
||
* An antibody can be [[PEGylated]] (attached to molecules of [[polyethylene glycol]]) to slow down its degradation by enzymes and to decrease its [[immunogenicity]];<ref name="Veronese" /> this is shown by the word ''pegol'' as in ''[[alacizumab pegol]]''.<ref name="Alacizumab" /> |
* An antibody can be [[PEGylated]] (attached to molecules of [[polyethylene glycol]]) to slow down its degradation by enzymes and to decrease its [[immunogenicity]];<ref name="Veronese" /> this is shown by the word ''pegol'' as in ''[[alacizumab pegol]]''.<ref name="Alacizumab" /> |
||
2016年8月8日 (月) 19:02時点における版
| 接頭辞 | 抗体の標的を表すサブステム | 抗体の起源(動物)を表すサブステム | 接尾辞 | |||
|---|---|---|---|---|---|---|
| 旧 | 新 | 意味 | 意味 | |||
| 任意 | -anibi- | — | 血管新生 (阻害) | -a- | ラット | -mab (-pab) |
| -ba(c)- | -b(a)- | 細菌 | -e- | ハムスター | ||
| -ci(r)- | -c(i)- | 循環系 | -i- | 霊長類 | ||
| -fung- | -f(u)- | 真菌 | -o- | マウス | ||
| -gr(o)- | -gr(o)- | 成長因子 | -u- | ヒト | ||
| -ki(n)- | -k(i)- | インターロイキン | -xi- | キメラ (ヒト/他種) | ||
| -les- | — | 炎症性の損傷 | -zu- | ヒト化 | ||
| -li(m)- | -l(i)- | 免疫系 | -xizu-* | キメラ/ヒト化-ハイブリッド | ||
| -mul- | — | 筋骨格系 | -axo- | ラット/マウス-ハイブリッド (en:trifunctional antibody参照) | ||
| -ne(u)(r)- | -n(e)-* | 神経系 | ||||
| -os- | -s(o)- | 骨 | ||||
| -toxa- | -tox(a)- | 毒素 | ||||
| -co(l)- | -t(u)- | 大腸腫瘍 | ||||
| -go(t)- | 精巣腫瘍 | |||||
| -go(v)- | 卵巣腫瘍 | |||||
| -ma(r)- | 乳腺腫瘍 | |||||
| -me(l)- | メラノーマ | |||||
| -pr(o)- | 前立腺腫瘍 | |||||
| -tu(m)- | 種々の腫瘍 | |||||
| -vi(r)- | -v(i)- | ウイルス | ||||
| * 2009年12月現在[update]の議論による | ||||||
モノクローナル抗体の命名法では、商標登録されていない名称である一般名をモノクローナル抗体に割り当てるための命名体系について解説する。
抗体はB細胞が分化してできる形質細胞によって産生されるタンパク質で、ヒトやその他の脊椎動物の免疫系において細菌やウイルスなどの外来物質を識別する役割を持つ。"モノクローナル"抗体は特に同一の細胞によって、しばしば人工的に産生される抗体であり、標的が単一である。モノクローナル抗体は医学用途を含め様々な方法で応用される[4]。
医薬品の命名のために世界保健機構の定める国際一般名 (INN)[5]と米国一般名 (USAN)[1]の両者がこの命名体系を用いている。一般に語幹(ステム)は医薬品のクラスを明らかにするために用いられ、多くの場合単語の終わりに置かれる。全てのモノクローナル抗体の名称は接尾辞である-マブ (-mab) で終わる。他の医薬品と異なるのは、モノクローナル抗体の命名がその形状や機能に合わせて接尾辞以外の単語の部品(形態素)を接尾辞に先行して用いる点にある。この形態素は公式にはサブステムと呼ばれるが、USAN会議自身が誤って接中辞と呼ぶ事もある[1]。
構成成分
語幹
語幹である-マブ (-mab) はモノクローナル抗体と同様に、1つでも可変領域(標的と結合する構造を含んだドメイン)を含んでいれば、モノクローナル抗体の部位にも使われる[6]。人工タンパク質の中でもFab領域[7]と一本鎖抗体 (scFv) [8]がこれにあたる。一方でFc領域のような抗体の標的認識に関わらない部分や、他の抗体に類似した構造を持つ分子には別の命名系が用いられる。
起源を表すサブステム

ヒトの配列を茶色で、ヒト以外の動物に由来する配列を青色で示す。可変領域は各抗体の頂上部の箱、CDRはその上部の3本のループ。
語幹に先行するサブステムは抗体の由来となる動物の種を表す[1]。初期のモノクローナル抗体はマウス(サブステム-オ- (-o-) がついて接尾辞が-オマブ (-omab) に変化、通常学名Mus musculus、ないしハツカネズミと呼ばれる)や、他のヒト以外の動物から得られた。INNもUSANもラット(原理的には-ア- (-a-)がつく)やハムスター(-エ- (-e-)がつく)や霊長類(-イ- (-i-)がつく)からの抗体をもはや求めていない[6]。
ヒト以外の動物から得られた抗体はヒトの免疫系に外来抗原として認識され、速やかな排泄、アレルギー反応、もしくはその両者を引き起こす可能性がある[9][10]。これを避けるために、抗体の一部がヒトの抗体のアミノ酸配列に置き換えられたり、あるいは完全なヒトの抗体が開発されたりする。定常領域がヒトのものと置換されると、生み出された抗体はキメラと呼ばれるようになり、-キシ- (-xi-) のサブステムが用いられる。可変領域の配列が部分的にヒトのものに置換されることもあり、これはヒト化と呼ばれ命名には-ズ- (-zu-) が用いられる。ヒト化抗体の場合、典型的には、可変領域の外側に飛び出る3本のループ状アミノ酸配列で、標的に結合する領域である相補性決定領域 (CDR) を除いた全体がヒトの配列に置き換えられる。抗体の片方の鎖がキメラでもう片方がヒト化されている場合は-キシズ- (-xizu-) を用いる。-キシ- (-xi-)、-ズ- (-zu-)、-キシズ- (-xizu-) の3つのサブステムは抗体の元となった動物種を意味しない。つまり、ヒト/マウスキメラ抗体であるバシリキシマブ (basiliximab) は-キシマブ (-ximab) で終わるが、これはヒト/マカク抗体であるゴミリキシマブでも同様である。完全なヒトの抗体には-ウ- (-u-)を用いる[2]。
ラット/マウスハイブリッド抗体は2つの異なる抗原と結合できる。このような薬品はトリファンクショナル抗体と呼ばれ、サブステム -アクソ- (-axo-) が用いられる[11]。
標的を表すサブステム
抗体の起源を表すサブステムの前に付くもう1つのサブステムは薬の標的を示す。標的の例として、腫瘍や、循環系のような器官、細菌やウイルスのような病原体が挙げられる。標的という語は抗体の使用目的を意味しない。つまり、治療目的か、予防目的か、あるいは診断用かといった区別はこの命名系ではなされない。
命名系が制定された当初、標的用のサブステムは子音-母音-子音という構成であった。ただし最後の子音は発音が困難になる場合欠落する事がある。例として循環系を示す-シ(ル)- (-ci(r)-)、免疫系を示す-リ(ム)- (-li(m)-)(limはリンパ球を意味する)、神経系を示す-ネ(ル)- (-ne(r)-) が例として挙げられる。最後の子音は続くサブステムが子音で始まる(例えば-ズ-(-zu-) や-キシ-(-xi-))場合、通常除かれるが、常に標的用サブステムが短い形でも用いられるとは限らない。例えば-ムル- (-mul-) は、キメラないしヒト化された筋骨格系を標的とする抗体がINNに登録されていないため、短縮形である-ム- (-mu-) が用いられた事は無い。標的用サブステムと起源用サブステムの組み合わせによって、免疫系を標的とするヒト抗体を意味する-リムマブ (-limumab) や、循環系を標的とするキメラ抗体で子音rが脱落した-シキシマブ (-ciximab) などで終わる名称が生じる[1]。
2009年には新しい短縮されたサブステムが採用された。新しいサブステムのほとんどは1つの子音のみからなるが、母音を伴う事もある。しかし、この母音は起源用サブステムが母音で始まる場合には省略される。例えば免疫系を標的としたヒト抗体は旧命名系における-リムマブ (-limumab) の代わりに-ルマブ (-lumab) で終わる名称が付けられる。-シキシマブ (-ciximab) のような一部の命名は変化しない[2]。旧体系においては腫瘍のタイプに応じて腫瘍を標的とするサブステムが7つ用いられていた。多くの抗体は複数の腫瘍を標的として開発されるため、新しい体系は-ト(ゥ)- (-t(u)-) のみが使用される[1]。
接頭辞
接頭辞は特別な意味を持たない。
参考文献
- ^ a b c d e f “AMA (USAN) Monoclonal antibodies”. United States Adopted Names (2007年8月7日). 2007年8月15日閲覧。
- ^ a b c “General policies for monoclonal antibodies” (PDF). World Health Organization (2009年12月18日). 2010年6月8日閲覧。
- ^ “The use of stems in the selection of International Nonproprietary Names (INN) for pharmaceutical substances” (PDF). World Health Organization. pp. 107–109, 168–169 (2009年). 2010年2月22日閲覧。
- ^ Janeway, CA, Jr.; Travers, P; Walport, M; Shlomchik, MJ (2001). Immunobiology (5th ed.). Garland Publishing. ISBN 0-8153-3642-X
- ^ “Guidelines on the Use of International Nonproprietary Names (INNs) for Pharmaceutical Substances” (PDF). pp. 27–28 (1997年). 2007年8月15日閲覧。
- ^ a b “International Nonproprietary Names”. WHO Drug Information (World Health Organization) 23 (3): 195–199. (2009) 2010年12月8日閲覧。.
- ^ “International Nonproprietary Names for Pharmaceutical Substances (INN)” (PDF). WHO Drug Information (World Health Organization) 18 (1): 61. (2004) 2010年6月8日閲覧。.
- ^ “International Nonproprietary Names for Pharmaceutical Substances (INN)” (PDF). WHO Drug Information (World Health Organization) 15 (2): 121. (2001) 2010年6月8日閲覧。.
- ^ Stern, M.; Herrmann, R. (2005). “Overview of monoclonal antibodies in cancer therapy: present and promise”. Critical Reviews in Oncology/Hematology 54 (1): 11–29. doi:10.1016/j.critrevonc.2004.10.011. PMID 15780905.
- ^ Tabrizi, M.; Tseng, C.; Roskos, L. (2006). “Elimination mechanisms of therapeutic monoclonal antibodies”. Drug Discovery Today 11 (1–2): 81–88. doi:10.1016/S1359-6446(05)03638-X. PMID 16478695.
- ^ Lordick, F; Ott, K; Weitz, J; Jäger, D (2008). “The evolving role of catumaxomab in gastric cancer”. Expert Opinion on Biological Therapy 8 (9): 1407–15. doi:10.1517/14712598.8.9.1407. PMID 18694358.
