形成性操作タンパク質
形成性操作タンパク質(けいせいせいそうさタンパクしつ、ディリジェントタンパク質、英: dirigent protein)は、他酵素によって合成される化合物の立体化学を決定づけるタンパク質である[1]。最初の形成性操作タンパク質はForsythia × intermediaにおいて発見された。このタンパク質はコニフェニルアルコール単量体からの(+)-ピノレシノールの立体選択的生合成を指示することが明らかにされている[2]。
"Dirigent"[ラテン語のdirigate(〜を導く、〜を並べる、という意味)由来]という用語は、このタンパク質を発見した研究グループによる造語である[3][4]。
リグナンの生合成は酸化酵素 (oxidative enzyme) によって触媒される[5]。試験管内では、反応は二量体化合物の不均一混合物を与える[6]。反応の間に形成性操作タンパク質が存在すると、1種類の化合物の1種類の立体異性体が高い選択性で得られる。形成性操作タンパク質それ自身は酸化的ラジカル形成活性を持たないように見える、酸化酵素がなければ反応は起こらない[7]。
近年、2番目のエナンチオ相補的形成性操作タンパク質がシロイヌナズナ(Arabidopsis thaliana)から発見された[8]。この酵素は (−)-ピノレシノールのエナンチオ選択的合成を指示する。
活性
[編集]リグナンの生合成において、酸化酵素は水素原子プロトン共役型電子移動によってモノリグノールから水素原子を取り除きラジカル中間体を形成する。これらの中間体は次にラジカル停止反応に連結し、リグナンとして知られる様々な二量体の中の一つを形成する[9]。酸化酵素存在下でのコニフェリルアルコール(一般的なモノリグノール)のin vitro反応では、様々な濃度の様々な異なる二量体が得られる[6]。Forsythia × intermedia由来の形成性操作タンパク質が存在すると、(+)-ピノレシノールの生成が著しく強化され、その他の生成物は極めて少なくなる。この強化が非常に明白なため、形成性操作タンパク質は (+)-ピノレシノールのみを生産し、様々な不均一混合物が生成するタンパク質が介在しない連結反応と競合している、との仮説が立てられている[10]。これは、異なる濃度の形成性操作タンパク質存在下で生成する様々な混合物を分析することによって確かめられている。この立体選択性が達成される機構は現時点でよく分かっていない。しかしながら、酸化酵素がなければ反応が進行しないため、形成性操作タンパク質自身はラジカルを形成するためのコニフェリルアルコールの酸化を触媒しないように見える。
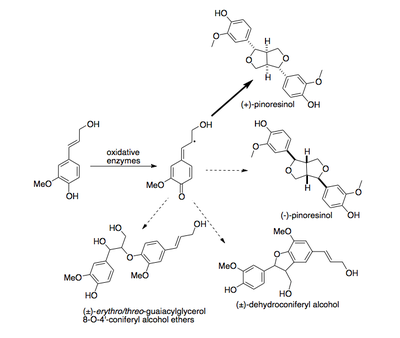
Forsythia intermedia由来の形成性操作タンパク質の活性はコニフェリルアルコール特異的である[11]。p-クマリルアルコールやシナピルアルコールといったその他のモノリグノールが形成性操作タンパク質存在下で酸化酵素とin vitroで反応した場合、形成性操作タンパク質非存在下での実験と区別できない生成物の不均一な混合物を与える。
構造
[編集]円偏光二色性実験により、Forsythia intermedia由来の形成性操作タンパク質の二次構造は主にβシートとループ構造から成ることが明らかにされている。三次構造は解かれていないが、タンパク質は二量体であることが確かめられている。それぞれの単量体は単一のコニフェリルアルコール結合部位を有し、全部で2つの結合部位が存在する[12]。1分子のコニフェリルアルコールがそれぞれの部位に結合できるため、2分子間の反応構造が限定されることによって、(+)-ピノレシノールの生成が増加し、その他の生成物の生成が阻害される。
脚注
[編集]- ^ Davin LB, Wang HB, Crowell AL, et al. (1997). “Stereoselective bimolecular phenoxy radical coupling by an auxiliary (dirigent) protein without an active center”. Science 275 (5298): 362–6. doi:10.1126/science.275.5298.362. PMID 8994027.
- ^ Davin LB, Wang HB, Crowell AL, et al. (1997). “Stereoselective bimolecular phenoxy radical coupling by an auxiliary (dirigent) protein without an active center”. Science 275 (5298): 362–6. doi:10.1126/science.275.5298.362. PMID 8994027.
- ^ Davin, Laurence B.; Lewis, Norman G. (2000). “Dirigent Proteins and Dirigent Sites Explain the Mystery of Specificity of Radical Precursor Coupling in Lignan and Lignin Biosynthesis”. Plant Physiology 123 (2): 453–462. doi:10.1104/pp.123.2.453.
- ^ "Dirigent" はドイツ語や北欧語では「指揮者」を意味する。
- ^ Ward R.S. (1982). “The synthesis of lignans and neolignans”. Chemical Society Reviews 11: 75–125. doi:10.1039/CS9821100075.
- ^ a b Fournand D, Cathala B, Lapierre C (January 2003). “Initial steps of the peroxidase-catalyzed polymerization of coniferyl alcohol and/or sinapyl aldehyde: capillary zone electrophoresis study of pH effect”. Phytochemistry 62 (2): 139–46. doi:10.1016/S0031-9422(02)00573-3. PMID 12482448.
- ^ Davin L.B., Lewis N.G. (August 2005). “Dirigent phenoxy radical coupling: advances and challenges”. Current Opinion in Biotechnology 16 (4): 398–406. doi:10.1016/j.copbio.2005.06.010.
- ^ Pickel B, Constantin M-A, Pfannsteil J, Conrad J, Beifuss U, Schaffer A (March 2007). “An Enantiocomplementary Dirigent Protein for the Enantioselective Laccase-Catalyzed Oxidative Coupling of Phenols”. Angewandte Chemistry 53 (4): 273–284. doi:10.1007/s10086-007-0892-x.
- ^ Sarkanen, Simo; Lewis, Norman (1998). Lignin and lignan biosynthesis. Columbus, OH: American Chemical Society. ISBN 0-8412-3566-X
- ^ Halls SC, Davin LB, Kramer DM, Lewis NG (2004). “Kinetic study of coniferyl alcohol radical binding to the (+)-pinoresinol forming dirigent protein”. Biochemistry 43 (9): 2587–95. doi:10.1021/bi035959o. PMID 14992596.
- ^ Kim, M.K., Jeon J-H, Fujita M, Davin L.B., Lewis N.G. (2002). “The western red cedar (Thuja plicata) 8-8′ DIRIGENT family displays diverse expression patterns and conserved monolignol coupling specificity”. Plant Molecular Biology 49 (2): 199–214. doi:10.1023/A:1014940930703.
- ^ Halls SC, Lewis NG (July 2002). “Secondary and quaternary structures of the (+)-pinoresinol-forming dirigent protein”. Biochemistry 41 (30): 9455–61. doi:10.1021/bi0259709. PMID 12135368.

