ネオペンタン
| ネオペンタン | |
|---|---|

|
|

| |
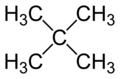
ネオペンタン(許容慣用名) | |
| 識別情報 | |
| CAS登録番号 | 463-82-1 |
| PubChem | 10041 |
| ChemSpider | 9646 |
| EC番号 | 207-343-7 |
| MeSH | Neopentane |
| ChEBI | |
| |
| 特性 | |
| 化学式 | C5H12 |
| モル質量 | 72.15 g mol−1 |
| 示性式 | C(CH3)4 |
| 精密質量 | 72.093900384 g mol−1 |
| 外観 | 無色気体 |
| 密度 | 0.63945 g cm-3 (4 ℃の液体) |
| 融点 |
−17 °C, 256 K, 1 °F |
| 沸点 |
10 °C, 283 K, 50 °F |
| 熱化学 | |
| 標準生成熱 ΔfH |
−168.1 kJ mol-1[1] |
| 標準燃焼熱 ΔcH |
−3514 kJ mol-1[2] |
| 標準モルエントロピー S |
306.28 J K−1 mol−1[1] |
| 危険性 | |
| EU分類 | |
| EU Index | 601-005-00-6 |
| NFPA 704 | |
| Rフレーズ | R12 R51/53 |
| Sフレーズ | S2 S9 S16 S33 S61 |
| 関連する物質 | |
| 関連するテトラブチル炭素 | テトラ-tert-ブチルメタン |
| 関連物質 | テトラメチルシラン テトラメチルスズ |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
ネオペンタン(英: Neopentane)は、2本の側鎖を持つ炭素数5の分岐鎖を有したアルカンである。IUPAC系統名は 2,2-ジメチルプロパン (2,2-dimethylpropane)だが、ネオペンタンはIUPAC許容慣用名として使用される。第4級炭素を有する化合物の中では、最も単純な構造の化合物であり、n-ペンタン、イソペンタンの構造異性体でもある。
物理的性質
[編集]常圧でのネオペンタンの沸点は9.5 °Cであり、常温常圧では引火性の高い気体として存在するものの、寒い日や高圧下では揮発性の液体として存在する。
構造異性体との沸点の比較
[編集]ネオペンタンの沸点は、他の構造異性体に比べて著しく低い。常圧でのイソペンタン(27.7 °C)およびn-ペンタン(36.0 °C)と比べて、ネオペンタン(9.5 °C)である。したがって、ネオペンタンは室温、大気圧下で気体だが、イソペンタンおよびn-ペンタンは辛うじてながら液体である。これについては、分岐鎖が増えたために分子の形状が球形に近付くため、直鎖の場合によりも分子の表面積が減少し、結果として分子間力が弱くしか作用しないからだと説明される[3]。
構造異性体との融点の比較
[編集]一方で、常圧でのネオペンタンの融点(−16.6 °C)は、イソペンタン(−159.9 °C)よりも140 °C高く、n-ペンタン(−129.8 °C)よりも110 °C高い。この異常に高い融点の原因は、正四面体型のネオペンタン分子が固相において、より良く密接しているために、固体の状態であれば、分子間力が強力に作用しているためだと説明されてきた。しかし、この説明は、ネオペンタンが他の2つの異性体よりも低い密度を有するという理由で疑われてきた。その上に、ネオペンタンの固体の融解エントロピーは、n-ペンタンおよびイソペンタンの融解エントロピーよりも低い。これは、ネオペンタンの高い融点が、より高い分子の対称性から生じるエントロピー効果による結果である事を示している。実際、ネオペンタンの融解エントロピーは、n-ペンタンおよびイソペンタンよりも約4倍低い[4]。
NMRスペクトル
[編集]ネオペンタンの分子は正4面体状に炭素が連なり、分子内の水素は全て、正4面体の中心の第4級炭素以外に結合した構造をしている。この分子の対称性のため、全てのプロトンは化学的に等価であり、四塩化炭素に溶解して1H NMRで、これらの水素の化学シフトを計測すると、単一のδ = 0.902という値を与える[5]。この点においてネオペンタンは、1H NMRで基準として用いられるテトラメチルシランと似ている。
ネオペンタン分子の対称性は、一部の水素原子が重水素原子によって置き換えられると壊れる。特に、もしそれぞれのメチル基が、異なる数の重水素原子(0、1、2、3)と結合した場合には、キラルな分子が得られる。
ネオペンチル基
[編集]
ネオペンチル基(Neopentyl substituent)とは、ネオペンタンから水素が1つ脱離した構造の部分を指し、しばしばNpと表記される。その構造は Me3C-CH2 と略記される場合もあり、例えば、ネオペンチルアルコールは Me3CCH2OH さらには NpOH と略記される場合もある。
出典
[編集]- ^ a b 『化学便覧 基礎編』 II、日本化学会 編(改訂6版)、丸善出版、2021年。ISBN 978-4-621-30521-8。 表10.10-2.
- ^ “Neopentane”. NIST. 2021年3月8日閲覧。
- ^ Harold Hart(著)、秋葉 欣哉・奥 彬(訳)『ハート基礎有機化学(改訂版)』 p.50 培風館 1994年3月20日発行 ISBN 4-563-04532-2
- ^ James Wei (1999). “Molecular Symmetry, Rotational Entropy, and Elevated Melting Points”. Ind. Eng. Chem. Res. 38 (12): 5019-5027. doi:10.1021/ie990588m.
- ^ “Proton NMR spectrum of neopentane”. Spectral Database for Organic Compounds. 2006年11月19日閲覧。

