トリフルオロメタンスルホン酸メチル
| トリフルオロメタンスルホン酸メチル | |
|---|---|
| |

| |
Methyl trifluoromethanesulfonate | |
別称 Triflic acid, methyl ester, methyl triflate | |
| 識別情報 | |
| CAS登録番号 | 333-27-7 |
| PubChem | 9526 |
| ChemSpider | 9153 |
| |
| 特性 | |
| 化学式 | C2H3F3O3S |
| モル質量 | 164.1 g mol−1 |
| 外観 | 無色液体 |
| 密度 | 1.496 g/mL |
| 融点 |
-64°C |
| 沸点 |
100°C |
| 水への溶解度 | 加水分解 |
| 危険性 | |
| 主な危険性 | 腐食性 |
| Rフレーズ | R10-R34 |
| Sフレーズ | S26-S36/37/39-S45 |
| 引火点 | 38°C |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
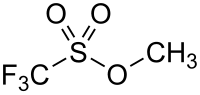
トリフルオロメタンスルホン酸メチル (または普通にメチルトリフラート (Methyl triflate) と呼ばれ、MeOTf と省略される) は、化学式 CF3SO2OCH3 で表される有機化合物である。無色の液体で、有機化学において強力なメチル化剤として用いられる[1]。フルオロスルホン酸メチルと非常に良く似ている。ヒトの死亡はまだ報告されていないが、フルオロスルホン酸メチル(LC50(ラット、1時間)= 5 ppm)についていくつかの症例が報告されている。メチルトリフラートは 入手可能な証拠によると、同じくらいの毒性であることが予想される[1]。
合成
[編集]メチルトリフラートは、市販品が入手できるが、研究室で硫酸ジメチルとトリフル酸 (triflic acid) から調製できる[2]。
- CF3SO2OH + (CH3O)2SO2 → CF3SO2OCH3 + CH3OSO2OH
反応性
[編集]この化合物は、水と接触すると激しく加水分解する。
- CF3SO2OCH3 + H2O → CF3SO2OH + CH3OH
メチル化
[編集]メチル化のランキングの 1つは (CH3)3O+ > CF3SO2OCH3 ≈ FSO2OCH3 > (CH3)2SO4 > CH3I である[2]。メチルトリフラートは、アルデヒド、アミド、ニトリルなどの非常に弱い求核試薬である多くの官能基をアルキル化する。ベンゼンやかさ高い 2,6-ジ-tert-ブチルピリジンはメチル化しない[1]。含窒素複素環に対するメチル化能力は、特定の脱保護スキームに利用される[3] 。
カチオン重合
[編集]メチルトリフラートは、ラクチド[4]および β-プロピオラクトン、ε-カプロラクトンおよびグリコリドを含む他のラクトンの リビングカチオン重合を開始する[5]。

トリメチレンカーボネート やネオペンチレンカーボネート (5,5-ジメチル-1,3-ジオキサン-2-オン) のような環状炭酸エステルは、重合させて対応するポリカーボネートにすることができる[6]。2-アルキル-2-オキサゾリン、例えば 2-エチル-2-オキサゾリンは、重合して ポリ (2-アルキルオキサゾリン) になる[7]。
関連項目
[編集]脚注
[編集]- ^ a b c Roger W. Alder; Justin G. E. Phillips; Lijun Huang; Xuefei Huang (2005). “Methyltrifluoromethanesulfonate”. Encyclopedia of Reagents for Organic Synthesis. doi:10.1002/047084289X.rm266m.pub2. ISBN 0471936235.
- ^ a b Stang, Peter J.; Hanack, Michael; Subramanian, L. R. (1982). “Perfluoroalkanesulfonic Esters: Methods of Preparation and Applications in Organic Chemistry”. Synthesis 1982 (2): 85–126. doi:10.1055/s-1982-29711. ISSN 0039-7881.
- ^ Albert I. Meyers; Mark E. Flanagan (1998). "2,2′-Dimethoxy-6-formylbiphenyl". Organic Syntheses (英語).; Collective Volume, vol. 9, p. 258
- ^ Rangel, Irma; Ricard, Michèle; Ricard, Alain (1994). “Polymerization of L-lactide and ε-caprolactone in the presence of methyl trifluoromethanesulfonate”. Macromolecular Chemistry and Physics 195 (9): 3095–3101. doi:10.1002/macp.1994.021950908.
- ^ Jonté, J. Michael; Dunsing, Ruth; Kricheldorf, Hans R. (1985). “Polylactones. 4. Cationic Polymerization of Lactones by Means of Alkylsulfonates” (英語). Journal of Macromolecular Science: Part A - Chemistry 22 (4): 495–514. doi:10.1080/00222338508056616. ISSN 0022-233X.
- ^ Kricheldorf, Hans R.; Weegen-Schulz, Bettina; Jenssen, Jörg (1998). “Cationic polymerization of aliphatic cyclocarbonates” (英語). Macromolecular Symposia 132 (1): 421–430. doi:10.1002/masy.19981320139.
- ^ Glassner, Mathias; D’hooge, Dagmar R.; Young Park, Jin; Van Steenberge, Paul H.M.; Monnery, Bryn D.; Reyniers, Marie-Françoise; Hoogenboom, Richard (2015). “Systematic investigation of alkyl sulfonate initiators for the cationic ring-opening polymerization of 2-oxazolines revealing optimal combinations of monomers and initiators” (英語). European Polymer Journal 65: 298–304. doi:10.1016/j.eurpolymj.2015.01.019. hdl:1854/LU-5924229.
