トリフルオロメタノール
| トリフルオロメタノール | |
|---|---|
| |
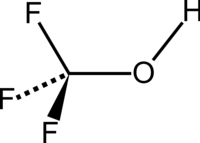
Trifluoromethanol | |
別称 Trifluoromethyl alcohol, perfluoromethanol | |
| 識別情報 | |
| CAS登録番号 | 1493-11-4 |
| PubChem | 73894 |
| ChemSpider | 66527 |
| |
| |
| 特性 | |
| 化学式 | CHF3O |
| モル質量 | 86.01 g mol−1 |
| 外観 | 無色液体 |
| 密度 | 1.5±0.1 g/cm3 |
| 融点 |
-110.64 |
| 沸点 |
22.4 °C, 296 K, 72 °F (±30.0°C) |
| 危険性 | |
| 引火点 | 18.9 °C (66.0 °F; 292.0 K) (±15.6°) |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
トリフルオロメタノール(Trifluoromethanol)は、化学式CHF3Oの有機化合物である[1]。パーフルオロメタノール(Perfluoromethanol)等とも呼ばれ、パーフルオロアルコールの中で最も単純な化合物である[2]。無色の気体で、室温では不安定である。
合成
[編集]全ての一級及び二級のパーフルオロアルコールと同様に、トリフルオロメタノールは、吸熱反応[3]でフッ化水素を脱離してフッ化カルボニルを形成する[4]。
- CF3OH ? COF2 + HF (I)
-120℃以内の温度で、トリフルオロメトキシクロリドと塩化水素から、次のように作ることができる。
- CF3OCl + HCl → CF3OH + Cl2 (II)
この反応では、トリフルオロメトキシクロリド内の部分正電荷を持つ塩素原子と塩化水素内の部分負電荷を持つ塩素原子の再結合が起こり、塩素原子として用いられる。塩素、塩化水素、クロロトリフルオロメタン等の副産物は、-110℃のエバポレーションで除去することができる。融点は-82℃、計算上の沸点は約-20℃であるため、沸点はメタノールよりも約85 K低い。このことは、分子間H-F結合がなく、気相赤外スペクトラムでも見えないことで説明できる。
より単純な合成では、上述の反応(I)を用いる。平衡は、低温では、熱力学的にトリフルオロメタノールの方に偏る。合成されたトリフルオロメタノールがフルオロアンチモン酸等の超酸によりプロトン化されると、平衡はより左側の望ましい生成物の方に偏る。
反応(I)と同様に、トリフルオロメトキシド(CF3O-)は、食塩型のフッ化物(例えばフッ化ナトリウム)とフッ化カルボニルから作ることができる。しかし、CF3O-イオンが酸によって水溶液に移された場合、トリフルオロメタノールは室温で分解する。
上層大気中での生成
[編集]トリフルオロメタノールは通常の環境下では不安定であるが、成層圏では、OF+ラジカルやF-ラジカルとの反応で、CF3-ラジカルやCF3O-ラジカルから生成する。この場合、反応エネルギーが高く活性化されるため、大気中でのトリフルオロメタノールの分解は無視できる。40 km以下の高度では、トリフルオロメタノールの寿命は数千年程度であると推測される[5][6]。
関連項目
[編集]出典
[編集]- ^ Kloeter, Gerhard; Seppelt, Konrad (January 1979). “Trifluoromethanol (CF3OH) and trifluoromethylamine (CF3NH2)”. J. Am. Chem. Soc. 101 (2): 347-349. doi:10.1021/ja00496a012.
- ^ Seppelt, Konrad (May 1977). “Trifluoromethanol, CF3OH”. Angewandte Chemie International Edition in English 16 (5): 322-323. doi:10.1002/anie.197703221.
- ^ Schneider, W. F. (April 11, 1996). “Energetics and Mechanism of Decomposition of CF3OH”. J. Phys. Chem. 100 (15): 6097-6103. doi:10.1021/jp952703m.
- ^ Seppelt, K. (1977). “Trifluormethanol, CF3OH. In: , .” (German). Angew. Chem. 325 (89): 325. doi:10.1002/ange.19770890509.
- ^ Schneider, W. F. (January 1995). “Atmospheric Chemistry of CF3OH: Is Photolysis Important?”. Environmental Science & Technology 29 (1): 247-250. doi:10.1021/es00001a031. PMID 22200226.
- ^ Wellington, T. J.; Schneider, W. F. (1994). “The Stratospheric Fate of CF3OH. In: Environmental Science & Technology 28/1994, S..”. Environ. Sci. Technol. 28 (6): 1198-1200. doi:10.1021/es00055a036. PMID 22176252.
