カルバゾール
表示
(グレーベ・ウルマン反応から転送)
| カルバゾール | |
|---|---|

| |
| |
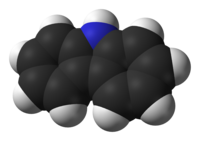
9H-カルバゾール | |
別称 9-アザフルオレン、ジベンゾピロール、ジフェニレンイミン、ジフェニレンイミド、USAF EK-600 | |
| 識別情報 | |
| CAS登録番号 | 86-74-8 |
| KEGG | C08060 |
| 特性 | |
| 化学式 | C12H9N |
| モル質量 | 167.206 g mol−1[1] |
| 融点 |
246.3 °C[1] |
| 沸点 |
354.69 °C[1] |
| 危険性 | |
| 引火点 | 220 °C[1] |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
カルバゾール (carbazole) とは、分子式が C12H9N と表される複素環式化合物の一種である。ピロールの b,d 辺(2,3-位と4,5-位)にベンゼン環がひとつずつ縮合した構造を持つ。水素の位置の違いによる互変異性体が考えられるが、通常は窒素上に水素を持つ 9H-カルバゾールを指す。自然界では原油などに含まれる。
性質・用途
[編集]環の中央に存在する窒素原子は電子を放出しやすいため、ベンゼン環のちょうど窒素から対角線の方向位置に電子求引基を導入すると、分子が電気双極子をもつようになる。
光導電性を生じる誘導体が存在し、その性質から最初に有機材料として複写機の感光ドラムに使われた[2]。
合成
[編集]実験室的にはボルシェ・ドレクセル環化によって合成される[3][4]。まず、フェニルヒドラジンをシクロヘキサノンと縮合させ、ヒドラゾンを合成する。次に塩酸を触媒として転位反応と閉環反応を行い、テトラヒドロカルバゾールを作る。最後に四酸化三鉛で酸化すればカルバゾールとなる。先の2段階をひとつにまとめた、酢酸を用いる変法も報告されている[5]。古典的な合成法としてブヘラのカルバゾール合成が知られる。
他の合成法としてグレーベ・ウルマン反応がある。まず N-フェニル-1,2-ジアミノベンゼン(N-フェニル-o-フェニレンジアミン)はジアゾニウム塩に変換され、これは即座に1,2,3-トリアゾールとなる。このトリアゾールは不安定であり、温度を上げると窒素が脱離し、カルバゾールが生成する[6][7][8]。
参考文献
[編集]- ^ a b c d Lide, David R. (2007). CRC Handbook of Chemistry and Physics, 88th Edition. CRC Press. pp. 3–86. ISBN 978-0849304880
- ^ [リンク切れ]
- ^ Borsche, W. (1908). “Ueber Tetra- und Hexahydrocarbazolverbindungen und eine neue Carbazolsynthese. (Mitbearbeitet von. A. Witte und W. Bothe.)”. Justus Liebigs Ann. Chem. 359 (1-2): 49–80. doi:10.1002/jlac.19083590103.
- ^ Drechsel, E. (1888). “Ueber Elektrolyse des Phenols mit Wechselströmen”. J. Prakt. Chem. 38 (1): 65–74. doi:10.1002/prac.18880380105.
- ^ Rogers, C. U.; Corson, B. B. (1950). "1,2,3,4-Tetrahydrocarbazole". Organic Syntheses (英語). 30: 90.; Collective Volume, vol. 4, p. 884
- ^ Graebe-Ullmann reaction
- ^ Graebe, C; Ullmann, F (1896). “Ueber eine neue Carbazolsynthese”. Justus Liebigs Ann. Chem. 291 (1): 16–17. doi:10.1002/jlac.18962910104.
- ^ Bremer, O. (1934). “Über die Bedeutung der Graebe-Ullmannschen Carbazolsynthese und deren Übertragung auf N-substituierte Pyridino-triazole”. Justus Liebigs Ann. Chem. 514: 279–291. doi:10.1002/jlac.19345140116.
