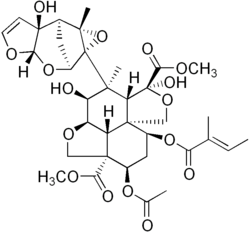
アザジラクチン
| アザジラクチン | |
|---|---|
| |

| |
dimethyl (2aR,3S,4S,R,S,7aS,8S,10R,10aS,10bR)- 10-(acetyloxy)- 3,5-dihydroxy- 4-[(1S,2S,6S,8S,9R,11S)- 2-hydroxy- 11-methyl- 5,7,10-trioxatetracyclo[6.3.1.02,6.09,11]dodec- 3-en- 9-yl]- 4-methyl- 8-{[(2E)- 2-methylbut- 2-enoyl]oxy}octahydro- 1H-furo[3',4':4,4a]naphtho[1,8-bc]furan- 5,10a(8H)-dicarboxylate | |
別称 dimethyl (2aR,3S,4S,4aR,5S,7aS,8S,10R,10aS,10bR)- 10-acetoxy- 3,5-dihydroxy- 4-[(1aR,S,3aS,6aS,7S,7aS)- 6a-hydroxy- 7a-methyl- 3a,6a,7,7a-tetrahydro- 2,7-methanofuro[2,3-b]oxireno[e]oxepin- 1a(2H)-yl]- 4-methyl- 8-{[(2E)-2-methylbut- 2-enoyl]oxy}octahydro- 1H-naphtho[1,8a-c:4,5-b'c']difuran- 5,10a(8H)-dicarboxylate | |
| 識別情報 | |
| CAS登録番号 | 11141-17-6 |
| PubChem | 5281303 |
| 日化辞番号 | J649.024G |
| KEGG | C08748 |
| |
| 特性 | |
| 化学式 | C35H44O16 |
| モル質量 | 720.71 g mol−1 |
| 外観 | 薄ベージュ色固体 |
| 融点 |
154 - 158 °C |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
アザジラクチン(azadirachtin)はリモノイドに分類される天然有機化合物である。インドセンダン Azadirachta indica(ニーム)の木の種子に含まれている二次代謝産物。アザジラクチンは高度に酸化されたテトラノルトリテルペノイドであり、エノールエーテルやアセタール、ヘミアセタール、四置換オキシラン、カルボン酸エステルなど多くの酸素官能基を有する。
化学
[編集]アザジラクチンはアザジラクチンは二級および三級ヒドロキシル基とテトラヒドロフランエーテル、16個の不斉中心を有しており、その内7個は4置換という複雑な分子構造を有しているため、1968年に化合物が単離されてから[1]、長い間化学的な合成の報告がなかった。
アザジラクチンの最初の全合成は2007年にスティーヴン・V・レイ(ケンブリッジ大学)により達成された[2]。
分布と応用
[編集]アザジラクチンは、初めはサバクトビバッタ (Schistocerca gregaria) に対して摂食阻害活性を示す物質として発見され、現在は200種類以上の昆虫に効果があることが知られている。主に摂食阻害剤、成長撹乱物質として作用し、昆虫に対して顕著な毒性を有する(LD50 (S. littoralis): 15 μg/g)。アザジラクチンは天然殺虫剤として合成化合物に取って換わるのに必要な基準の多くを満たしている。アザジラクチンは生分解性であり(光と水に曝らされると100時間以内に分解する)、ほ乳類に対する毒性は非常に低い(マウスに対するLD50は> 3,540 mg/kgであり実質的に無毒)。
本化合物はインドセンダン (Azadirachta indica、ニーム) の木の種子に重量比 0.2 - 0.8 %程含まれている(したがって、化合物名のAzaは、炭素原子が窒素原子に置換されたことを示す接頭辞ではなく、学名に由来する)。インドセンダンの種子や葉、樹皮からは多くのアザジラクチン関連化合物が単離されており、それらもまた様々な害虫に対して強力な生理活性を示す[3][4]。
これらの調整された物質の有益な節足動物に対する効果は一般的にごく小さいと考えられている。いくつかの実験室やフィールド研究によって、インドセンダン抽出物が生物駆除に適応できることが明らかにされている。ピュアなニームオイルはアザジラクチンの他にも殺虫、殺菌成分を含むため、殺虫剤として使用する際には一般的に 1オンス/ガロン(7.6 mL/L)の濃度で水と混合する。
アザジラクチンは複雑な生合成経路で作られるが、ニームのトリテルペノイド二次代謝産物の前駆体はステロイドのチルカロール (tirucallol) であると考えられている。チルカロールは、2分子のファルネシル二リン酸 (FPP) からC30トリテルペンが合成され、次に3つのメチル基を失いC27ステロイドになることで合成される。チルカロールはアリル異性化を受けブチロスペルモール (butyrospermol) となり、続いて酸化を受ける。酸化されたブチロスペルモールはワーグナー・メーヤワイン1,2-メチル転位によりアポチルカロール (apotirucallol) となる。
アポチルカロールは側鎖末端の炭素原子4つが切断されテトラノルトリテルペノイドとなる。側鎖の残りの炭素は環化によりフラン環を形成し、さらに酸化されアザジロン (azadirone) およびアザジラジオン (azadiradione) となる。次にステロイドにおけるC環が開環し酸化されることでニンビン (nimbin)や、ニンビジニン (nimbidinin)、サランニン (salannin) などのC-seco-リモノイドとなる。これらはL--イソロイシン由来のチグリン酸とエステルを形成する。現在は、アザジロンからサラニンが合成され、続いて高度に酸化、環化されることでアザジラクチンが生合成される経路が提唱されている。
脚注
[編集]- ^ J. H. Butterworth and E. D. Morgan (1968). “Isolation of a substance that suppresses feeding in locusts”. Chem. Commun. (London): 23-24. doi:10.1039/C19680000023.
- ^ Gemma E. Veitch, Edith Beckmann, Brenda J. Burke, Alistair Boyer, Sarah L. Maslen, Steven V. Ley (2007). “Synthesis of Azadirachtin: A Long but Successful Journey”. Angew. Chem. Intl. Ed. 46 (40): 7629. doi:10.1002/anie.200703027. PMID 17665403.
- ^ Senthil-Nathan, S., Kalaivani, K., Murugan, K., Chung, G. (2005). “The toxicity and physiological effect of neem limonoids on Cnaphalocrocis medinalis (Guenée) the rice leaffolder”. Pesticide Biochemistry and Physiology 81: 113. doi:10.1016/j.pestbp.2004.10.004.
- ^ Senthil-Nathan, S., Kalaivani, K., Murugan, K., Chung, P.G. (2005). “Effects of neem limonoids on malarial vector Anopheles stephensi Liston (Diptera: Culicidae)”. Acta Tropica 96 (1): 47. doi:10.1016/j.actatropica.2005.07.002. PMID 16112073.
- ^ 総説:S. V. Ley, A. A. Denholm and A. Wood (1993). “The chemistry of azadirachtin”. Nat. Prod. Rep. 10: 109-157. doi:10.1039/NP9931000109.
関連項目
[編集]外部リンク
[編集]- 佐藤健太郎 (2007年8月2日). “アザジラクチン・22年目の陥落”. 有機化学美術館・分館. 2010年11月8日閲覧。
- cosine (2007年9月23日). “アザジラクチン”. 身のまわりの分子 -Chem-Station-. 2009年11月25日時点のオリジナルよりアーカイブ。2010年11月8日閲覧。
- cosine (2007年10月22日). “アザジラクチンの全合成”. 化学者のつぶやき -Chem-Station-. 2010年11月8日閲覧。
- Extoxnet
- Neem: The wonder tree
