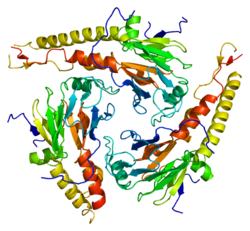
SMAD4
SMAD4(SMAD family member 4)は、全ての後生動物に存在する、高度に保存されたタンパク質である。転写因子のSMADファミリーに属し、TGF-βシグナル伝達の媒介因子として作用する。TGF-βファミリーのサイトカインは後生動物の生活環を通じて重要な過程を調節し、胚発生、組織の恒常性、再生、免疫調節に重要な役割を果たしている[5]。
SMAD4はco-SMAD(common mediator SMAD)と呼ばれるグループに属する。大部分の後生動物において、SMAD4は既知の唯一のco-SMADである。哺乳類のSMAD4は、Medeaと呼ばれるショウジョウバエタンパク質のホモログである[6]。
SMAD4は、SMAD2、SMAD3、SMAD1、SMAD5、SMAD9(SMAD8とも呼ばれる)などのR-SMAD(receptor-regulated SMAD)と相互作用し、ヘテロ三量体型複合体を形成する。核内に移行すると、SMAD4と2分子のR-SMADからなる複合体はDNAに結合し、細胞の状況に依存してさまざまな遺伝子の発現を調節する[6]。SMAD4が関与する細胞内の反応は、TGF-βファミリーの成長因子が細胞表面受容体に結合することで開始される。SMADが関与する一連の細胞内反応はSMAD経路、もしくは細胞がTGF-βを認識することで開始されるためTGF-β経路と呼ばれる。
遺伝子
[編集]ヒトでは、SMAD4遺伝子は18番染色体のq21.1領域に位置する[7][8]。

タンパク質
[編集]SMAD4は552アミノ酸、60,439 Daからなるポリペプチドである。SMAD4はMH1、MH2と呼ばれる2つの機能ドメインから構成される。
2分子のSMAD3(もしくは2分子のSMAD2)と1分子のSMAD4からなる複合体は、MH1ドメインの相互作用を介してDNAに直接結合する。これらの複合体は、状況依存的なTGF-βの作用の決定を担う系統決定的転写因子(lineage-defining transcription factors、LDTF)によって、ゲノム中の結合部位へリクルートされる。SMADタンパク質のDNA結合特異性に関する初期の知見はオリゴヌクレオチド結合スクリーニングから得られたもので、SMAD3とSMAD4のMH1ドメインの高親和性結合配列として、5'–GTCTAGAC–3'回文配列が同定されている[9]。プロモーターやエンハンサー領域には他のモチーフも同定されている。そうした部位としてはCAGCCモチーフやGGC(GC)|(CG)コンセンサス配列があり、後者は5GC部位とも呼ばれている[10]。5GCモチーフはゲノム中のSMAD結合領域にクラスターとして高度に密集して存在している。SMAD3/SMAD4複合体はTPA応答エレメント(TPA-responsive element)にも結合し、このエレメントにはTGAGTCAGモチーフが含まれる[11]。
構造
[編集]MH1ドメインとDNAとの複合体
[編集]最初に解かれたDNA結合型SMAD4の構造は、回文配列であるGTCTAGACモチーフとの複合体である[12]。SMAD4のMH1ドメインが数種類のの5GCモチーフに結合した構造も決定されている。全ての複合体において、DNAとの相互作用にはMH1ドメインに存在する保存されたβヘアピンが関与している。ヘアピン構造の一部は溶液中では柔軟であり、そのコンフォメーションの高度な柔軟性によってさまざまな5塩基対配列の認識が可能となっている。GC部位との効率的な相互作用はGヌクレオチドが主溝の深部に位置している場合にのみ行われ、Arg81のグアニジニウム基との水素結合が確立される。この相互作用は、SMADのDNA結合ヘアピンとDNAの主溝との相補的な表面接触を促進する。他の直接的相互作用にはLys88とGln83が関与している。センモウヒラムシTrichoplax adhaerensのSMAD4のMH1ドメインがGGCGCモチーフに結合した複合体のX線結晶構造は、後生動物を通じてこの相互作用が高度に保存されていることを示している[10]。



MH2ドメインの複合体
[編集]C末端に位置するMH2ドメインは、受容体の認識と他のSMADとの結合を担う。SMAD4のMH2ドメインはR-SMADのMH2ドメインと相互作用し、ヘテロ二量体やヘテロ三量体を形成する。一部の腫瘍で検出されるSMAD4変異体では、MH1ドメインとMH2ドメインとの間の相互作用が亢進している[13]。
機能と作用機序
[編集]SMAD4はSMAD経路(TGF-β経路)に必要不可欠なエフェクタータンパク質である。SMAD4はTGF-βファミリーの細胞外成長因子とと細胞核内の遺伝子との間の媒介因子として機能する。SMAD4はco-SMADに分類されるSMADであり、"co"とは"common mediator"の略である。
TGF-β経路においては、TGF-β二量体はII型受容体と呼ばれる細胞表面膜貫通受容体によって認識される。TGF-βの結合によってII型受容体が活性化されると、II型受容体はI型受容体をリン酸化する。I型受容体も細胞表面受容体であり、この受容体はSMAD2やSMAD3などの細胞内のR-SMAD(receptor-regulated SMAD)をリン酸化する。そしてリン酸化されたR-SMADはSMAD4に結合する。このR-SMAD/SMAD4ヘテロ複合体は細胞質から核へ移行する。SMAD4とR-SMADはヘテロ三量体、ヘテロ六量体、ヘテロ二量体を形成する可能性がある。
SMAD4はERK/MAPK[14]とGSK3[15]の基質である。FGF経路の刺激は古典的MAPKであるERKによるSMAD4のThr277のリン酸化を引き起こす。このリン酸化はSMAD4の活性に対して2つの意味を持つ。まず、このリン酸化はSMAD4のリンカー領域に位置する成長因子調節転写活性化ドメインであるSAD(Smad activation domain)を活性化し、SMAD4の転写活性を最大化する[16]。また、MAPKによるSMAD4のリン酸化はGSK3によるリン酸化のためのプライミングとなり、これによって転写阻害が引き起こされるとともに、ユビキチンE3リガーゼであるβ-TrCPのドッキング部位となるホスホデグロン(phosphodegron)が作り出される。β-TrCPはSMAD4をポリユビキチン化し、プロテアソームによる分解の標的とする[17]。GSK3によるSMAD4のリン酸化は、膵臓がんや結腸がんのプログレッション時のタンパク質安定性を調節していることが提唱されている[18]。
核内では、SMADのヘテロ複合体はプロモーターに結合し、転写アクチベーターと相互作用する。SMAD3/SMAD4複合体はSMAD結合エレメント(Smad-binding DNA element、SBE)に直接結合することができる。こうした結合は弱く、遺伝子発現の調節にはAP-1ファミリーのメンバーやTFE3、FOXG1など他の転写因子を必要とする[19]。
臨床的意義
[編集]Smad4ノックアウトマウスでは、卵母細胞の発生時にホルモンや成長因子を分泌する顆粒膜細胞の早期の黄体化が生じ、卵胞刺激ホルモン受容体(FSHR)の発現レベルが低く、黄体形成ホルモン受容体(LHR)の発現レベルは高い。こうした変化の一因は、SMAD4シグナル伝達経路を利用するBMP7の機能不全によるものである可能性がある[20][21]。
SMAD1やSMAD5をコードする遺伝子の欠失もマウスでは転移性顆粒膜細胞腫と関連付けられている[22]。
SMAD4は多くのがんでしばしば変異が観察される。変異は遺伝性のものである場合も後天性のものである場合もある。遺伝性の場合には変異は体細胞と生殖器官の細胞の双方に影響を与え、後天的なものの場合には特定の体細胞でのみ影響がみられることとなる。SMAD4は全ての細胞で合成されているわけではなく、このタンパク質は皮膚、膵臓、結腸、子宮、上皮細胞に存在する。線維芽細胞でも産生される。機能的なSMAD4はTGF-βシグナル伝達経路の調節に関与し、この経路は上皮細胞の成長や細胞外マトリックスを負に調節する。SMAD4の構造が変化した場合、細胞成長に関与する遺伝子の発現は調節を受けなくなり、いかなる阻害も受けない細胞増殖が行われる場合がある。細胞分裂の増加は腫瘍形成、そしてmultiploid大腸癌や膵癌をもたらす。SMAD4は膵癌の少なくとも50%で不活性化されている[23]。
SMAD4は、常染色体優性遺伝疾患である若年性ポリポーシス症候群(JPS)においても変異が発見されている。JPSは消化管の過誤腫性ポリープによって特徴づけられる疾患である。こうしたポリープは通常は良性であるが、消化管がん、特に結腸がん発生のリスクが高くなる。JPSの原因となる約60種類の変異が同定されている。これらの変異は、R-SMADとの結合ならびにヘテロ複合体の形成が妨げられる、ドメインを欠く小さなタンパク質の産生と関連付けられている[8]。
SMAD4の変異(大部分は置換)は、希少遺伝疾患であるMyhre症候群の原因となる場合がある。この疾患は精神遅滞、低身長、特異な顔貌、骨のさまざまな異常によって特徴づけられる[24][25]。
出典
[編集]- ^ a b c GRCh38: Ensembl release 89: ENSG00000141646 - Ensembl, May 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000024515 - Ensembl, May 2017
- ^ Human PubMed Reference:
- ^ Mouse PubMed Reference:
- ^ Massagué, Joan (2012). “TGFβ signalling in context” (英語). Nature Reviews Molecular Cell Biology 13 (10): 616–630. doi:10.1038/nrm3434. ISSN 1471-0080. PMC 4027049. PMID 22992590.
- ^ a b Massagué, J. (1998). “TGF-β SIGNAL TRANSDUCTION”. Annual Review of Biochemistry 67 (1): 753–791. doi:10.1146/annurev.biochem.67.1.753. ISSN 0066-4154. PMID 9759503.
- ^ “SMAD4 SMAD family member 4”. Entrez Gene. 2022年8月7日閲覧。
- ^ a b “SMAD 4”. The Genetics Home Reference Website. 2022年8月7日閲覧。
- ^ “Human Smad3 and Smad4 are sequence-specific transcription activators”. Molecular Cell 1 (4): 611–617. (Mar 1998). doi:10.1016/s1097-2765(00)80061-1. PMID 9660945.
- ^ a b Martin-Malpartida, Pau; Batet, Marta; Kaczmarska, Zuzanna; Freier, Regina; Gomes, Tiago; Aragón, Eric; Zou, Yilong; Wang, Qiong et al. (2017-12-12). “Structural basis for genome wide recognition of 5-bp GC motifs by SMAD transcription factors” (英語). Nature Communications 8 (1): 2070. Bibcode: 2017NatCo...8.2070M. doi:10.1038/s41467-017-02054-6. ISSN 2041-1723. PMC 5727232. PMID 29234012.
- ^ Zhang, Ying; Feng, Xin-Hua; Derynck, Rik (1998). “Smad3 and Smad4 cooperate with c-Jun/c-Fos to mediate TGF-β-induced transcription”. Nature 394 (6696): 909–913. Bibcode: 1998Natur.394..909Z. doi:10.1038/29814. ISSN 0028-0836. PMID 9732876.
- ^ Baburajendran, Nithya; Jauch, Ralf; Tan, Clara Yueh Zhen; Narasimhan, Kamesh; Kolatkar, Prasanna R. (2011). “Structural basis for the cooperative DNA recognition by Smad4 MH1 dimers”. Nucleic Acids Research 39 (18): 8213–8222. doi:10.1093/nar/gkr500. ISSN 1362-4962. PMC 3185416. PMID 21724602.
- ^ Hata, Akiko; Lo, Roger S.; Wotton, David; Lagna, Giorgio; Massagué, Joan (1997). “Mutations increasing autoinhibition inactivate tumour suppressors Smad2 and Smad4”. Nature 388 (6637): 82–87. Bibcode: 1997Natur.388R..82H. doi:10.1038/40424. ISSN 0028-0836. PMID 9214507.
- ^ “Phosphorylation of threonine 276 in Smad4 is involved in transforming growth factor-beta-induced nuclear accumulation”. American Journal of Physiology. Cell Physiology 285 (4): C823–30. (Oct 2003). doi:10.1152/ajpcell.00053.2003. PMID 12801888.
- ^ “The tumor suppressor Smad4/DPC4 is regulated by phosphorylations that integrate FGF, Wnt, and TGF-β signaling”. Cell Reports 9 (2): 688–700. (Oct 2014). doi:10.1016/j.celrep.2014.09.020. PMID 25373906.
- ^ de Caestecker, Mark P. (2000). “The Smad4 Activation Domain (SAD) Is a Proline-rich, p300-dependent Transcriptional Activation Domain”. The Journal of Biological Chemistry 275 (3): 2115–2122. doi:10.1074/jbc.275.3.2115. PMID 10636916.
- ^ Demagny, Hadrien; De Robertis, Edward M. (2015). “Smad4/DPC4: a Barrier against Tumor Progression driven by RTK/Ras/Erk and Wnt/GSK3 signaling”. Molecular & Cellular Oncology 3 (2): e989133. doi:10.4161/23723556.2014.989133. PMC 4905428. PMID 27308623.
- ^ Demagny, Hadrien; De Robertis, Edward M. (2015). “Point Mutations in the Tumor Suppressor Smad4/DPC4 Enhance its Phosphorylation by GSK3 and Reversibly Inactivate TGF-β Signaling”. Molecular & Cellular Oncology 3 (1): e1025181. doi:10.1080/23723556.2015.1025181. PMC 4845174. PMID 27308538.
- ^ “Linking Smads and transcriptional activation”. The Biochemical Journal 386 (Pt 1): e1–e3. (Feb 2005). doi:10.1042/bj20042133. PMC 1134782. PMID 15702493.
- ^ “Bone morphogenetic protein 7 (BMP-7) increases the expression of follicle-stimulating hormone (FSH) receptor in human granulosa cells”. Fertility and Sterility 93 (4): 1273–9. (Mar 2010). doi:10.1016/j.fertnstert.2008.11.014. PMID 19108831.
- ^ “Premature luteinization and cumulus cell defects in ovarian-specific Smad4 knockout mice”. Molecular Endocrinology 20 (6): 1406–22. (Jun 2006). doi:10.1210/me.2005-0462. PMID 16513794.
- ^ “Smad1-Smad5 ovarian conditional knockout mice develop a disease profile similar to the juvenile form of human granulosa cell tumors”. Endocrinology 150 (12): 5208–17. (2009). doi:10.1210/en.2009-0644. PMC 2819741. PMID 19819941.
- ^ Cotran, Ramzi S.; Kumar, Vinay; Fausto, Nelson; Robbins, Stanley L.; Abbas, Abul K. (2005). Robbins and Cotran pathologic basis of disease (7th ed.). St. Louis, Mo: Elsevier Saunders. ISBN 0-7216-0187-1
- ^ “Growth-Mental Deficiency Syndrome of Myhre”. National Organization for rare disorders. 2022年8月14日閲覧。
- ^ “Novel SMAD4 mutation causing Myhre syndrome”. American Journal of Medical Genetics Part A 164A (7): 1835–40. (Jul 2014). doi:10.1002/ajmg.a.36544. PMID 24715504.
関連文献
[編集]- “TGF-beta signaling by Smad proteins”. Cytokine & Growth Factor Reviews 11 (1–2): 15–22. (2000). doi:10.1016/S1359-6101(99)00025-8. PMID 10708949.
- “The Smad pathway”. Cytokine & Growth Factor Reviews 11 (1–2): 5–13. (2000). doi:10.1016/S1359-6101(99)00024-6. PMID 10708948.
- “Remarkable versatility of Smad proteins in the nucleus of transforming growth factor-beta activated cells”. Cytokine & Growth Factor Reviews 10 (3–4): 187–99. (2000). doi:10.1016/S1359-6101(99)00012-X. PMID 10647776.
- “TGF-beta signal transduction”. Annual Review of Biochemistry 67: 753–91. (1998). doi:10.1146/annurev.biochem.67.1.753. PMID 9759503.
- “High-level inducible Smad4-reexpression in the cervical cancer cell line C4-II is associated with a gene expression profile that predicts a preferential role of Smad4 in extracellular matrix composition”. BMC Cancer 7: 209. (2008). doi:10.1186/1471-2407-7-209. PMC 2186346. PMID 17997817.
- “Mutant p53 attenuates the SMAD-dependent transforming growth factor beta1 (TGF-beta1) signaling pathway by repressing the expression of TGF-beta receptor type II”. Molecular and Cellular Biology 27 (23): 8228–42. (Dec 2007). doi:10.1128/MCB.00374-07. PMC 2169171. PMID 17875924.
- “High proportion of large genomic deletions and a genotype phenotype update in 80 unrelated families with juvenile polyposis syndrome”. Journal of Medical Genetics 44 (11): 702–9. (Nov 2007). doi:10.1136/jmg.2007.052506. PMC 2752176. PMID 17873119.
- “The utility of SMAD4 as a diagnostic immunohistochemical marker for pancreatic adenocarcinoma, and its expression in other solid tumors”. Diagnostic Cytopathology 35 (10): 644–8. (Oct 2007). doi:10.1002/dc.20715. PMID 17854080.
- “Common variants in the BMP2, BMP4, and HJV genes of the hepcidin regulation pathway modulate HFE hemochromatosis penetrance”. American Journal of Human Genetics 81 (4): 799–807. (Oct 2007). doi:10.1086/520001. PMC 2227929. PMID 17847004.
- “Evaluation of clinical relevance of examining K-ras, p16 and p53 mutations along with allelic losses at 9p and 18q in EUS-guided fine needle aspiration samples of patients with chronic pancreatitis and pancreatic cancer”. World Journal of Gastroenterology 13 (27): 3714–20. (Jul 2007). doi:10.3748/wjg.v13.i27.3714. PMC 4250643. PMID 17659731.
- “Smad4-independent, PP2A-dependent apoptotic effect of exogenous transforming growth factor beta 1 in lymphoma cells”. Experimental Cell Research 313 (15): 3167–74. (Sep 2007). doi:10.1016/j.yexcr.2007.05.028. PMID 17643425.
- “TGF-beta1 stimulates human AT1 receptor expression in lung fibroblasts by cross talk between the Smad, p38 MAPK, JNK, and PI3K signaling pathways”. American Journal of Physiology. Lung Cellular and Molecular Physiology 293 (3): L790–9. (Sep 2007). doi:10.1152/ajplung.00099.2007. PMC 2413071. PMID 17601799.
- “Arkadia activates Smad3/Smad4-dependent transcription by triggering signal-induced SnoN degradation”. Molecular and Cellular Biology 27 (17): 6068–83. (Sep 2007). doi:10.1128/MCB.00664-07. PMC 1952153. PMID 17591695.
- “Proinvasive activity of BMP-7 through SMAD4/src-independent and ERK/Rac/JNK-dependent signaling pathways in colon cancer cells”. Cellular Signalling 19 (8): 1722–32. (Aug 2007). doi:10.1016/j.cellsig.2007.03.008. PMID 17478078.
- “Involvement of deterioration in S100C/A11-mediated pathway in resistance of human squamous cancer cell lines to TGFbeta-induced growth suppression”. Journal of Molecular Medicine 85 (7): 753–62. (Jul 2007). doi:10.1007/s00109-007-0180-7. PMID 17476473.
- “The expression of S100A8 in pancreatic cancer-associated monocytes is associated with the Smad4 status of pancreatic cancer cells”. Proteomics 7 (11): 1929–40. (Jun 2007). doi:10.1002/pmic.200700072. PMID 17469085.
- “K-ras and Dpc4 mutations in chronic pancreatitis: case series”. Croatian Medical Journal 48 (2): 218–24. (Apr 2007). PMC 2080529. PMID 17436386.
- “Loss of Smad4 expression predicts liver metastasis in human colorectal cancer”. Oncology Reports 17 (5): 1095–9. (May 2007). doi:10.3892/or.17.5.1095. PMID 17390050.
- “Smad4 is critical for self-renewal of hematopoietic stem cells”. The Journal of Experimental Medicine 204 (3): 467–74. (Mar 2007). doi:10.1084/jem.20060465. PMC 2137898. PMID 17353364.
- “Smad4 is essential for down-regulation of E-cadherin induced by TGF-beta in pancreatic cancer cell line PANC-1”. Journal of Biochemistry 141 (3): 345–51. (Mar 2007). doi:10.1093/jb/mvm039. PMID 17301079.