Dicer
Dicerは、ヒトではDICER1遺伝子によってコードされる酵素である。DicerはRNase IIIファミリーに属し、二本鎖RNA(dsRNA)とpre-miRNAをそれぞれsiRNA、miRNAと呼ばれる短いdsRNA断片へと切断する。これらの断片は約20–25塩基対の長さであり、3'末端に2塩基のオーバーハングが存在する。DicerはRNAiに必要不可欠なRNA誘導サイレンシング複合体(RISC)の活性化を促進する。RISCは触媒を担う構成要素としてArgonauteを持ち、ArgonauteはmRNAを分解するエンドヌクレアーゼである。
発見
[編集]Dicerは、コールド・スプリング・ハーバー研究所のグレゴリー・ハノンの研究室で研究を行っていた、ニューヨーク州立大学ストーニーブルック校の博士課程の学生Emily Bernsteinによって2001年に命名された。Bernsteinは、dsRNAから低分子RNA断片の生成を担う酵素を発見しようとしていた。Dicerが約22ヌクレオチドのRNA断片を生成する能力は、dsRNAのトランスフェクションによってRNAi経路を開始した後のRISC酵素複合体からDicerを分離することで発見された。この実験では、RISCが低分子ヌクレオチド断片の生成を担っているわけではないことが示された。その後、RNase IIIファミリーの酵素のRNA断片形成能力を試験することで目的の酵素の候補はショウジョウバエのCG4792へと絞り込まれ、このタンパク質が現在Dicerと呼ばれているものである[5]。
Dicerのオルソログは他の多くの生物に存在する[6]。ヒメツリガネゴケPhyscomitrella patensでは、4種類のDICERタンパク質のうちの1つであるDCL1bはmiRNAの生合成ではなく、miRNAの標的転写産物の切断(dicing)に関与している。ここから新たな遺伝子発現調節機構である、miRNAによる遺伝子のエピジェネティックなサイレンシングが発見された[7]。
最初に構造生物学的解析がなされたDicerは原生生物のジアルジアGiardia intestinalis由来のものであり、PAZドメインと2つのRNase IIIドメインがX線結晶構造解析によって解かれた。このタンパク質のサイズは82 kDaであるが、他の生物のDicerはもっと大きく、例えばヒトでは219 kDaである。ヒトとG. intestinalisのDicerのサイズの違いは、ヒトのDicerには少なくとも5つの異なるドメインが存在するためである。これらのドメインはDicerの活性の調節、dsRNAのプロセシング、RNAiに関係するタンパク質の機能に重要である[8]。
機能的ドメイン
[編集]
ヒトのDicer(hsDicer、DICER1)はRNase IIIファミリーに分類され、ヘリカーゼドメイン、PAZ(Piwi/Argonaute/Zwille)ドメイン、2つのRNase IIIドメイン、2つの二本鎖RNA結合ドメイン(DUF283、dsRBD)を持つ[8][10][11][12]。
現在の研究では、PAZドメインがdsRNAの3'側の2ヌクレオチドのオーバーハングに結合し、RNase III触媒ドメインがdsRNAの周囲に擬二量体を形成することで鎖の切断が開始されるとされている。その結果、dsRNA鎖の切断による短縮が機能的に行われる。PAZドメインとRNase IIIドメインの距離はコネクターヘリックスの角度によって決定され、その角度によってmiRNA産物の長さに影響が生じる[9]。dsRBDはdsRNAに結合するが、このドメイン中の特異的な結合部位は決定されていない。このドメインは他の調節タンパク質(ヒトではTRBP、ショウジョウバエではR2D2、Loqs)との複合体の一部として機能し、RNase IIIドメインを効果的に配置して低分子RNA産物の特異性を制御している可能性がある[13]。ヘリカーゼドメインは長い基質のプロセシングに関与していると考えられている[13]。
RNAiにおける役割
[編集]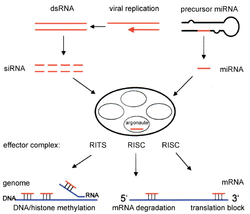
miRNA
[編集]RNAiは、RNA分子をmiRNAへプロセシングし、宿主のmRNA配列特異的に遺伝子発現を阻害する過程である。miRNAの産生は、まず核内のpri-miRNA(primary miRNA)から開始され、長いpri-miRNAはより小さな前駆体であるpre-miRNA(precursor miRNA)へと切断される。pri-miRNAはDGCR8によって認識され、Droshaによって切断されてpre-miRNAが形成される。この過程は核内で行われる。pre-mRNAは約70ヌクレオチドからなり、ヘアピン構造を持つ。その後、pre-miRNAは細胞質へ輸送され、そこでDicerによって切断されて成熟したmiRNAが形成される[15]。
siRNA
[編集]siRNAはmiRNAと同じような方法で、dsRNAがDicerによって長さ21–23ヌクレオチドの小さな断片へと切断されることで形成され、機能する[13]。siRNAはRISCを活性化し、RISCは相補的な標的mRNAを探してRNAを切断する[16]。その結果、RNAiの過程によって特定の遺伝子がサイレンシングされる[17]。siRNAは一般的にmRNA配列特異的であるのに対し、miRNAはmRNAの配列に対して完全に相補的ではないという点で、両者は異なる。miRNAは類似した配列を持つ複数の標的と相互作用し、翻訳を阻害することができる[18]。一般的にRNAiはヒトなどの生体内の正常な過程に必要不可欠なものであり、がんを標的とした診断・治療ツールとしての研究が行われている[15]。

疾患
[編集]黄斑変性
[編集]加齢に伴う黄斑変性は、先進国における失明の主要な要因である。この疾患におけるDicerの役割は、この疾患の患者の網膜色素上皮(RPE)においてDicerのレベルが低下していることが発見されたことから明らかとなった。RPEでのみDicerを欠失させたノックアウトマウスでは、この疾患と類似した症状がみられる。しかしながら、DroshaやPashaなど、RNAi経路に重要な他のタンパク質を欠失したマウスでは、Dicerノックアウトマウスのような黄斑変性の症状はみられない。このことは、Dicerの網膜の健康に対する役割は、si/miRNAの形成機能とは異なる、RNAi経路とは独立したものであることを示唆している。Dicerが不十分な患者では、Alu RNA(Aluエレメントの転写産物)と呼ばれるRNAが増加していることが判明している。こうしたノンコーディングRNAはループを形成してdsRNA構造をとり、健康な網膜ではDicerによって分解される。しかしながら、Dicerレベルが低下するとAlu RNAは蓄積し、炎症の結果RPEの変性が引き起こされる[19][20]。
がん
[編集]悪性腫瘍におけるmiRNAの発現プロファイルの変化は、がんの発生や予後に対するmiRNA、ひいてはDicerの役割の重要性を示唆している。miRNAはがん抑制因子として機能する場合もあり、そのため発現の変化は発がんに至る可能性がある[21]。肺がんや卵巣がんの解析からは、患者の予後の悪さや生存時間の短さはDicerやDroshaの発現の低下と相関していることが示されている。DicerのmRNAレベルの低下は、腫瘍のステージの進行と相関している。しかしながら、前立腺がん[22]や食道がんなど他のがんでは、Dicerの発現の高さが患者の予後の悪さと相関していることが示されている。こうしたがんの種類による相違は、Dicerが関与するRNAi調節過程が腫瘍の種類によって異なることを示唆している[15]。
DicerはDNA修復にも関与している。Dicerの発現が低下した哺乳類細胞では、DNA損傷修復などの機構の効率の低下の結果、DNA損傷が増加する。例えば、二本鎖切断に由来するsiRNA(Dicerによって形成される)は二本鎖切断修復機構に関与するタンパク質複合体のガイドとして機能する可能性があり、またクロマチン修飾を指示する場合もある。また、電離放射線や紫外線によるDNA損傷の結果、miRNAの発現パターンは変化する。RNAi機構はトランスポゾンのサイレンシングを担い、Dicerがノックアウトまたはノックダウンされた場合などのように、その機構が存在しない場合には、DNA損傷の原因となるトランスポゾンの活性化につながる可能性がある。DNA損傷が蓄積すると、発がん性変異を持つ細胞が出現し、腫瘍が形成される可能性がある[15]。
ウイルスの病原性
[編集]RNAウイルスの感染はRNAiカスケードの引き金となる場合がある。植物細胞や動物細胞に感染するウイルスにはRNAi応答を阻害するように作られたタンパク質が含まれており、Dicerはウイルスに対する免疫に関与している可能性が高い。ヒトに感染するウイルスでは、HIV-1、インフルエンザウイルス、ワクシニアウイルスなどがこうしたRNAi抑制タンパク質をコードしている。DicerはウイルスのdsRNAを切断してRISCにロードし、ウイルスmRNAを標的とした分解を引き起こすことで感染に対抗することができるため、Dicerの阻害はウイルスにとって有益である。Dicerの遮断による細胞のmiRNA経路の阻害も、ウイルスの病原性に寄与しうる機構である[23]。
昆虫
[編集]昆虫はDicerを強力な抗ウイルスタンパク質として利用する。ウエストナイルウイルス、デングウイルス、黄熱ウイルスなど、命に関わる可能性のあるアルボウイルスを含む多くのウイルス性疾患の伝染をカ(蚊)が担っていることを考えると、このことは特に重要である[24]。カ、より具体的にはネッタイシマカAedes aegyptiは、これらのウイルスの媒介者ではあるが、意図的にウイルスの宿主となっているわけではない。感染は、メスのカが卵を育てるために脊椎動物の血液を必要とすることから起こる。昆虫のRNAi経路は、他の動物のものと非常に類似している。Dicer-2はウイルスRNAを切断してRISC複合体にロードし、一方の鎖はRNAi産物の鋳型となり、もう一方の鎖は分解される。RNAi経路の構成要素が機能しなくなる変異を持つ昆虫は、自身が運搬するウイルスの量が増えたり、自身が宿主となるウイルスに対する感受性が高くなったりすることが知られている。ヒトのウイルスと同様に、昆虫のウイルスもRNAi経路を回避する機構を進化させている。例えば、ショウジョウバエCウイルスはdsRNAに結合するタンパク質1Aをコードしており、Dicerによる切断やRISCへのローディングから保護している。タバコガアスコウイルス3aはDicerのRNase IIIドメインに類似したRNase III酵素をコードしており、dsRNA基質を競合したり、siRNA二本鎖を分解してRISCへのローディングを防いだりしている可能性がある[25]。
診断・治療への応用
[編集]Dicerの発現レベルは、体内に腫瘍が存在するかどうかの特定に利用することができる。がんを持つ多くの患者ではDicerの発現レベルが低下していることが研究で示されている。その研究では、Dicerの発現の低下は患者の生存期間の減少と相関していることが示されている[15]。診断ツールとしてだけでなく、Dicerは遺伝子サイレンシングを目的とした外因性siRNAの静脈注入による治療にも利用される[26]。
マウスなどの哺乳類では、siRNAは2通りの方法でのデリバリーが示されている。1つは系へ直接注入する方法で、これにはDicerの機能は必要ない。もう1つの方法は、shRNA(short hairpin RNA)をコードするプラスミドを介して導入する方法であり、shRNAはDicerによって切断されてsiRNAとなる[27]。
現在用いられている抗体や低分子阻害剤などと比較して、治療を目的としたsiRNAの産生にDicerを利用する利点は、標的に対する特異性が高くまた多様である点である。一般に、低分子阻害剤は特異性の点で問題があり、耐え難い副作用を伴う。抗体はsiRNAと同様に特異的であるが、その対象はリガンドや細胞表面受容体に限定される。一方、siRNAの注入の主な障害は細胞内への取り込み効率の低さである[15]。注入されたsiRNAは血中での安定性が低く、非特異的免疫を刺激する[28]。治療目的でのmiRNAの産生は、miRNAのmRNAへの結合には6–8ヌクレオチドの対合で十分であるため、特異性に欠ける[29]。
Dicer様タンパク質
[編集]植物のゲノムには、動物や昆虫のDicerと類似した機能とドメインを持つDicer様タンパク質がコードされている。例えば、モデル生物であるシロイヌナズナArabidopsis thalianaでは、4種類のDicer様タンパク質が合成されており、DCL1からDCL4と命名されている。DCL1はmiRNAの生成と逆向き反復配列からのsRNAの産生に関与している。DCL2はシスに作用するアンチセンス転写産物からsiRNAを作り出し、ウイルスに対する免疫と防御を補助する。DCL3はクロマチン修飾を補助するsiRNAを生成し、DCL4はトランス作用性siRNA(tasiRNA)の代謝と転写後段階での転写産物のサイレンシングに関与している。さらに、DCL1とDCL3は開花に重要である。シロイヌナズナでは、これらDCLのノックアウトが発生に大きな問題を引き起こすことはない。
イネやブドウもDCLタンパク質を産生し、Dicerの機構は多くの生物に共通した防御戦略となっている。イネは他の機能も持つ5種類のDCLを産生しており、シロイヌナズナの場合よりも機能と発生の面で重要な役割を果たしている。さらに、イネでは細胞の種類によってDCLの発現パターンが異なるのに対し、シロイヌナズナではより均質である。イネのDCLの発現は、渇水、塩分、寒さなどの生物学的ストレスの影響を受け、そのためこうしたストレス因子は植物のウイルス耐性を低下させる可能性がある。シロイヌナズナとは異なり、イネではDCLタンパク質の機能喪失は発生上の欠陥を引き起こす[30]。
出典
[編集]- ^ a b c GRCh38: Ensembl release 89: ENSG00000100697 - Ensembl, May 2017
- ^ a b c GRCm38: Ensembl release 89: ENSMUSG00000041415 - Ensembl, May 2017
- ^ Human PubMed Reference:
- ^ Mouse PubMed Reference:
- ^ Bernstein, E.; Caudy, A. A.; Hammond, S. M.; Hannon, G. J. (2001-01-18). “Role for a bidentate ribonuclease in the initiation step of RNA interference”. Nature 409 (6818): 363–366. doi:10.1038/35053110. ISSN 0028-0836. PMID 11201747.
- ^ “Role of Dicer in posttranscriptional RNA silencing”. Current Topics in Microbiology and Immunology 320: 77–97. (2008). doi:10.1007/978-3-540-75157-1_4. ISBN 978-3-540-75156-4. PMID 18268840.
- ^ “Transcriptional control of gene expression by microRNAs”. Cell 140 (1): 111–22. (Jan 2010). doi:10.1016/j.cell.2009.12.023. PMID 20085706.
- ^ a b “Structure of the human Dicer-TRBP complex by electron microscopy”. Structure 17 (10): 1326–32. (Oct 2009). doi:10.1016/j.str.2009.08.013. PMC 2880462. PMID 19836333.
- ^ a b “Structural basis for double-stranded RNA processing by Dicer”. Science 311 (5758): 195–8. (Jan 2006). Bibcode: 2006Sci...311..195M. doi:10.1126/science.1121638. PMID 16410517.
- ^ “Entrez Gene: DICER1 Dicer1, Dcr-1 homolog (Drosophila)”. 2022年1月24日閲覧。
- ^ “Molecular cloning and characterization of a novel human gene (HERNA) which encodes a putative RNA-helicase”. Biochimica et Biophysica Acta (BBA) - Gene Structure and Expression 1490 (1–2): 163–9. (Jan 2000). doi:10.1016/S0167-4781(99)00221-3. PMID 10786632.
- ^ “Dicing and slicing: the core machinery of the RNA interference pathway”. FEBS Letters 579 (26): 5822–9. (Oct 2005). doi:10.1016/j.febslet.2005.08.079. PMID 16214139.
- ^ a b c “Phosphate and R2D2 restrict the substrate specificity of Dicer-2, an ATP-driven ribonuclease”. Molecular Cell 42 (2): 172–84. (Apr 2011). doi:10.1016/j.molcel.2011.03.002. PMC 3115569. PMID 21419681.
- ^ “An RNA-directed nuclease mediates post-transcriptional gene silencing in Drosophila cells”. Nature 404 (6775): 293–6. (Mar 2000). Bibcode: 2000Natur.404..293H. doi:10.1038/35005107. PMID 10749213.
- ^ a b c d e f “The dicey role of Dicer: implications for RNAi therapy”. Cancer Research 70 (7): 2571–4. (Apr 2010). doi:10.1158/0008-5472.CAN-09-2536. PMC 3170915. PMID 20179193.
- ^ “The contributions of dsRNA structure to Dicer specificity and efficiency”. RNA 11 (5): 674–82. (May 2005). doi:10.1261/rna.7272305. PMC 1370754. PMID 15811921.
- ^ Watson JD (2008). Molecular Biology of the Gene. San Francisco, CA: Cold Spring Harbor Laboratory Press. pp. 641–648. ISBN 978-0-8053-9592-1
- ^ “MicroRNAs and small interfering RNAs can inhibit mRNA expression by similar mechanisms”. Proceedings of the National Academy of Sciences of the United States of America 100 (17): 9779–84. (Aug 2003). Bibcode: 2003PNAS..100.9779Z. doi:10.1073/pnas.1630797100. PMC 187842. PMID 12902540.
- ^ “Vision: Dicer leaps into view”. Nature 471 (7338): 308–9. (Mar 2011). Bibcode: 2011Natur.471..308M. doi:10.1038/471308a. PMID 21412326.
- ^ “DICER1 loss and Alu RNA induce age-related macular degeneration via the NLRP3 inflammasome and MyD88”. Cell 149 (4): 847–59. (May 2012). doi:10.1016/j.cell.2012.03.036. PMC 3351582. PMID 22541070.
- ^ “The role of dicer in DNA damage repair”. International Journal of Molecular Sciences 13 (12): 16769–78. (2012). doi:10.3390/ijms131216769. PMC 3546719. PMID 23222681.
- ^ “Up-regulation of dicer, a component of the MicroRNA machinery, in prostate adenocarcinoma”. The American Journal of Pathology 169 (5): 1812–20. (Nov 2006). doi:10.2353/ajpath.2006.060480. PMC 1780192. PMID 17071602.
- ^ “The interplay between virus infection and the cellular RNA interference machinery”. FEBS Letters 580 (12): 2896–902. (May 2006). doi:10.1016/j.febslet.2006.02.070. PMC 7094296. PMID 16563388.
- ^ “Mosquito-borne Diseases”. National Center for Infections Disease, Center for Disease Control and Prevention. 31 January 2014時点のオリジナルよりアーカイブ。22 April 2014閲覧。
- ^ “The long and short of antiviral defense: small RNA-based immunity in insects”. Current Opinion in Virology 7: 19–28. (Aug 2014). doi:10.1016/j.coviro.2014.03.010. PMID 24732439.
- ^ “Intravenous injection of siRNA directed against hypoxia-inducible factors prolongs survival in a Lewis lung carcinoma cancer model”. Cancer Gene Therapy 16 (3): 195–205. (Mar 2009). doi:10.1038/cgt.2008.71. PMID 18818708.
- ^ “Gene silencing by RNA interference is being used routinely to study gene function in cultured mammalian cells”. Life Technologies. 23 April 2014閲覧。
- ^ “Cancer siRNA therapy by tumor selective delivery with ligand-targeted sterically stabilized nanoparticle”. Nucleic Acids Research 32 (19): e149. (2004). doi:10.1093/nar/gnh140. PMC 528817. PMID 15520458.
- ^ “Argonaute HITS-CLIP decodes microRNA-mRNA interaction maps”. Nature 460 (7254): 479–86. (Jul 2009). Bibcode: 2009Natur.460..479C. doi:10.1038/nature08170. PMC 2733940. PMID 19536157.
- ^ “Dicer-like (DCL) proteins in plants”. Functional & Integrative Genomics 9 (3): 277–86. (Aug 2009). doi:10.1007/s10142-009-0111-5. PMID 19221817.