「ホパノイド」の版間の差分
| (6人の利用者による、間の10版が非表示) | |||
| 1行目: | 1行目: | ||
[[ファイル: |
[[ファイル:Hopene.svg|thumb|ホパノイド化合物であるジプロプテン]] |
||
[[ファイル:Cholesterol |
[[ファイル:Cholesterol.svg|thumb|ステロール化合物であるコレステロール]] |
||
'''ホパノイド''' (Hopanoids) は[[ホパン]]骨格を持つ天然の五環式化合物である。 |
'''ホパノイド''' (Hopanoids) は[[トリテルペノイド]]の中で、[[ホパン]]骨格を持つ天然の五環式化合物である。最初に報告されたホパノイドはヒドロキシホパノンで、[[ナショナル・ギャラリー (ロンドン)|ナショナル・ギャラリー]]の2人の化学者が絵画のニスとして用いられる[[ダンマル樹脂]]の研究中に単離したものである<ref>{{Cite journal|last=Mills|first=J. S.|last2=Werner|first2=A. E. A.|date=1955|title=The chemistry of dammar resin|url=http://xlink.rsc.org/?DOI=jr9550003132|journal=Journal of the Chemical Society (Resumed)|pages=3132|language=en|doi=10.1039/jr9550003132|issn=0368-1769}}</ref>。ホパンという名は、この樹脂が得られる[[フタバガキ科]]の{{Snamei||Hopea}}属から取られた(属名は植物学者[[ジョン・ホープ (植物学者)|ジョン・ホープ]]に由来する)。ホパノイドは一部の陸上植物や菌類などの真核生物からも見つかっているが、[[細菌]]により広く分布していることが現在では知られている<ref name=":0">{{Cite journal|last=Volkman|first=John K.|date=2005-02|title=Sterols and other triterpenoids: source specificity and evolution of biosynthetic pathways|url=https://linkinghub.elsevier.com/retrieve/pii/S0146638004001615|journal=Organic Geochemistry|volume=36|issue=2|pages=139–159|language=en|doi=10.1016/j.orggeochem.2004.06.013}}</ref>。真核生物内では構造的に類似した[[ステロイド]](例えば[[コレステロール]])の方が広く分布しており、ホパノイドの分布は限定的である。ホパノイドは地中で分解されにくいため、砂礫中や[[石油貯留層]]から様々な種類のものが発見されており、過去の地球の歴史においてバクテリアの存在およびその種類を示す[[:en:Biomarker_(petroleum)|バイオマーカー]]として広く用いられている<ref>{{cite journal|last1=Hunt|first1=John M.|last2=Philp|first2=R.Paul|last3=Kvenvolden|first3=Keith A.|title=Early developments in petroleum geochemistry|journal=Organic Geochemistry|volume=33|issue=9|year=2002|pages=1025–1052|issn=01466380|doi=10.1016/S0146-6380(02)00056-6}}</ref>。[[古細菌]]からは発見されていない<ref>{{cite web | author = William W. Christie | title = The AOCS Lipid Library. Sterols 4. Hopanoids and related lipids | url = http://lipidlibrary.aocs.org/lipids/hopanoids/index.htm | publisher = AOCS |accessdate=2015-02-09}}</ref><ref>{{cite book | author = Larry L Barton | title = Structural and Functional Relationships in Prokaryotes | publisher = Springer | year = 2005 | isbn = 0-387-20708-2}}</ref>。 |
||
== 機能 == |
== 機能 == |
||
シーケンシングが行われた細菌[[ゲノム]]の約10%には、ホパノイド合成酵素である{{仮リンク|スクアレンホペンシクラーゼ|en|Squalene-hopene cyclase|label=}}をコードすると推定される遺伝子が存在している。ホパノイドの生理機能についてはいまだ明確ではないものの、[[細胞膜]]中に存在し細胞を保護する役目を果たしていると推測されている。一部の生物では極限環境への適応を可能にしている<ref name=":1">{{Cite journal|last=Fischer|first=W. W.|last2=Summons|first2=R. E.|last3=Pearson|first3=A.|date=2005-01|title=Targeted genomic detection of biosynthetic pathways: anaerobic production of hopanoid biomarkers by a common sedimentary microbe|url=http://doi.wiley.com/10.1111/j.1472-4669.2005.00041.x|journal=Geobiology|volume=3|issue=1|pages=33–40|language=en|doi=10.1111/j.1472-4669.2005.00041.x|issn=1472-4677}}</ref>。 |
|||
ホパノイドは細菌の[[細胞膜]]において、[[脂質ラフト]]の形成のほか、細胞膜透過性・剛性・流動性など様々な性質を調整している。[[真核生物]]では、[[ステロール]]が似たような機能を担っている<ref name="saenz">{{Cite journal | last1 = Sáenz | first1 = JP. | last2 = Sezgin | first2 = E. | last3 = Schwille | first3 = P. | last4 = Simons | first4 = K. | title = Functional convergence of hopanoids and sterols in membrane ordering. | journal = Proc Natl Acad Sci U S A | volume = 109 | issue = 35 | pages = 14236–40 | month = Aug | year = 2012 | doi = 10.1073/pnas.1212141109 | pmid = 22893685 }}</ref>。この生化学構造と細胞機能の関係は、細菌の細胞膜で見られるホパノイド化合物である[[ジプロプテン]]と真核生物の細胞膜で見られるステロール化合物である[[コレステロール]]の構造の類似性に見ることができる<ref name="saenz" />。多くの細菌でホパノイドは、細胞膜の透過性を調整し、極端な環境条件に適応させるのに重要な役割を果たしている。土壌細菌[[ストレプトマイセス属]]の空気中の[[菌糸]]では、細胞膜から空気中への水の損失を最小限にしていると考えられている<ref name=Poralla_2000>{{cite journal | author = Poralla K, Muth G, Härtner T | title = Hopanoids are formed during transition from substrate to aerial hyphae in Streptomyces coelicolor A3(2) | journal = FEMS Microbiol Lett | volume = 189 | issue = 1 | pages = 93–5 | year = 2000 | pmid = 10913872 | doi = 10.1111/j.1574-6968.2000.tb09212.x}}</ref>。[[フランキア属]]細菌において[[窒素固定]]を行う diazovesicle という器官では、[[脂質二重層]]をより引き締め、酸素を透過しにくくすると考えられている<ref name=Berry_1993>{{cite journal | author = Berry A, Harriott O, Moreau R, Osman S, Benson D, Jones A | title = Hopanoid lipids compose the ''Frankia'' vesicle envelope, presumptive barrier of oxygen diffusion to nitrogenase | journal = Proc Natl Acad Sci USA | volume = 90 | issue = 13 | pages = 6091–4 | year = 1993 | pmid = 11607408 | doi = 10.1073/pnas.90.13.6091 | pmc = 46873|bibcode = 1993PNAS...90.6091B }}</ref>。 |
|||
ホパノイドは細菌の[[細胞膜]]において、[[脂質ラフト]]の形成のほか、細胞膜透過性・剛性・流動性など様々な性質を調整していると推定される。[[真核生物]]では[[ステロール]]が同等の機能を担っている<ref name="saenz">{{Cite journal|last1=Sáenz|first1=JP.|last2=Sezgin|first2=E.|last3=Schwille|first3=P.|last4=Simons|first4=K.|month=Aug|year=2012|title=Functional convergence of hopanoids and sterols in membrane ordering.|journal=Proc Natl Acad Sci U S A|volume=109|issue=35|pages=14236–40|doi=10.1073/pnas.1212141109|pmid=22893685}}</ref>。ホパノイドとステロールの機能の類似性は、細菌の細胞膜でよく見られるホパノイドである[[ジプロプテン]]と、動物の細胞膜に普遍的に存在するステロールである[[コレステロール]]の構造の類似性に見ることができる<ref name="saenz" />。ホパノイドはステロールの欠乏を完全に補うことはできないようであるが、ステロール同様、膜を凝縮させ透過性を低下させる<ref name=":2">{{Cite journal|last=Belin|first=Brittany J.|last2=Busset|first2=Nicolas|last3=Giraud|first3=Eric|last4=Molinaro|first4=Antonio|last5=Silipo|first5=Alba|last6=Newman|first6=Dianne K.|date=05 2018|title=Hopanoid lipids: from membranes to plant-bacteria interactions|url=https://www.ncbi.nlm.nih.gov/pubmed/29456243|journal=Nature Reviews. Microbiology|volume=16|issue=5|pages=304–315|doi=10.1038/nrmicro.2017.173|issn=1740-1534|pmid=29456243|pmc=6087623}}</ref>。また、一部の[[ガンマプロテオバクテリア綱|ガンマプロテオバクテリア]]や、[[地衣類]]や[[コケ植物]]などの真核生物ではステロールとホパノイドの双方を産生することが示されており、両者はそれぞれ異なる機能を担っている可能性が示唆される<ref name=":0" /><ref>{{Cite journal|last=Tippelt|first=A.|last2=Jahnke|first2=L.|last3=Poralla|first3=K.|date=1998-03-30|title=Squalene-hopene cyclase from Methylococcus capsulatus (Bath): a bacterium producing hopanoids and steroids|url=https://www.ncbi.nlm.nih.gov/pubmed/9555026|journal=Biochimica Et Biophysica Acta|volume=1391|issue=2|pages=223–232|doi=10.1016/s0005-2760(97)00212-9|issn=0006-3002|pmid=9555026}}</ref>。ホパノイドが細胞膜に詰め込まれる方法は、どのような官能基が付加されているかによって変化する。バクテリオホパンテトロール(bacteriohopanetetrol)は[[脂質二重層]]中で直立して存在していると推測されるが、ジプロプテンは内側と外側の層の間に局在し、膜を厚くして透過性を低下させていると推測される<ref>{{Cite journal|last=Poger|first=David|last2=Mark|first2=Alan E.|date=2013-12-19|title=The relative effect of sterols and hopanoids on lipid bilayers: when comparable is not identical|url=https://www.ncbi.nlm.nih.gov/pubmed/24299489|journal=The Journal of Physical Chemistry. B|volume=117|issue=50|pages=16129–16140|doi=10.1021/jp409748d|issn=1520-5207|pmid=24299489}}</ref>。 |
|||
| ⚫ | |||
天然の有機分子としては、地球上に最も豊富に存在する物質である可能性があり、その年代や起源によらずあらゆる堆積物中に出現する<ref>Ourisson G, Albrecht P | title = Hopanoids. 1. Geohopanoids: the most abundant natural products on earth? Acc Chem Res; 1992 25:398–402</ref>。このことから、地球の進化の再現や地質学において重要な[[分子化石]]となる<ref name=Knoll_2006>{{cite book | author = Knoll A H | title = Life on a Young Planet: The first three billion years of evolution on the planet earth | edition = 1st | publisher = Princeton University Press | year = 2003 | isbn = 0-691-00978-3 }}</ref>。 |
|||
ジプロプテロールは、細菌の一般的な膜脂質である[[リピドA]]と相互作用することで膜構造を整える。その方法は、真核生物の細胞膜でコレステロールと[[スフィンゴ脂質]]が相互作用する方法と類似している<ref name="saenz" />。ジプロプテロールとコレステロールは、[[スフィンゴミエリン]]の単分子層と[[糖鎖]]修飾されたリピドAの単分子層の双方において、凝縮を促進し[[ゲル]]相の形成を阻害することが示されている。さらにジプロプテロールとコレステロールは、糖鎖修飾されたリピドA単分子層のpH依存的な相転移を防ぐ<ref name="saenz" />。膜を介した酸耐性におけるホパノイドの役割は、スクアレンホペンシクラーゼに変異を持つホパノイド欠損細菌の細胞膜では酸による生育阻害や細胞膜の形態異常が観察されることからもさらに支持される<ref>{{Cite journal|last=Schmerk|first=Crystal L.|last2=Bernards|first2=Mark A.|last3=Valvano|first3=Miguel A.|date=2011-12|title=Hopanoid production is required for low-pH tolerance, antimicrobial resistance, and motility in Burkholderia cenocepacia|url=https://www.ncbi.nlm.nih.gov/pubmed/21965564|journal=Journal of Bacteriology|volume=193|issue=23|pages=6712–6723|doi=10.1128/JB.05979-11|issn=1098-5530|pmid=21965564|pmc=3232912}}</ref><ref>{{Cite journal|last=Welander|first=Paula V.|last2=Hunter|first2=Ryan C.|last3=Zhang|first3=Lichun|last4=Sessions|first4=Alex L.|last5=Summons|first5=Roger E.|last6=Newman|first6=Dianne K.|date=2009-10|title=Hopanoids play a role in membrane integrity and pH homeostasis in Rhodopseudomonas palustris TIE-1|url=https://www.ncbi.nlm.nih.gov/pubmed/19592593|journal=Journal of Bacteriology|volume=191|issue=19|pages=6145–6156|doi=10.1128/JB.00460-09|issn=1098-5530|pmid=19592593|pmc=2747905}}</ref>。 |
|||
[[ロジャー・サモンズ]]らは、[[ピルバラ]]の27億年前の[[頁岩]]の中から、[[藍藻]]等の光合成細菌由来の2-α-メチルホパンを含むホパノイドを発見した<ref name=Brocks_1999>{{cite journal | author = Brocks J, Logan G, Buick R, Summons R | title = Archean molecular fossils and the early rise of eukaryotes | journal = Science | volume = 285 | issue = 5430 | pages = 1033–6 | year = 1999 | pmid = 10446042 | doi = 10.1126/science.285.5430.1033}}</ref>。これらの頁岩に大量の2-α-メチルホパンが保存されていることは、大気が酸化されるずっと前の27億年前から、酸素を生成する光合成が進化していた可能性があることを示唆している。しかしFischerらは{{Snamei||Geobacter sulfurreducens}} を用いた実験において、2-α-メチルホパンこそ生成されなかったものの、この細菌が厳密に嫌気的な環境下でも多様なホパノイドを合成できることを示した<ref name=Fischer_2005>{{cite journal | author = Fischer, W. W., Summons, R. E., Pearson, A. | title = Targeted genomic detection of biosynthetic pathways: anaerobic production of hopanoid biomarkers by a common sedimentary microbe | journal = Geobiology | volume = 3 | pages = 3340 | year = 2005 | doi = 10.1111/j.1472-4669.2005.00041.x}}</ref>。 |
|||
土壌細菌[[ストレプトマイセス属]]の空気中の[[菌糸]]では、細胞膜から空気中への水の損失を最小限にしていると考えられている<ref name="Poralla_2000">{{cite journal | author = Poralla K, Muth G, Härtner T | title = Hopanoids are formed during transition from substrate to aerial hyphae in Streptomyces coelicolor A3(2) | journal = FEMS Microbiol Lett | volume = 189 | issue = 1 | pages = 93–5 | year = 2000 | pmid = 10913872 | doi = 10.1111/j.1574-6968.2000.tb09212.x}}</ref>。[[フランキア属]]細菌において[[窒素固定]]を行う diazovesicle という器官の膜の脂質二重層をより引き締め、酸素を透過しにくくすると考えられている<ref name="Berry_1993">{{cite journal | author = Berry A, Harriott O, Moreau R, Osman S, Benson D, Jones A | title = Hopanoid lipids compose the ''Frankia'' vesicle envelope, presumptive barrier of oxygen diffusion to nitrogenase | journal = Proc Natl Acad Sci USA | volume = 90 | issue = 13 | pages = 6091–4 | year = 1993 | pmid = 11607408 | doi = 10.1073/pnas.90.13.6091 | pmc = 46873|bibcode = 1993PNAS...90.6091B }}</ref>。[[ブラディリゾビウム属]]では、リピドAに化学的に結合したホパノイドは膜の安定性と剛性を高め、ストレス耐性と{{仮リンク|クサネム属|en|Aeschynomene|label=}}の植物内での生存を高める<ref>{{Cite journal|last=Silipo|first=Alba|last2=Vitiello|first2=Giuseppe|last3=Gully|first3=Djamel|last4=Sturiale|first4=Luisa|last5=Chaintreuil|first5=Clémence|last6=Fardoux|first6=Joel|last7=Gargani|first7=Daniel|last8=Lee|first8=Hae-In|last9=Kulkarni|first9=Gargi|date=2014-10-30|title=Covalently linked hopanoid-lipid A improves outer-membrane resistance of a Bradyrhizobium symbiont of legumes|url=https://www.ncbi.nlm.nih.gov/pubmed/25355435|journal=Nature Communications|volume=5|pages=5106|doi=10.1038/ncomms6106|issn=2041-1723|pmid=25355435}}</ref>。[[シアノバクテリア]]''Nostoc punctiforme''では、{{仮リンク|アキネート|en|Akinete|label=}}と呼ばれる生存のための構造体の外膜に大量の2-メチルホパノイドが局在している<ref>{{Cite journal|last=Doughty|first=D. M.|last2=Hunter|first2=R. C.|last3=Summons|first3=R. E.|last4=Newman|first4=D. K.|date=2009-12|title=2-Methylhopanoids are maximally produced in akinetes of Nostoc punctiforme: geobiological implications|url=https://www.ncbi.nlm.nih.gov/pubmed/19811542|journal=Geobiology|volume=7|issue=5|pages=524–532|doi=10.1111/j.1472-4669.2009.00217.x|issn=1472-4669|pmid=19811542|pmc=2860729}}</ref>。 |
|||
== 生合成 == |
|||
=== スクアレン合成 === |
|||
ホパノイドはC<sub>30</sub>テルペノイド([[トリテルペン|トリテルペノイド]])である。生合成はC<sub>5</sub>[[イソペンテニル二リン酸]](IPP)とC<sub>5</sub>[[ジメチルアリル二リン酸]](DMAPP)から開始され、両者が結合してより長鎖の[[イソプレノイド]]が形成される<ref name=":3">{{Cite journal|last=Sohlenkamp|first=Christian|last2=Geiger|first2=Otto|date=2016-01|title=Bacterial membrane lipids: diversity in structures and pathways|url=https://www.ncbi.nlm.nih.gov/pubmed/25862689|journal=FEMS microbiology reviews|volume=40|issue=1|pages=133–159|doi=10.1093/femsre/fuv008|issn=1574-6976|pmid=25862689}}</ref>。IPPおよびDMAPPの合成は、種に応じて[[メバロン酸経路]]と[[非メバロン酸経路]]のいずれかを介して進行する。真核生物では前者が一般的であるのに対し、細菌では後者がより一般的である<ref>{{Cite journal|last=Pérez-Gil|first=Jordi|last2=Rodríguez-Concepción|first2=Manuel|date=2013-05-15|title=Metabolic plasticity for isoprenoid biosynthesis in bacteria|url=https://portlandpress.com/biochemj/article-abstract/452/1/19/46166/Metabolic-plasticity-for-isoprenoid-biosynthesis?redirectedFrom=fulltext|journal=Biochemical Journal|volume=452|issue=1|pages=19–25|language=en|doi=10.1042/BJ20121899|issn=0264-6021|pmid=23614721}}</ref>。DMAPPは1分子のIPPと縮合してC<sub>10</sub>[[ゲラニル二リン酸]](GPP)となり、さらに次のIPP分子と縮合してC<sub>15</sub>[[ファルネシル二リン酸]](FPP)となる<ref name=":3" />。{{仮リンク|スクアレン合成酵素|en|Farnesyl-diphosphate farnesyltransferase|label=}}が2つのファルネシル二リン酸分子の縮合を触媒し、[[ニコチンアミドアデニンジヌクレオチドリン酸|NADPH]]が酸化されてC<sub>30</sub>[[スクアレン]]が合成される<ref>{{Cite journal|last=Pan|first=Jian-Jung|last2=Solbiati|first2=Jose O.|last3=Ramamoorthy|first3=Gurusankar|last4=Hillerich|first4=Brandan S.|last5=Seidel|first5=Ronald D.|last6=Cronan|first6=John E.|last7=Almo|first7=Steven C.|last8=Poulter|first8=C. Dale|date=2015-05-27|title=Biosynthesis of Squalene from Farnesyl Diphosphate in Bacteria: Three Steps Catalyzed by Three Enzymes|journal=ACS Central Science|volume=1|issue=2|pages=77–82|doi=10.1021/acscentsci.5b00115|issn=2374-7943|pmid=26258173|pmc=4527182}}</ref>。細菌では3つの酵素(HpnCDE)がFPPからスクアレンの合成を触媒するが、真核生物では1つの酵素だけで同じ反応が完了する<ref>{{Cite journal|last=Pan|first=Jian-Jung|last2=Solbiati|first2=Jose O.|last3=Ramamoorthy|first3=Gurusankar|last4=Hillerich|first4=Brandan S.|last5=Seidel|first5=Ronald D.|last6=Cronan|first6=John E.|last7=Almo|first7=Steven C.|last8=Poulter|first8=C. Dale|date=2015-05-27|title=Biosynthesis of Squalene from Farnesyl Diphosphate in Bacteria: Three Steps Catalyzed by Three Enzymes|url=https://pubs.acs.org/doi/10.1021/acscentsci.5b00115|journal=ACS Central Science|volume=1|issue=2|pages=77–82|language=en|doi=10.1021/acscentsci.5b00115|issn=2374-7943|pmid=26258173|pmc=4527182}}</ref>。 |
|||
[[File:Cyclase activesite.png|thumb|321x321px|''Methylococcus capsulatus''のスクアレンホペンシクラーゼの活性部位。取り込まれた基質のスクアレンが金色で示されている。ホモ二量体のうちの単量体が示されている。]] |
|||
=== 環化 === |
|||
[[File:Mcapshc bbarrel colored big.png|thumb|right|250px|''Methylococcus capsulatus''のスクアレンホペンシクラーゼのαバレル構造]] |
|||
続いて、スクアレンホペンシクラーゼがスクアレンの精巧な環化反応を触媒する。スクアレンはエネルギー的に有利な全いす型の立体配座となり、5つの環、6つの共有結合、9つのキラル中心が1段階の反応で形成される<ref name=":4">{{Cite journal|last=Siedenburg|first=Gabriele|last2=Jendrossek|first2=Dieter|date=2011-06-15|title=Squalene-Hopene Cyclases|journal=Applied and Environmental Microbiology|volume=77|issue=12|pages=3905–3915|language=en|doi=10.1128/AEM.00300-11|issn=0099-2240|pmid=21531832|pmc=3131620}}</ref><ref name=":7">{{Cite journal|last=Hoshino|first=Tsutomu|last2=Sato|first2=Tsutomu|date=2002-02-12|title=Squalene–hopene cyclase: catalytic mechanism and substrate recognition|url=https://pubs.rsc.org/en/content/articlelanding/2002/cc/b108995c|journal=Chemical Communications|issue=4|pages=291–301|language=en|doi=10.1039/B108995C|issn=1364-548X|pmid=12120044}}</ref>。''shc''遺伝子にコードされるこの酵素は、テルペノイドの生合成を担う酵素に特徴的な2つのαバレルフォールドを持ち<ref>{{Cite journal|last=Syrén|first=Per-Olof|last2=Henche|first2=Sabrina|last3=Eichler|first3=Anja|last4=Nestl|first4=Bettina M.|last5=Hauer|first5=Bernhard|date=2016-12-01|title=Squalene-hopene cyclases—evolution, dynamics and catalytic scope|url=http://www.sciencedirect.com/science/article/pii/S0959440X16300549|journal=Current Opinion in Structural Biology|volume=41|pages=73–82|language=en|doi=10.1016/j.sbi.2016.05.019|issn=0959-440X|pmid=27336183|series=Multi-protein assemblies in signaling • Catalysis and regulation}}</ref>、細胞内ではモノトピック、すなわち細胞膜に埋め込まれているが貫通していない、ホモ二量体として存在する<ref name=":4" /><ref>{{Cite journal|last=Dang|first=Tongyun|last2=Prestwich|first2=Glenn D.|date=2000-08-01|title=Site-directed mutagenesis of squalene–hopene cyclase: altered substrate specificity and product distribution|url=https://www.cell.com/cell-chemical-biology/abstract/S1074-5521(00)00003-X|journal=Chemistry & Biology|volume=7|issue=8|pages=643–649|language=English|doi=10.1016/S1074-5521(00)00003-X|issn=1074-5521|pmid=11048954|doi-access=free}}</ref>。''[[In vitro]]''では、この酵素の基質特異性は低く、{{仮リンク|2,3-オキシドスクアレン|en|2,3-Oxidosqualene|label=}}の環化も行う<ref>{{Cite journal|last=Rohmer|first=Michel|last2=Anding|first2=Claude|last3=Ourisson|first3=Guy|date=1980|title=Non-specific Biosynthesis of Hopane Triterpenes by a Cell-Free System from Acetobacter pasteurianum|journal=European Journal of Biochemistry|volume=112|issue=3|pages=541–547|language=en|doi=10.1111/j.1432-1033.1980.tb06117.x|issn=1432-1033|pmid=7460938}}</ref>。 |
|||
活性部位の芳香族残基は、基質にエネルギー的に不利な[[カルボカチオン]]を形成するが、迅速な多環化反応によってクエンチされる<ref name=":7" />。スクアレンの末端のアルケン結合を構成する電子がE環を閉じるためにホペニルカルボカチオンを攻撃した後の、環化反応の最後のサブステップでは、C-22カルボカチオンをクエンチする機構によって異なるホパノイド産物が形成される。水の求核攻撃によってジプロプテロールが形成される一方、近接する炭素の脱プロトン化によってホペン異性体のうちの1つ、多くの場合ジプロプテンが形成される<ref name=":0" />。 |
|||
=== 官能基付加 === |
|||
環化反応の後、ホパノイドは同じ[[オペロン]]の''shc''、''hpn''にコードされる他のホパノイド合成酵素による修飾を受ける<ref>{{Cite journal|last=Perzl|first=Michael|last2=Reipen|first2=Ina G.|last3=Schmitz|first3=Susanne|last4=Poralla|first4=Karl|last5=Sahm|first5=Hermann|last6=Sprenger|first6=Georg A.|last7=Kannenberg|first7=Elmar L.|date=1998-07-31|title=Cloning of conserved genes from Zymomonas mobilis and Bradyrhizobium japonicum that function in the biosynthesis of hopanoid lipids1EMBL accession number for the nucleotide sequence from Z. mobilis is AJ001401 and for the nucleotide sequence from B. japonicum, X86552.1|url=http://www.sciencedirect.com/science/article/pii/S0005276098000642|journal=Biochimica et Biophysica Acta (BBA) - Lipids and Lipid Metabolism|volume=1393|issue=1|pages=108–118|language=en|doi=10.1016/S0005-2760(98)00064-2|issn=0005-2760|pmid=9714766}}</ref>。例えば、ラジカル[[S-アデノシルメチオニン|SAM]]タンパク質HpnHはジプロプテンに[[アデノシン|アデノシル]]基を付加することでC<sub>35</sub>ホパノイドであるアデノシルホパンを形成し、さらに他の''hpn''遺伝子産物によってさらに修飾されてバクテリオホパンテトロール(BHT)が形成される<ref>{{Cite journal|last=Bradley|first=Alexander S.|last2=Pearson|first2=Ann|last3=Sáenz|first3=James P.|last4=Marx|first4=Christopher J.|date=2010-10-01|title=Adenosylhopane: The first intermediate in hopanoid side chain biosynthesis|url=http://www.sciencedirect.com/science/article/pii/S0146638010001853|journal=Organic Geochemistry|volume=41|issue=10|pages=1075–1081|language=en|doi=10.1016/j.orggeochem.2010.07.003|issn=0146-6380}}</ref><ref>{{Cite journal|last=Liu|first=Wenjun|last2=Sakr|first2=Elias|last3=Schaeffer|first3=Philippe|last4=Talbot|first4=Helen M.|last5=Donisi|first5=Janina|last6=Härtner|first6=Thomas|last7=Kannenberg|first7=Elmar|last8=Takano|first8=Eriko|last9=Rohmer|first9=Michel|date=2014|title=Ribosylhopane, a Novel Bacterial Hopanoid, as Precursor of C35 Bacteriohopanepolyols in Streptomyces coelicolor A3(2)|journal=ChemBioChem|volume=15|issue=14|pages=2156–2161|language=en|doi=10.1002/cbic.201402261|issn=1439-7633|pmid=25155017|pmc=4245026}}</ref>。さらに[[グリコシルトランスフェラーゼ]]HpnIによってBHTは''N''-アセチルグルコサミニル-BHTに変換される<ref name=":8">{{Cite journal|last=Schmerk|first=Crystal L.|last2=Welander|first2=Paula V.|last3=Hamad|first3=Mohamad A.|last4=Bain|first4=Katie L.|last5=Bernards|first5=Mark A.|last6=Summons|first6=Roger E.|last7=Valvano|first7=Miguel A.|date=2015|title=Elucidation of the Burkholderia cenocepacia hopanoid biosynthesis pathway uncovers functions for conserved proteins in hopanoid-producing bacteria|url=https://pureadmin.qub.ac.uk/ws/files/18054125/Schmerk_EMI_2014_0306_revised_nofields.pdf|journal=Environmental Microbiology|volume=17|issue=3|pages=735–750|language=en|doi=10.1111/1462-2920.12509|issn=1462-2920|pmid=24888970}}</ref>。続いて、ホパノイド生合成関連タンパク質HpnKがグルコサミニル-BHTへの脱アセチル化を媒介し、そしてラジカルSAMタンパク質HpnKによってシクリトールエーテルが作り出される<ref name=":8" />。 |
|||
C<sub>30</sub>ホパノイドとC<sub>35</sub>ホパノイドは、ラジカルSAM[[メチルトランスフェラーゼ]]HpnPとHpnRによって、それぞれC-2位とC-3位がメチル化される<ref name=":9">{{Cite journal|last=Welander|first=Paula V.|last2=Coleman|first2=Maureen L.|last3=Sessions|first3=Alex L.|last4=Summons|first4=Roger E.|last5=Newman|first5=Dianne K.|date=2010-05-11|title=Identification of a methylase required for 2-methylhopanoid production and implications for the interpretation of sedimentary hopanes|journal=Proceedings of the National Academy of Sciences|volume=107|issue=19|pages=8537–8542|language=en|doi=10.1073/pnas.0912949107|issn=0027-8424|pmid=20421508|pmc=2889317}}</ref><ref>{{Cite journal|last=Welander|first=Paula V.|last2=Summons|first2=Roger E.|date=2012-08-07|title=Discovery, taxonomic distribution, and phenotypic characterization of a gene required for 3-methylhopanoid production|journal=Proceedings of the National Academy of Sciences|volume=109|issue=32|pages=12905–12910|language=en|doi=10.1073/pnas.1208255109|issn=0027-8424|pmid=22826256|pmc=3420191}}</ref>。これらのメチル化されたホパノイド(2-および3-メチルホパノイド)は地質学的に安定であり、過去の生物史を復元するための[[:en:Biomarker_(petroleum)|バイオマーカー]]として広く利用されてきた<ref name=":2" />。しかしゲノムデータの蓄積にともない、これらメチル化されたホパノイドが従来の予想以上に多くの生物種に分布していることが明らかとなり、現在ではその有用性に疑問が持たれている<ref>{{Cite journal|last=Ricci|first=Jessica N|last2=Coleman|first2=Maureen L|last3=Welander|first3=Paula V|last4=Sessions|first4=Alex L|last5=Summons|first5=Roger E|last6=Spear|first6=John R|last7=Newman|first7=Dianne K|date=2014-03|title=Diverse capacity for 2-methylhopanoid production correlates with a specific ecological niche|url=http://www.nature.com/articles/ismej2013191|journal=The ISME Journal|volume=8|issue=3|pages=675–684|language=en|doi=10.1038/ismej.2013.191|issn=1751-7362|pmid=24152713|pmc=3930323}}</ref>。 |
|||
一部の細菌([[アルファプロテオバクテリア綱|アルファプロテオバクテリア]]など)では、ジプロプテンから別の五環式トリテルペノイドである{{仮リンク|テトラヒマノール|en|Tetrahymanol|label=}}が合成されるが、一部の真核生物([[繊毛虫]]など)ではスクアレンから固有のシクラーゼによって、ジプポプテンを経由せず直接合成される<ref>{{Cite journal|last=Banta|first=Amy B.|last2=Wei|first2=Jeremy H.|last3=Welander|first3=Paula V.|date=2015-11-03|title=A distinct pathway for tetrahymanol synthesis in bacteria|journal=Proceedings of the National Academy of Sciences|volume=112|issue=44|pages=13478–13483|language=en|doi=10.1073/pnas.1511482112|issn=0027-8424|pmid=26483502|pmc=4640766}}</ref>。 |
|||
| ⚫ | |||
天然の有機分子としては、地球上に最も豊富に存在する物質である可能性があり、その年代や起源によらずあらゆる堆積物中に出現する<ref>{{Cite journal|last=Ourisson|first=Guy|last2=Albrecht|first2=Pierre|date=1992-09|title=Hopanoids. 1. Geohopanoids: the most abundant natural products on Earth?|url=https://pubs.acs.org/doi/abs/10.1021/ar00021a003|journal=Accounts of Chemical Research|volume=25|issue=9|pages=398–402|language=en|doi=10.1021/ar00021a003|issn=0001-4842}}</ref>。DNAやタンパク質などの生体分子は[[続成作用]]の過程で分解されるが、多環脂質はその連結された安定な構造のため、地質学的なタイムスケールで環境中に存在し続ける<ref name=":5">{{Cite book|title=Fundamentals of Geobiology|first2=Sara A.|editor3-first=Kurt O.|editor2-last=Canfield|editor2-first=Donald E.|editor-last=Knoll|editor-first=Andrew H.|last2=Lincoln|last=Summons|url=http://doi.wiley.com/10.1002/9781118280874.ch15|first=Roger E.|doi=10.1002/9781118280874.ch15|pages=269–296|isbn=978-1-118-28087-4|location=Chichester, UK|date=2012-03-30|publisher=John Wiley & Sons, Ltd|editor3-last=Konhauser}}</ref>。ホパノイドやステロールは堆積の過程で官能基が除去され[[ホパン]]や[[ステラン]]に還元されるが、これらの飽和[[炭化水素]]は初期生命と地球の共進化の研究に有用な[[:en:Biomarker_(petroleum)|バイオマーカー]](分子化石)である<ref name=":5" /><ref name=Knoll_2006>{{cite book | author = Knoll A H | title = Life on a Young Planet: The first three billion years of evolution on the planet earth | edition = 1st | publisher = Princeton University Press | year = 2003 | isbn = 0-691-00978-3 }}</ref>。 |
|||
[[:en:Roger_Everett_Summons|ロジャー・サモンズ]]らは、オーストラリアの[[ピルバラ]]地域にある27億年前の[[頁岩]]の中から、酸素発生型[[光合成細菌]]である[[藍藻|シアノバクテリア]]由来の2-α-メチルホパンを発見した<ref name="Brocks_1999">{{cite journal|author=Brocks J, Logan G, Buick R, Summons R|year=1999|title=Archean molecular fossils and the early rise of eukaryotes|journal=Science|volume=285|issue=5430|pages=1033–6|doi=10.1126/science.285.5430.1033|pmid=10446042}}</ref>。これらの頁岩に大量の2-α-メチルホパンが保存されていることは、少なくとも27億年前から酸素を生成する光合成が存在していた証拠として解釈され、これは24億年前から確認されている地球大気中の酸素の出現([[:en:Great_Oxidation_Event|大酸化イベント]])に3億年も先行して酸素発生型代謝がすでに存在していたことを示唆する。しかし2-メチルホパンの酸素発生型光合成のバイオマーカーとしての完全性は、その後、シアノバクテリア以外の細菌、例えば[[光栄養生物]]である''[[:en:Rhodopseudomonas palustris|Rhodopseudomonas palustris]]''が無酸素環境下で2-メチルBHPを産生するという発見により弱まることとなった<ref>{{Cite journal|last=Rashby|first=Sky E.|last2=Sessions|first2=Alex L.|last3=Summons|first3=Roger E.|last4=Newman|first4=Dianne K.|date=2007-09-18|title=Biosynthesis of 2-methylbacteriohopanepolyols by an anoxygenic phototroph|url=https://www.ncbi.nlm.nih.gov/pubmed/17848515|journal=Proceedings of the National Academy of Sciences of the United States of America|volume=104|issue=38|pages=15099–15104|doi=10.1073/pnas.0704912104|issn=0027-8424|pmid=17848515|pmc=1986619}}</ref>。さらに、すべてのシアノバクテリアがメチルホパノイドを生成するわけではないこと、メチルトランスフェラーゼHpnPをコードする遺伝子が光合成を行わない[[アルファプロテオバクテリア綱|アルファプロテオバクテリア]]や[[アキドバクテリウム門|アシドバクテリア]]にも存在していることを判明した結果、メチルホパンをシアノバクテリアおよび酸素発生型光合成のバイオマーカーとすることには疑問符が付けられることとなった<ref name=":9" /><ref>{{Cite journal|last=Talbot|first=Helen M.|last2=Summons|first2=Roger E.|last3=Jahnke|first3=Linda L.|last4=Cockell|first4=Charles S.|last5=Rohmer|first5=Michel|last6=Farrimond|first6=Paul|date=2008-02|title=Cyanobacterial bacteriohopanepolyol signatures from cultures and natural environmental settings|url=https://linkinghub.elsevier.com/retrieve/pii/S0146638007001933|journal=Organic Geochemistry|volume=39|issue=2|pages=232–263|language=en|doi=10.1016/j.orggeochem.2007.08.006}}</ref>。 |
|||
さらには[[ピルバラクラトン]]の頁岩に含まれていたとされる27億年前のバイオマーカーは、その後の詳細な分析により後世の汚染物質であると結論付けられ、否定された<ref>{{Cite journal|last=French|first=Katherine L.|last2=Hallmann|first2=Christian|last3=Hope|first3=Janet M.|last4=Schoon|first4=Petra L.|last5=Zumberge|first5=J. Alex|last6=Hoshino|first6=Yosuke|last7=Peters|first7=Carl A.|last8=George|first8=Simon C.|last9=Love|first9=Gordon D.|date=2015-05-12|title=Reappraisal of hydrocarbon biomarkers in Archean rocks|url=https://www.ncbi.nlm.nih.gov/pubmed/25918387|journal=Proceedings of the National Academy of Sciences of the United States of America|volume=112|issue=19|pages=5915–5920|doi=10.1073/pnas.1419563112|issn=1091-6490|pmid=25918387|pmc=4434754}}</ref>。現在認められている最古のトリテルペノイドは、オーストラリアの盆地で得られた16.4億年前の中原生代の(メチル)ホパンである<ref>{{Cite journal|last=Brocks|first=Jochen J.|last2=Love|first2=Gordon D.|last3=Summons|first3=Roger E.|last4=Knoll|first4=Andrew H.|last5=Logan|first5=Graham A.|last6=Bowden|first6=Stephen A.|date=2005-10-06|title=Biomarker evidence for green and purple sulphur bacteria in a stratified Palaeoproterozoic sea|url=https://www.ncbi.nlm.nih.gov/pubmed/16208367|journal=Nature|volume=437|issue=7060|pages=866–870|doi=10.1038/nature04068|issn=1476-4687|pmid=16208367}}</ref>。ただし、[[分子時計]]による解析では、ホパノイドと生合成回路が大部分共通しているステロールはすでに23億年前頃、{{仮リンク|大酸化イベント|en|Great Oxidation Event|label=}}とほぼ同時期に出現していた可能性がある。そのため、合成に酸素を必要としないホパノイドはステロールよりもさらに早くから出現していた可能性がある<ref>{{Cite journal|last=Gold|first=David A.|last2=Caron|first2=Abigail|last3=Fournier|first3=Gregory P.|last4=Summons|first4=Roger E.|date=03 16, 2017|title=Paleoproterozoic sterol biosynthesis and the rise of oxygen|url=https://www.ncbi.nlm.nih.gov/pubmed/28264195|journal=Nature|volume=543|issue=7645|pages=420–423|doi=10.1038/nature21412|issn=1476-4687|pmid=28264195}}</ref>。 |
|||
ホパノイド合成酵素(スクアレンホペンシクラーゼ)は細菌に広く分布しているのに対し、ステロール合成酵素({{仮リンク|酸化スクアレン環化酵素|en|Oxidosqualene cyclase|label=オキシドクスアレンシクラーゼ}})は真核生物および一部の細菌に限定される。オキシドスクワレンシクラーゼの基質(オキシドスクアレン)の生合成には酸素が必須であるため<ref>{{Cite journal|last=Summons|first=Roger E|last2=Bradley|first2=Alexander S|last3=Jahnke|first3=Linda L|last4=Waldbauer|first4=Jacob R|date=2006-06-29|title=Steroids, triterpenoids and molecular oxygen|url=https://royalsocietypublishing.org/doi/10.1098/rstb.2006.1837|journal=Philosophical Transactions of the Royal Society B: Biological Sciences|volume=361|issue=1470|pages=951–968|language=en|doi=10.1098/rstb.2006.1837|issn=0962-8436|pmid=16754609|pmc=1578733}}</ref>、オキシドスクアレンシクラーゼの出現は大酸化イベント以降と一般には考えられている。対してスクアレンホペンシクラーゼは分子系統解析の結果、大酸化イベント以前、細菌の進化の初期段階からすでに存在していた可能性が示唆されている<ref>{{Cite journal|last=Santana-Molina|first=Carlos|last2=Rivas-Marin|first2=Elena|last3=Rojas|first3=Ana M|last4=Devos|first4=Damien P|editor-last=Ursula Battistuzzi|editor-first=Fabia|date=2020-07-01|title=Origin and Evolution of Polycyclic Triterpene Synthesis|url=https://academic.oup.com/mbe/article/37/7/1925/5775509|journal=Molecular Biology and Evolution|volume=37|issue=7|pages=1925–1941|language=en|doi=10.1093/molbev/msaa054|issn=0737-4038|pmid=32125435|pmc=7306690}}</ref>。実際、ステロールと違いホパノイドの合成に酸素は必要とされない。そのため、ホパノイドは地球大気に酸素が出現する以前からステロールのように細胞膜の調整に利用されていた可能性がある<ref name=":6">{{Cite journal|last=Welander|first=Paula V.|date=08 20, 2019|title=Deciphering the evolutionary history of microbial cyclic triterpenoids|url=https://www.ncbi.nlm.nih.gov/pubmed/31071437|journal=Free Radical Biology & Medicine|volume=140|pages=270–278|doi=10.1016/j.freeradbiomed.2019.05.002|issn=1873-4596|pmid=31071437}}</ref>。また、スクアレンホペンシクラーゼがスクアレンだけでなくオキシドスクアレンも環化する基質特異性の低さも、一部の科学者がオキシドスクアレンシクラーゼよりも進化的に先に生じていたと考える根拠となっている<ref name=":10">{{Cite journal|last=Ourisson|first=Guy|last2=Albrecht|first2=Pierre|last3=Rohmer|first3=Michel|date=1982-07|title=Predictive microbial biochemistry — from molecular fossils to procaryotic membranes|url=https://linkinghub.elsevier.com/retrieve/pii/0968000482900287|journal=Trends in Biochemical Sciences|volume=7|issue=7|pages=236–239|language=en|doi=10.1016/0968-0004(82)90028-7}}</ref>。ちなみに、スクアレンはスクアレンホペンシクラーゼに低エネルギーの全いす(chair-chair-chair-chair; CCCC)型立体配座で結合するが、オキシドスクアレンはより拘束されたchair-boat-chair (CBC)型立体配座でオキシドスクアレンシクラーゼに結合する<ref name=":0" /><ref name=":10" />。一つの説ではスクアレンホペンシクラーゼとオキシドスクアレンシクラーゼは、三環式マラバリカノイド(tricyclic malabaricanoid)または四環式ダンマリノイド(tetracyclic dammarinoid)を産生するシクラーゼの共通祖先から分岐したと考えている<ref name=":6" /><ref>{{Cite journal|last=Fischer|first=W. W.|last2=Pearson|first2=A.|date=2007-02-09|title=Hypotheses for the origin and early evolution of triterpenoid cyclases|url=http://doi.wiley.com/10.1111/j.1472-4669.2007.00096.x|journal=Geobiology|volume=0|issue=0|pages=070210031741002–???|language=en|doi=10.1111/j.1472-4669.2007.00096.x|issn=1472-4677}}</ref>。 |
|||
== 産業との関係 == |
|||
スクアレンホペンシクラーゼの脱プロトン活性の背後にあるエレガントな分子機構は、ドイツのシュトゥットガルト大学の化学技術者によって評価と応用がなされている。活性部位のエンジニアリングにより、ホパノイドを形成する酵素の能力は失われたが、[[モノテルペノイド]]である[[ゲラニオール]]、エポキシゲラニオール、[[シトロネラール]]の[[立体選択性|立体選択的]]な環化反応の[[ブレンステッド酸]]触媒が可能となった<ref>{{Cite journal|last=Hammer|first=Stephan C.|last2=Marjanovic|first2=Antonija|last3=Dominicus|first3=Jörg M.|last4=Nestl|first4=Bettina M.|last5=Hauer|first5=Bernhard|date=February 2015|title=Squalene hopene cyclases are protonases for stereoselective Brønsted acid catalysis|url=https://www.nature.com/articles/nchembio.1719|journal=Nature Chemical Biology|volume=11|issue=2|pages=121–126|language=en|doi=10.1038/nchembio.1719|issn=1552-4469|pmid=25503928}}</ref>。 |
|||
== 農業との関係 == |
|||
植物共生微生物の環境抵抗性を高める生物肥料技術として、ホパノイドやホパノイド産生窒素固定生物の応用が提案され、特許が取得されている<ref>{{Citation|title=Hopanoids producing bacteria and related biofertilizers, compositions, methods and systems|url=https://patents.google.com/patent/US20170107160A1/en|date=2016-10-19|accessdate=2020-05-15|language=en}}</ref>。 |
|||
== 医療との関係 == |
|||
''[[:en:Methylobacterium extorquens|Methylobacterium extorquens]]''におけるジプロプテロールとリピドAの相互作用の研究から、多剤輸送がホパノイド依存的過程であることが発見された。多剤排出は膜貫通輸送タンパク質を介した薬剤耐性機構であるが、多剤排出が可能な野生株に由来するスクアレンホペンシクラーゼ変異体は、多剤輸送とホパノイド合成の双方の能力が失われていた<ref name="Sáenz 11971–11976">{{Cite journal|last=Sáenz|first=James P.|last2=Grosser|first2=Daniel|last3=Bradley|first3=Alexander S.|last4=Lagny|first4=Thibaut J.|last5=Lavrynenko|first5=Oksana|last6=Broda|first6=Martyna|last7=Simons|first7=Kai|date=2015-09-22|title=Hopanoids as functional analogues of cholesterol in bacterial membranes|journal=Proceedings of the National Academy of Sciences|volume=112|issue=38|pages=11971–11976|language=en|doi=10.1073/pnas.1515607112|issn=0027-8424|pmid=26351677|pmc=4586864}}</ref>。研究者らは、ホパノイドによって輸送タンパク質が直接制御されている可能性と、膜構造の変化によって間接的に輸送系が失われている可能性を示唆している<ref name="Sáenz 11971–11976"/>。 |
|||
==出典== |
==出典== |
||
2023年9月12日 (火) 20:00時点における最新版

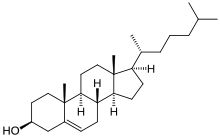
ホパノイド (Hopanoids) はトリテルペノイドの中で、ホパン骨格を持つ天然の五環式化合物である。最初に報告されたホパノイドはヒドロキシホパノンで、ナショナル・ギャラリーの2人の化学者が絵画のニスとして用いられるダンマル樹脂の研究中に単離したものである[1]。ホパンという名は、この樹脂が得られるフタバガキ科のHopea属から取られた(属名は植物学者ジョン・ホープに由来する)。ホパノイドは一部の陸上植物や菌類などの真核生物からも見つかっているが、細菌により広く分布していることが現在では知られている[2]。真核生物内では構造的に類似したステロイド(例えばコレステロール)の方が広く分布しており、ホパノイドの分布は限定的である。ホパノイドは地中で分解されにくいため、砂礫中や石油貯留層から様々な種類のものが発見されており、過去の地球の歴史においてバクテリアの存在およびその種類を示すバイオマーカーとして広く用いられている[3]。古細菌からは発見されていない[4][5]。
機能
[編集]シーケンシングが行われた細菌ゲノムの約10%には、ホパノイド合成酵素であるスクアレンホペンシクラーゼをコードすると推定される遺伝子が存在している。ホパノイドの生理機能についてはいまだ明確ではないものの、細胞膜中に存在し細胞を保護する役目を果たしていると推測されている。一部の生物では極限環境への適応を可能にしている[6]。
ホパノイドは細菌の細胞膜において、脂質ラフトの形成のほか、細胞膜透過性・剛性・流動性など様々な性質を調整していると推定される。真核生物ではステロールが同等の機能を担っている[7]。ホパノイドとステロールの機能の類似性は、細菌の細胞膜でよく見られるホパノイドであるジプロプテンと、動物の細胞膜に普遍的に存在するステロールであるコレステロールの構造の類似性に見ることができる[7]。ホパノイドはステロールの欠乏を完全に補うことはできないようであるが、ステロール同様、膜を凝縮させ透過性を低下させる[8]。また、一部のガンマプロテオバクテリアや、地衣類やコケ植物などの真核生物ではステロールとホパノイドの双方を産生することが示されており、両者はそれぞれ異なる機能を担っている可能性が示唆される[2][9]。ホパノイドが細胞膜に詰め込まれる方法は、どのような官能基が付加されているかによって変化する。バクテリオホパンテトロール(bacteriohopanetetrol)は脂質二重層中で直立して存在していると推測されるが、ジプロプテンは内側と外側の層の間に局在し、膜を厚くして透過性を低下させていると推測される[10]。
ジプロプテロールは、細菌の一般的な膜脂質であるリピドAと相互作用することで膜構造を整える。その方法は、真核生物の細胞膜でコレステロールとスフィンゴ脂質が相互作用する方法と類似している[7]。ジプロプテロールとコレステロールは、スフィンゴミエリンの単分子層と糖鎖修飾されたリピドAの単分子層の双方において、凝縮を促進しゲル相の形成を阻害することが示されている。さらにジプロプテロールとコレステロールは、糖鎖修飾されたリピドA単分子層のpH依存的な相転移を防ぐ[7]。膜を介した酸耐性におけるホパノイドの役割は、スクアレンホペンシクラーゼに変異を持つホパノイド欠損細菌の細胞膜では酸による生育阻害や細胞膜の形態異常が観察されることからもさらに支持される[11][12]。
土壌細菌ストレプトマイセス属の空気中の菌糸では、細胞膜から空気中への水の損失を最小限にしていると考えられている[13]。フランキア属細菌において窒素固定を行う diazovesicle という器官の膜の脂質二重層をより引き締め、酸素を透過しにくくすると考えられている[14]。ブラディリゾビウム属では、リピドAに化学的に結合したホパノイドは膜の安定性と剛性を高め、ストレス耐性とクサネム属の植物内での生存を高める[15]。シアノバクテリアNostoc punctiformeでは、アキネートと呼ばれる生存のための構造体の外膜に大量の2-メチルホパノイドが局在している[16]。
生合成
[編集]スクアレン合成
[編集]ホパノイドはC30テルペノイド(トリテルペノイド)である。生合成はC5イソペンテニル二リン酸(IPP)とC5ジメチルアリル二リン酸(DMAPP)から開始され、両者が結合してより長鎖のイソプレノイドが形成される[17]。IPPおよびDMAPPの合成は、種に応じてメバロン酸経路と非メバロン酸経路のいずれかを介して進行する。真核生物では前者が一般的であるのに対し、細菌では後者がより一般的である[18]。DMAPPは1分子のIPPと縮合してC10ゲラニル二リン酸(GPP)となり、さらに次のIPP分子と縮合してC15ファルネシル二リン酸(FPP)となる[17]。スクアレン合成酵素が2つのファルネシル二リン酸分子の縮合を触媒し、NADPHが酸化されてC30スクアレンが合成される[19]。細菌では3つの酵素(HpnCDE)がFPPからスクアレンの合成を触媒するが、真核生物では1つの酵素だけで同じ反応が完了する[20]。

環化
[編集]
続いて、スクアレンホペンシクラーゼがスクアレンの精巧な環化反応を触媒する。スクアレンはエネルギー的に有利な全いす型の立体配座となり、5つの環、6つの共有結合、9つのキラル中心が1段階の反応で形成される[21][22]。shc遺伝子にコードされるこの酵素は、テルペノイドの生合成を担う酵素に特徴的な2つのαバレルフォールドを持ち[23]、細胞内ではモノトピック、すなわち細胞膜に埋め込まれているが貫通していない、ホモ二量体として存在する[21][24]。In vitroでは、この酵素の基質特異性は低く、2,3-オキシドスクアレンの環化も行う[25]。
活性部位の芳香族残基は、基質にエネルギー的に不利なカルボカチオンを形成するが、迅速な多環化反応によってクエンチされる[22]。スクアレンの末端のアルケン結合を構成する電子がE環を閉じるためにホペニルカルボカチオンを攻撃した後の、環化反応の最後のサブステップでは、C-22カルボカチオンをクエンチする機構によって異なるホパノイド産物が形成される。水の求核攻撃によってジプロプテロールが形成される一方、近接する炭素の脱プロトン化によってホペン異性体のうちの1つ、多くの場合ジプロプテンが形成される[2]。
官能基付加
[編集]環化反応の後、ホパノイドは同じオペロンのshc、hpnにコードされる他のホパノイド合成酵素による修飾を受ける[26]。例えば、ラジカルSAMタンパク質HpnHはジプロプテンにアデノシル基を付加することでC35ホパノイドであるアデノシルホパンを形成し、さらに他のhpn遺伝子産物によってさらに修飾されてバクテリオホパンテトロール(BHT)が形成される[27][28]。さらにグリコシルトランスフェラーゼHpnIによってBHTはN-アセチルグルコサミニル-BHTに変換される[29]。続いて、ホパノイド生合成関連タンパク質HpnKがグルコサミニル-BHTへの脱アセチル化を媒介し、そしてラジカルSAMタンパク質HpnKによってシクリトールエーテルが作り出される[29]。
C30ホパノイドとC35ホパノイドは、ラジカルSAMメチルトランスフェラーゼHpnPとHpnRによって、それぞれC-2位とC-3位がメチル化される[30][31]。これらのメチル化されたホパノイド(2-および3-メチルホパノイド)は地質学的に安定であり、過去の生物史を復元するためのバイオマーカーとして広く利用されてきた[8]。しかしゲノムデータの蓄積にともない、これらメチル化されたホパノイドが従来の予想以上に多くの生物種に分布していることが明らかとなり、現在ではその有用性に疑問が持たれている[32]。
一部の細菌(アルファプロテオバクテリアなど)では、ジプロプテンから別の五環式トリテルペノイドであるテトラヒマノールが合成されるが、一部の真核生物(繊毛虫など)ではスクアレンから固有のシクラーゼによって、ジプポプテンを経由せず直接合成される[33]。
古生物学への応用
[編集]天然の有機分子としては、地球上に最も豊富に存在する物質である可能性があり、その年代や起源によらずあらゆる堆積物中に出現する[34]。DNAやタンパク質などの生体分子は続成作用の過程で分解されるが、多環脂質はその連結された安定な構造のため、地質学的なタイムスケールで環境中に存在し続ける[35]。ホパノイドやステロールは堆積の過程で官能基が除去されホパンやステランに還元されるが、これらの飽和炭化水素は初期生命と地球の共進化の研究に有用なバイオマーカー(分子化石)である[35][36]。
ロジャー・サモンズらは、オーストラリアのピルバラ地域にある27億年前の頁岩の中から、酸素発生型光合成細菌であるシアノバクテリア由来の2-α-メチルホパンを発見した[37]。これらの頁岩に大量の2-α-メチルホパンが保存されていることは、少なくとも27億年前から酸素を生成する光合成が存在していた証拠として解釈され、これは24億年前から確認されている地球大気中の酸素の出現(大酸化イベント)に3億年も先行して酸素発生型代謝がすでに存在していたことを示唆する。しかし2-メチルホパンの酸素発生型光合成のバイオマーカーとしての完全性は、その後、シアノバクテリア以外の細菌、例えば光栄養生物であるRhodopseudomonas palustrisが無酸素環境下で2-メチルBHPを産生するという発見により弱まることとなった[38]。さらに、すべてのシアノバクテリアがメチルホパノイドを生成するわけではないこと、メチルトランスフェラーゼHpnPをコードする遺伝子が光合成を行わないアルファプロテオバクテリアやアシドバクテリアにも存在していることを判明した結果、メチルホパンをシアノバクテリアおよび酸素発生型光合成のバイオマーカーとすることには疑問符が付けられることとなった[30][39]。
さらにはピルバラクラトンの頁岩に含まれていたとされる27億年前のバイオマーカーは、その後の詳細な分析により後世の汚染物質であると結論付けられ、否定された[40]。現在認められている最古のトリテルペノイドは、オーストラリアの盆地で得られた16.4億年前の中原生代の(メチル)ホパンである[41]。ただし、分子時計による解析では、ホパノイドと生合成回路が大部分共通しているステロールはすでに23億年前頃、大酸化イベントとほぼ同時期に出現していた可能性がある。そのため、合成に酸素を必要としないホパノイドはステロールよりもさらに早くから出現していた可能性がある[42]。
ホパノイド合成酵素(スクアレンホペンシクラーゼ)は細菌に広く分布しているのに対し、ステロール合成酵素(オキシドクスアレンシクラーゼ)は真核生物および一部の細菌に限定される。オキシドスクワレンシクラーゼの基質(オキシドスクアレン)の生合成には酸素が必須であるため[43]、オキシドスクアレンシクラーゼの出現は大酸化イベント以降と一般には考えられている。対してスクアレンホペンシクラーゼは分子系統解析の結果、大酸化イベント以前、細菌の進化の初期段階からすでに存在していた可能性が示唆されている[44]。実際、ステロールと違いホパノイドの合成に酸素は必要とされない。そのため、ホパノイドは地球大気に酸素が出現する以前からステロールのように細胞膜の調整に利用されていた可能性がある[45]。また、スクアレンホペンシクラーゼがスクアレンだけでなくオキシドスクアレンも環化する基質特異性の低さも、一部の科学者がオキシドスクアレンシクラーゼよりも進化的に先に生じていたと考える根拠となっている[46]。ちなみに、スクアレンはスクアレンホペンシクラーゼに低エネルギーの全いす(chair-chair-chair-chair; CCCC)型立体配座で結合するが、オキシドスクアレンはより拘束されたchair-boat-chair (CBC)型立体配座でオキシドスクアレンシクラーゼに結合する[2][46]。一つの説ではスクアレンホペンシクラーゼとオキシドスクアレンシクラーゼは、三環式マラバリカノイド(tricyclic malabaricanoid)または四環式ダンマリノイド(tetracyclic dammarinoid)を産生するシクラーゼの共通祖先から分岐したと考えている[45][47]。
産業との関係
[編集]スクアレンホペンシクラーゼの脱プロトン活性の背後にあるエレガントな分子機構は、ドイツのシュトゥットガルト大学の化学技術者によって評価と応用がなされている。活性部位のエンジニアリングにより、ホパノイドを形成する酵素の能力は失われたが、モノテルペノイドであるゲラニオール、エポキシゲラニオール、シトロネラールの立体選択的な環化反応のブレンステッド酸触媒が可能となった[48]。
農業との関係
[編集]植物共生微生物の環境抵抗性を高める生物肥料技術として、ホパノイドやホパノイド産生窒素固定生物の応用が提案され、特許が取得されている[49]。
医療との関係
[編集]Methylobacterium extorquensにおけるジプロプテロールとリピドAの相互作用の研究から、多剤輸送がホパノイド依存的過程であることが発見された。多剤排出は膜貫通輸送タンパク質を介した薬剤耐性機構であるが、多剤排出が可能な野生株に由来するスクアレンホペンシクラーゼ変異体は、多剤輸送とホパノイド合成の双方の能力が失われていた[50]。研究者らは、ホパノイドによって輸送タンパク質が直接制御されている可能性と、膜構造の変化によって間接的に輸送系が失われている可能性を示唆している[50]。
出典
[編集]- ^ Mills, J. S.; Werner, A. E. A. (1955). “The chemistry of dammar resin” (英語). Journal of the Chemical Society (Resumed): 3132. doi:10.1039/jr9550003132. ISSN 0368-1769.
- ^ a b c d Volkman, John K. (2005-02). “Sterols and other triterpenoids: source specificity and evolution of biosynthetic pathways” (英語). Organic Geochemistry 36 (2): 139–159. doi:10.1016/j.orggeochem.2004.06.013.
- ^ Hunt, John M.; Philp, R.Paul; Kvenvolden, Keith A. (2002). “Early developments in petroleum geochemistry”. Organic Geochemistry 33 (9): 1025–1052. doi:10.1016/S0146-6380(02)00056-6. ISSN 01466380.
- ^ William W. Christie. “The AOCS Lipid Library. Sterols 4. Hopanoids and related lipids”. AOCS. 2015年2月9日閲覧。
- ^ Larry L Barton (2005). Structural and Functional Relationships in Prokaryotes. Springer. ISBN 0-387-20708-2
- ^ Fischer, W. W.; Summons, R. E.; Pearson, A. (2005-01). “Targeted genomic detection of biosynthetic pathways: anaerobic production of hopanoid biomarkers by a common sedimentary microbe” (英語). Geobiology 3 (1): 33–40. doi:10.1111/j.1472-4669.2005.00041.x. ISSN 1472-4677.
- ^ a b c d Sáenz, JP.; Sezgin, E.; Schwille, P.; Simons, K. (Aug 2012). “Functional convergence of hopanoids and sterols in membrane ordering.”. Proc Natl Acad Sci U S A 109 (35): 14236–40. doi:10.1073/pnas.1212141109. PMID 22893685.
- ^ a b Belin, Brittany J.; Busset, Nicolas; Giraud, Eric; Molinaro, Antonio; Silipo, Alba; Newman, Dianne K. (05 2018). “Hopanoid lipids: from membranes to plant-bacteria interactions”. Nature Reviews. Microbiology 16 (5): 304–315. doi:10.1038/nrmicro.2017.173. ISSN 1740-1534. PMC 6087623. PMID 29456243.
- ^ Tippelt, A.; Jahnke, L.; Poralla, K. (1998-03-30). “Squalene-hopene cyclase from Methylococcus capsulatus (Bath): a bacterium producing hopanoids and steroids”. Biochimica Et Biophysica Acta 1391 (2): 223–232. doi:10.1016/s0005-2760(97)00212-9. ISSN 0006-3002. PMID 9555026.
- ^ Poger, David; Mark, Alan E. (2013-12-19). “The relative effect of sterols and hopanoids on lipid bilayers: when comparable is not identical”. The Journal of Physical Chemistry. B 117 (50): 16129–16140. doi:10.1021/jp409748d. ISSN 1520-5207. PMID 24299489.
- ^ Schmerk, Crystal L.; Bernards, Mark A.; Valvano, Miguel A. (2011-12). “Hopanoid production is required for low-pH tolerance, antimicrobial resistance, and motility in Burkholderia cenocepacia”. Journal of Bacteriology 193 (23): 6712–6723. doi:10.1128/JB.05979-11. ISSN 1098-5530. PMC 3232912. PMID 21965564.
- ^ Welander, Paula V.; Hunter, Ryan C.; Zhang, Lichun; Sessions, Alex L.; Summons, Roger E.; Newman, Dianne K. (2009-10). “Hopanoids play a role in membrane integrity and pH homeostasis in Rhodopseudomonas palustris TIE-1”. Journal of Bacteriology 191 (19): 6145–6156. doi:10.1128/JB.00460-09. ISSN 1098-5530. PMC 2747905. PMID 19592593.
- ^ Poralla K, Muth G, Härtner T (2000). “Hopanoids are formed during transition from substrate to aerial hyphae in Streptomyces coelicolor A3(2)”. FEMS Microbiol Lett 189 (1): 93–5. doi:10.1111/j.1574-6968.2000.tb09212.x. PMID 10913872.
- ^ Berry A, Harriott O, Moreau R, Osman S, Benson D, Jones A (1993). “Hopanoid lipids compose the Frankia vesicle envelope, presumptive barrier of oxygen diffusion to nitrogenase”. Proc Natl Acad Sci USA 90 (13): 6091–4. Bibcode: 1993PNAS...90.6091B. doi:10.1073/pnas.90.13.6091. PMC 46873. PMID 11607408.
- ^ Silipo, Alba; Vitiello, Giuseppe; Gully, Djamel; Sturiale, Luisa; Chaintreuil, Clémence; Fardoux, Joel; Gargani, Daniel; Lee, Hae-In et al. (2014-10-30). “Covalently linked hopanoid-lipid A improves outer-membrane resistance of a Bradyrhizobium symbiont of legumes”. Nature Communications 5: 5106. doi:10.1038/ncomms6106. ISSN 2041-1723. PMID 25355435.
- ^ Doughty, D. M.; Hunter, R. C.; Summons, R. E.; Newman, D. K. (2009-12). “2-Methylhopanoids are maximally produced in akinetes of Nostoc punctiforme: geobiological implications”. Geobiology 7 (5): 524–532. doi:10.1111/j.1472-4669.2009.00217.x. ISSN 1472-4669. PMC 2860729. PMID 19811542.
- ^ a b Sohlenkamp, Christian; Geiger, Otto (2016-01). “Bacterial membrane lipids: diversity in structures and pathways”. FEMS microbiology reviews 40 (1): 133–159. doi:10.1093/femsre/fuv008. ISSN 1574-6976. PMID 25862689.
- ^ Pérez-Gil, Jordi; Rodríguez-Concepción, Manuel (2013-05-15). “Metabolic plasticity for isoprenoid biosynthesis in bacteria” (英語). Biochemical Journal 452 (1): 19–25. doi:10.1042/BJ20121899. ISSN 0264-6021. PMID 23614721.
- ^ Pan, Jian-Jung; Solbiati, Jose O.; Ramamoorthy, Gurusankar; Hillerich, Brandan S.; Seidel, Ronald D.; Cronan, John E.; Almo, Steven C.; Poulter, C. Dale (2015-05-27). “Biosynthesis of Squalene from Farnesyl Diphosphate in Bacteria: Three Steps Catalyzed by Three Enzymes”. ACS Central Science 1 (2): 77–82. doi:10.1021/acscentsci.5b00115. ISSN 2374-7943. PMC 4527182. PMID 26258173.
- ^ Pan, Jian-Jung; Solbiati, Jose O.; Ramamoorthy, Gurusankar; Hillerich, Brandan S.; Seidel, Ronald D.; Cronan, John E.; Almo, Steven C.; Poulter, C. Dale (2015-05-27). “Biosynthesis of Squalene from Farnesyl Diphosphate in Bacteria: Three Steps Catalyzed by Three Enzymes” (英語). ACS Central Science 1 (2): 77–82. doi:10.1021/acscentsci.5b00115. ISSN 2374-7943. PMC 4527182. PMID 26258173.
- ^ a b Siedenburg, Gabriele; Jendrossek, Dieter (2011-06-15). “Squalene-Hopene Cyclases” (英語). Applied and Environmental Microbiology 77 (12): 3905–3915. doi:10.1128/AEM.00300-11. ISSN 0099-2240. PMC 3131620. PMID 21531832.
- ^ a b Hoshino, Tsutomu; Sato, Tsutomu (2002-02-12). “Squalene–hopene cyclase: catalytic mechanism and substrate recognition” (英語). Chemical Communications (4): 291–301. doi:10.1039/B108995C. ISSN 1364-548X. PMID 12120044.
- ^ Syrén, Per-Olof; Henche, Sabrina; Eichler, Anja; Nestl, Bettina M.; Hauer, Bernhard (2016-12-01). “Squalene-hopene cyclases—evolution, dynamics and catalytic scope” (英語). Current Opinion in Structural Biology. Multi-protein assemblies in signaling • Catalysis and regulation 41: 73–82. doi:10.1016/j.sbi.2016.05.019. ISSN 0959-440X. PMID 27336183.
- ^ Dang, Tongyun; Prestwich, Glenn D. (2000-08-01). “Site-directed mutagenesis of squalene–hopene cyclase: altered substrate specificity and product distribution” (English). Chemistry & Biology 7 (8): 643–649. doi:10.1016/S1074-5521(00)00003-X. ISSN 1074-5521. PMID 11048954.
- ^ Rohmer, Michel; Anding, Claude; Ourisson, Guy (1980). “Non-specific Biosynthesis of Hopane Triterpenes by a Cell-Free System from Acetobacter pasteurianum” (英語). European Journal of Biochemistry 112 (3): 541–547. doi:10.1111/j.1432-1033.1980.tb06117.x. ISSN 1432-1033. PMID 7460938.
- ^ Perzl, Michael; Reipen, Ina G.; Schmitz, Susanne; Poralla, Karl; Sahm, Hermann; Sprenger, Georg A.; Kannenberg, Elmar L. (1998-07-31). “Cloning of conserved genes from Zymomonas mobilis and Bradyrhizobium japonicum that function in the biosynthesis of hopanoid lipids1EMBL accession number for the nucleotide sequence from Z. mobilis is AJ001401 and for the nucleotide sequence from B. japonicum, X86552.1” (英語). Biochimica et Biophysica Acta (BBA) - Lipids and Lipid Metabolism 1393 (1): 108–118. doi:10.1016/S0005-2760(98)00064-2. ISSN 0005-2760. PMID 9714766.
- ^ Bradley, Alexander S.; Pearson, Ann; Sáenz, James P.; Marx, Christopher J. (2010-10-01). “Adenosylhopane: The first intermediate in hopanoid side chain biosynthesis” (英語). Organic Geochemistry 41 (10): 1075–1081. doi:10.1016/j.orggeochem.2010.07.003. ISSN 0146-6380.
- ^ Liu, Wenjun; Sakr, Elias; Schaeffer, Philippe; Talbot, Helen M.; Donisi, Janina; Härtner, Thomas; Kannenberg, Elmar; Takano, Eriko et al. (2014). “Ribosylhopane, a Novel Bacterial Hopanoid, as Precursor of C35 Bacteriohopanepolyols in Streptomyces coelicolor A3(2)” (英語). ChemBioChem 15 (14): 2156–2161. doi:10.1002/cbic.201402261. ISSN 1439-7633. PMC 4245026. PMID 25155017.
- ^ a b Schmerk, Crystal L.; Welander, Paula V.; Hamad, Mohamad A.; Bain, Katie L.; Bernards, Mark A.; Summons, Roger E.; Valvano, Miguel A. (2015). “Elucidation of the Burkholderia cenocepacia hopanoid biosynthesis pathway uncovers functions for conserved proteins in hopanoid-producing bacteria” (英語). Environmental Microbiology 17 (3): 735–750. doi:10.1111/1462-2920.12509. ISSN 1462-2920. PMID 24888970.
- ^ a b Welander, Paula V.; Coleman, Maureen L.; Sessions, Alex L.; Summons, Roger E.; Newman, Dianne K. (2010-05-11). “Identification of a methylase required for 2-methylhopanoid production and implications for the interpretation of sedimentary hopanes” (英語). Proceedings of the National Academy of Sciences 107 (19): 8537–8542. doi:10.1073/pnas.0912949107. ISSN 0027-8424. PMC 2889317. PMID 20421508.
- ^ Welander, Paula V.; Summons, Roger E. (2012-08-07). “Discovery, taxonomic distribution, and phenotypic characterization of a gene required for 3-methylhopanoid production” (英語). Proceedings of the National Academy of Sciences 109 (32): 12905–12910. doi:10.1073/pnas.1208255109. ISSN 0027-8424. PMC 3420191. PMID 22826256.
- ^ Ricci, Jessica N; Coleman, Maureen L; Welander, Paula V; Sessions, Alex L; Summons, Roger E; Spear, John R; Newman, Dianne K (2014-03). “Diverse capacity for 2-methylhopanoid production correlates with a specific ecological niche” (英語). The ISME Journal 8 (3): 675–684. doi:10.1038/ismej.2013.191. ISSN 1751-7362. PMC 3930323. PMID 24152713.
- ^ Banta, Amy B.; Wei, Jeremy H.; Welander, Paula V. (2015-11-03). “A distinct pathway for tetrahymanol synthesis in bacteria” (英語). Proceedings of the National Academy of Sciences 112 (44): 13478–13483. doi:10.1073/pnas.1511482112. ISSN 0027-8424. PMC 4640766. PMID 26483502.
- ^ Ourisson, Guy; Albrecht, Pierre (1992-09). “Hopanoids. 1. Geohopanoids: the most abundant natural products on Earth?” (英語). Accounts of Chemical Research 25 (9): 398–402. doi:10.1021/ar00021a003. ISSN 0001-4842.
- ^ a b Summons, Roger E.; Lincoln, Sara A. (2012-03-30). Knoll, Andrew H.; Canfield, Donald E.; Konhauser, Kurt O.. eds. Fundamentals of Geobiology. Chichester, UK: John Wiley & Sons, Ltd. pp. 269–296. doi:10.1002/9781118280874.ch15. ISBN 978-1-118-28087-4
- ^ Knoll A H (2003). Life on a Young Planet: The first three billion years of evolution on the planet earth (1st ed.). Princeton University Press. ISBN 0-691-00978-3
- ^ Brocks J, Logan G, Buick R, Summons R (1999). “Archean molecular fossils and the early rise of eukaryotes”. Science 285 (5430): 1033–6. doi:10.1126/science.285.5430.1033. PMID 10446042.
- ^ Rashby, Sky E.; Sessions, Alex L.; Summons, Roger E.; Newman, Dianne K. (2007-09-18). “Biosynthesis of 2-methylbacteriohopanepolyols by an anoxygenic phototroph”. Proceedings of the National Academy of Sciences of the United States of America 104 (38): 15099–15104. doi:10.1073/pnas.0704912104. ISSN 0027-8424. PMC 1986619. PMID 17848515.
- ^ Talbot, Helen M.; Summons, Roger E.; Jahnke, Linda L.; Cockell, Charles S.; Rohmer, Michel; Farrimond, Paul (2008-02). “Cyanobacterial bacteriohopanepolyol signatures from cultures and natural environmental settings” (英語). Organic Geochemistry 39 (2): 232–263. doi:10.1016/j.orggeochem.2007.08.006.
- ^ French, Katherine L.; Hallmann, Christian; Hope, Janet M.; Schoon, Petra L.; Zumberge, J. Alex; Hoshino, Yosuke; Peters, Carl A.; George, Simon C. et al. (2015-05-12). “Reappraisal of hydrocarbon biomarkers in Archean rocks”. Proceedings of the National Academy of Sciences of the United States of America 112 (19): 5915–5920. doi:10.1073/pnas.1419563112. ISSN 1091-6490. PMC 4434754. PMID 25918387.
- ^ Brocks, Jochen J.; Love, Gordon D.; Summons, Roger E.; Knoll, Andrew H.; Logan, Graham A.; Bowden, Stephen A. (2005-10-06). “Biomarker evidence for green and purple sulphur bacteria in a stratified Palaeoproterozoic sea”. Nature 437 (7060): 866–870. doi:10.1038/nature04068. ISSN 1476-4687. PMID 16208367.
- ^ Gold, David A.; Caron, Abigail; Fournier, Gregory P.; Summons, Roger E. (03 16, 2017). “Paleoproterozoic sterol biosynthesis and the rise of oxygen”. Nature 543 (7645): 420–423. doi:10.1038/nature21412. ISSN 1476-4687. PMID 28264195.
- ^ Summons, Roger E; Bradley, Alexander S; Jahnke, Linda L; Waldbauer, Jacob R (2006-06-29). “Steroids, triterpenoids and molecular oxygen” (英語). Philosophical Transactions of the Royal Society B: Biological Sciences 361 (1470): 951–968. doi:10.1098/rstb.2006.1837. ISSN 0962-8436. PMC 1578733. PMID 16754609.
- ^ Santana-Molina, Carlos; Rivas-Marin, Elena; Rojas, Ana M; Devos, Damien P (2020-07-01). Ursula Battistuzzi, Fabia. ed. “Origin and Evolution of Polycyclic Triterpene Synthesis” (英語). Molecular Biology and Evolution 37 (7): 1925–1941. doi:10.1093/molbev/msaa054. ISSN 0737-4038. PMC 7306690. PMID 32125435.
- ^ a b Welander, Paula V. (08 20, 2019). “Deciphering the evolutionary history of microbial cyclic triterpenoids”. Free Radical Biology & Medicine 140: 270–278. doi:10.1016/j.freeradbiomed.2019.05.002. ISSN 1873-4596. PMID 31071437.
- ^ a b Ourisson, Guy; Albrecht, Pierre; Rohmer, Michel (1982-07). “Predictive microbial biochemistry — from molecular fossils to procaryotic membranes” (英語). Trends in Biochemical Sciences 7 (7): 236–239. doi:10.1016/0968-0004(82)90028-7.
- ^ Fischer, W. W.; Pearson, A. (2007-02-09). “Hypotheses for the origin and early evolution of triterpenoid cyclases” (英語). Geobiology 0 (0): 070210031741002–???. doi:10.1111/j.1472-4669.2007.00096.x. ISSN 1472-4677.
- ^ Hammer, Stephan C.; Marjanovic, Antonija; Dominicus, Jörg M.; Nestl, Bettina M.; Hauer, Bernhard (February 2015). “Squalene hopene cyclases are protonases for stereoselective Brønsted acid catalysis” (英語). Nature Chemical Biology 11 (2): 121–126. doi:10.1038/nchembio.1719. ISSN 1552-4469. PMID 25503928.
- ^ (英語) Hopanoids producing bacteria and related biofertilizers, compositions, methods and systems, (2016-10-19) 2020年5月15日閲覧。
- ^ a b Sáenz, James P.; Grosser, Daniel; Bradley, Alexander S.; Lagny, Thibaut J.; Lavrynenko, Oksana; Broda, Martyna; Simons, Kai (2015-09-22). “Hopanoids as functional analogues of cholesterol in bacterial membranes” (英語). Proceedings of the National Academy of Sciences 112 (38): 11971–11976. doi:10.1073/pnas.1515607112. ISSN 0027-8424. PMC 4586864. PMID 26351677.
