「リボ核酸」の版間の差分
Anesth Earth (会話 | 投稿記録) {{Template:Genetics sidebar}} |
m Robot: ウィキ文法修正 1: Template contains useless word template |
||
| 1行目: | 1行目: | ||
{{Redirect|RNA}}{{ |
{{Redirect|RNA}}{{Genetics sidebar}} |
||
'''リボ核酸'''('''RNA''': Ribonucleic acid)は、[[リボース]]を糖成分とする'''[[核酸]]'''である。[[リボヌクレオチド|'''リボ'''ヌクレオチド]]が多数重合したもので、一本鎖をなし、[[アデニン]]、[[グアニン]]、[[シトシン]]、[[ウラシル]]の四種の[[塩基]]を含む。 一般に[[デオキシリボ核酸|DNA]](デオキシリボ'''核酸''')を[[鋳型]]として合成され、その遺伝情報の伝達や[[タンパク質]]の合成を行う。 |
'''リボ核酸'''('''RNA''': Ribonucleic acid)は、[[リボース]]を糖成分とする'''[[核酸]]'''である。[[リボヌクレオチド|'''リボ'''ヌクレオチド]]が多数重合したもので、一本鎖をなし、[[アデニン]]、[[グアニン]]、[[シトシン]]、[[ウラシル]]の四種の[[塩基]]を含む。 一般に[[デオキシリボ核酸|DNA]](デオキシリボ'''核酸''')を[[鋳型]]として合成され、その遺伝情報の伝達や[[タンパク質]]の合成を行う。 |
||
2024年4月28日 (日) 23:59時点における最新版
| 遺伝学 |
|---|
 |
リボ核酸(RNA: Ribonucleic acid)は、リボースを糖成分とする核酸である。リボヌクレオチドが多数重合したもので、一本鎖をなし、アデニン、グアニン、シトシン、ウラシルの四種の塩基を含む。 一般にDNA(デオキシリボ核酸)を鋳型として合成され、その遺伝情報の伝達やタンパク質の合成を行う。
歴史
[編集]核酸は1868年(一説によると1869年)にフリードリッヒ・ミーシャーにより発見された。細胞核内から発見されたため、核酸と命名された。その後、核を持たない原核生物からも核酸が発見されたが、名称が変わることはなかった。1939年、Torbjörn Caspersson、Jean Brachet、Jack Schultz らによりRNAがタンパク質合成に関与しているという説が提唱された。その後 Hubert Chantrenne はRNAがリボソームに対してタンパク質情報を伝達するという役割があることを解明した。1964年にはロバート・W・ホリーが出芽酵母の tRNA の配列と構造を解明し、1968年にノーベル生理学賞を受賞した。1976年にはバクテリオファージMS2のレプリカーゼ遺伝子のRNA配列が決定された[1]。
構造
[編集]核酸塩基
[編集]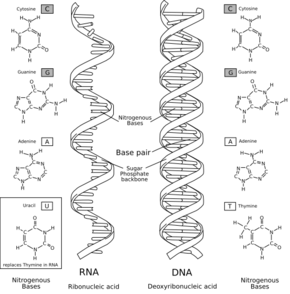
RNAの核酸塩基はアデニン (A)、グアニン (G)、シトシン (C)、ウラシル (U) の4種で構成されている。アデニン、グアニン、シトシンは DNA にも同じ構造が見られるが、DNAにおけるチミン (T) がRNAではウラシルに置き換わっており、相補的な塩基はアデニンとなる。チミンとウラシルは共にピリミジン環を持つ非常に似た塩基である。
シトシンが化学分解されるとウラシルが生成されてしまうため、DNAではウラシルの代わりにチミンが用いられるようになった。これによりシトシンの分解により誤って生成してしまったウラシルを検出し、修復することが可能になるなどの利点が生じた。
修飾RNA
[編集]主に生化学において、生体高分子の特定の官能基をメチル化やアセチル化などで変化させ、機能を活性や反応性を変化させることを「化学修飾」(あるいは単に「修飾」)という[2]。RNAには修飾がなされた様々な修飾RNAが存在し、それぞれが異なる役割を持つ。シュードウリジン(プソイドウリジン, en:Pseudouridine, Ψ)や2'-O-メチル化修飾は比較的多く見られる修飾である。リボチミジン(T, rT)、シュードウリジン(Ψ)はtRNAのTΨCループによく見られる。アデノシンが脱アミノ化されたイノシン (I) は、RNAエディティングにより生ずるものとtRNAの部位特異的に生ずるものが知られ、グアノシンに似た性質を持つ。他にも約100種の修飾塩基が存在しているが、全容は解明されていない。
プラス鎖RNAとマイナス鎖RNA
[編集]RNAは通常一本の鎖状に連なるポリヌクレオチドであり[3]、RNA鎖上に遺伝子コードがあるものをプラス鎖RNA、相補的なRNA鎖にコードが現れるものをマイナス鎖RNAと呼ぶ。
一本鎖のRNAは自由度が高く高次構造を形成する。
官能基
[編集]RNAの構造的特徴として、DNAには存在しない 2'位のヒドロキシ基が存在するというものがある。
DNAとの比較
[編集]DNAとRNAはともにヌクレオチドの重合体である核酸であるが、両者の生体内の役割は明確に異なっている。DNAは主に核の中で情報の蓄積・保存、RNAはその情報の一時的な処理を担い、DNAと比べて、必要に応じて合成・分解される頻度は顕著である。DNAとRNAの化学構造の違いの意味することの第一は「RNAはDNAに比べて不安定である」。両者の安定の度合いの違いが、DNAは静的でRNAは動的な印象を与える。
化学構造の相違
[編集]DNAとRNAの化学構造の違いの第一は、ヌクレオチド中の糖は、RNAはリボースで、DNAは2'位の水酸基が水素で置換された2'-デオキシリボースである点にある。このため、DNAではリボースがC2'-エンド型構造を取るが、RNAでは2'位のヒドロキシ基の存在により立体障害が生じ、リボースがC3'-エンド型構造を取る。これに伴って、DNAはB型らせん構造を取りやすく、RNAはA型らせん構造を取りやすくなるという違いが生じる。この結果RNAのらせん構造はメジャーグルーブが深く狭くなり、マイナーグルーブが浅く広くなる。らせん構造についての詳細は、記事二重らせんに詳しいものが載っている。
DNAと比較すると、RNAは一般に不安定である。RNAに存在する2'位水酸基の酸素には孤立電子対が2つあるため、例えば、塩基性条件下、隣接したリン酸は水酸基から求核攻撃を受け、ホスホジエステル結合が切れ、主鎖が開裂するなどDNAと比べて不安定である。この特性から、翻訳の役割を終えたmRNAを直ちに分解することが可能になる(バクテリアでは数分、動物細胞でも数時間後には分解される)。安定RNAでは1本鎖に水素結合を形成し、らせん構造となるなど、多様な二次構造、三次構造を取り、安定性を増している。
構成する塩基にも違いがある。RNAを構成する塩基はA、C、G、Uの4種だが、大多数の生物のDNAではUの代わりにTが用いられる。これは配列情報の同一性を保持するためと考えられる。
というのも、塩基Cは脱アミノ化という反応によってUに変化することがある。最初からUだったものとCから変異したUは(1本鎖のRNAであれば)区別不可能で、元の配列が分からなくなってしまう。これに対しDNAで用いられる塩基Tは、分子の構造的にUに自然に変わることは容易には起こらないので、Uを本来含んでいないDNAであればCが脱アミノ化を起こしても容易に認識できる。以上のことから、Uの代わりにTを用いる方が有利なのでDNAではそれが一般的になったと考えられる。
物理化学的性質の相違
[編集]DNAとRNAの物理化学的性質について。DNAとRNAはともに紫外線である波長260nm付近に吸収極大を持ち、230nm付近に吸収極小を持つ。この吸光度はタンパク質の280nmよりもずっと大きいが、これはDNAとRNAがプリンまたはピリミジンを塩基として有するためである。ただし、二重らせんを形成しているDNAの場合、溶液を加熱するとその吸光度は増す(濃色効果)。これは、DNAは規則正しい2重らせん構造を有しているため、全体の吸光度が個々の塩基の吸光度の総和より小さい(淡色効果)が、加熱により2重らせん構造が解け(核酸の変性)、個々の塩基が自由になり、独自に光を吸収するためである。また、DNAとRNAはアルカリ溶液中で挙動が異なる。RNAは弱塩基でも容易に加水分解するが、DNAは安定して存在する。
生合成
[編集]RNAは転写という作用によって合成される。転写は専らDNAを鋳型として行われ、そこには複数の酵素が関与する。
DNAを基に転写が行われる場合、DNAヘリカーゼという酵素が2本鎖を一時的に1本鎖に分割し、その1本鎖にRNAポリメラーゼという別の酵素が結合することでDNAに相補的なRNAが合成される。
RNAを鋳型とするRNAポリメラーゼも存在する。例えば、ある種のRNAウイルス(ポリオウイルスなど)はこのようなタイプのRNAポリメラーゼを用いて、自らの持つRNAを増幅させる。また多くの生命体では、この種のRNAポリメラーゼがRNA干渉に必要だということが知られている。
鋳型となる塩基配列には、RNAの合成をどこから始めてどこで終えるかの目印が存在する(プロモーター・ターミネーター)。
生化学的な活性
[編集]伝令RNA (mRNA)
[編集]伝令RNAは、メッセンジャーRNA、mRNAとも呼ばれ、細胞中でタンパク質合成部位であるリボソームにDNAの情報を伝える役割をするRNAである。遺伝情報をもとにタンパク質が合成される場合には、RNAポリメラーゼの働きにより、DNAに対して相補的な配列を持つmRNAが転写され、次にリボソームにより、mRNAの配列に基づいたタンパク質の合成が行われる(翻訳)。このように、DNAがいったんRNAへと転写され、RNAを鋳型としてタンパク質への翻訳が行われるという、一連の遺伝情報の流れをセントラルドグマと呼ぶ。セントラルドグマはタンパク質が遺伝子産物であることを前提としているため、ノンコーディングRNA遺伝子の場合には当てはまらないと解釈されている。一定の時間が経過すると、mRNAはRNA分解酵素の働きによりヌクレオチドへと分解される。多くの場合、mRNAは短命であるが(大腸菌では約5分ともいわれている)、哺乳類の精子中に見られるように、極端に安定なmRNAも知られている。
運搬RNA (tRNA)
[編集]運搬RNAは、トランスファーRNA、tRNAとも呼ばれ、タンパク質を合成する翻訳の際に、特定のアミノ酸をリボソーム内部へと導入するRNAである。74-93塩基からなる短いRNA鎖である。アミノ酸結合部位と、mRNAのコドンと水素結合を作るためのアンチコドン部位を持つ。非コードRNA(下記参照)の一種である。
リボソームRNA (rRNA)
[編集]リボソームRNA (rRNA) は、細胞内でタンパク質合成を行うリボソームを構成しているRNAである。真核生物のリボソームのrRNAは4本のRNA鎖 (18S, 5.8S, 28S, 5S) から構成されている。このうちの3つは核小体で合成され、残りの1つは他の部位で合成される。rRNAは非常に大量に存在する種のRNAであり、典型的な真核細胞に存在するRNAの少なくとも80%がrRNAとして存在している(tRNA: 10数%、mRNA: 数%)。
ノンコーディングRNA (ncRNA)
[編集]ノンコーディングRNA (ncRNA) は、タンパク質に翻訳されないRNAの総称である。最も有名なものとしては、前述の運搬RNAとリボソームRNAが挙げられる。この2つはどちらも翻訳に関連しているが、1990年代後半からは新しいタイプのノンコーディングRNAの発見が相次ぎ、ノンコーディングRNAは以前に考えられていたよりも重要な役割を果たしている可能性があると考えられるようになった。
1990年代後半から2000年代前半にかけて、ヒトをはじめとする高等生物の細胞では複雑な転写が行われている証拠が得られてきた。これは生物学においてRNAがより広い領域で、特に遺伝子発現の調節に用いられているという可能性を指摘するものであった。特にノンコーディングRNAの一種であるマイクロRNA (miRNA) は、線虫からヒトに至るまでの多くの後生動物で見られ、他の遺伝子の制御といった重要な役割を果たしていることが明らかにされた。
2004年にRassoulzadeganのグループは、RNAが生殖細胞系に何らかの影響を及ぼしているという説をNature誌に投稿した。これが実際に確認されれば、従来の遺伝学に大きな影響を与え、DNA-RNAの役割や相互作用に関する多くの謎が解明されると考えられている。2015年、ペンシルバニア大学のTracy L. Baleらは、精子中のマイクロRNAの発現量が子に伝わり、父の獲得形質が子に受け継がれることを明らかにした[4]。彼女らは、オスのマウスに過度なストレスを与えて、そのマウスをメスのマウスと交配させた。生まれたマウスに過度なストレスを与えたところ、ストレスに対する耐性が父のマウスよりも高くなっていた。彼女らは、その原因としてマイクロRNAを挙げた。彼女らは父のマウスの精子中のマイクロRNAの発現量が増加していることを発見し、このマイクロRNAが受精卵内のmRNAを破壊している事実を明らかにした。これらのことは、父が獲得した形質がマイクロRNAを通して子に伝わることを示唆している。
触媒作用を持つRNA
[編集]タンパク質によく用いられる20種のアミノ酸と比較すると、RNAは4つの核酸塩基しか持たないにもかかわらず、ある種のRNAは酵素活性を持っており、それらはリボザイム (ribozyme = ribose + enzyme) と呼ばれている。RNA鎖の切断や結合を行うRNA触媒も存在しており、ペプチド鎖の合成を行うリボソーム中でもRNAが触媒活性中心となっている。
二重鎖RNA (dsRNA)
[編集]二重鎖RNA (dsRNA) は、2本の相補的な配列を持つRNA鎖がDNAに見られるような二重鎖を組んだものである。dsRNAはある種のRNAウイルスの持つ遺伝情報部位やミトコンドリアDNA内のrRNA、tRNAなどに見られる。真核生物ではRNA干渉の引き金となったり、siRNA生成の中間体となっている(siRNAはmiRNAとしばしば混同される。siRNAは二重鎖であるが、miRNAは1本鎖である)。未成熟miRNAなどでは、1本鎖であっても分子内でヘアピン構造を取る部分が存在している。
RNAワールド仮説
[編集]RNAワールド仮説は、生命が発生した頃にはRNAが遺伝情報の維持(現在のDNAの役割)と、酵素のような生化学的触媒の両方の役割を担っていたとする仮説である。これは無生物的な環境下に於いてRNAがDNAと比較して容易に合成されることなどを根拠としている。
この仮説では生物は遺伝情報(ゲノム)の貯蔵媒体としてRNAを使用し、その後の変異と進化によりDNAとタンパク質が徐々に台頭してきたと考えられている。ただしRNAはDNAと違って相補性が確保されておらず、修飾を受けやすい不安定な分子であり、生物においてゲノムを安定に保持する機能は主にDNAが担っている。一方で、非生物の特性を併せ持つウイルスでは、ゲノムを持つRNAウイルスとしては、プラス鎖のもの(コロナウイルスなど)とマイナス鎖のもの(インフルエンザウイルスなど)の両方が見つかっている。現時点(2006年)では、ゲノムの保持にDNAではなくてRNAを用いているのはウイルスだけであると考えられている(ウイルスにはゲノムの保持媒体にRNAを用いているものとDNAを用いているものの2種類がある)。
RNAの高次構造
[編集]機能性の1本鎖RNAは、タンパク質と同じように特別な三次構造を取ることが要求される。三次構造の形成では、水素結合が駆動力となっている。二次構造で表現可能な「部位」として、ヘアピンループやバルジ、インターナルループなどが存在する。RNAの二次構造は水素結合部位やドメインなどの組み合わせを自由エネルギーについて計算し、コンピューターである程度予測することができる。
RNA干渉
[編集]RNAi(RNA interfernce、RNA干渉)とはsiRNA(small interfering RNA)または二本鎖RNA(double stranded RNA、dsRNA)によって配列特異的に遺伝子の発現が抑制される現象である。
哺乳類のRNAiのメカニズム
[編集]二本鎖RNA(double stranded RNA、dsRNA)はDicerと呼ばれるRNase III酵素によって約21〜25塩基長の短鎖二本鎖RNAに切断される。この短鎖二本鎖RNA断片をsiRNA(small interfering RNA)とよぶ。そのsiRNA二量体はRISC (RNA-induced silencing complex)と呼ばれるArgonaute(Ago)タンパク質を含む複合体に取り込まれる。その後、ターゲットとなるmRNAと塩基対合するsiRNA(ガイド鎖)を残し、その反対鎖であるパッセンジャー鎖はAgoタンパク質によって切断され分解される。残ったガイド鎖の5’末端と3’末端の1塩基はAgoタンパク質のポケット構造にはまり込んで固定される。特に5’末端がアデニンまたはウラシルである場合にはAgoタンパク質と高い親和性固定される。さらに、5’末端から2〜8塩基目の塩基はAgoタンパク質の構造と電荷をうまく利用して表面に載ることができる。この2〜8塩基目の塩基の部分はシード配列と呼ばれ、塩基配列の相補性をもつmRNAを識別し、最初に塩基対合する場所である。その後、siRNAは残りの9〜20塩基目もターゲットとなるmRNAと塩基対合する。塩基対合したmRNAはAgoタンパク質によって切断される。この過程を遺伝子ノックダウンという。
- Dicer
DicerはdsRNAをsiRNAへと、またはpre-miRNAをmiRNAへと切断するRNase III酵素である。
- RISC
RISC(RNA-induced silencing complex)はショウジョウバエにおいてdsRNAを導入することによって誘導される配列特異的に標的RNAを分解する活性をもった複合体としてHannonらによって提唱された。RISCの中核となるのはArgonaute(Ago)タンパク質である。その他の構成要素としてRNA結合タンパク質、RNAヘリカーゼ、ヌクレアーゼなど様々なタンパク質が同定されている。
siRNAとmiRNA
[編集]短鎖RNAは由来によって名称が異なる。人工的に作られたものやin vivoでdsRNA前駆体から生じたものはsiRNAという。miRNAは遺伝子から作られる前駆体RNAに由来する。この遺伝子が発現する細胞内で特定の遺伝子調節機能を発揮する。miRNAはmiRNA遺伝子から長い一次転写産物であるpri-miRNAとして転写される。pri-miRNAの中には将来miRNAとなる配列が含まれておりその部分はヘアピン状の高次構造をとっている。DroshaというRNase III酵素がヘアピン構造を切断しpre-miRNAにする。核内のpre-miRNAはExportin-5によって細胞質に運ばれ細胞質でDicerによってpre-miRNAは切断されmiRNAとなる。miRNAはRISCを形成し、標的RNAを認識するガイド分子として働く。このようにsiRNAもmiRNAも21塩基前後の長さの機能性ncRNAであり、RISCの中のsiRNAとmiRNAを化学組成や機能で見分けることはできず、あくまで由来で分類する。
RNAiの問題点
[編集]- オフターゲット効果
ターゲット遺伝子に対する抑制効果に加えてシード領域のみが対合した遺伝子群もオフターゲット効果と呼ばれる機構によって抑制される場合が多い。オフターゲット効果ではmRNAは切断されるのではなく、翻訳が抑制されることによって遺伝子機能が抑制されると考えられている。
- インターフェロン応答
哺乳動物細胞に30bp以上の長いdsRNAを導入すると一部の細胞集団を除いてほとんどの細胞で細胞死が起こる。これはインターフェロン応答または抗ウイルス反応とよばれるディフェンス機構と考えられている。
存在
[編集]リボヌクレオチドおよびその結合体であるポリヌクレオチド、DNA・RNAなどのリボ核酸は、生物を原料とするほとんどの食品に微量含まれている。重量比では、酵母(Baker's yeast/Saccharomyces cerevisiae)や海苔(Purple laver)などでリボ核酸の検出値が比較的高い。[5]
経口摂取と産業利用
[編集]リボ核酸を摂取すると、体内でいったんヌクレオチドに分解されて、DNA・RNAを合成する材料となる。核酸摂取と核酸合成との関係は未解明な点が多く今後の研究が待たれる。
RNAを多量に含む食品が商業的に生産されている。RNAを効率的に分離するためのRNA源としてビール酵母などの酵母が利用されている[6]。
利用例
[編集]- 健康食品
- 健康食品として錠剤や粉末のものが市販されている。
- 食品添加物
- 母乳にはウリジル酸などの各種ヌクレオチドとDNA・RNAが含まれ、乳児の免疫調節や記憶力の向上に役立っていると考えられており、市販の乳児用粉ミルクの多くにヌクレオチドの形で添加されている[7][8]。最近ではRNAの形で添加する例もあり、総称して核酸関連物質と表示されている場合がある。
脚注
[編集]出典
[編集]- ^ Fiers W et al., Complete nucleotide-sequence of bacteriophage MS2-RNA - primary and secondary structure of replicase gene, Nature, 1976, 260, 500-507.
- ^ 「化学修飾」『化学辞典 第2版』。コトバンクより2020年7月9日閲覧。
- ^ “RNAの特徴”. 医学生物学研究所. 2020年3月18日閲覧。
- ^ Ali B. Rodgers, Christopher P. Morgan, N. Adrian Leu, and Tracy L. Bale. Transgenerational epigenetic programming via sperm microRNA recapitulates effects of paternal stress. Proceedings of the National Academy of Sciences 112.44 (2015): 13699-13704.
- ^ “Nucleic Acid Contents of Japanese Foods”. NIPPON SHOKUHIN KOGYO GAKKAISHI 36 (11): Table 2. (1989). doi:10.3136/nskkk1962.36.11_934.
- ^ リボ核酸|エル・エスコーポレーション
- ^ Schaller, Joseph P.; Kuchan, Matthew J.; Thomas, Debra L.; Cordle, Christopher T.; Winship, Timothy R.; Buck, Rachael H.; Baggs, Geraldine E.; Wheeler, J. Gary (2004-12). “Effect of Dietary Ribonucleotides on Infant Immune Status. Part 1: Humoral Responses” (英語). Pediatric Research 56 (6): 883–890. doi:10.1203/01.PDR.0000145576.42115.5C. ISSN 1530-0447.
- ^ Buck, Rachael H.; Thomas, Debra L.; Winship, Timothy R.; Cordle, Christopher T.; Kuchan, Matthew J.; Baggs, Geraldine E.; Schaller, Joseph P.; Wheeler, J. Gary (2004-12). “Effect of Dietary Ribonucleotides on Infant Immune Status. Part 2: Immune Cell Development” (英語). Pediatric Research 56 (6): 891–900. doi:10.1203/01.PDR.0000145577.03287.FA. ISSN 1530-0447.
関連項目
[編集]外部リンク
[編集]- 核酸 (DNA, RNA) - 素材情報データベース<有効性情報>(国立健康・栄養研究所)
- 生命起源の鍵?自己複製できる最小のRNAを早稲田大/東大が発見 (PC Watch, 2023年7月5日)
