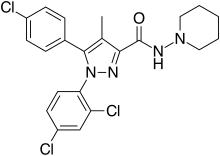
リモナバン
 | |
 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| Drugs.com |
患者向け情報(英語) Consumer Drug Information |
| ライセンス | EMA:リンク |
| 胎児危険度分類 |
|
| 法的規制 | |
| 薬物動態データ | |
| 生物学的利用能 | Undetermined |
| 血漿タンパク結合 | Nearly 100% |
| 代謝 | Hepatic, CYP3A4 involved |
| 半減期 | Variable: 6 to 9 days with normal BMI 16 days if BMI >30 |
| 排泄 | Fecal (86%) and renal (3%) |
| データベースID | |
| CAS番号 |
168273-06-1 158681-13-1 |
| ATCコード | A08AX01 (WHO) |
| PubChem | CID: 104850 |
| IUPHAR/BPS | 743 |
| DrugBank |
DB06155 |
| ChemSpider |
94641 |
| UNII |
RML78EN3XE |
| KEGG |
D05731 |
| ChEMBL |
CHEMBL111 |
| 化学的データ | |
| 化学式 | C22H21Cl3N4O |
| 分子量 | 463.79 g·mol−1 |
| |
リモナバン(リモナバント, 英語: Rimonabant, SR141716)は、選択的なカンナビノイド受容体タイプ1の拮抗薬で、食欲抑制剤または抗肥満薬 である。
かつての製品名はアコンプリア(Acomplia)やスリモナ(Slimona)。
歴史
[編集]2006年に欧州各国で承認されたが、2008年に自殺企図など動面での副作用によって市場から撤退した[3]。日本を含め、進行していた治験は中止された[3]。
欧州の規制当局が神経精神的な副作用を容認できないと判断したため心血管イベント予防の臨床試験でフォローアップ(投与中止後)平均13.8か月目に試験が中止された。リモナバン群とプラセボ群の有害事象は、精神神経系が32%:21%で、自殺既遂が4例:1例(有意差不明)であった[4][5][6][7]。
薬理
[編集]体内にある内因性のカンナビノイドは、食欲を司るカンナビノイド受容体タイプ1に作用することで食欲を起こす。 リモナバンは逆にこれに拮抗して食欲を抑制する。逆に、大麻の成分であるテトラヒドロカンナビノール (THC) は、ここに作用することで食欲を起こす。
アデニリルシクラーゼの活性を阻止し、輸精管の収縮を抑える[8]。
有効性
[編集]食事療法と併行し1年間継続的に服用した結果、5%の体重減少が約50%の頻度で、10%の体重減少が約27%の頻度でみられたとの報告がある[9]。偽薬群は、5%の体重減少が19.7%の頻度で、10%の体重減少が7.8%の頻度であった[9]。
副作用
[編集]英国の1998から2011年の有害事象報告では、うつ病の報告数と自殺未遂の割合が2番目に多かった[10]。リモナバンの自殺既遂はランク外で目立っていない。サノフィ社による市販後調査において、約1-10%の頻度で抑うつが、約1%の頻度で自殺企図が、自発報告されていた[11]。
禁忌
[編集]うつ病患者あるいは抗うつ薬を服用している人への投与は禁忌となっている。さらに、本薬は母乳中へ移行することが動物実験で示されており、授乳期の母親への投与は禁忌である。
また、ケトコナゾール、イトラコナゾールなどの抗真菌薬、テリスロマイシンやクラリスロマイシンなどの抗菌薬といった肝臓のCYP3A4阻害薬との併用はリモナバンの効果を増幅するので、注意を要する。
出典
[編集]- ^ Sam, AH; Salem, V; Ghatei, MA (2011). “Rimonabant: From RIO to Ban.”. Journal of Obesity 2011: 432607. doi:10.1155/2011/432607. PMC 3136184. PMID 21773005.
- ^ Moreira, FA; Crippa, JA (June 2009). “The psychiatric side-effects of rimonabant.”. Revista Brasileira de Psiquiatria 31 (2): 145–53. doi:10.1590/s1516-44462009000200012. PMID 19578688.
- ^ a b 綿引智成「カンナビノイド系を標的とした医薬品開発状況」『ファルマシア』第52巻第9号、2016年9月、850-854頁、doi:10.14894/faruawpsj.52.9_850。
- ^ “Rimonabant for prevention of cardiovascular events (CRESCENDO): a randomised, multicentre, placebo-controlled trial”. Lancet 376 (9740): 517–23. (2010). doi:10.1016/S0140-6736(10)60935-X. PMID 20709233.
- ^ “Rimonabant: suicide and depression. Depression and suicidal tendencies are about twice as frequent with rimonabant as with placebo”. Prescrire Int 16 (92): 250. (2007). PMID 18092422.
- ^ “Rimonabant: depression and suicide”. Prescrire Int 18 (99): 24. (2009). PMID 19391291.
- ^ “Concerns over participant suicides prematurely abort a clinical trial of potentially significant impact on public health: how will we make progress in timid times?”. Curr Psychiatry Rep 13 (2): 80–1. (2011). doi:10.1007/s11920-011-0179-1. PMC 3069144. PMID 21267679.
- ^ Rimonabant | CAS:168273-06-1 (2016-2-26) - Funakoshi フナコシ株式会社 2016年10月06日閲覧
- ^ a b Sanofi-Aventis. Acomplia prescription information. HTML(2007年9月28日時点のアーカイブ)2016年10月01日閲覧
- ^ Thomas KH, Martin RM, Potokar J, Pirmohamed M, Gunnell D. (2014-9-30). “Reporting of drug induced depression and fatal and non-fatal suicidal behaviour in the UK from 1998 to 2011.”. BMC Pharmacology and Toxicology. 15 (54). doi:10.1186/2050-6511-15-54. PMC 4184159. PMID 25266008.
- ^ Sanofi-Aventis. Increased frequency of reports of depression in patients treated with Acomplia. PDF(2007年9月28日時点のアーカイブ)2016年10月01日閲覧
