ボツリヌストキシン
 | |
| 臨床データ | |
|---|---|
| 法的規制 |
|
| データベースID | |
| CAS番号 | 93384-43-1 |
| ATCコード | M03AX01 (WHO) |
| PubChem | CID: 5485225 |
| DrugBank | BTD00092 |
| 化学的データ | |
| 化学式 | |
| 分子量 | 149.320 kDa |

ボツリヌストキシン(Botulinum toxin (BTX) or Botox)は、分子量が15万ほどのタンパク質で、ボツリヌス菌が産生する複合体毒素である。ボツリヌス毒素とも呼ばれる。毒素産生菌は、毒素型によりA,B,C,D,E,F,G の7種類に大別されているが、産生される毒素も抗原性の違いによりA,B,C,D,E,F,G の7種類に分けられている。医薬品としては筋肉を収縮させないよう働く作用を利用して、痙縮の緩和や美容に用いられる。
概要
[編集]ヒトでは、A,B,E,F型毒素で中毒を発生する事が多く、鳥類と哺乳類では C,D型毒素で中毒する事が多い[1]。毒素が含まれる食品の喫食はボツリヌス菌食中毒の原因となり、極めて毒性が強い(致死量:ヒトに対しA型毒素を経口投与した場合、体重1kgあたりの致死量が1μg[2] と推定されている。マウスに対する最小致死量 (MLD) は 0.0003 μg/kg[3]。)。毒素としては、破傷風菌が産生するテタノスパスミンをも上回る毒性を持つと言われている。しかし、100℃で10分間[4]加熱するかアルカリで処理すると失活して毒性がなくなるため、十分加熱すれば安全である(ただし、ボツリヌス菌の芽胞は耐熱性を持つ)。ボツリヌストキシンは毒素の抗原性の違いによりA~G型に分類されるが、サルへの経口投与によるデータではB型毒素への感受性が最も高い。
ボツリヌストキシンは神経筋接合部などでアセチルコリンの放出を妨げる働きをするが、作用は末梢性に限られる。中毒症状としては、消化器症状(下痢・悪心・嘔吐など、ただし毒素の作用ではない[要説明])に続き、めまい・頭痛や視力低下・複視などを起こし、その後自律神経障害、四肢麻痺に至る。
中毒患者は、ギラン・バレー症候群と誤診される場合があるが、脳脊髄液の検査で判別できる。
発見・研究史
[編集]1895年にエミール・ヴァン・エルメンゲムが毒素を発見し、1897年にウォルター・ケンプナーによってエルメンゲムの発見した毒素に対する血清が発明された。しかし1910年にダルムシュタットで起こったシロインゲンマメの缶詰めによる食中毒でエルメンゲムの発見した毒素とは別の毒素が検出され、これ以降発見順にA型・B型・C型・・・・・と区別される様になった。1946年にはA型毒素の単結晶化が報告されている。
日本では獣医学者、細菌学者の阪口玄二が構造決定に大きく貢献した[5][6]。
作用メカニズム
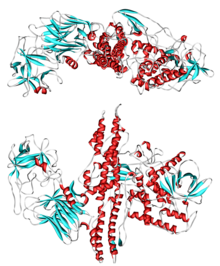
[編集]ボツリヌストキシンは、分子量約15万のタンパク質であり、細胞外に分泌された後に、菌自身のプロテアーゼまたは動物消化管のトリプシンによって、分子量約5万の活性サブユニット(Aサブユニット、軽鎖)と、約10万の結合サブユニット(Bサブユニット、重鎖)とに切断される[7]。この両者がジスルフィド結合によって一分子ずつ結合した、AB型毒素に分類される細菌外毒素である。活性サブユニットが、毒素の本体である亜鉛結合性の金属プロテアーゼであり、結合サブユニットは標的となる神経細胞表面に特異的に存在する特定のタンパク質(毒素受容体となる)との結合に関与する。
体内に取り込まれた毒素が神経筋接合部に到達すると、神経細胞側の細胞膜(シナプス前膜)に存在する毒素受容体タンパク質と、毒素の結合サブユニットが結合する。結合した毒素はエンドサイトーシスによって、分泌小胞様の小胞の内部に取り込まれ、神経細胞内でこの小胞の内部が酸性化すると、サブユニットが切断されて、細胞質内に活性サブユニットが遊離する。
神経細胞の内部には、アセチルコリンなどの神経伝達物質を内包する、脂質二重膜で覆われたシナプス小胞が存在する。神経細胞が興奮すると、このシナプス小胞がシナプス側の細胞膜の方に移動し、細胞膜と膜融合を起こすことで、小胞内部の神経伝達物質がシナプス間隙に放出される。この膜融合には、シナプス小胞の表面のシナプトブレビン (VAMP/Synaptobrevin)、細胞膜側にある、シンタキシン (Syntaxin) およびSNAP-25という、SNAREタンパク質とよばれる3つのタンパク質が関与しており、この3つが会合することによって膜融合と、神経伝達物質の放出が行われている。
細胞質に遊離したボツリヌストキシンの活性サブユニットは、この3つのSNAREタンパク質を標的として特異的に切断し、破壊してしまう。SNAREタンパク質のいずれかが破壊されると、シナプス小胞と細胞膜の膜融合が起こらなくなり、神経伝達物質の放出が阻害される結果、神経伝達が遮断される。これがボツリヌストキシンの作用メカニズムである。ボツリヌストキシンが標的とするタンパク質は、毒素の種類によって異なっており、B,D,F,G型毒素はシナプトブレビンを、A,E型毒素はSNAP-25を、C型毒素はSNAP-25とシンタキシンを、それぞれ切断する[8]。
この、神経細胞のSNAREタンパク質を標的に切断するという機構は、同じクロストリジウム属である破傷風菌の毒素(テタノスパスミン)と共通の機構であるが、ボツリヌストキシンの作用は神経筋接合部に限られるのに対して、テタノスパスミンはより上位の神経に到達して作用する。これは神経細胞内に取り込まれる際、受容体タンパク質の違いによって、取り込まれる小胞の種類に差があるからだと考えられている[9]。それぞれの受容体タンパク質の全容は明らかではないが、ボツリヌストキシンではシナプトタグミンと呼ばれる、シナプス前膜とシナプス小胞内部に発現するタンパク質が受容体になることが明らかになっており、小胞膜の脂質やタンパク質を再回収するための小胞に毒素が取り込まれると考えられている。この小胞は細胞内で速やかにその内部の酸性化を起こすため、ボツリヌストキシンは最初に取り込まれた末梢部だけで作用すると考えられている。これに対して、テタノスパスミンを取り込んだ小胞はすぐには酸性化されずに、軸索に沿って逆行性に輸送され、神経細胞の細胞体のある脊髄や海馬に到達して作用する。また、ボツリヌストキシンが血液脳関門を通過できないことも、作用が末梢性に限られる理由にあげられる。
培養液中や汚染食品中では、ボツリヌストキシンの毒素蛋白は1あるいは4種類の無毒蛋白と会合し、複合体を形成する。この複合体をプロジェニター毒素あるいはボツリヌス毒素複合体と呼ぶ。ボツリヌス毒素中の毒素蛋白は、動物の消化器官において分解されやすく不安定であるが、複合体を形成することで、消化器官内での分解作用から保護されていると考えられている。
開発の歴史
[編集]兵器
[編集]ボツリヌストキシンの研究は、第二次世界大戦当時に進展した。生物兵器としての研究であり、精製法についてはこの時期に確立されている。「細菌兵器(生物兵器)及び毒素兵器の開発、生産及び貯蔵の禁止並びに廃棄に関する条約」(生物兵器禁止条約)が発効した1975年以降は、開発・生産・貯蔵・輸出入が国際的に制限されているが、湾岸戦争時代にイラクが兵器として保有していたのをはじめ、テロリストに保有されやすい側面を持つ。
しかしながら、オウム真理教が実験に失敗したことが示すように、エアロゾル化して大気に散布したとしても、1分間に数%ずつ失活していく[10]ことや、気象条件に左右されることから、殺人兵器としての実用性は疑問視される部分もある[要出典]。
医薬品
[編集]医療用医薬品としては Alan B. Scott により、斜視に対し極めて微量のA型毒素が使用されたのを初め、2010年現在、83ヵ国で様々な疾患に用いられている。
日本においては、A型ボツリヌス毒素製剤(商品名:ボトックス注用50単位・100単位)が注射剤として、1996年に眼瞼痙攣、2000年に片側顔面痙攣、2001年に痙性斜頸、2009年に2歳以上の小児脳性麻痺患者における下肢痙縮に伴う尖足、2010年に上肢痙縮・下肢痙縮、2012年に重度の原発性腋窩多汗症の適応で承認・診療報酬に掲載されている。また、2011年にB型ボツリヌス毒素(商品名:ナーブロック筋注2500単位)が痙性斜頸の適応で承認されている。なお、日本では使用にあたり講習を受けなければならない。
アメリカ合衆国においては、斜視、痙性斜頸、眼瞼痙攣、上肢痙縮、多汗症に加え、神経学的疾患による過活動性膀胱、慢性片頭痛の適応で承認されている。過活動膀胱に対するボトックス注射による治療は2020年4月より日本でも保険適用になった[11]。
近年では医療用としてだけでなく、美容外科領域において筋弛緩作用を応用した「眉間やアゴのシワ取り」や「輪郭補正(エラ取り)」の美容目的で使用されていることが多く、日本においても2009年にアラガン社からボトックスビスタという商品名で発売された[12][信頼性要検証]。ボトックスビスタの美容医療業界における市場占有率は半数を超える[13]。世界で1,100万人以上が美容医療分野での治療を受けており、他社薬剤との臨床比較試験においても、持続期間やしわの改善率などに「ボトックスビスタ」が優れているとの結果が報告されている[14]。
また、アカラシアの治療にもボツリヌストキシンの局所注射が有効という報告がある。ただし、これらに関して日本では自由診療である。
ボトックスの日本以外における適応取得状況(抜粋、2010年)
[編集]- オーストラリア - 眼瞼痙攣、片側顔面痙攣、第7脳神経障害(12歳以上)、小児脳性麻痺患者における下肢痙縮に伴う尖足(2歳以上)、痙性斜頸、腋窩の多汗症、眉間の皺、痙縮(成人)、痙攣性発声障害、斜視、上顔面部の皺
- カナダ - 斜視、眼瞼痙攣、第7脳神経障害(12歳以上)、痙性斜頸(成人)、小児脳性麻痺患者における下肢痙縮、多汗症、痙縮(脳卒中後の上肢痙縮を含む)、上顔面部の皺
- チリ - 斜視、眼瞼痙攣、第7脳神経障害(12歳以上)、脳性麻痺、痙縮(成人)、振戦、ジストニア、ミオクローヌス、片側顔面痙攣、痙性斜頸、発声障害、痙性障害、攣縮に伴う背部・頸部・脊椎痛、歯軋り、眉間の皺、腋窩の多汗症、排尿筋過活動による尿失禁
- フランス - 眼瞼痙攣、片側顔面痙攣、痙性斜頸、眼球運動障害(斜視、動眼神経麻痺および甲状腺神経障害)、小児脳性麻痺患者における下肢痙縮に伴う尖足(2歳以上)、脳卒中後の上肢痙縮、腋窩の多汗症、眉間の皺(65歳未満)、上肢・下肢の痙縮
- ドイツ - 眼瞼痙攣、片側顔面痙攣、痙性斜頸、小児脳性麻痺による下肢痙縮(2歳以上)、脳卒中後の上肢痙縮、腋窩の多汗症、眉間の皺(65歳未満)
- イタリア - 眼瞼痙攣、痙性斜頸、小児脳性麻痺による下肢痙縮(2歳以上)、片側顔面痙攣、脳卒中後の上肢痙縮、腋窩の多汗症、眉間の皺
- 韓国 - 斜視、眼瞼痙攣、第7脳神経障害(12歳以上)、小児脳性麻痺患者における下肢痙縮に伴う尖足(2歳以上、痙性斜頸、腋下の多汗症(18歳以上)、脳卒中後の痙縮、眉間の皺
- メキシコ - 斜視、眼瞼痙攣、片側顔面痙攣、脳性麻痺、痙性斜頸、片頭痛、膀胱排尿筋過活動、発声障害、多汗症、顔面の表情皺、筋の過緊張による背部痛、歯軋り、裂肛、アカラシア、振戦、ミオクローヌス性障害
- イギリス - 眼瞼痙攣、片側顔面痙攣、痙性斜頸、小児脳性麻痺による下肢痙縮(2歳以上)、腋窩の多汗症、脳卒中後の上肢痙縮、眉間の皺、片頭痛
医薬品としての安全性
[編集]眼瞼痙攣に使用した場合に眼瞼下垂、痙性斜頸に使用した場合に嚥下障害などの報告がある[15]。一般的にボツリヌストキシンの有害事象は一過性で、筋弛緩作用が強く発現したことによるものが多い。有害事象の多くは薬理作用の減弱とともに回復する。注意すべきケースは頸部筋に施注する場合で、全身状態の悪い患者に用いた場合、嚥下障害が悪化することが稀にある。通常、医療目的では推定致死量の数百-数十分の一(注射にて換算)という微量を用いるが、用量設定を誤らない限りにおいては概して安全である。
ボトックスは毒性が高く安全性の観点から疑問視されることもあり、ボトックスに比較して急性毒性が低く注射ではない外用剤のアルジルリンが開発されている[16]。
関連法規
[編集]強い毒性を有するため幾つかの法規による規制があり、違反の場合懲役または200万円以下の罰金が科せられるなど、生物テロの未然防止の観点から厳重な罰則規定がある[17]。例えば、病原体等管理業務に関し取り扱う毒素量が規制対象以下(0.1mg)である場合には所持の制限を受けないが、毒素量が0.1mg以下であることの根拠を示す必要がある[18]。
- 二種病原体等に分類され、平成19年6月1日施行の感染症法に基づき、検査、治療、医薬品その他厚生労働省令で定める製品の製造又は試験研究目的にボツリヌス菌・毒素を所持する者は、「感染症発生予防規程の届出」「病原体等取扱主任者の選定」「教育訓練」等が義務づけられている。また、所持や輸入する場合にはあらかじめ厚生労働大臣の許可が必要となる[18]。なお、医療目的で通常用量の所持の場合は、同法の対象にならない。
- 厚生労働大臣が指定したものは規制対象から除外で、ボツリヌス毒素では 0.1mg以下のボツリヌス毒素、A型ボツリヌス毒素を含有する製剤500単位以下のもの、またはB型ボツリヌス毒素を含有する製剤10,000単位以下のもの[18]。
- 国家公安委員会規則
- 米国CDCでは生物兵器として利用される可能性が高い病原体として、ボツリヌストキシンおよびボツリヌス菌を最も危険度、優先度の高いカテゴリーAに分類している。この他、ペスト菌、炭疽菌、野兎病菌、天然痘ウイルス、エボラウイルスなどの出血熱ウイルスもカテゴリーAに指定されている。
脚注
[編集]- ^ 阪口玄二、「ボツリヌス菌毒素の構造と機能」『日本細菌学雑誌』 1988年 43巻 6号 p.951-960 , doi:10.3412/jsb.43.951。
- ^ JAMA 2001;285:1059-1070
- ^ Merck Index 13th ed., 1345.
- ^ ボツリヌス症 (PDF) 国立感染症研究所 平成24年12月07日
- ^ 藤永由佳子, 松村拓大, 阿松翔, 菅原庸, 油谷雅広, 「ボツリヌス毒素研究の新知見」『日本食品微生物学会雑誌』 2015年 32巻 2号 p.104-109, 日本食品微生物学会, doi:10.5803/jsfm.32.104。
- ^ 小崎俊司、「阪口玄二先生とボツリヌス毒素研究」『日本食品微生物学会雑誌』 2015年 32巻 2号 p.101-103, 日本食品微生物学会,doi:10.5803/jsfm.32.101。
- ^ 吉田眞一、柳雄介、吉開泰信編『戸田新細菌学』改訂33版、南山堂、2007年 ISBN 9784525160135
- ^ Rossetto O, Seveso M, Caccin P, Schiavo G, Montecucco C. "Tetanus and botulinum neurotoxins: turning bad guys into good by research." Toxicon. 39 27-41 (2001) PMID 10936621
- ^ Montecucco C, Rossetto O, Schiavo G. "Presynaptic receptor arrays for clostridial neurotoxins." Trends Microbiol. 12 442-446 (2004) PMID 15381192
- ^ 米軍生物研究所公表資料、1964年
- ^ ボトックス注射を使った過活動膀胱治療が、やっと日本でも保険適用されました!! 泌尿器科|五本木クリニック
- ^ “エラボトックス10選!安いおすすめクリニック・効果・デメリットまとめ”. quuuun.com. 2022年1月27日閲覧。
- ^ 桑満おさむボトックスの種類と特徴、代表的な3つのボツリヌストキシン製剤について (五本木クリニック)
- ^ “ボトックス|美容皮膚科・さいたま市浦和|OZI SKIN CLINIC”. www.ozi-skin.com. 2021年11月26日閲覧。
- ^ グラクソ・スミスクライン株式会社インタビューフォーム
- ^ Seng Han Lim, Yuanyuan Sun, Thulasi Thiruvallur Madanagopal, Vinicius Rosa, Lifeng Kang (2018-1). “Enhanced Skin Permeation of Anti-wrinkle Peptides via Molecular Modification”. Scientific reports 8 (1): 1596. doi:10.1038/s41598-017-18454-z. PMC 5785486. PMID 29371611.
- ^ 感染症法に基づく特定病原体等の管理規制について 厚生労働省
- ^ a b c 感染症法改正に伴うボツリヌス菌・毒素のバイオセキュリティ対応 国立感染症研究所 感染症情報センター 病原微生物検出情報 Vol.29 p.42-44: 2008年2月号
外部リンク
[編集]- ボツリヌス菌毒素の構造と作用 IASR Vol.29 p.37-38: 2008年2月号 国立感染症研究所 感染症情報センター
- 高橋元秀、「日本のボツリヌストキソイドワクチンの開発」『日本食品微生物学会雑誌』 2015年 32巻 2号 p.110-114, 日本食品微生物学会, doi:10.5803/jsfm.32.110
