ドクササコ
| ドクササコ Clitocybe acromelalga | ||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
 ドクササコ(左上:胞子、左:全体、右:ひだ)
| ||||||||||||||||||||||||||||||
| 分類 | ||||||||||||||||||||||||||||||
| ||||||||||||||||||||||||||||||
| 学名 | ||||||||||||||||||||||||||||||
| Paralepistopsis acromelalga (Ichimura) Vizzini | ||||||||||||||||||||||||||||||
| 和名 | ||||||||||||||||||||||||||||||
| ドクササコ (毒笹子) |
ドクササコ(毒笹子[1]、学名: Paralepistopsis acromelalga)は担子菌門のハラタケ綱 ハラタケ目に属し、キシメジ科のParalepistopsis属に分類される中型の毒キノコの一種である。誤食すると、手足の先が赤く腫れ上がって激痛が1か月以上続く中毒症状の激しさから、ヤケドキン、ヤケドタケ、ジゴクモタシなどの異名がある。
形態
[編集]子実体は傘と柄からなる。傘は径5-10センチメートル (cm) 程度。はじめ中央が窪んだまんじゅう形であるが、のちに漏斗状に中央が窪み、縁は内側に巻き込むことが多い[2][3]。表面は平滑でほとんど粘性を欠き、橙褐色ないし帯赤黄褐色を呈し[2]、乾時にはややビロード状に見えることがある[3]。傘の周縁部はゆるく波打つとともに往々にして浅い裂け目を生じ[2](爪で押し当てたような斑紋があったり[3])、幼時には内側に強く巻き込んでおり、条線や条溝を生じない。傘裏のひだは密で、柄に長く直生ないし垂生し、ごく密で淡クリーム色から次第に黄褐色を帯びる[2][3]。肉は薄く、幼時はほぼ白色であるが次第にクリーム色ないし淡黄褐色を呈し[2]、変色性を欠き、やや強靭な繊維状肉質で裂けやすく、味もにおいも温和で特徴的なものはない。
柄は上下同大または基部がやや膨らみ、表面は傘とほとんど同色かやや淡色、中空であるが強靱な繊維質で縦に裂けやすい[2][3]。基部は膨らむものが多く、しばしば白色かつ綿毛状の菌糸に包まれるとともに[2]、厚い白色の菌糸のマットを形成することが多い。
胞子紋は純白色である。胞子は幅広い楕円形ないし卵形で無色・薄壁、しばしば一個の油球を含み、ヨウ素溶液で染まらない(非アミロイド性)。シスチジアはなく、菌糸は薄壁でゼラチン化せず、かすがい連結を備える。かさの表皮は、表面に対して平行に匍匐した細い菌糸(淡褐色の内容物を含み、ゼラチン化はみられず、薄壁でかすがい連結を有する)で構成されている。
生態
[編集]腐生菌[2](腐生性[1])。秋、おもに竹やぶや笹やぶの落ち葉の上に散生、または群生する[1][2]。まれに、コナラなどを主とした広葉樹林[4]、あるいはスギ林の地上に発生することもある[5][6]。発生環境下では、白い綿毛状の菌糸のマットを落ち葉層に形成するのが認められ、子実体の組織をタマネギ煎汁培地などに植えつければ純粋培養が可能である[7]。
分布
[編集]日本と韓国に分布する[2]。日本では山形・宮城・福島・長野・新潟[8]富山[6]・石川(鳳至・羽咋・鹿島などに集中して中毒例が知られ、能美地区における中毒例もある[5])・滋賀・京都[8]・兵庫[9]・和歌山・鳥取[8]・島根など、本州の東北地方や日本海側を中心に分布する[1]。四国では、愛媛県西条市、東温市、松山市、久万高原町、宇和島市からの報告がある[10]。関東地方では見かけることはなく[1]、北海道および九州からも見出されていない。
なお、長らく日本特産種であるとされてきたが、韓国にも分布するという[6][11]。
分類学上の位置づけ
[編集]石川県金沢市の第四高等学校教授であった市村塘(つつみ)により、新種記載がなされた[12][13]。なお、新種記載に際して用いられた標本について、原記載には「石川県輪島市門前町剱地周辺の竹林の地上で採取されたものである(ad terram in silvis Bambusarum, Tsurugiji, Noto, Japonia.)」と記述されているが、採取年月日については記されておらず、タイプ標本としての指定もなされていない[13]。さらに標本の収蔵機関などについても記述がなく、原記載に用いられた標本は、現時点では所在が不明となっている。また、Clitocybe amblicata (Schaeff.) Quél.との異同について疑問を呈する研究者もある[14]。
かさの裏面がひだ状であること、ひだが柄に対して垂生し子実体の側面観が多少とも逆三角形を呈すること、胞子が無色(胞子紋が白色)でありヨウ素溶液で呈色しない(非アミロイド性である)こと、ひだなどの組織には顕著なシスチジアを欠くこと、かさの表皮がゼラチン化しないことなどの形質は、旧来の形質分類学上におけるカヤタケ属(Clitocybe)の定義にほぼ合致するため、菌学者の間では長きにわたりClitocybe acromelalgaの学名が使用されてきた。
なお、ドクササコをNeoclitocybe属(タイプ種はN. byssiseda (Berk.) Sing.)に置く意見[15]もあった。Neoclitocybeは、原記載[16]によれば、柄の基部に厚い綿毛状の菌糸マットを備えること、およびかさの表皮層の構成菌糸が多数の短い側枝を生じて魚の骨状をなす(ラメアレス構造 Rameales-structureと称される)ことによって定義づけられており、原記載の段階ではタイプ種を含め9種が所属させられていた。のちにその定義は多少の修正・補足が加えられるとともに、計18種が分類されることとなった[15]が、ドクササコのかさの表皮層の構造はNeoclitocybe属の定義とは異なっており、これをNeoclitocybeに包含して扱うことに賛同する研究者は少なかった。
近年の分子系統的な観点からの再検討により、形質的所見に基づいた旧来のカヤタケ属は解体され、ホテイシメジ属(Ampulloclitocybe)[17]・カヤタケ属(Infundibulicybe)[18]およびハイイロシメジ属(Clitocybe)の三つの属に再編成された。この時点では、供試材料に日本産のドクササコは含まれておらず、上記の三属の定義に照らして最も矛盾がないハイイロシメジ属に含められていた[14][8]。
その後、供試材料として日本産のドクササコをも用いた分子系統的研究[19] が行われた結果、新たに設立されたParalepistopsis 属へと移され、2014年11月末の時点ではP. acromelalga (Ichimura) Vizzini の学名が用いられている。ちなみに、Paralepistopsis 属の基準種であるP. amoenolens (Malençon) Vizzini は、ドクササコ同様にかつては広義のカヤタケ属に所属するものとして扱われていた種で、ヒトが誤って食べればドクササコと同様の特異な中毒症状を起こす(後述)。また、Paralepistopsisの所属種としては、ドクササコとP. amoenolensとの二種のみが認められている[19]。
中毒
[編集]おだやかなキノコ臭があり、いかにも食べられそうな見た目で、味も温和なため、食用キノコと間違えて中毒する事故が多い[2][3]。また色や形がアカハツ(Lactarius akahatsu)などに、発生状況がナラタケ(Armillaria mellea)などにやや似ていることから、これらキノコとの誤食も報告されている[3]。
症状
[編集]絶命することはないものの、食べると早い場合は6時間ほど、遅い場合は1週間ほどしてから強い中毒症状が現れ、手足の先などが赤く腫れ上がって火傷のような激しい痛みが1か月以上も続き、苦痛に耐え続けなければならない[1][3]。
ヒトの場合
[編集]
他の多くの毒キノコとは異なる、薬理学的にも特異な中毒を起こす。主要な症状として、目の異物感や軽い吐き気、あるいは皮膚の知覚亢進などを経て、四肢の末端(指先)・鼻端・陰茎など、身体の末梢部分が発赤するとともに火傷を起こしたように腫れ上がり、その部分に赤焼した鉄片を押し当てられるような激痛が生じ、いわゆる肢端紅痛症(末端紅痛症とも、Acromelalgia)をきたす。症状が著しいケースでは、膝・肘の関節部あるいは耳たぶにまで及ぶこともあるという[20]。また、ときには患部に水泡を生じ、重症の場合は末梢部の壊死・脱落をきたす場合がある[21][22]。消化器系の症状はまったくなく、体温・脈拍などの変化もほとんど起こらない。また、血圧や血液中の白血球数なども正常なままで推移する[23]。
発赤と腫脹および疼痛は昼夜の別なく、長期間(しばしば1か月以上)にわたって続く。患者が成人である場合、死に至ることはまれだが、老人あるいは子供では死亡例も報告されている。ただし、死亡例のほとんどは、ドクササコの有毒成分そのものによるものではなく、激痛を緩和するために患部を水に浸し続けた結果、皮膚の水潤・剥離などにより、二次的に感染症などを起こした事によるものである。また、この長期に渡る症状がもたらす精神的苦痛も軽視できず、激痛から逃れるための自殺や、睡眠障害に起因する体力消耗の結果としての衰弱死と見られる例も存在する。平成元年(1989年)10月下旬の例として、石川県鳥屋町において、モミとタケとの混生林内に発生したドクササコを誤食し、68歳の女性が約2週間後に死亡した例がある[5]。
なお、ドクササコの成分に直接に起因するものか、それとも二次的なものかは断定されていないが、消化管(胃および十二指腸)壁からの潰瘍性出血をみた例が知られている[24]。
ドクササコ中毒の際立った特徴として、摂食から発症までの潜伏期間が1-7日程度におよび、食中毒としては際立って発症が遅い[20]ことが挙げられる。このため、家畜投餌や微量摂食による毒性のチェックもすり抜けてしまい、また発症しても原因が特定しにくく、医学者の間でさえ一種の風土病ではないかと推定されるほどであった。なお、きのこを食べた量が多いほど潜伏期が短く、潜伏期が短い症例ほど重くなる傾向がある[20]。
ドクササコによるのではないかと推定される中毒事件としては、1890(明治23)年10月に福島県信夫郡平野村(現在の飯坂町平野)において、11歳から48歳までの男女5人が患者となった例[25][26]があり、その翌年の1891(明治24)年には京都府[27]および福島県 [28]からも報告された。しかし、この時点ではきのこの正確な同定はなされず、また医学界においてさえ周知が徹底されなかった上、ましてや一般人への啓蒙も行き届かなかった。1899(明治32)年に、新潟県頚城郡において起こった中毒(7名が発症)例においても、主治医となった小池亮琢からの聞き取り調査に対し、中毒患者らは「思い当たる原因がなく不安に陥り、神の祟りを恐れて村の占者に相談したが、家屋新築したことによる金神の祟であると告げられた」と答えている。さらに重ねての医師からの問診により、ようやく、自宅近くの神社の境内で、俗に「ゴミ茸」あるいは「チョク(猪口)茸」と称されるきのこを採取し、発症の7日前の夕食の献立に加えて食べた、との証言が患者から得られ、初めてきのこが原因となった食中毒ではないかとの推測がなされたという。ただし、この中毒例でも、原因となったきのこの分類学的な位置づけは最後までなされないままに終わっている[29][30]。また、石川県鹿島郡の龍尾村においても、先端紅痛症を主な症状とする症例が毎年のように発生し、死亡者も出ていた事例があるが、この例については、1911(明治44)年に公にされた報文[31]中でさえも「原因不明」とされ、きのこ中毒である可能性は看過されていた。ちなみに、龍尾村の例では、秋になると毎年のように先端紅痛症をきたす患者もあったが、きのこに原因を求める者はやはりなかったという[31]。
近年の中毒例としては、2012年10月下旬に奈良県宇陀市の50代男性が[32]、2013年10月下旬に新潟県魚沼市の男性2名が[33]それぞれドクササコ中毒により手足の痛みやしびれを訴えて手当てを受けたが、いずれも命に別条はなかった。
動物の場合
[編集]ドクササコの子実体を乾燥・粉砕し、水に浸して得たエキスは、ラットやマウス・モルモット、あるいはカエルに対して致死的毒性を示すが、個々の生物への水エキス投与によって発現する症状は、ヒトのドクササコ中毒によるものとは大きく異なっている。カエルでは反射運動阻害・呼吸運動阻害がみられ、いっぽうでラットやマウス・モルモットでは呼吸中枢の麻痺による呼吸困難ないし停止が起こる。モルモットでは筋肉の痙攣がみられるが、それ以外の動物では発現せず、交感神経の興奮・脈拍増大・血管収縮と血圧の上昇はマウスにのみ起こる[34]。
ニワトリに対し、乾燥・粉砕したドクササコを直接与えた実験では、体重1 kg当り100 mgを一日一回投与することによって、7日めごろから衰弱および食欲不振があらわれ、鶏冠が黄色みを帯びてくる。10日めには歩行困難となり、およそ30日ほどで死亡する。また、変色した鶏冠には壊疽が発現する。この過程は投与量を多くすると早まり、1000 mg/kgを毎日与えた場合には、死亡までの期間は7日前後となるという。死亡後のニワトリの鶏冠の組織を詳細に検査した結果から、壊疽の発現は鶏冠部の血管の異常な拡張によるものと推定されている[35]。
ヒト以外の動物(ラット・マウス・モルモット・ウサギ・ニワトリ・カエルなど)では、ドクササコの子実体を経口投与しても、ヒトのドクササコ中毒における典型的な症状である末端紅痛症は発現しない。ただし、ナイアシンをまったく含まず、かつトリプトファンの含有量を抑えた制限食を飼料として与え、ナイアシン欠乏状態にしたラットでは、ドクササコ(乾燥粉末)を加えた飼料を与えてから3日後に、四肢の先端の発赤・腫脹が発現した[36]。
治療法
[編集]確実に症状を軽減する有効な治療法はなく、対症療法が優先される。
ドクササコ中毒患者の主訴である身体末梢部の熱感および激しい疼痛に対しては、鎮痛剤の投与はほとんど無効である。モルヒネは、ラットに対する腹腔内投与試験では、疼痛を抑制する効果が認められた[37]が、ヒトのドクササコ中毒に対する臨床現場では著効をみた例がほとんどない。また、非ステロイド性抗炎症薬の一種であるケトロラック(Ketrolac)によっても、鎮痛効果は示されなかった[37]。
実用上で有効な鎮痛方法は局所麻酔による硬膜外神経ブロックに限られており[38]、完全な治療法は確立されていない。赤く腫れ上がった患部を切開しての瀉血 [39][40]や血液透析、あるいはナイアシン [38][39]とATPとの投与により、症状が軽減することがある[38]ともされるが、それらによる効果も確実なものではない[41]。ナイアシンの投与は、ナイアシン欠乏症に陥ったラットにドクササコを与えることでヒトと同様の末端紅痛症が発現したこと[36]に着想を得たものであるが、実際にはドクササコを投与されたラットにおいては、トリプトファン-ナイアシン転換経路は阻害されずにむしろ亢進されることから、外部からのナイアシンの投与・補給による治療効果を疑問視する意見もある[42]。
なお、発症から約3週間を経過した後、左右の股動脈から7パーセント炭酸水素ナトリウム水溶液を一日当り20-40 mLずつ注入すると疼痛は軽減しはじめ、これを9日間継続した結果、ほとんど消失したとの報告がある[23]。また、抗ヒスタミン剤(ピリベンザミン)およびエフェドリンの投与によって、3日ほどで疼痛が軽減して患部の冷水浴が不要となり、7日目には浮腫が消失した[43]。
注意喚起など
[編集]色調や形態に毒々しさがなく、味も温和であり、さらに子実体が繊維状肉質で容易に縦に裂けるなど、食用きのこと判断される形質を備えていることや、ひとたび見出されたおりには多数の子実体が得られることが少なくないことなどから、誤食される危険が高い[4][44][45][46]毒きのこの一つである。本種の分布が確認された地域では、自治体による注意喚起がしばしば行われている。
成分
[編集]毒成分は、アクロメリン酸類、スチゾロビン酸、スチゾロビニン酸などの中枢神経毒、クリチジン(マウス致死性毒)とされる[2][3]。その他化合物として、クリチオネイン、異常アミノ酸類、キノリン酸、アミノキノリン酸、オビン類が含まれている[3]。
毒性画分
[編集]ドクササコの毒成分として最初に単離されたのは、ヌクレオシドに属するクリチジン(Clitidine、1,4-ジヒドロ-4-イミノ-1-(β-D-リボフラノシル)-3-ピリジンカルボン酸)である[47][48]。4-アミノキノリン酸(後述:アスパラギン酸とジヒドロキシアセロンリン酸とから作られたキノリン酸がアミノ化されて生じる)と5-ホスホリボシル-1-ピロリン酸とに酵素が働いて4-アミノニコチン酸モノヌクレオチドとなり、さらに脱リン酸およびアミノ基還元を経て生合成されるものと推定されている[42][49]。
クリチジンは無色の針状結晶で、水によく溶け融点210 ℃、紫外線吸収スペクトルは270 nm(log =ε 4.29,H2O)に極大吸収を示す。マウスに対し50 mg/kgを腹腔内注射で投与すれば7-10日、100 mg/kgでは15-25時間で死亡する。投与を受けたマウスは尾を挙げた姿勢をとるとともに、後足が硬直して前足のみで動くようになるという。いっぽう、ニワトリに対しては、皮下注射で50 mg/kgを与えても、衰弱はみられるものの鶏冠の変化はまったく観察されなかった[21]。また、注射によって投与した場合、注射箇所のまわりには硬化現象が見られ、それは4-5日後には乾燥性の壊疽へと移行する[21]。
クリチジンはまた、血管拡張作用を有する[41][50]が、あまり著しいものではない。イヌの動脈へのクリチジン(結晶の水溶液)注射によって発現する血管拡張作用は、ニコチンアミドや4-アミノニコチン酸によってもたらされるそれとほぼ同等で、6-アミノニコチン酸によるものよりもやや弱い程度である[21]。
クリチジンに次いで単離された毒成分として、非たんぱく性アミノ酸の一種であるアクロメリン酸(Acromelic acid)およびクリチジル酸(Clitidic acid、クリチジン5’-モノヌクレオチド)[51]などがある。
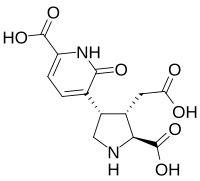
アクロメリン酸にはA、B[52][53]、C[54]、D、E[55]の5種が存在する。アクロメリン酸A-Eの、ドクササコ子実体中における含有量はごく微量であり、たとえばアクロメリン酸Aは、生の子実体16.2 kg から110 μg、Bは同じく40 μgしか得られない[53]。カイニン酸やドウモイ酸に類似した基本骨格を持ち[52][53]、後二者と同様に、脳のグルタミン酸受容体を介した著しい神経興奮作用を有し、神経毒として働く[56][57]。これらのうちでは、発見・単離の歴史が比較的古いAおよびBについての研究がより進んでいる。
アクロメリン酸Aをラットに経口投与すると、脊髄の腰仙髄部の神経細胞が傷害される。腰仙髄部の神経細胞に対するアクロメリン酸Aの半数効果濃度はおおむね2.5 μMで、カイニン酸のそれ(70 μM)に比べて非常に小さく、非N-メチル-D-グルタミン酸受容体に直接に作用して壊死させると考えられている[58]。非N-メチル-D-グルタミン酸受容体の阻害物質(たとえば2,3-ジヒドロ-9-ニトロ-7-スルファモイルベンゼンなど)や、AMPA受容体に対するカルシウム浸透型の阻害剤としてのジョロウグモ毒素は、アクロメリン酸Aによる末端紅痛症の発現を阻害するが、アクロメリン酸Bに対しては無効である[59]。
なお、ラットへの腹腔内投与における最低効果濃度は、アクロメリン酸Aでは50 ag/kgないし0.5 pg/kg、アクロメリン酸Bでは50 pg/kgないし50 ng/kgであり、Aのほうが強力に作用し、Bの100万倍の低濃度で効果をあらわす[59] 。上述のように脊髄の神経細胞に対するアクロメリン酸Aの効果は、カイニン酸のそれに比べてはるかに強力である。これに加え、海馬の培養細胞に対するアクロメリン酸Aの半数効果濃度はやや大きい(18 μM)のに対し、カイニン酸では、脊髄に対するのと同等の濃度で作用することなどから、脊髄においては、アクロメリン酸Aに対する特異的な受容体が存在するのではないかと推定されている[58]。また、ラットの前肢の長指伸筋-総腓骨神経に分布する機械感受性筋C線維受容器(伝導速度:2.0 m/s 以下)を材料とした研究によれば、機械感受性筋C線維の約半数にアクロメリン酸Aへの感受性が認められたことから、脊髄ばかりではなく、末梢侵害受容器の終末部分にもアクロメリン酸Aの受容体が存在する可能性が示唆されている[60]。アクロメリン酸Cについても、体重kg当り10 mgの投与によってマウスに致死毒性を発現させるとの報告[54]がある。なお、Sprague-Dawleyラットを用い、アクロメリン酸Aを投与した実験(ラット足背部への皮下注射: 100 μL、1~1000 fmol/部位)では、NMDA(D-アスパラギン酸メチル)受容体への拮抗薬としてのD-AP5 (D-(−)-2-アミノ-5-ホスホノペンタン酸:50 μM)や非NMDA受容体拮抗薬としてのCNQX (6-シアノ-7-ニトロキノキサリン-2,3-ジオン、10 μM)、非ステロイド性抗炎症薬であるKetrolac (10 mg/kg, i.p.)、あるいはモルヒネ (3 mg/kg, i.p.) などを前投与したところ、モルヒネのみに鎮痛作用が認められたとされている[37]。
また、アクロメリン酸のオルソ位がアニシル化された異性体(ドクササコの子実体には含まれていない)は、アクロメリン酸Aよりもさらに低濃度の投与で、ラットの紅痛症を惹起する[61]。
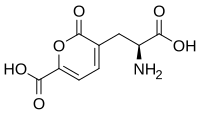
ドクササコの子実体からは、神経毒性を持つ化合物としてスチゾロビン酸(Stizolobic acid)およびスチゾロビニン酸(Stizolobinic acid)も見出されている。アクロメリン酸の構成要素となっているピリドン骨格は、D-DOPAを出発点とし、スチゾロビン酸やスチゾロビニン酸を経て生合成するものと推定される[62][49]。
アクロメロビニン酸(Acromelobinic acid、(S)-(−)-3-(6-カルボキシ-2-オクソ-3-ピリジル)-L-アラニン)およびその異性体のアクロメロビン酸(Acromelobic acid、(S)-(−)-3-(6-カルボキシ-2-オクソ-4-ピリジル)-L-アラニン)は非たんぱく性アミノ酸の一種で、ラットに対して神経興奮性を示す[63]。これら2種、あるいはドクササコの子実体から見出されたもう一つの非たんぱく性アミノ酸であるN-[2-(3-ピリジル)エチル]-L-グルタミン酸は、いずれも、クリチジン、クリチオネイン、アクロメリン酸など、より高分子の有毒成分の生合成過程における中間体として存在するものと考えられている[49][64]。
非毒性画分
[編集]子実体に含有される成分のうち、非毒性の化合物としては、クリチオネイン(Clithioneine)[65][66]や、4-アミノピリジン-2,3-ジカルボン酸(4-Aminopyridine-2,3-dicarboxylic acid:別名 4-アミノキテリン酸)[67]が見出されている。前者はアミノ酸ベタインの一種であるが、マウスに対し 100 mg/kgを投与してもなんら影響を与えなかった[41]。後者はピリジン誘導体の一種である。
また、イソニペコチン酸誘導体の一種であるピペリジン-2,4,5-トリカルボン酸[68]および 4-アミノキノリン酸[41]なども検出されている。イソニペコチン酸はGABAAの受容体の一つであるが、ドクササコに含まれるピペリジン-2,4,5-トリカルボン酸の生理活性作用については、まだ十分に検討されていない。一方、4-アミノキノリン酸は、トリプトファン-ナイアシン代謝系の中間体であるキノリン酸の誘導体であり、ドクササコの子実体中においては、有毒成分であるクリチジンの生合成過程における中間体として存在するのではないかと推定されている[42]。
ドクササコの子実体には、このほかにジペプチドの一種であるN-(γ-アミノブチリル)-L-グルタミン酸[69]、あるいはオパイン類(アミノ酸の一種であるが菌類における産生例は珍しい)に属するバリノピン、エピロイシノピン、イソロイシノピン、フェニルアラニノピン[70]などが含まれているが、これらの成分の、ドクササコの代謝系における役割あるいはヒトその他の生物に与える生理活性などについては、まだ十分に知見が集積されていない。なお、糖アルコールとしてD-マンニトールも見出されている[71]が、これはドクササコに限らず、多くのきのこに普遍的に存在する成分の一つである。
類似種
[編集]無毒種
[編集]
カヤタケ(Infundiblicybe gibba:カヤタケ属の基準種)は、子実体がより柔らかくて淡色(特に柄の部分)であり、かさは多少ビロード状をなすことが多く、一般に光沢に乏しい。さらに、タケやぶやササやぶに限らず、種々の林内、あるいは草原などの地上に発生することで異なる[72]。食用にされることもあるが、ドクササコとの識別が難しい場合もあり、あまり推奨できない。
ハイイロシメジ属に置かれるアカチャイヌシメジ(Clitocybe sinopica)は、かつてはヤブシメジモドキの仮称で呼ばれた[73]こともあり、橙褐色のかさや柄および白っぽいひだを有する点でドクササコに類似しているが、一般にドクササコより子実体が小さく、肉がもろくて縦に裂けにくいこと・ひだがより荒くて幅広いこと・全体に粉くさい臭気を有すること・カヤタケ属のきのことしては胞子が非常に大きいことなどの点で異なる。また、タケやぶやササやぶに限られることなく、庭園・公園内の植え込みの中や人家の生垣の下など、人為の影響を受けやすい場所に好んで発生することでも区別される[74]。
北方系のコブミノカヤタケ(Paralepista flaccida)も褐色系のきのこで、外観はドクササコと非常にまぎらわしいが、おもに針葉樹(アカエゾマツなど)の林内に発生することと、胞子が明瞭ないぼ状突起を備えることで異なる[19][75]。
チチタケ (Lactifluus volemus) やナラタケ類 (Armillaria mellea) と誤食された例もあるが、両者ともにドクササコとはかなり縁が遠いキノコである。チチタケは子実体がもろくて縦に裂けず、新鮮なものを傷つけると牛乳のような乳液を多量に分泌する[72]が、ドクササコでは白い乳液が出ないうえ、縦に裂けることで区別することができる[2]。また、ナラタケ類は普通はドクササコよりもきゃしゃであり、通常は枯れ木上あるいは樹木の切り株の周囲(地中の、枯れた根を栄養源とする)などに発生すること・かさは光沢に乏しく、一般的には深い漏斗状にくぼむことはなく、しばしば黒くて微細な粒状のささくれを備えること・柄に明瞭な膜質のつばを有することなどにおいて異なっている[72]。
有毒種
[編集]ドクササコと同様の中毒症状を起こすきのことして、パラレピストプシス・アモエノレンス(Paralepistopsis amoenolens)が知られている。この菌は、モロッコ産の標本をタイプとして記載されたものである[76]が、その有毒性については、記載されてからも長期にわたって明らかになっていなかった。しかし、1996年にフランスのサヴォア県(モーリエンヌ渓谷周辺)において発生した、ドクササコに似た症状をきたす中毒の原因となったきのこを詳しく調査した結果、P. amoenolensであることが確認された[77]。
Paralepistopsis amoenolensは、日本産のドクササコに多少似た外観を有するが、全体により小形であり、かさは赤みが弱くて淡黄褐色ないしクリーム色を呈すること、モミ属の樹木を主とした針葉樹林に発生することで異なる[78][79]。また、末端紅痛症を起こす点ではドクササコと共通するが、きのこを食べてから発症までの潜伏期が短く、早い場合には24時間経過後には症状が発現する。ラットへの投与実験においては、うずくまり、歩行困難や体重減少などとともに四肢の末端の発赤が生じ、また、坐骨神経の軸索密度の減少と神経線維の変性とが認められた[80]。また、ドクササコと異なり特有の臭気を持つ[81]。
Paralepistopsis amoenolensの子実体が含有する成分としては、日本産ドクササコと共通してアクロメリン酸Aが見出されたが、ドクササコをも用いて定量を行い、両種の含有量を比較したところ、P. amoenolensでは乾燥した子実体1 mg当り325 ng、ドクササコでは同じく283 ngであったという。その他の成分に関してはまだ十分に研究されていない[82]。
Paralepistopsis amoenolensによる中毒症例に対して、英語では「Acromelalga-Syndrome」の呼称が用いられている。P. amoenolensはイタリア[83]、トルコ(レバノンスギの樹下に発生する)[84]からも見出されているが、日本に分布するか否かは不明である。
カラハツタケ(Lactarius torminosus)もまた、かさが多少とも漏斗状を呈し、かつ赤褐色を帯びる点ではドクササコとの共通点がないではないが、日本ではおもにカンバ属(Betula)の樹下に発生すること・かさが粗雑な毛状物に縁どられること・組織に多数の嚢状細胞を含むために、子実体は縦に裂けにくいこと、子実体を傷つけると白い乳液を多量に分泌すること、著しい辛味を有すること、胞子が類球形でその表面に刺状の突起とそれを互いに結合する畝状の紋様とを持つことなどの点で、ドクササコとはまったく異なる菌である[4][6][39][85]。カラハツタケについて末端紅痛症の原因となるとの報告がなされたこともあったが[26]、これは、ドクササコの中毒患者からの、中毒からの回復後における事情聴取(中毒経験者からは「アカハツ(Lactarius akahatsu)によく似て、タケやぶに発生するきのこであった」との発言があったという[26])や、中毒事件が起こった地域の外で得られたさまざまなきのこを中毒経験者に送付しての間接的な照らし合わせなどによる誤りであるとされている。ただし、末端紅痛症の原因となり得る化合物が検出されていないとはいえ、カラハツタケは激しい辛味を持ち、消化器系を刺激して中毒症状を起こすとされている[86]。さらに、カラハツタケのほか数種のチチタケ属のきのこに含有されるベレラールなどの成分もまた、人体には好ましくない影響をもたらすとされている[87][88][89]ため、食用にはしないほうがよい[90]。
和名・学名・方言名
[編集]和名ドクササコの由来は、笹やぶに生える毒キノコであることから名付けられている[1]。中毒症状の激しさからヤケドタケ[3]、ヤケドキンの異名もある[2]。
新種記載[12]がなされた時点では、提唱された和名はヤケドキン(火傷菌)で、別名としてヤブシメジ(藪占地)の名が挙げられている[要出典]。少なくとも明治の終わりから大正時代にかけての時期において、石川県下では、竹林やササやぶに生えるきのこ類(必ずしもドクササコのみとは限らない)を総称した方言名としてヤブシメジの呼称が用いられていたとされる[91]。また、ヤブシメジの名を正式名とする研究者もあった[23][71]が、のちに、中毒患者を扱った内科医の山田詩郎によってドクササコ(毒笹子)の名が提唱された[91][20]。いっぽう、昭和30年代後半以降に発行されたきのこ類図鑑には、ヤブシメジの和名を用いたものがなお少なくない[4][92][44][45]が、ドクササコの名を当てたものも僅かにあった。昭和の末から平成にかけては、再びドクササコの名を当てる文献が大半を占めるにいたっている[39][93][94]。
属名の Paralepistopsis は、「コブミノカヤタケ属(Paralepista )まがいの」の意である。Paralepista は、ギリシア語の前置詞または副詞 para(παρά:~に近似の)[95]と、属名 Lepista (ムラサキシメジ属)とを結合したもの[19]であり、さらにLepista はラテン語の「酒器」あるいは「杯」を起源とし、十分に開いたかさが浅い漏斗状にくぼむことに由来するという[4]。種小名 acromelalga は、中毒症状として発現する先端紅痛症(Acromelalgia)に因む[12]。
ドクササコの文献上にあらわれた方言名ないしは異称の例としては、以下のようなものがある。
- 秋田県:コノハタケ[20]・ヤケドハツ(由利本荘市周辺)[96]・ジゴクモタシ[3]
- 福島県:タケモタシ・ヤブタケ・ササタケ(信夫郡平野村=現:福島市)[20]・ササモタシ(下磐前郡平町=現:いわき市)] [20]・タケモタシ[96]
- 宮城県:ケヤキモタシ(伊具郡角田町=現:角田市)[20]
- 新潟県:キキョウタケ(佐渡郡水津村=現:佐渡市)[20]
- 石川県:ヤブシメジ[91]・チョクタケ[91]・ヤブタケ(鳳至郡劔地=現:輪島市門前町剱地)[20]
- 京都府:ササタケ(山科)[20]
保護状況
[編集]長野県では絶滅危惧I B類(EN)[97]、三重県では情報不足(DD)[98]、兵庫県では要調査種[99]、愛媛県では県調査種[10]にそれぞれ分類されているが、具体的な保護対策としては、兵庫県において発生環境の保全が指摘されているに過ぎない。
脚注
[編集]- ^ a b c d e f g 大作晃一 2015, p. 9.
- ^ a b c d e f g h i j k l m n 大作晃一・吹春俊光 2010, pp. 108–109
- ^ a b c d e f g h i j k l 長沢栄史 監修 2009, p. 32.
- ^ a b c d e 今関六也, 本郷次雄, 椿啓介『菌類(きのこ・かび)』保育社〈標準原色図鑑全集 第14巻〉、1970年。ISBN 4586320141。 NCID BN01317824。全国書誌番号:69022174。
- ^ a b c 池田良幸、1996. 石川のきのこ図鑑. 北國新聞社出版局、金沢. ISBN 978-4-833-00933-1.
- ^ a b c d 池田良幸、2005. 北陸のきのこ図鑑. 橋本確文堂、金沢. ISBN 978-4-893-79092-7
- ^ 黒野吾市、1957,ヤブシメジ(火傷菌)の培養に関する研究,金沢大学薬学部研究年報7: 14-21.
- ^ a b c d 今関六也, 大谷吉雄, 本郷次雄, 青木孝之, 保坂健太郎, 細矢剛, 長澤栄史, 伊沢正名『日本のきのこ』(増補改訂新版)山と溪谷社〈山渓カラー名鑑〉、2011年。ISBN 4635090205。 NCID BB08110477。
- ^ 兵庫きのこ研究会(編著)、2007,のじぎく文庫 兵庫のキノコ,神戸新聞総合出版センター、神戸, ISBN 978-4-34300-428-4
- ^ a b 愛媛県貴重野生動植物検討委員会(編)、愛媛県の絶滅のおそれのある野生生物 愛媛県レッドデータブック ドクササコ 愛媛県県民環境部環境局自然保護課、松山,
- ^ Saviuc, P., and V. Danel, 2006. New Syndromes in Mushroom Poisoning. Toxicological Reviews 25: 199-209., doi:10.2165/00139709-200625030-00004
- ^ a b c T. Ichimura (1918). “A New Poisonous Mushroom”. Botanical Gazette (University of Chicago Press) 65 (1): 109-111. ISSN 00068071.
- ^ a b 布村塘、1918,火傷菌の学名,金澤醫科大學十全會雑誌23: 1-4.
- ^ a b 勝本謙, 安藤勝彦『日本産菌類集覧』日本菌学会関東支部,松香堂 (発売)、2010年。ISBN 9784879746245。 NCID BB02344045。
- ^ a b Singer, R. (1986). The Agaricales in Modern Taxonomy (4th and revised edition ed.). Koenigstein: Koeltz Scientific Book. ISBN 3- 87429-254-1
- ^ Singer, R. (1961). “Diagnoses Fungorum novorum Agaricalium II”. Sydowia 15: 45-83.
- ^ Redhead, S. A., Lutzoni, F., Moncalvo, J. M., and R. Vilgalys (2002). “Phylogeny of agarics: partial systematics solution for core omphalinoid genera in the Agaricales (euagarics)”. Mycotaxon 83: 18-57. NAID 10019950608.
- ^ Harmaja, H. (2003). “Notes on Clitocybe s. lato (Agaricales)”. Annales Botanici Fennici 40: 213-218.
- ^ a b c d Vizzini, A., and E. Ercole (2012). “Paralepistopsis gen. nov. and Paralepista (Basidiomycota, Agaricales)”. Mycotaxon 120: 253-267.
- ^ a b c d e f g h i j k 眞田淸一郞, 佐々木基, 松枝勝夫「「エリトロメラルギー症狀ヲ冸ヘル菌中毒エピデミー」ニ就テ」『金澤醫科大學十全會雜誌』第037巻第09号、金澤醫科大學十全會、=1932-09、2053-2072頁、ISSN 00227226。
- ^ a b c d 牛沢勇, 平則夫, 片桐清弥, 加藤鉄三、「ドクササコの有毒成分とその薬理作用」 『ファルマシア』 1978年 14巻 9号 p.773-777, doi:10.14894/faruawpsj.14.9_773, 日本薬学会
- ^ Konno, K., Hayano, K., Shirahama, H., Saito, H., and T. Matsumoto, 1982. Clitidine, a new toxic pyridine nucleoside from Clitocybe acromelalga. Tetrahedron 38: 3281-3284., doi:10.1016/0040-4020(82)80107-5
- ^ a b c 山口政雄「茸中毒による肢端紅痛症」『十全医学会雑誌』第56巻第9号、金沢大学十全医学会、1954年9月、587-590頁、ISSN 00227226、NAID 110007027807。
- ^ 串上元彦, 池田好秀, 高尾敏彦, 横山申彦, 池田栄夫, 西岡新吾, 矢高勲、「ヤブシメジ中毒により発生した急性胃十二指腸病変の4例」『日本消化器病学会雑誌』 1991年 88巻 2号 p.180-184, 日本消化器病学会
- ^ 川村清一. (1909) 奇ナル中毒症ヲ發スル毒菌からはつだけ (新稱) ニ就テ. 植物学雑誌 23(275, p.487-501. doi:10.15281/jplantres1887.23.275_487
- ^ a b c Kawamura, S. (1911). “On a poisonous fungus, Lactarius torminosus (SCHAEFF.) FR. which causes inflammation of human limbs”. 植物学雑誌 25 (291): 104-115. doi:10.15281/jplantres1887.25.291_104.
- ^ 猪子吉人、1891,菌中毒ノ一奇症,東京医学会雑誌 5: 228-231.
- ^ 磯昇、1891,菌中毒患者一奇症,東京医学会雑誌5: 219-227,
- ^ 小池亮琢・三宅一郎、1900. 「エリトロメラルギー」=肢端紅痛症ノ実験,東京医事新誌(1138): 11-15.
- ^ 登木口進、2011,新潟県のドクササコの歴史(明治時代). 新潟県医師会報(733): 52-53.
- ^ a b 楠田利一郎、1911、「紅肢痛ニ就テ」『十全會雜誌』 1911年 62号 p.1-4, 金澤醫學專門學校十全會
- ^ 【H23.10.31】ドクササコ(キノコ)食中毒の発生について、奈良県、2012年10月31日、2013年11月20日閲覧
- ^ 【魚沼】ドクササコ食中毒が発生しました、新潟県、2013年10月30日、2013年11月20日閲覧[リンク切れ]
- ^ Miura, O. (1936). “Über die pharmakologische Wirkung von Clitocybe acromelalga Ichimura”. Tohoku Journal of Experimental Medicine 30: 150-169. doi:10.1620/tjem.30.150.
- ^ Miura, O. (1936). “Über die Wirkung von Clitocybe acromelalga, Ichimura auf Hähne”. Tohoku Journal of Experimental Medicine 30: 196-202. doi:10.1620/tjem.30.196.
- ^ a b 福渡努, 杉本悦郎, 横山和正, 柴田克己、「ドクササコ(Clitocybe acromelalga)の毒性発現機構解明のためのモデル動物の作成」『食品衛生学雑誌』 2001年 42巻 3号 p.185-189, doi:10.3358/shokueishi.42.185, 日本食品衛生学会
- ^ a b c 田口徹「キノコ毒(アクロメリン酸)の末梢痛み(侵害)受容器における作用機構の探索」(PDF)『上原記念生命科学財団研究報告集』第24巻、上原記念生命科学財団、2010年、1-3頁、2022年1月23日閲覧。
- ^ a b c 白川健一, 星允, 栗林和敏「ドクササコ中毒の3症例:とくに神経症状と治療法について」『新潟医学会雑誌』第94巻第11号、新潟医学会、1980年11月、745-753頁、ISSN 00290440、NAID 40002790239。 (
 要購読契約)
要購読契約)
- ^ a b c d 小川眞(編著)、1987, 見る・採る・食べる きのこカラー図鑑, 講談社、東京, ISBN 4-06-141391-0
- ^ 今関六也、1974,カラー日本のキノコ(山溪カラーガイド64),山と溪谷社、東京, ISBN 9-784-63502-664-2
- ^ a b c d Konno, K. (1989). “Toxic principles from the fungus Clitocybe acromelalga (Dokusasako)”. Nippon Nougeikagaku Kaishi 63: 876-879. doi:10.1271/nogeikagaku1924.63.876.
- ^ a b c 福渡努・杉本悦郎・柴田克己、ドクササコ(Clitocybe acromelalga) の投与がトリプトファン-ナイアシン代謝に及ぼす影響」 『食品衛生学雑誌』 2001年 42巻 3号 p.190-196, doi:10.3358/shokueishi.42.190, 日本食品衛生学会
- ^ 児玉栄一郎・高橋晃二, 龍山秀一、「ドクササコ Clitocybe acromelalga Ichim. による中毒について (PDF) 」『秋田県衛生研究所報』 第3号(昭和31年度)4 調査・研究, (p.38-40}
- ^ a b 今関六也・本郷次雄、1965,続原色日本菌類図鑑,保育社、大阪, ISBN 978-4-586-30042-6,
- ^ a b 大谷吉雄、1968,きのこ-その見分け方-,北隆館、東京,ISBN 978-4-83260-100-0.
- ^ 清水大典、1968.原色きのこ全科-見分け方と食べ方.家の光協会、東京. ISBN 978-4-25953-309-0.
- ^ Konno, K., Hayano, K., Shirahama, H., Saito, H., and T. Matsumoto (1982). “Clitidine, a new toxic pyridine nucleoside from Clitocybe acromelalga”. Tetrahedron 38 (22): 3281-3284. doi:10.1016/0040-4020(82)80107-5.
- ^ 紺野勝弘, 白浜晴久, 松本毅、 「56 ドクササコ有毒成分の研究」 『天然有機化合物討論会講演要旨集』 1982年 25巻 セッションID:56, p.421-428, doi:10.24496/tennenyuki.25.0_421, 天然有機化合物討論会実行委員会
- ^ a b c K. Yamano., and H. Shirahama (1992). “New amino acids from the poisonous mushroom Clitocybe acromelalga”. Tetrahedron 48 (8): 1457-1464. doi:10.1016/S0040-4020(01)92234-3.
- ^ 牛沢勇, 片桐信弥, 加藤鉄三, 平則夫、「ドクササコの毒成分」『医学と生物学』 1977年 94巻 3号 p,251-254, NAID 40000108868
- ^ Yamano, K., and H. Shirahama (1994). “Clitidine 5’-mononucleotide, a toxic pyridine nucleotide from Clitocybe acromelalga”. Phytochemistry 35: 897-899. doi:10.1016/S0031-9422(00)90634-4.
- ^ a b Konno, K., Shirahama, H., and T. Matsumoto (1983). “Isolation and structure of acromelic acid A and B. New kainoids of Clitocybe acromelalga”. Tetrahedron Lett. 23: 939-942. doi:10.1016/S0040-4039(00)81571-3.
- ^ a b c Konno, K., Hashimoto, K., Ohfune. Y., Shirahama, H., and T. Matsumoto (1988). “Acromelic acids A and B. Potent neuroexcitatory amino acids isolated from Clitocybe acromelalga”. J. Am. Chem. Soc. 110: 4807-4815. doi:10.1021/ja00222a044.
- ^ a b Fushiya, S., Sato, S., Kanazawa, T., Kusano, G., and S. Nozoe (1990). “Acromelic acid C. A new toxic constituent of Clitocybe acromelalga : An efficient isolation of acromelic acids”. Tetrahedron Lett. 31: 3901-3904. doi:10.1016/S0040-4039(00)97501-4.
- ^ Fushiya, S., Sato, S., Kera, Y., and S. Nozoe (1992). “Isolation of acromelic acids D and E from Clitocybe acromelalga”. Heterocycles 34: 1277-1280. doi:10.3987/COM-92-6065.
- ^ Shinozaki, H. (1988). “Pharmacology of the glutamate receptors”. Progress of Neurobiology 30: 399-435. doi:10.1016/0301-0082(88)90009-3.
- ^ 篠崎温彦、1987,グルタミル酸類似物質,代謝24: 807-815.
- ^ a b Tsuji, K., Nakamura, Y., Ogata, T., Mitani, A., Kataoka, K., Shibata, T., Ishida, M., and H. Shinozaki (1995). “Neurotoxicity of acromelic acid in cultured neurons from rat spinal cord”. Neuroscience 68: 585-591. doi:10.1016/0306-4522(95)00149-D. PMID 7477968.
- ^ a b Minami, T., Matsumura, S., Nishizawa, M., Sasaguri, Y., Hamanaka, N., and S. Ito (2004). “Acute and late effects on induction of allodynia by acromelic acid, a mushroom poison related structurally to kainic acid”. Br. J. Pharmacol. 142: 679-688. doi:10.1038/sj.bjp.0705834. PMC 1575046. PMID 15159282.
- ^ Taguchi, T., Tomotoshi, K., and K. Mizumura (2009). “Excitatory actions of mushroom poison (acromelic acid) on unmyelinated muscular afferents in the rat”. Neurosci. Lett. 456: 69-73. doi:10.1016/j.neulet.2009.03.102. PMID 19429136.
- ^ Baldwin, J. E., Fryer, A. M. and G. J. Pritchard (2000). “Novel C-4 Heteroaromatic Kainoid Analogues: A Parallel Synthesis Approach”. Bioorg. Med. Chem. Lett. 10: 309-311. doi:10.1016/S0960-894X(99)00690-3. PMID 10698461.
- ^ Fushiya, S., Sato, S., and S. Nozoe (1992). “L-Stizolobic acid and L-stizolobinic acid from Clitocybe acromelalga, precursors of acromelic acids”. Phytochemistry 31: 2337-2339. doi:10.1016/0031-9422(92)83276-5.
- ^ Yamano, K., Hashimoto, K., and H. Shirahama (1992). “Novel Neuroexcitatory Amino Acid from Clitocybe acromelalga”. Heterocycles 34: 445-448. doi:10.3987/COM-91-5950.
- ^ Yamano, K., and H. Shirahama (1993). “New amino acids from Clitocybe acromelalga. Possible intermediates in the biogenesis of mushroom toxins, acromelic acids”. Tetrahedron 49: 2427-2436. doi:10.1016/S0040-4020(01)86321-3.
- ^ Konno. K., Shirahama, H., and T. Matsumoto (1981). “Isolation and structure of Clithioneine, a new amino acid betaine from Clitocybe acromelalga”. Tetrahedron Lett. 22: 1617-1618. doi:10.1016/S0040-4039(01)90392-2.
- ^ Konno, K., Shirahama, H., and T. Matsumoto (1984). “Clithioneine, an amino acid betaine from Clitocybe acromelalga”. Phytochemistry 23: 1003-1006. doi:10.1016/S0031-9422(00)82600-X.
- ^ Hirayama, F., Konno, K., Shirahama, H., and M. Matsumoto (1989). “4-Aminopyridine-2,3-dicarboxylic acid from Clitocybe acromelalga”. Phytochemistry 18: 1133-1135. doi:10.1016/0031-9422(89)80196-7.
- ^ Yamano, K., and H. Shirahama (1994). “A Piperidine Amino Acid, 2,4,5-Piperidine tricarboxylic Acid from Clitocybe acromelalga”. Z. Naturforsch. C 49: 707-711. doi:10.1515/znc-1994-11-1203. PMID 7865029.
- ^ Yamano, K., and H. Shirahama (1994. The structure of a new dipeptide from the mushroom, Clitocybe acromelalga). Z. Naturforsch. C 49: 157-162. doi:10.1515/znc-1994-3-401. PMID 8018249.
- ^ Fushiya, S., Matsuda, M., Yamada, S., and S. Nozoe (1996). “New opine type amino acids from a poisonous mushroom, Clitocybe acromelalga”. Tetrahedron 52: 877-886. doi:10.1016/0040-4020(95)00929-9.
- ^ a b 黒野吾一・酒井健・栃折妍子・瀬尾信雄、1958,ヤブシメジ(火傷菌) Clitocybe acromelalga Ichimura 中のD-mannitolの存在について,金沢大学薬学部研究報告 8: 40-41,
- ^ a b c 今関六也, 本郷次雄(編著)、1987. 原色日本新菌類図鑑(Ⅰ). 保育社. ISBN 4-586-30075-2
- ^ 青木実・日本きのこ同好会(著),名部みち代(編)、2008,日本きのこ図版(第一巻:ヒラタケ科・ヌメリガサ科・キシメジ科),日本きのこ同好会2、神戸,
- ^ 本郷次雄、1997,日本菌類誌資料(50),日本菌学会会報38: 99-100.
- ^ Murata, Y. (1979). “New records of gill fungi from Hokkaido (5)”. Transactions of the Mycological Society of Japan 20: 133-140.
- ^ Malençon, G. and R. Bertault., 1975. Flore des champignons supérieurs du Maroc, tome 2. Trav. Inst. Scient. Chérifien et Faculté des Sciences de Rabat, Série Botanique et Biologie Végétale n°33: 1-540 + 22 pls. en couleurs.
- ^ Saviuc, P., de Matteis, M.., Bessard, J., Mézin, P., Moreau, P. A., Chane-Yene, Y., Mallaret, M., Guez, D., and V. Danel (2001). “Erythromelalgia and mushroom poisoning (Clitocybe amoenolens)”. Eur. J. Emerg. Med. 8: 74.
- ^ Moreau, P.-A., Courtecuisse, R., Guez, D., Garcin, R., Neville, P., Saviuc, P., and F. Seigle-Murandi (2001). “Analyse taxinomique d'une espèce toxique: Clitocybe amoenolens Malençon”. Cryptogamie Mycologie 22: 95-117. doi:10.1016/S0181-1584(01)80003-8.
- ^ Stijve, T. (2001). “Beware of those brown Clitocybes ! – a new poisonous mushroom in Europe”. Field Mycology 2: 77-79. doi:10.1016/S1468-1641(10)60101-6.
- ^ Saviuc, P., Dematteis, M., Mezin, P., Danel, V., and M. Mallaret (2003). “Toxicity of the Clitocybe amoenolens mushroom in the rat”. Vet. Hum. Toxicol. 45: 180-182. PMID 12882485.
- ^ (仮訳)Paralepistopsis amoenolens:トルコ新産の稀な毒きのこ, 大菌林
- ^ Bessard, J., Saviuc, P., Chane-Yene, Y., Monnet, S., G. Bessard (2004). “Mass spectrometric determination of acromelic acid A from a new poisonous mushroom: Clitocybe amoenolens”. J. Chromatogr. A 1055: 99-107. doi:10.1016/j.chroma.2004.08.133. PMID 15560485.
- ^ Haro, L. de (2009). “Mushroom intoxications: situation in France with discovery of new syndromes”. Pagine di Micologia 32: 59-63.
- ^ Paralepistopsis amoenolens: First Record of A Rare and Poisonous Taxon in Turkey
- ^ 今関六也・本郷次雄(編著)、1989. 原色日本新菌類図鑑(Ⅱ). 保育社、大阪. ISBN 4-586-30076-0.
- ^ Elvin-Lewis, M. P. F., and W. h. Lewis (2003). Medical Botany: Plants Affecting Human Health. Chichester, UK: John Wiley & Sons. pp. 832. ISBN 0-471-62882-4
- ^ Camazine, S., and T. L. Lupo Jr. (1984). “Labile toxic compounds of the Lactarii: the role of the laticiferous hyphae as a storage depot for precursors of pungent dialdehydes”. Mycologia 76: 355–3588. doi:10.2307/3793113.
- ^ Widen, K. G., and E. L. Seppa (1979). “15-Hydroxyblennin A, a new lactarane-type sesquiterpene lactone isolated from Lactarius torminosus”. Phytochemistry 18: 1226–1227. doi:10.1016/0031-9422(79)80144-2.
- ^ Abraham, W.-R. (2001). “Bioactive sesquiterpenes produced by fungi: are they useful for humans as well?”. Curr. Med. Chem. 8: 583–606. doi:10.2174/0929867013373147. PMID 11281843.
- ^ 長沢栄史(監修)、2009,増補改訂版 日本の毒きのこ (フィールドベスト図鑑),pp. 288. 学習研究社、東京,ISBN 978-4054042636
- ^ a b c d 山田詩郎、1932,末端紅痛症ヲ主訴トセル菌(どくさゝこ-新邦名)中毒ニ就テ,診断ト治療19: 1080-1103,
- ^ 今関六也・本郷次雄、1957,原色日本菌類図鑑,保育社、大阪, ISBN 458630023X
- ^ 幼菌の会(編)、2001,カラー版 きのこ図鑑, 家の光協会、東京,ISBN 4259539671,
- ^ 今関六也・大谷吉雄・本郷次雄(編)、2011. 山溪カラー名鑑 日本のきのこ(増補改訂新版),山と溪谷社、東京, ISBN 978-4-635-09044-5,
- ^ Liddell, H. J., and R. Scott, 1996. Greek-English Lexicon (with a reviced supplement). Oxford University Press, Oxford, UK. ISBN 978-0198642268.
- ^ a b 奥沢康正・奥沢正紀、1999,きのこの語源・方言事典,山と溪谷社、東京,ISBN 978-4-63588-031-2,
- ^ 長野県環境保全研究所・長野県生活環境部環境自然保護課(編). 2005. 長野県版レッドデータブック 長野県の絶滅のおそれのある野生生物 非維管束植物編・植物群落編,長野県環境保全研究所、長野,
- ^ 三重県生物多様性調査検討委員会(編)、2005,三重県レッドデータブック 2005,財団法人 三重県環境保全事業団、津,
- ^ 兵庫県農政環境部環境創造局自然環境課(編)、2011,兵庫の貴重な自然 兵庫県版レッドデータブック2010,財団法人ひょうご環境創造協会、神戸,
参考文献
[編集]- 大作晃一『きのこの呼び名事典』世界文化社、2015年9月10日。ISBN 978-4-418-15413-5。
- 大作晃一・吹春俊光『おいしいきのこ毒きのこ : 見分け方がよくわかる!』主婦の友社〈主婦の友ベストBOOKS〉、2010年9月30日。ISBN 978-4-07-273560-2。
- 長沢栄史 監修 学習研究社 編『日本の毒きのこ』学習研究社〈増補改訂フィールドベスト図鑑 13〉、2009年9月28日。ISBN 978-4-05-404263-6。