トリス(エチレンジアミン)コバルト(III)塩化物
| トリス(エチレンジアミン)コバルト(III)塩化物 Tris(ethylenediamine)cobalt(III) chloride | |
|---|---|

| |
|
|
cobalt tris(ethylenediamine) chloride | |
別称 tris(ethylenediamine)cobalt(III) chloride | |
| 識別情報 | |
| CAS登録番号 | 207802-43-5 |
| PubChem | dihydrate:: 71311392trihydrate:: 73995044 |
| ChemSpider | 147079 |
| |
| |
| 特性 | |
| 化学式 | C6H24N6Cl3Co |
| モル質量 | 345.59 |
| 外観 | 黄金色の固体 |
| 融点 |
275 °C, 548 K, 527 °F (分解) |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
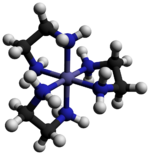
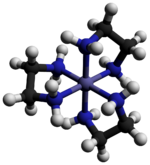
トリス(エチレンジアミン)コバルト(III)塩化物(英語: Tris(ethylenediamine)cobalt(III) chloride)は、[Co(en)3]Cl3(en = エチレンジアミン)の化学式を持つ無機化合物である[1]。これは、配位錯体[Co(en)3]3+の塩化物塩である。この三価カチオンは、その安定性と立体化学のために、配位化学の歴史において重要な役割を果たした。多くの異なる塩が報告されている。この錯体は、アルフレッド・ウェルナーによって初めて報告され[1]、彼はこの塩を黄金色の針状結晶として単離した。
合成と構造
[編集]この化合物は、エチレンジアミンと、塩化コバルト(II)など、事実上あらゆるコバルト(II)塩の水溶液から調製される。この溶液に空気を吹き込み、コバルト(II)-エチレンジアミン錯体をコバルト(III)に酸化する。反応は95%の収率で進行し、この三価カチオンは様々なアニオンを用いて単離できる。大規模合成の詳細な生成物分析により、副生成物の一つとして、珍しい単座配位のエチレンジアミン配位子(プロトン化)を含む[Co(en)2Cl(H2NCH2CH2NH3)]Cl3が少量得られることが明らかになった[2]。
カチオン[Co(en)3]3+は、1.947–1.981Åの範囲のCo-N距離を持つ八面体形である[3]。N-Co-N角は、キレート環内では85°、隣接する環の窒素原子間では90°である。
立体化学
[編集]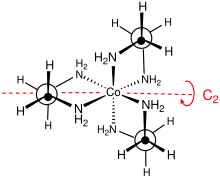
この錯体の点群はD3である。この錯体は、ΔおよびΛと表記されるエナンチオマーに分割できる。通常、分割には酒石酸塩が用いられる[4]。光学分割は無機合成のコースの標準的な要素である[5]。その非平面性のために、MN2C2環は、λおよびδという記号で表される2つの立体配座のいずれかをとることができる。これらの環の立体配座と金属中心の絶対配置との関係は、lel(en骨格がC3対称軸と平行な場合)またはob(en骨格がこのC3軸と逆の場合)という用語で表される。したがって、以下のジアステレオマー立体配座を識別できる。Δ-(lel)3、Δ-(lel)2(ob)、Δ-(lel)(ob)2、およびΔ-(ob)3。もちろん、これらの種の鏡像異性体も存在する[6]。
水和物
[編集]アンモニアおよびアルキルアミンのカチオン性配位錯体は、典型的には結晶格子中に水和水を含んで結晶化し、その化学量論は結晶化の条件、およびキラル錯体の場合はカチオンの光学純度によって異なる場合がある。ラセミ体[Co(en)3]Cl3は、ほとんどの場合、二水和物または三水和物として得られる。光学的に純粋な塩としては、(+)-[Co(en)3]Cl3·1.5H2O、(+)-[Co(en)3]Cl3·0.5NaCl·3H2O、および(+)-[Co(en)3]Cl3·H2Oも知られている[3]。
参考文献
[編集]- ^ a b A.Werner (1912). “ZurKenntnisdesasymmetrischenKobaltatoms.V”. ChemischeBerichte 45 (1): 121–130. doi:10.1002/cber.19120450116 2024年10月1日閲覧。.
- ^ JackM.Harrowfield; MarkI.Ogden; BrianW.Skelton; AllanH.White (2005). “AlfredWernerRevisited:SomeSubtletiesofComplexIonSynthesisandIsomerism”. ComptesRendusChimie 8 (2): 121–128. doi:10.1016/j.crci.2004.10.013. hdl:20.500.11937/8231 2024年10月1日閲覧。.
- ^ a b D.Witiak,J.C.Clardy,andD.S.Martin,Jnr. (1972). “TheCrystalStructureof(+)-D-Tris(ethylenediamine)cobalt(III)Nitrate”. ActaCrystallographica B28 (9): 2694–2699. Bibcode: 1972AcCrB..28.2694W. doi:10.1107/S056774087200679X.
- ^ J.A.Broomhead; F.P.Dwyer; J.W.Hogarth (1960). “ResolutionoftheTris(Ethylenediamine)Cobalt(III)Ion”. InorganicSyntheses. VI. pp. 183–186. doi:10.1002/9780470132371.ch58. ISBN 978-0-470-13237-1
- ^ Girolami,G.S.;Rauchfuss,T.B.andAngelici,R.J.,SynthesisandTechniqueinInorganicChemistry,UniversityScienceBooks:MillValley,CA,1999ISBN 0-935702-48-2
- ^ vonZelewsky,A."StereochemistryofCoordinationCompounds"JohnWiley:Chichester,1995ISBN 047195599X
