ダームスタチウム
原文と比べた結果、この記事には多数の(または内容の大部分に影響ある)誤訳があることが判明しています。情報の利用には注意してください。 (2023年1月) |
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 外見 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|---|
| 不明 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 一般特性 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 名称, 記号, 番号 | ダームスタチウム, Ds, 110 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 分類 | 遷移金属 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 族, 周期, ブロック | 10, 7, d | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子量 | [281] | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 電子配置 | [Rn]7s15f146d9 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 電子殻 | 2, 8, 18, 32, 32, 17, 1(画像) | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 物理特性 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 相 | 不明 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 原子特性 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 共有結合半径 | 128 pm | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| その他 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| CAS登録番号 | 54083-77-1 | ||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 主な同位体 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| 詳細はダームスタチウムの同位体を参照 | |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
| |||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||||
ダームスタチウム(英: darmstadtium [dɑːrmˈstætiəm, dɑːrmˈʃtætiəm])は、元素記号Ds、原子番号110の化学元素である。放射性が非常に高い人工元素で、最も安定な同位体であるダームスタチウム281の半減期は約12.7秒である。1994年にドイツ・ダルムシュタットの重イオン研究所で初めて合成され、都市の名前に因んで命名された。
周期表上では、dブロック元素である。第7周期元素、第10族元素であるが、第10族元素の白金の同族元素として振る舞うことを確認する化学実験は未だ行われていない。計算では、より軽い同族元素であるニッケル、パラジウム、白金と似た性質を持つとされる。
導入
[編集]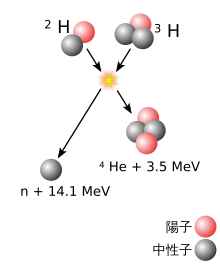
重い[注釈 1]原子核は、2つの異なる原子核[注釈 2]の核融合反応により形成され、おおまかに、2つの原子核の質量の差が大きいほど、反応の可能性は高くなる[6]。重い方の原子核を持つ物質を標的とし、軽い原子核の粒子線を照射することで、2つの原子核が十分に接近すると、1つの原子核への融合が起こりうる。通常、陽電荷を持つ2つの原子核は、クーロンの法則により互いに反発する。原子核同士が非常に近づくときのみ、強い相互作用がこの反発力に打ち克つ。そのため、粒子線となる原子核の速度を、この反発力が無視できる程度まで、加速器で加速する必要がある。ただし、2つの原子核が融合するためには、2つの原子核が単に近づくだけでは不十分である。2つの原子核が近づいただけでは、通常、1つの原子核に融合するのではなく、10-20秒間だけ一緒に留まった後、離れていく(この時、反応前と同じ構成とは限らない)[7][8]。核融合が起こる場合、複合核と呼ばれる一時的な融合状態が励起状態となる。励起エネルギーを失い、より安定な状態に達すると、複合核は核分裂反応を起こすか、1つまたはいくつかの原子核の核破砕反応を起こして、エネルギーを持ち去る[注釈 3]。この事象は、最初の衝突の約10-16秒後に起こる[9][注釈 4]
粒子線が標的を通り過ぎると、次のチェンバーであるセパレーターに移送される。新しい原子核ができていると、この粒子線により運ばれる[12]。セパレーターでは、生成した原子核は他の原子核(粒子線の原子核やその他の反応生成物)から分離され[注釈 5]、表面障壁型半導体検出器に運ばれる。粒子はそこで停止し、検出器上での正確な衝突位置とそのエネルギー、到達時間が記録される[12]。移送には約10-6秒を必要とし、検出までに原子核はこの長時間を生き残る必要がある[15]。崩壊が起こると、原子核の位置、エネルギー、崩壊時間が再度記録される[12]。
原子核の安定性は、強い相互作用によってもたらされる。しかしそれが及ぶ範囲は非常に短く、原子核が大きくなるほど、最外殻の核子(陽子と中性子)が強い相互作用から受ける影響は小さくなっていく。同時に、陽子間の静電反発により原子核は引き裂かれ、これは範囲の制約がない[16]。そのため、重元素の原子核は、このような反発によるアルファ崩壊や自発核分裂[注釈 6]のようなモードが主要な崩壊過程になると理論的に予測されており[18]、これまで実際の観測もそれを裏付けてきた[19]。このような崩壊モードは、超重元素の原子核には支配的なものである。アルファ崩壊は、放出されたアルファ粒子により記録され、崩壊生成物は実際の崩壊前に容易に決定できる。一度の崩壊や連続した崩壊により既知の原子核が生成されると、計算により反応の出発点となる原子核が決定できる[注釈 7]。しかし、自発核分裂では生成物として様々な原子核が生じ、そのため、娘核からは、出発点となる原子核が決定できない[注釈 8]。
重い元素を合成しようとする物理学者が得られる情報は、このように検出器により収集される、粒子が検出器に衝突した距離、エネルギー、時間と、崩壊の際の同様の情報となる。物理学者はこのデータを分析し、これが新元素によって引き起こされたものであり、他の核種により引き起こされたものではないと結論付けようとする。しばしば、得られたデータは、新元素の生成を確定するには不十分なものであったり、解釈の誤りの元となりうる[注釈 9]。
歴史
[編集]
発見
[編集]1994年11月9日にシグルド・ホフマンの指揮の下、ペーター・アルムブルスターとゴットフリート・ミュンツェンベルクが率いる重イオン研究所の国際チームによって初めて合成された。チームは、重イオン加速器中で鉛208の標的にニッケル62の加速した原子核を照射し、ダームスタチウム269の1つの原子核を検出した[29]。
- 20882Pb + 6228Ni → 269110Ds + 10n
11月12日と17日にさらに2つの原子が得られた[29](当初は11日にもう1つの原子も合成されたと報告されたが、これはヴィクトル・ニノフによる捏造されたデータに基づくもので、後に撤回された[30])。
同じ一連の実験で、同じチームがより重いニッケル64を用いた反応も行った。2回の実験で、2原子の271Dsの検出が既知の娘核種の崩壊特性との相関により確認された[31]。
- 20882Pb + 6428Ni → 271110Ds + 10n
この前の1986-1987年に、当時ソビエト連邦のドゥブナ合同原子核研究所において、また1990年に重イオン研究所において、合成の試みが行われて失敗していた。1995年には、ローレンス・バークレー国立研究所によるビスマス209にコバルト59を照射する試みで、新しい同位体である267Dsの発見を示す兆候が見られたが、確定には至らなかった。同様に、1994年にドゥブナ合同原子核研究所で244Puと34Sから273Ds合成の兆候が見られたが、確定はしていない。元素110については、それぞれのチームが独自の命名を提案した。アメリカのチームは、長い間論争を続けていた元素105の命名を巡る議論の解決に向けて、オットー・ハーンに因んだハーニウムという名前を提案した。ロシアのチームは、アンリ・ベクレルに因むベクレリウム、ドイツのチームは、彼らの研究所が所在するダルムシュタットに因むダームスタチウムという名前を提案した[32]。IUPAC/IUPAP合同作業部会は、2001年の報告でドイツのチームを発見者と認定し、命名権を与えた[33]。
命名
[編集]ドミトリ・メンデレーエフによる未命名・未発見元素の命名規則により、110番元素は、エカ白金として知られていた。1979年、国際純正・応用化学連合は勧告を出し、それにより110番元素は発見が確定し正式に命名されるまでの間、ウンウンニリウム(記号:Uun)と呼ばれることになった[34]。この名前は、化学の授業からより上級の教科書まで、あらゆるレベルの化学コミュニティで広く使われているが、この分野の多くの科学者からはほぼ無視されており、「元素110」と呼ばれたり、E110、(110)または単に110という記号で表される[35]。
1996年、ロシアのチームは、アンリ・ベクレルの名前に因んでベクレリウムという名前を提案した[36]。1997年にアメリカのチームは、オットー・ハーンの名前に因んでハーニウムという名前を提案した[37](それまでこの名前は、105番元素に対して提案されていた)。
ダームスタチウムという名前は、発見地であるダルムシュタットに因んで、重イオン研究所のチームにより提案された[38][39]。ドイツのチームは当初、発見地のダルムシュタット郊外にあるヴィクスハウゼンに因んだヴィクスハウジウムという名前も検討していたが、最終的にダームスタチウムに決定した[40]。ドイツの緊急通報の番号が1-1-0であることから、ポリシウムという名前もジョークとして提案された。ダームスタチウムという新しい名前は、2003年8月16日に国際純正・応用化学連合により正式に認定された[38]。
同位体
[編集]ダームスタチウムは安定な同位体や天然に生成する同位体を持たない。いくつかの放射性同位体が、より軽い原子核の融合かより重い原子核の崩壊の中間体として、研究室内で合成されている。原子量が267、269-271、273、276、277、279-281(267は未確定)の10個の同位体が報告されている。そのうち、原子量が270、271と281のものは、未確定の準安定状態を持つ(281は未確定)[41]。これらの崩壊の大部分はアルファ崩壊によるものであるが、自発核分裂するものもいくつかある[42]。
安定性と半減期
[編集]
全てのダームスタチウム同位体は非常に不安定で放射性が高い。一般的に、より重い同位体であるほどより安定性が高い。最も安定な既知の同位体は、既知の最も重い同位体でもある281Dsであり、半減期は12.7秒である。279Dsの半減期は0.18秒、未確定の281mDsの半減期は0.9秒である。残り7つの同位体、2つの準安定状態の半減期は、1ミリ秒から70ミリ秒の間である[42]。しかし、未知の同位体がより長い半減期を持つ可能性がある[44]。
トンネル効果モデルに基づく理論計算により、既知の同位体に対して、実験的によるアルファ崩壊の半減期のデータが再現された[45][46]。また、中性子の魔法数(184)を持つ未発見の同位体294Ds[35]のアルファ崩壊の半減期は311年と予測された。しかし、全く同じ方法で非魔法数の293Dsのアルファ崩壊の半減期は約350年と予測される[44][47]。
予測される性質
[編集]核特性を除き、ダームスタチウム及びその化合物の性質は測定されていない。これは、合成が非常に限られており、また高価なことと[6]、非常に速く崩壊するためである。金属ダームスタチウムの性質は、予測値のみが利用可能である。
化学的性質
[編集]ダームスタチウムは、6dブロックの8番目の遷移元素である[39]。イオン化ポテンシャルや原子半径、イオン半径の計算は、より軽いホモログである白金と類似しており、そのため、ダームスタチウムの基本的な性質は第10族のニッケル、パラジウム、白金と類似していることが示唆される[35]。貴金属であると予測されている。
ダームスタチウムの化学的性質の予測は、最近あまり関心を持たれていない。標準電極電位は、Ds2+ / Ds対に対して1.7 Vと予測される[35]。より軽い第10族元素の最も安定な酸化状態に基づき、ダームスタチウムの最も安定な酸化状態は+6、+4と+2であると予測される。しかし、水溶液中では中性状態が最も安定と予測される。対照的に、第10族の中で最大の酸化状態である+6を示すのはパラジウムと白金のみであり、ニッケルとパラジウムにとって、最も安定な酸化状態は+4と+2である。さらに、ボーリウム(原子番号107)からダームスタチウム(原子番号110)の元素の最大酸化状態は、気相で安定であり、水溶液中ではない[35]。六フッ化ダームスタチウムは、六フッ化白金と非常に似た電子配置とイオン化ポテンシャルを持っており、非常によく似た性質を持つと予測され[35][48][49]、同じ八面体形分子構造を持つと予測される[50]。ほかに予測される分子には、炭化ダームスタチウム、四塩化ダームスタチウム等があり、どちらもより軽いホモログと同様に振る舞うと予測されている[50]。+2の酸化状態でシアン化物(Pt(CN)2)を形成しやすい白金とは異なり、ダームスタチウムは中性状態を保ったまま多重結合の性質を持つ強いDs-C結合を形成し、Ds(CN)22-を形成する傾向がある[51]。
物理学的性質
[編集]標準状態では固体であり、電子電荷密度が異なるため、面心立方格子に結晶化するより軽い同族体とは異なり、体心立方格子に結晶化する[52]。実測された中で最も密度が高いオスミウムの22.61 g/cm3に対し、密度が約26-27 g/cm3と非常に重い金属である[53][54]。
最外殻の電子配置は6d8 7s2と計算され、構造原理に従い、白金の最外殻電子配置5d9 6s1とは異なる。これは、第7周期元素に共通する7s2電子対の相対論的安定化のためであり、そのため、原子番号104番から112番の元素で、構造原理に反する電子配置を持つものはない。原子半径は、約132 pmと推定される[35]。
ダームスタチウムに関する実験
[編集]同位体の半減期が短く、小規模での実験が可能な揮発性化合物の数が限られているため、化学的性質はまだはっきりとは分かっていない[55]。十分な揮発性を持つ可能性がある数少ないダームスタチウムの化合物には、60℃以上で揮発性を持つ六フッ化白金(PtF6)のアナログである六フッ化ダームスタチウム(DsF6)がある[39]。また、揮発性を持つ八フッ化物(DsF8)も存在できる可能性がある[35]。超アクチノイド元素の化学研究のためには、半減期が1秒以上、1週間に1原子以上の合成速度で、少なくとも4原子以上の合成が必要となる[39]。最も安定な281Dsの半減期は12.7秒であり、化学研究を行うのに十分な長さを持つが、統計的に有意な結果が得られるよう、実験を数週間から数か月続けるために、合成速度を上げる必要がある。重い元素の収量は軽い元素よりも少ないと予測されるため、気相及び溶液内の化学実験を自動化されたシステムで行うためには、ダームスタチウム同位体の分離と検出を連続して行うことが必要である。このために、ボーリウムやハッシウムの合成で使われた分離技術を再利用することができる。しかし、コペルニシウムからリバモリウムまでのより重い元素と比べて、ダームスタチウムの実験化学に対する関心は高くない[35][55][56]。
中性子の数が多い同位体ほど安定であり[42]、化学研究に有望であるが[35][39]、これらはより重い元素のアルファ崩壊による間接的な合成しかできず[57][58][59]、間接的な合成法は、化学研究にとって、直接的な合成法ほど望ましくない[35]。276Dsや277Dsは、トリウム232やカルシウム48の反応から直接合成できる可能性があるが、収率は低いと考えられている[35][60][61]。何度も失敗した後、1原子の276Dsが2022年にこの反応で合成されたが、正確な値は未公表であるものの、予測通り、半減期は短く低収率であった[62]。さらに、277Dsは、285Flの孫娘核として間接的な方法で合成され、化学研究を行うには短すぎる3.5ミリ秒の半減期であることが分かった[63][58]。化学研究を行うのに十分な長さの半減期を持つ既知の同位体は281Dsであり、289Flの孫娘核として合成できる[64]。
脚注
[編集]- ^ 核物理学では、原子番号の大きい元素は、「重い」元素と呼ばれる。原子番号82の鉛は、重い元素の一例である。「超重元素」という用語は、通常、原子番号103番以降の元素を指す(ただし、原子番号100[1]以降とするものや112以降[2]とするもの等、いくつかの定義がある。超アクチノイド元素と同義の言葉として使われることもある[3])。ある元素における「重い同位体」や「重い核」という言葉は、各々、質量の大きい同位体、質量の大きい核を指す。
- ^ 2009年、ユーリイ・オガネシアン率いるドゥブナ合同原子核研究所のチームは、対称の136Xe + 136Xe反応におるハッシウム合成の試みの結果について公表した。彼らはこの反応で単原子を観測できず、反応断面積の上限を2.5 pbとした[4]。対称的に、ハッシウムの発見に繋がった反応である208Pb + 58Feの反応断面積は、発見者らにより19+19-11pbと推定された[5]。
- ^ 励起エネルギーが大きくなるほど、より多くの中性子が放出される。励起エネルギーが、各々の中性子を残りの核子に結び付けるエネルギーより低い場合、中性子は放出されない。その代わり、複合核はガンマ線を放出して脱励起する[9]。
- ^ 共同作業部会による定義では、その核が10-14秒にわたり崩壊しない場合にのみ、発見として認定される。この値は、原子核が外側の電子を獲得して化学的性質を示すのにかかる時間の推定値として選択された[10]。また、一般的に考えられる複合核の寿命の上限値を示すものでもある[11]。
- ^ この分離は、生成した原子核が未反応の粒子線の原子核よりも、標的の上をよりゆっくり通り過ぎることに基づく。セパレーター内には、特定の粒子速度で移動する粒子への影響が相殺される電磁場がある[13]。このような分離は、飛行時間型質量分析計や反跳エネルギー測定でも用いられ、この2つを組み合わせて、原子核の質量を推定することが可能となる[14]。
- ^ 全ての崩壊モードが静電反発を原因とするのではなく、例えば、ベータ崩壊の原因は弱い相互作用である[17]。
- ^ 原子核の質量は直接測定されず、ほかの原子核の値から計算され、このような方法を間接的と呼ぶ。直接測定も可能であるが、もっとも重い原子核についてはほとんどの場合可能ではない[20]。超重元素の質量の直接測定は、2018年にローレンス・バークレー国立研究所により初めて報告された[21]。
- ^ 自発核分裂は、ドゥブナ合同原子核研究所を率いていたゲオルギー・フリョロフにより発見され[22]、この研究所の得意分野となった[23]。対称的に、ローレンス・バークレー国立研究所の科学者は、自発核分裂から得られる情報は新元素の合成を裏付けるのに不十分であると信じていた。これは、複合核が中性子だけを放出し、陽子やアルファ粒子のような荷電粒子を放出しないことを立証するのは困難なためである[11]。そのため彼らは、連続的なアルファ崩壊により、新しい同位体を既知の同位体と結び付ける方法を好んだ[22]。
- ^ 例えば、1957年にスウェーデンのノーベル物理学研究所は、102番元素を誤同定した[24]。これ以前にこの元素の合成に関する決定的な主張はなく、発見者により、ノーベリウムと命名されたが、後に、この同定は誤りであったことが分かった[25]。翌年、ローレンス・バークレー国立研究所は、ノーベル物理学研究所による結果は再現性がなく、代わりに彼ら自身がこの元素を合成したと発表したが、この主張も後に誤りであったことが判明した[25]。ドゥブナ合同原子核研究所は、彼らこそがこの元素を最初に合成したと主張し、ジョリオチウムと命名したが[26]、この名前も認定されなかった(ドゥブナ合同原子核研究所は、のちに、102番元素の命名は「性急」であったと述べた)[27]。「ノーベリウム」という名前は、広く使われていたため、変更されなかった[28]。
出典
[編集]- ^ Kramer, K. (2016年). “Explainer: superheavy elements”. Chemistry World. 2020年3月15日閲覧。
- ^ “Discovery of Elements 113 and 115”. Lawrence Livermore National Laboratory. 2015年9月11日時点のオリジナルよりアーカイブ。2020年3月15日閲覧。
- ^ Eliav, E.; Kaldor, U.; Borschevsky, A. (2018). "Electronic Structure of the Transactinide Atoms". In Scott, R. A. (ed.). Encyclopedia of Inorganic and Bioinorganic Chemistry. John Wiley & Sons. pp. 1–16. doi:10.1002/9781119951438.eibc2632. ISBN 978-1-119-95143-8. S2CID 127060181。
- ^ Oganessian, Yu. Ts.; Dmitriev, S. N.; Yeremin, A. V. et al. (2009). “Attempt to produce the isotopes of element 108 in the fusion reaction 136Xe + 136Xe”. Physical Review C 79 (2): 024608. doi:10.1103/PhysRevC.79.024608. ISSN 0556-2813.
- ^ Munzenberg, G.; Armbruster, P.; Folger, H. et al. (1984). “The identification of element 108”. Zeitschrift fur Physik A 317 (2): 235-236. Bibcode: 1984ZPhyA.317..235M. doi:10.1007/BF01421260. オリジナルの7 June 2015時点におけるアーカイブ。 20 October 2012閲覧。.
- ^ a b Subramanian, S. (2019年). “Making New Elements Doesn't Pay. Just Ask This Berkeley Scientist”. Bloomberg Businessweek. November 14, 2020時点のオリジナルよりアーカイブ。2020年1月18日閲覧。
- ^ Ivanov, D. (2019年). “Сверхтяжелые шаги в неизвестное” [Superheavy steps into the unknown] (ロシア語). N+1. 2020年2月2日閲覧。
- ^ Hinde, D. (2014年). “Something new and superheavy at the periodic table”. The Conversation. 2020年1月30日閲覧。
- ^ a b Krasa, A. (2010年). “Neutron Sources for ADS”. Czech Technical University in Prague. pp. 4-8. 2019年3月3日時点のオリジナルよりアーカイブ。October 20, 2019閲覧。
- ^ Wapstra, A. H. (1991). “Criteria that must be satisfied for the discovery of a new chemical element to be recognized”. Pure and Applied Chemistry 63 (6): 883. doi:10.1351/pac199163060879. ISSN 1365-3075 2020年8月28日閲覧。.
- ^ a b Hyde, E. K.; Hoffman, D. C.; Keller, O. L. (1987). “A History and Analysis of the Discovery of Elements 104 and 105”. Radiochimica Acta 42 (2): 67-68. doi:10.1524/ract.1987.42.2.57. ISSN 2193-3405.
- ^ a b c Chemistry World (2016年). “How to Make Superheavy Elements and Finish the Periodic Table [Video]”. Scientific American. 2020年1月27日閲覧。
- ^ Hoffman, Ghiorso & Seaborg 2000, p. 334.
- ^ Hoffman, Ghiorso & Seaborg 2000, p. 335.
- ^ Zagrebaev, Karpov & Greiner 2013, p. 3.
- ^ Beiser 2003, p. 432.
- ^ Beiser 2003, p. 439.
- ^ Staszczak, A.; Baran, A.; Nazarewicz, W. (2013). “Spontaneous fission modes and lifetimes of superheavy elements in the nuclear density functional theory”. Physical Review C 87 (2): 024320-1. arXiv:1208.1215. Bibcode: 2013PhRvC..87b4320S. doi:10.1103/physrevc.87.024320. ISSN 0556-2813.
- ^ Audi et al. 2017, pp. 030001-128–030001-138.
- ^ Oganessian, Yu. Ts.; Rykaczewski, K. P. (2015). “A beachhead on the island of stability”. Physics Today 68 (8): 32-38. Bibcode: 2015PhT....68h..32O. doi:10.1063/PT.3.2880. ISSN 0031-9228. OSTI 1337838.
- ^ Grant, A. (2018). “Weighing the heaviest elements”. Physics Today. doi:10.1063/PT.6.1.20181113a.
- ^ a b Robinson, A. E. (2019). “The Transfermium Wars: Scientific Brawling and Name-Calling during the Cold War”. Distillations 2020年2月22日閲覧。.
- ^ “Популярная библиотека химических элементов. Сиборгий (экавольфрам)” [Popular library of chemical elements. Seaborgium (eka-tungsten)] (ロシア語). n-t.ru. 2020年1月7日閲覧。 Reprinted from “Экавольфрам [Eka-tungsten]” (ロシア語). Популярная библиотека химических элементов. Серебро - Нильсборий и далее [Popular library of chemical elements. Silver through nielsbohrium and beyond]. Nauka. (1977)
- ^ “Nobelium - Element information, properties and uses | Periodic Table”. Royal Society of Chemistry. 2020年3月1日閲覧。
- ^ a b Kragh 2018, pp. 38–39.
- ^ Kragh 2018, p. 40.
- ^ Ghiorso, A.; Seaborg, G. T.; Oganessian, Yu. Ts. et al. (1993). “Responses on the report 'Discovery of the Transfermium elements' followed by reply to the responses by Transfermium Working Group”. Pure and Applied Chemistry 65 (8): 1815-1824. doi:10.1351/pac199365081815. オリジナルの25 November 2013時点におけるアーカイブ。 7 September 2016閲覧。.
- ^ Commission on Nomenclature of Inorganic Chemistry (1997). “Names and symbols of transfermium elements (IUPAC Recommendations 1997)”. Pure and Applied Chemistry 69 (12): 2471-2474. doi:10.1351/pac199769122471.
- ^ a b Hofmann, S.; Ninov, V.; Hesberger, F. P.; Armbruster, P.; Folger, H.; Munzenberg, G.; Schott, H. J.; Popeko, A. G. et al. (1995). “Production and decay of 269110”. Zeitschrift fur Physik A 350 (4): 277. Bibcode: 1995ZPhyA.350..277H. doi:10.1007/BF01291181.
- ^ Dalton, Rex (2002). “California lab fires physicist over retracted finding”. Nature 418 (6895): 261. Bibcode: 2002Natur.418..261D. doi:10.1038/418261b. PMID 12124581.
- ^ Hofmann, S (1998). “New elements - approaching”. Reports on Progress in Physics 61 (6): 639. Bibcode: 1998RPPh...61..639H. doi:10.1088/0034-4885/61/6/002.
- ^ Barber, R. C.; Greenwood, N. N.; Hrynkiewicz, A. Z.; Jeannin, Y. P.; Lefort, M.; Sakai, M.; Ulehla, I.; Wapstra, A. P. et al. (1993). “Discovery of the transfermium elements. Part II: Introduction to discovery profiles. Part III: Discovery profiles of the transfermium elements”. Pure and Applied Chemistry 65 (8): 1757. doi:10.1351/pac199365081757. (Note: for Part I see Pure Appl. Chem., Vol. 63, No. 6, pp. 879-886, 1991)
- ^ Karol, P. J.; Nakahara, H.; Petley, B. W.; Vogt, E. (2001). “On the discovery of the elements 110-112 (IUPAC Technical Report)”. Pure and Applied Chemistry 73 (6): 959. doi:10.1351/pac200173060959.
- ^ Chatt, J. (1979). “Recommendations for the naming of elements of atomic numbers greater than 100”. Pure and Applied Chemistry 51 (2): 381-384. doi:10.1351/pac197951020381.
- ^ a b c d e f g h i j k l Hoffman, Darleane C.; Lee, Diana M.; Pershina, Valeria (2006). “Transactinides and the future elements”. In Morss; Edelstein, Norman M.; Fuger, Jean. The Chemistry of the Actinide and Transactinide Elements (3rd ed.). Dordrecht, The Netherlands. ISBN 978-1-4020-3555-5
- ^ “Chemistry : Periodic Table : darmstadtium : historical information” (January 17, 2005). January 17, 2005時点のオリジナルよりアーカイブ。2022年12月16日閲覧。
- ^ Albert, Ghiorso; Darleane, Hoffman C; Glenn, Seaborg T (2000-01-21). Transuranium People, The: The Inside Story. ISBN 9781783262441
- ^ a b Corish, J.; Rosenblatt, G. M. (2003). “Name and symbol of the element with atomic number 110”. Pure Appl. Chem. 75 (10): 1613-1615. doi:10.1351/pac200375101613. オリジナルの2022-10-09時点におけるアーカイブ。 17 October 2012閲覧。.
- ^ a b c d e Griffith, W. P. (2008). “The Periodic Table and the Platinum Group Metals”. Platinum Metals Review 52 (2): 114-119. doi:10.1595/147106708X297486.
- ^ “Chemistry in its element - darmstadtium”. Chemistry in its element. Royal Society of Chemistry. 17 October 2012閲覧。
- ^ Hofmann, S.; Heinz, S.; Mann, R.; Maurer, J.; Khuyagbaatar, J.; Ackermann, D.; Antalic, S.; Barth, W. et al. (2012). “The reaction 48Ca + 248Cm → 296116* studied at the GSI-SHIP”. The European Physical Journal A 48 (5): 62. Bibcode: 2012EPJA...48...62H. doi:10.1140/epja/i2012-12062-1.
- ^ a b c Sonzogni, Alejandro. “Interactive Chart of Nuclides”. National Nuclear Data Center: Brookhaven National Laboratory. August 1, 2020時点のオリジナルよりアーカイブ。2008年6月6日閲覧。
- ^ Koura, H. (2011). Decay modes and a limit of existence of nuclei in the superheavy mass region (PDF). 4th International Conference on the Chemistry and Physics of the Transactinide Elements. 2022年10月9日時点のオリジナルよりアーカイブ (PDF)。2018年11月18日閲覧。
- ^ a b P. Roy Chowdhury; C. Samanta & D. N. Basu (2008). “Search for long lived heaviest nuclei beyond the valley of stability”. Phys. Rev. C 77 (4): 044603. arXiv:0802.3837. Bibcode: 2008PhRvC..77d4603C. doi:10.1103/PhysRevC.77.044603.
- ^ P. Roy Chowdhury; C. Samanta & D. N. Basu (2006). “α decay half-lives of new superheavy elements”. Phys. Rev. C 73 (1): 014612. arXiv:nucl-th/0507054. Bibcode: 2006PhRvC..73a4612C. doi:10.1103/PhysRevC.73.014612.
- ^ C. Samanta; P. Roy Chowdhury & D.N. Basu (2007). “Predictions of alpha decay half lives of heavy and superheavy elements”. Nucl. Phys. A 789 (1-4): 142-154. arXiv:nucl-th/0703086. Bibcode: 2007NuPhA.789..142S. doi:10.1016/j.nuclphysa.2007.04.001.
- ^ P. Roy Chowdhury; C. Samanta & D. N. Basu (2008). “Nuclear half-lives for α -radioactivity of elements with 100 - Z - 130”. Atomic Data and Nuclear Data Tables 94 (6): 781-806. arXiv:0802.4161. Bibcode: 2008ADNDT..94..781C. doi:10.1016/j.adt.2008.01.003.
- ^ Rosen, A.; Fricke, B.; Morovic, T.; Ellis, D. E. (1979). “Relativistic molecular calculations of superheavy molecules”. Journal de Physique Colloques 40: C4-218-C4-219. doi:10.1051/jphyscol:1979467.
- ^ Waber, J. T.; Averill, F. W. (1974). “Molecular orbitals of PtF6 and E110 F6 calculated by the self-consistent multiple scattering Xα method”. J. Chem. Phys. 60 (11): 4460-70. Bibcode: 1974JChPh..60.4466W. doi:10.1063/1.1680924.
- ^ a b Thayer, John S. (2010), “Relativistic Effects and the Chemistry of the Heavier Main Group Elements”, Relativistic Methods for Chemists, Challenges and Advances in Computational Chemistry and Physics, 10, p. 82, doi:10.1007/978-1-4020-9975-5_2, ISBN 978-1-4020-9974-8
- ^ Demissie, Taye B.; Ruud, Kenneth (25 February 2017). “Darmstadtium, roentgenium, and copernicium form strong bonds with cyanide”. International Journal of Quantum Chemistry 2017: e25393. doi:10.1002/qua.25393. hdl:10037/13632. オリジナルの2022-10-09時点におけるアーカイブ。.
- ^ Östlin, A.; Vitos, L. (2011). “First-principles calculation of the structural stability of 6d transition metals”. Physical Review B 84 (11): 113104. Bibcode: 2011PhRvB..84k3104O. doi:10.1103/PhysRevB.84.113104.
- ^ Gyanchandani, Jyoti; Sikka, S. K. (10 May 2011). “Physical properties of the 6 d -series elements from density functional theory: Close similarity to lighter transition metals”. Physical Review B 83 (17): 172101. Bibcode: 2011PhRvB..83q2101G. doi:10.1103/PhysRevB.83.172101.
- ^ Kratz; Lieser (2013). Nuclear and Radiochemistry: Fundamentals and Applications (3rd ed.). p. 631
- ^ a b Dullmann, Christoph E. (2012). “Superheavy elements at GSI: a broad research program with element 114 in the focus of physics and chemistry”. Radiochimica Acta 100 (2): 67-74. doi:10.1524/ract.2011.1842.
- ^ Eichler, Robert (2013). “First foot prints of chemistry on the shore of the Island of Superheavy Elements”. Journal of Physics: Conference Series 420 (1): 012003. arXiv:1212.4292. Bibcode: 2013JPhCS.420a2003E. doi:10.1088/1742-6596/420/1/012003.
- ^ Oganessian, Y. T.; Utyonkov, V.; Lobanov, Y.; Abdullin, F.; Polyakov, A.; Shirokovsky, I.; Tsyganov, Y.; Gulbekian, G. et al. (2004). “Measurements of cross sections for the fusion-evaporation reactions 244Pu(48Ca,xn)292-x114 and 245Cm(48Ca,xn)293?x116”. Physical Review C 69 (5): 054607. Bibcode: 2004PhRvC..69e4607O. doi:10.1103/PhysRevC.69.054607.
- ^ a b Public Affairs Department (26 October 2010). “Six New Isotopes of the Superheavy Elements Discovered: Moving Closer to Understanding the Island of Stability”. Berkeley Lab 2011年4月25日閲覧。
- ^ Yeremin, A. V. (1999). “Synthesis of nuclei of the superheavy element 114 in reactions induced by 48Ca”. Nature 400 (6741): 242-245. Bibcode: 1999Natur.400..242O. doi:10.1038/22281.
- ^ “JINR Publishing Department: Annual Reports (Archive)”. www1.jinr.ru. 2022年12月16日閲覧。
- ^ Feng, Z; Jin, G.; Li, J.; Scheid, W. (2009). “Production of heavy and superheavy nuclei in massive fusion reactions”. Nuclear Physics A 816 (1): 33. arXiv:0803.1117. Bibcode: 2009NuPhA.816...33F. doi:10.1016/j.nuclphysa.2008.11.003.
- ^ SHE Factory Experiments - FLNR
- ^ Utyonkov, V. K.; Brewer, N. T.; Oganessian, Yu. Ts.; Rykaczewski, K. P.; Abdullin, F. Sh.; Dimitriev, S. N.; Grzywacz, R. K.; Itkis, M. G. et al. (30 January 2018). “Neutron-deficient superheavy nuclei obtained in the 240Pu+48Ca reaction”. Physical Review C 97 (14320): 014320. Bibcode: 2018PhRvC..97a4320U. doi:10.1103/PhysRevC.97.014320.
- ^ Moody, Ken (2013-11-30). “Synthesis of Superheavy Elements”. In Schadel, Matthias; Shaughnessy, Dawn. The Chemistry of Superheavy Elements (2nd ed.). Springer Science & Business Media. pp. 24-8. ISBN 9783642374661
関連文献
[編集]- Audi, G.; Kondev, F. G.; Wang, M. et al. (2017). “The NUBASE2016 evaluation of nuclear properties”. Chinese Physics C 41 (3): 030001. Bibcode: 2017ChPhC..41c0001A. doi:10.1088/1674-1137/41/3/030001.
- Beiser, A. (2003). Concepts of modern physics (6th ed.). McGraw-Hill. ISBN 978-0-07-244848-1. OCLC 48965418
- Hoffman, D. C.; Ghiorso, A.; Seaborg, G. T. (2000). The Transuranium People: The Inside Story. World Scientific. ISBN 978-1-78-326244-1
- Kragh, H. (2018). From Transuranic to Superheavy Elements: A Story of Dispute and Creation. Springer Science+Business Media. ISBN 978-3-319-75813-8
- Zagrebaev, V.; Karpov, A.; Greiner, W. (2013). “Future of superheavy element research: Which nuclei could be synthesized within the next few years?”. Journal of Physics: Conference Series 420 (1): 012001. arXiv:1207.5700. Bibcode: 2013JPhCS.420a2001Z. doi:10.1088/1742-6596/420/1/012001. ISSN 1742-6588.
外部リンク
[編集] ウィキメディア・コモンズには、ダームスタチウムに関するカテゴリがあります。
ウィキメディア・コモンズには、ダームスタチウムに関するカテゴリがあります。- Darmstadtium at The Periodic Table of Videos (University of Nottingham)
| 1 | 2 | 3 | 4 | 5 | 6 | 7 | 8 | 9 | 10 | 11 | 12 | 13 | 14 | 15 | 16 | 17 | 18 | ||||||||||||||||
| 1 | H | He | |||||||||||||||||||||||||||||||
| 2 | Li | Be | B | C | N | O | F | Ne | |||||||||||||||||||||||||
| 3 | Na | Mg | Al | Si | P | S | Cl | Ar | |||||||||||||||||||||||||
| 4 | K | Ca | Sc | Ti | V | Cr | Mn | Fe | Co | Ni | Cu | Zn | Ga | Ge | As | Se | Br | Kr | |||||||||||||||
| 5 | Rb | Sr | Y | Zr | Nb | Mo | Tc | Ru | Rh | Pd | Ag | Cd | In | Sn | Sb | Te | I | Xe | |||||||||||||||
| 6 | Cs | Ba | La | Ce | Pr | Nd | Pm | Sm | Eu | Gd | Tb | Dy | Ho | Er | Tm | Yb | Lu | Hf | Ta | W | Re | Os | Ir | Pt | Au | Hg | Tl | Pb | Bi | Po | At | Rn | |
| 7 | Fr | Ra | Ac | Th | Pa | U | Np | Pu | Am | Cm | Bk | Cf | Es | Fm | Md | No | Lr | Rf | Db | Sg | Bh | Hs | Mt | Ds | Rg | Cn | Nh | Fl | Mc | Lv | Ts | Og | |
| |||||||||||||||||||||||||||||||||

