ジクロロブテン
表示
| ジクロロブテン | |
|---|---|

| |
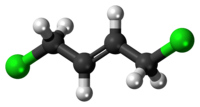
| |
1,4-Dichlorobut-2-ene | |
別称 trans-1,4-Dichlorobutene | |
| 識別情報 | |
| CAS登録番号 | 110-57-6 |
| ChemSpider | 14394 |
| EC番号 | 203-779-7 |
| |
| |
| 特性 | |
| 化学式 | C4H6Cl2 |
| モル質量 | 125 g mol−1 |
| 外観 | Colorless liquid |
| 密度 | 1.13 g/mL |
| 融点 |
1 °C, 274 K, 34 °F |
| 沸点 |
125.5 °C, 399 K, 258 °F |
| 危険性 | |
| GHSピクトグラム |    
|
| GHSシグナルワード | 危険(DANGER) |
| Hフレーズ | H350, H330, H311, H301, H314, H410 |
| EU分類 | Carc. Cat. 2 Very toxic (T+) Corrosive (C) Dangerous for the environment (N) |
| EU Index | 602-073-00-X |
| Rフレーズ | R45-R24/25-R26-R34-R50/53 |
| Sフレーズ | S53-S45-S60-S61 |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
ジクロロブテン(1,4-Dichlorobut-2-ene)は、塩素化したブテンである。工業的にクロロプレンを合成する際の中間体となり、工業用クロロプレンの主な不純物である[1]。(E)-異性体は、セプトリンの全合成の出発物質でもある[2]。
クロロプレンの合成
[編集]クロロプレンは、ネオプレン(クロロプレンゴム)等の合成ゴムの原料となるモノマーである。この物質は、ブタジエンから3段階で合成される。第1段階は、ブタジエンを液相または気相で塩素化して、3,4-ジクロロブト-1-エンと1,4-ジクロロブト-2-エンからなる異性体の混合物を得る。第2段階は、この混合物を触媒下で60-120℃に加熱することにより異性化して、純粋な3,4-ジクロロブト-1-エンとする。最終段階で、3,4-ジクロロブト-1-エンを重合阻害剤の存在下で希薄水酸化ナトリウム溶液中で脱塩化水素化して、粗クロロプレンを得る[3]。
出典
[編集]- ^ Re-evaluation of Some Organic Chemicals, Hydrazine and Hydrogen Peroxide, IARC Monographs on the Evaluation of Carcinogenic Risks to Humans 71, Lyon, France: International Agency for Research on Cancer, (1999), pp. 227-50, ISBN 92-832-1271-1.
- ^ Birman, Vladimir B.; Jiang, Xun-Tian (2004), “Synthesis of Sceptrin Alkaloids”, Org. Lett. 6 (14): 2369-71, doi:10.1021/ol049283g, PMID 15228281. Baran, Phil S.; Zografos, Alexandros L.; O'Malley, Daniel P. (2004), “Short Total Synthesis of (±)-Sceptrin”, J. Am. Chem. Soc. 126 (12): 3726-27, doi:10.1021/ja049648s, PMID 15038721.
- ^ Kleinschmidt, P. (1986), “Chlorinated hydrocarbons. 6.4. 2-Chloro-1,3-butadiene”, in Gerhartz, W.; Yamamoto, Y. S., Ullmann’s Encyclopedia of Industrial Chemistry, A6 (5th ed.), Weinheim: VCH, pp. 315-18. Stewart, C. A., Jr. (1993), “Chlorocarbons, -hydrocarbons (chloroprene)”, in Kroschwitz, J. I.; Howe-Grant, M., Kirk-Othmer Encyclopedia of Chemical Technology, 6 (4th ed.), New York: John Wiley, pp. 70-78.
