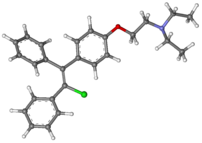
クロミフェン
 | |
 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| Drugs.com | Micromedex Detailed Consumer Information |
| 胎児危険度分類 | |
| 法的規制 |
|
| 薬物動態データ | |
| 生物学的利用能 | High (>90%) |
| 代謝 | Hepatic (with enterohepatic circulation) |
| 半減期 | 5-7 days |
| 排泄 | Mainly renal, some biliary |
| データベースID | |
| CAS番号 |
911-45-5 |
| ATCコード | G03GB02 (WHO) |
| PubChem | CID: 2800 |
| IUPHAR/BPS | 4159 |
| DrugBank | DB00882en:Template:drugbankcite |
| ChemSpider |
2698 |
| UNII |
1HRS458QU2 |
| KEGG | D07726 en:Template:keggcite |
| ChEBI | CHEBI:3752en:Template:ebicite |
| ChEMBL | CHEMBL1200667en:Template:ebicite |
| 化学的データ | |
| 化学式 | C26H28ClNO |
| 分子量 | 406 or 598.10 (with citrate) |
| |
クロミフェン(Clomifene)は選択的エストロゲン受容体修飾薬(SERM)の一つであり、排卵誘発薬として無排卵症または排卵過少症の治療に広く処方される。商品名クロミッド。
効能・効果
[編集]日本で承認されている効能・効果は「排卵障害に基づく不妊症の排卵誘発」である[1]。
クロミフェンは無排卵または排卵過少による不妊の治療に有用である[2]。このような患者に対する臨床試験の結果、無治療の場合の妊娠率は1.3〜4.2%であるのに対し、クロミフェンを用いた場合の妊娠率は5.6%であった。原因不明の不妊に対する有効性は不明である[3]。
他の生殖補助技術の成功率を高めるために補助的に用いられる事もある[4]。
クロミフェンの投与開始時の用量は50mg/日×5日間とする。月経期の初日をday1とする時、day3〜5から5日間服用する。クロミフェン導入後は、特に排卵予想日(day9〜18)に性行為を頻繁に行うべきである。黄体形成ホルモン(LH)テストが実施可能であるなら、クロミフェン服用5日目から3〜4日後(day4〜8にクロミフェンを服用した場合はday11辺りから)にテストを開始し、排卵が確認される(テストが陽性になる)までまたはday18まで継続する。自発的なホルモン分泌がない場合、直径20mm以上の卵胞がある時には人工的な卵子放出法、すなわちhCG10,000単位の筋注等を試す事ができる[5]。しかし、日常的なhCG使用による卵母細胞の放出は、頻回にLHテストをして確認する場合と比べて妊娠の機会を減少させている様に思われる[2]。
誘導された排卵サイクルのモニタリングのためには次の事をする:[5]
- クロミフェンの服用終了後4〜6日から経膣超音波法で卵胞をモニタリングする。継続的にモニタリングする事で卵胞の大きさや数が判る。また排卵前卵胞の突発性崩壊や直腸子宮窩の体液増加の推定根拠の一つとなり得る。排卵後は、予備の卵胞数や内部エコーの出現等の黄体形成の兆候を明らかにすることができる[2]。
- クロミフェンの服用終了後4〜6日から血清エストラジオール濃度を測定する。
- 排卵の1〜3日前から性交後のテストを実施し、高倍率視野中に少なくとも5つの活動性精子が居ることを確認する。
- クロミフェン最終服用日から3〜4日後、適切にLHが分泌されていることを尿中LH測定で確認する。
- 必要に応じて、排卵の7〜9日後の黄体中プロゲステロンが少なくとも10ng/mLであることを確認する。
治療を継続する場合には、30日周期で5日間連続服用を繰り返す。用量は、排卵が起こるまで50mgから段階的に増量する(最大100mg)[2]。製造業者は6サイクルを超えて服用しない様に推奨している[6]。
各治療サイクル前に残りの卵胞を大きくするために超音波を照射することは、推奨されていない[2]。
副作用
[編集]重大な副作用としては、卵巣過剰刺激症候群が知られている[1]。
10%以上の患者に可逆性卵巣肥大[7]が発現する。1〜10%の患者に視覚症状(霧視、複視、飛蚊症、羞明、暗点)、頭痛、血管運動性潮紅(一過性熱感)、異常子宮出血/腹部不快感が発現する[7]。
クロミフェンは複数の卵胞を排卵させるので、双生児(通常1%程度が10%に増加)や多胎児が増加する。
クロミフェンを1年以上続けて服用すると卵巣腫瘍のリスクが増加する[3]。これは妊娠経験がなく治療効果が上がらない場合に限られる[8]。その後の研究ではこれらの関係は見出されていない[2]。これには結論が出ていないが、有意なリスク増加はないと思われている[9]。
クロミフェンで受胎した場合の胎児や新生児の異常の発生数は、一般の場合と変わらない。先天性異常や自然流産の確率上昇を示すデータはない[7][10]。
作用機序
[編集]クロミフェンは視床下部のエストロゲン受容体を阻害し、性腺刺激ホルモンの分泌について負のフィードバックを遮断して視床下部-下垂体-性腺軸を増強する[11]。ズクロミフェン(クロミフェンのZ 体)はE 体よりも活性が強く、長時間エストロゲン受容体に結合する。クロミフェンはステロイドではない。
正常な生理学的女性ホルモンのサイクルでは、排卵の7日後、多量のエストロゲンとプロゲステロンが黄体から放出され、視床下部および下垂体前葉でGnRH、FSH、LHを 生産の高いレベルでのGnRH、FSHおよびLHを抑制する。排卵後に受精が起こらないと、hCGの欠如によって黄体は崩壊する。hCGは通常胚で産生され、妊娠中のプロゲステロンおよびエストロゲンの濃度を維持する。
治療的には、クロミフェンは生理周期の早い時点で投与される。一般的にはday3から5日間である。この時までにはFSH濃度は高い状態を保たれ、いくつかの卵胞を形成する。形成された卵胞はエストロゲンを生成し、エストロゲンが血中を巡る。クロミフェンが存在すると、身体は前周期のday22と同程度にエストロゲンが低濃度であると認識し、エストロゲンは視床下部での負のフィードバックができず、GnRH分泌の脈動はより早くなり、下垂体からのゴナドトロピン(FSH、LH)分泌が増加する。(GnRHの脈動が早く弱くなるとLHとFSHの分泌が増加する。例外的にGnRHの脈動が強くなると、LH/FSH比が低下する。)FSH濃度の上昇は卵胞を成長させ、卵胞を破り、排卵を引き起こす。排卵は通常、クロミフェン投与の6〜7日後に発生する。
化学的特徴
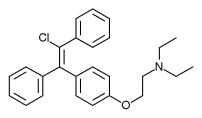
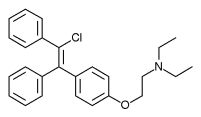
[編集]クロミフェンは2つの幾何異性体、エンクロミフェン(E-クロミフェン)とズクロミフェン(Z-クロミフェン)の混合物である。これら2つの異性体は、クロミフェンのエストロゲン様作用と抗エストロゲン作用に寄与していることが見出されている。
 |
 |
男性の低ゴナドトロピン血症への適応外投与
[編集]クロミフェンは多くの場合、二次性類宦官症の治療に有効である[12]。コストおよび服薬(経口投与。テストステロンは注射またはゲル剤)の利便性から、テストステロン補充療法(TRT)よりも有用であると思われる[13]。従来のTRTとは異なり精巣萎縮が起こらず、妊孕性が維持される。またTRTでは低用量hCGを併用しても化学的去勢が発生し得るが、クロミフェンでは予防可能で可逆的である[14]。クロミフェンの男性への投与はED治療や不妊治療等において行われている[15]。クロミフェンの異性体の一つ、エンクロミフェンが男性への投与について第III相試験の段階にある[16][17]。
ドーピング
[編集]クロミフェンはアナボリックステロイド使用の最終段階等で、エストロゲン高値による女性化乳房等の影響を除くために用いられる。クロミフェンはホルモン調整薬で、一般的には排卵誘発剤として使用されるが、スポーツ分野では筋肉増強剤の副作用を抑える目的で使用されるケースが多いとされる [18]。クロミフェンはエストロゲン受容体に結合し、ホルモンの結合を阻害する事で効果を発揮する。ステロイドでバランスを崩した身体のテストステロン産生を正常化させる効果もある。[19]スポーツにおける違法薬物として世界アンチ・ドーピング機関のリストにS4(ホルモン調整薬)として掲載されている[20]。
開発の経緯
[編集]クロミフェンは1960年台から使用されている[21]。最初は希発月経の治療に用いられたが、治療中の女性の妊娠率が高かったので無排卵症の治療にも適応拡大された[22]。
1989年4月、女性の妊孕性予測へのクロミフェンの使用が特許取得された。妊娠を維持できる女性はクロミフェン服用中は骨量が多く、骨量は妊孕性指標となり、その変化はCTスキャンで測定できる[23][24]。
出典
[編集]- ^ a b “クロミッド錠50mg 添付文書” (2016年5月). 2016年7月1日閲覧。
- ^ a b c d e f “Use of clomiphene citrate in infertile women: a committee opinion”. Fertil. Steril. 100 (2): 341–8. (August 2013). doi:10.1016/j.fertnstert.2013.05.033. PMID 23809505.
- ^ a b Hughes, E; Brown, J; Collins, JJ; Vanderkerchove, P (Jan 20, 2010). “Clomiphene citrate for unexplained subfertility in women.”. The Cochrane database of systematic reviews (1): CD000057. doi:10.1002/14651858.CD000057.pub2. PMID 20091498.
- ^ Seli, Emre. “Ovulation induction with clomiphene citrate”. UpToDate. 21 April 2014閲覧。
- ^ a b Clomiphene Citrate, Clomid. By Robert B. McWilliams. The Center for Reproduction and Women's Health Care, Houston, Texas. Retrieved May 2014
- ^ Trabert, B.; Lamb, E. J.; Scoccia, B.; Moghissi, K. S.; Westhoff, C. L.; Niwa, S.; Brinton, L. A. (2013). “Ovulation-inducing drugs and ovarian cancer risk: Results from an extended follow-up of a large US infertility cohort”. Fertility and Sterility 100 (6): 1660–6. doi:10.1016/j.fertnstert.2013.08.008. PMID 24011610.
- ^ a b c Clomid. Lexi-Comp Online, Hudson, Ohio: Lexi-Comp, Inc.; Accessed on April 19, 2014
- ^ Trabert, B; Lamb, EJ; Scoccia, B; Moghissi, KS; Westhoff, CL; Niwa, S; Brinton, LA (Dec 2013). “Ovulation-inducing drugs and ovarian cancer risk: results from an extended follow-up of a large United States infertility cohort.”. Fertility and Sterility 100 (6): 1660–6. doi:10.1016/j.fertnstert.2013.08.008. PMID 24011610.
- ^ Gadducci, A; Guerrieri, ME; Genazzani, AR (Jan 2013). “Fertility drug use and risk of ovarian tumors: a debated clinical challenge.”. Gynecological endocrinology : the official journal of the International Society of Gynecological Endocrinology 29 (1): 30–5. doi:10.3109/09513590.2012.705382. PMID 22946709.
- ^ Clomid [package insert]. Bridgewater, NJ, Sanofi-aventis. 2013
- ^ DrugBank > Clomifene. Updated on April 19, 2011
- ^ Ioannidoukadis, Stella; Wright, Pat J.; Neely, R. Dermot; Quinton, Richard (2006). “Complete reversal of adult-onset isolated hypogonadotropic hypogonadism with clomiphene citrate”. Fertility and Sterility 86 (5): 1513.e5–9. doi:10.1016/j.fertnstert.2006.03.065. PMID 17070201.
- ^ Taylor, Frederick; Levine, Laurence (2010). “Clomiphene Citrate and Testosterone Gel Replacement Therapy for Male Hypogonadism: Efficacy and Treatment Cost”. Journal of Sexual Medicine 7 (1 Pt 1): 269–76. doi:10.1111/j.1743-6109.2009.01454.x. PMID 19694928.
- ^ Kaminetsky, Jed; Hemani, Micah L (2009). “Clomiphene citrate and enclomiphene for the treatment of hypogonadal androgen deficiency”. Expert Opinion on Investigational Drugs 18 (12): 1947–55. doi:10.1517/13543780903405608. PMID 19938905.
- ^ “男性不妊の検査 診断 治療の手順(方針)|東邦大学医療センター大森病院 リプロダクションセンター(泌尿器科)”. www.lab.toho-u.ac.jp. 2019年9月7日閲覧。
- ^ Androxal website
- ^ Hill, S.; Arutchelva, V.; Quinton, R. (2009). “Enclomiphene, an estrogen receptor antagonist for the treatment of testosterone deficiency in men”. IDrugs 12 (2): 109–19. PMID 19204885.
- ^ “健康産業界の総合専門紙・健康産業流通新聞”. www.him-news.com. 2019年9月7日閲覧。
- ^ Tan, RS; Vasudevan, D. (Jan 2003). “Use of clomiphene citrate to reverse premature andropause secondary to steroid abuse”. Fertil Steril 79 (1): 203–5. doi:10.1016/s0015-0282(02)04550-8. PMID 12524089.
- ^ The WADA Prohibited List 2012 (keyword clomiphene)
- ^ Holtkamp DE, Greslin JG, Root CA, Lerner LJ (October 1960). “Gonadotrophin inhibiting and anti-fecundity effects of chloramiphene”. Proc. Soc. Exp. Biol. Med. 105: 197–201. doi:10.3181/00379727-105-26054. PMID 13715563.
- ^ Hughes E, Collins J, Vandekerckhove P (2000). “Clomiphene citrate for ovulation induction in women with oligo-amenorrhoea”. Cochrane Database Syst Rev (2): CD000056. doi:10.1002/14651858.CD000056. PMID 10796477.
- ^ Andrews, Edmund L. (29 April 1989). “Patents; A Method to Determine Fertility in Women”. http://www.nytimes.com/1989/04/29/business/patents-a-method-to-determine-fertility-in-women.html?smid=pl-share
- ^ “Use of clomiphene to predict fertility in a human female”. US PAtent US4820736 A. Google/. 4 April 2014閲覧。
