クロフィブラート
表示
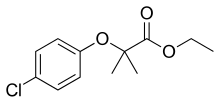 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| Drugs.com | Micromedex Detailed Consumer Information |
| 胎児危険度分類 | |
| 法的規制 |
|
| 薬物動態データ | |
| 血漿タンパク結合 | Variable, 92–97% at therapeutic concentrations |
| 代謝 | Hydrolyzed to clofibric acid; hepatic glucuronidation |
| 半減期 | Highly variable; average 18–22 hours. Prolonged in renal failure |
| 排泄 | Renal, 95 to 99% |
| データベースID | |
| CAS番号 |
637-07-0 |
| ATCコード | C10AB01 (WHO) |
| PubChem | CID: 2796 |
| IUPHAR/BPS | 2667 |
| DrugBank |
DB00636 |
| ChemSpider |
2694 |
| UNII |
HPN91K7FU3 |
| KEGG |
D00279 |
| ChEBI |
CHEBI:3750 |
| ChEMBL |
CHEMBL565 |
| 化学的データ | |
| 化学式 | C12H15ClO3 |
| 分子量 | 242.70 g·mol−1 |
| |
| 物理的データ | |
| 沸点 | 148 °C (298 °F) |
クロフィブラート(Clofibrate)は、血中高コレステロールおよび高トリグリセリド値のコントロールに用いられるフィブラート系脂質低下剤である。リポタンパク質リパーゼ活性を高めてVLDLからLDLへの変換を促進し、VLDLを減少させる。また、HDLを増加させる効果もある。
米国で1963年に医療用として承認された[1]が、2002年に副作用の問題で販売が中止された。
日本では1985年8月に承認され[2]:1、現在も流通している。
効能又は効果
[編集]高脂質血症
副作用
[編集]重大な副作用
[編集]横紋筋融解症、無顆粒球症
合併症と問題点
[編集]SIADH(抗利尿ホルモン(ADH、バソプレッシン)不適合分泌症候群)を誘発する可能性がある。また、胆嚢内にコレステロール結石を形成する可能性がある。
虚血性心疾患の一次予防に関する世界保健機関(WHO)協賛観察研究(平均観察期間:投与中5.3年、投与終了後7.9年)では、血清コレステロールの低下にもかかわらず、非投与の高コレステロール群に比べて高い死亡率(投与中で47%、投与後で5%増加)が確認された。死因は心臓疾患以外も含む様々な原因によるもので、未だ「説明不能」である[3]。
参考資料
[編集]- ^ (英語) Analogue-based Drug Discovery. John Wiley & Sons. (2006). p. 474. ISBN 9783527607495
- ^ “クロフィブラートカプセル250mg インタビューフォーム”. PMDA. 2021年4月25日閲覧。
- ^ “WHO cooperative trial on primary prevention of ischaemic heart disease with clofibrate to lower serum cholesterol: final mortality follow-up. Report of the Committee of Principal Investigators”. Lancet 2 (8403): 600–4. (September 1984). doi:10.1016/s0140-6736(84)90595-6. PMID 6147641.
