ガドテリドール
表示
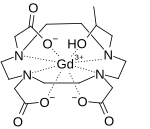 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| Drugs.com | Micromedex Detailed Consumer Information |
| 法的規制 | |
| データベースID | |
| CAS番号 |
120066-54-8 |
| ATCコード | V08CA04 (WHO) |
| PubChem | CID: 60714 |
| DrugBank |
DB00597 |
| ChemSpider |
54719 |
| UNII |
0199MV609F |
| KEGG |
D01137 |
| ChEBI |
CHEBI:31643 |
| ChEMBL |
CHEMBL1200593 |
| 別名 | (10-(2-(hydroxy-κO)propyl)-1,4,7,10-tetraazacyclododecane-1,4,7-triacetato(3−)-κN1,κN4,κN7,κN10,κO1,κO4,κO7)-gadolinium |
| 化学的データ | |
| 化学式 | C17H29GdN4O7 |
| 分子量 | 558.69 g·mol−1 |
| |
ガドテリドール(INN、英語: gadoteridol)は、ガドリニウムMRI造影剤の1つで、特に中枢神経系の画像診断に用いられる。商品名ProHanceで販売されている[2]。ガドテリドールは1992年に米国で初めて使用が承認された[3]。
出典
[編集]- ^ “Prohance Product information”. Health Canada (30 July 1998). 19 April 2024閲覧。
- ^ Bracco Diagnostic Inc. (26 October 2022). “Gadoteridol (ProHance) prescribing information”. DailyMed. U.S. National Library of Medicine. 17 May 2023閲覧。
- ^ “Assessment of adverse reaction rates during gadoteridol-enhanced MR imaging in 28,078 patients”. Radiology 259 (1): 109–16. (April 2011). doi:10.1148/radiol.10100906. PMID 21248237. "Specifically, the rate of nausea (0.530%) was less than half the rate (1.4%) in clinical trials of 1251 patients, leading to FDA approval in 1992."
