過酸化水素
| 過酸化水素 | |
|---|---|

| |

|
|
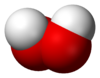
Hydrogen Peroxide, dioxidane | |
別称 Hydroperoxide Hydrogen dioxide | |
| 識別情報 | |
| CAS登録番号 | 7722-84-1 |
| KEGG | D00008 |
| 特性 | |
| 化学式 | H2O2 |
| モル質量 | 34.0 |
| 外観 | 無色液体 |
| 密度 | 1.4 g/cm3(90 %水溶液の場合) |
| 融点 |
-11℃ (90 %水溶液の場合) |
| 沸点 |
141℃ (90 %水溶液の場合) |
| 危険性 | |
| 安全データシート(外部リンク) | 厚生労働省モデルSDS |
| GHSピクトグラム |     [1] [1]
|
| GHSシグナルワード | 危険 [1] |
| Hフレーズ |
|
| 出典 | |
| ICSC 0164 | |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
過酸化水素(かさんかすいそ、英: hydrogen peroxide)は、化学式 H2O2 で表される化合物。しばしば過水(かすい)と略称される。主に水溶液で扱われる。対象により強力な酸化剤にも還元剤にもなり、殺菌剤、漂白剤として利用される。発見者はフランスのルイ・テナール。
性質
[編集]35 %水溶液は、常温では無色の、水よりわずかに粘度の高い弱酸性の液体[2]。エタノール、エーテル、水に可溶。わずかにオゾンに似た臭いがする[3]。
過酸化水素は不安定で酸素を放出しやすく、非常に強力な酸化力を持つヒドロキシラジカルを生成しやすい。過酸化水素は活性酸素の一種ではあるが、フリーラジカルではない。
強い腐食性を持ち、高濃度のものが皮膚に付着すると痛みをともなう白斑が生じる。また、可燃物と混合すると過酸化物を生成し、発火させることがある。水に溶けると、分解されるまでは水生生物に対して若干の毒性を持つ[2]。
実験室では、酸素を得る際に使われる。この反応式は以下の通りである。
- 反応で98.05 kJ/mol発熱する。[4]
反応速度を大きくするため触媒として二酸化マンガンや酵素の一種カタラーゼを使用する。傷口の消毒時に生じる泡は体内にあるカタラーゼが触媒として働いて生じる酸素である。
なお、過酸化水素は消防法第2条第7項および別表第一第6類2号により危険物第6類(酸化性液体)に指定されている。また、重量%で6 %を超える濃度の水溶液などの製剤は毒物及び劇物取締法により劇物に指定されている。
利用
[編集]
工業原料としての利用
[編集]過酸化水素全体の使用量では、製紙の際のパルプ漂白や廃水処理、半導体の洗浄など、工業的な利用が大部分を占める。塩素系の漂白剤などが多量の廃棄物を生じるのに対し、過酸化水素は最終的には無害な水と酸素に分解するため、工業利用するには環境にやさしい物質であると言われ、近年工業的な過酸化水素の利用は拡大してきている。
試薬用としては、濃度30w/v%(約10mol/ℓ[5])の過酸化水素水が市販されている。主に酸化剤として用いられる。過酸化水素を酸化剤に用いた環境負荷の低い新規酸化反応法などが精力的に研究されている[6]。同様の観点から合成への利用も数多く検討されているが、費用の高さのため、実用化されたプロセスはシクロヘキサノンオキシム合成[7]など限られており、利用用途におけるシェアはまだ低い。
閉鎖系エンジン(非大気依存推進)の酸素源としても利用が検討された。1930年頃からドイツのヘルムート・ヴァルターによって、高濃度過酸化水素の分解により酸素を発生させ、内燃機関を作動させるアイディアが研究され、ヴァルター機関が開発された。各国で開発が進められ、第二次世界大戦中にはドイツでUボートXVIIB型が建造された。
第二次世界大戦後、戦勝国がその成果を持ち帰り、イギリスではエクスプローラー級潜水艦、ソビエト連邦ではS-99が建造されて試験に供されたが、いずれも成果は芳しくなかったこと、高濃度過酸化水素の取扱いが難しく事故を起こしたことに加え、アメリカ海軍において艦船に搭載可能な原子力機関の開発が成功したこともあって、ヴァルター機関はそれ以上省みられることなく、潜水艦の水中動力源としては実用化には至らなかった。日本でも第二次世界大戦中にドイツから技術提供を受けてヴァルター機関が研究されたが、実用化される前に終戦を迎えた。
一方で魚雷の動力源としては、海上自衛隊の72式魚雷やイギリス海軍の21インチ マーク12魚雷、ソビエトの65型魚雷で使用され、一定の成果を収めている。しかし、マーク12魚雷はHMS Sidon、65型魚雷はクルスクで、それぞれ推進剤の高濃度過酸化水素に起因すると見られる事故を起こして、搭載艦が沈没している。
その他にもロケット飛行機であるメッサーシュミット Me163のエンジンHWK 109-509や秋水の特呂二号原動機、Hs 293誘導弾、ロケットベルトの推進剤として使用され、磁気浮上式鉄道のKOMET (Komponentenmeßtrager) で1975年に401.3 km/hの速度記録を樹立するときにも使用された。他にV2ロケットではターボポンプの駆動ガスの発生にも使用され、イギリスのアームストロング・シドレー ステンター、アームストロング・シドレー ベータ、ブリストル・シドレー ガンマ、ブリストル・シドレー BS.605、デ・ハビランド スペクター等のロケットエンジンでも酸化剤として使用された。
軍用機以外では、水上速度記録更新を狙ったロケット推進型パワーボート「ディスカバリーII」[8]、2014年11月9日に333 km/hを記録したフランソワ・ギッシー (Francois Gissy) 操縦のロケット推進自転車 “Kamikaze V”[9] の推進剤としても用いられている。
漂白剤としての利用
[編集]過酸化水素は衣料用漂白剤としても利用される。液体の衣料用酸素系漂白剤は希薄過酸化水素の溶液である。一方、過酸化水素と炭酸ナトリウムの錯体である過炭酸ナトリウムは、粉末で安定のため粉末の酸素系漂白剤として利用される。過炭酸ナトリウムは水に溶解すると炭酸ナトリウム (洗剤としても知られている)と過酸化水素とに解離する。また、髪の脱色に使用されることもあり、過酸化水素によって脱色した「偽の」ブロンドは、英語で peroxide blonde または bottle blonde と呼ばれる。
食品分野ではうどん、かまぼこ等の漂白目的の食品添加物として認可されているが、日本では1948年(昭和23年)に食品添加物として初めて指定され、1969年(昭和44年)に「うどん、かまぼこ、ちくわにあっては0.1g/kg以上、その他の食品にあっては0.03g/kg以上残存してはならない」とする使用基準が設けられた。その後、弱い動物発がん性が認められたとの報告があったことを踏まえて、過酸化水素が分解しやすいという特性から、1980年(昭和55年)2月に使用基準が「最終食品の完成前に過酸化水素を分解し、または除去しなければならない。」と改められた。2016年(平成28年)2月には使用基準が「釜揚げしらす及びしらす干しにあってはその1kgにつき0.005g以上残存しないように使用しなければならない。その他の食品にあっては、最終食品の完成前に過酸化水素を分解し、又は除去しなければならない。」と改められた[10]。
2015年現在の基準でカズノコの殺菌・漂白に使用されていながら表示がないのは、カタラーゼで分解処理を施し残存させないため加工助剤となり法律上表示が必要な食品添加物には該当しないためである[11][12]。
落花生、ほたて貝、しらす干しなど製造工程に関係なく、細胞内酸化反応および脂質の酸化等により天然由来の過酸化水素が数µg/g検出される食品が存在するため、殺菌・漂白の工程を示すものとは限らない[13]。
審美歯科において歯のホワイトニングに利用されている[14]。
殺菌剤としての利用
[編集]2.5〜3.5 w/v%の過酸化水素は医療用の外用消毒剤として利用され、オキシドール (oxydol) という日本薬局方名、またはオキシフル (oxyfull) という商品名でも呼ばれる。北米やイギリスで販売されている洗濯用洗剤のブランド「オキシドール」(Oxydol)とは無関係である。
飲料生産の充填工程で、飲料を充填する前に低濃度の過酸化水素水を紙パック内に噴霧して内部を殺菌する飲料充填機も存在する。この際、パック内に噴霧された過酸化水素水はパック内に送風を行うことで分解・乾燥し無害化する。ただし、噴霧量が多すぎるなどして飲料に過酸化水素水が混入するというトラブルが起こるリスクもある。
多くの生物種は過酸化水素分解酵素のカタラーゼを持つため、生体内での過酸化水素の寿命は極めて短い。つまり、傷の内面を含む体内に過酸化水素が侵入すると速やかに酸素に分解される。実際にオキシドールを傷口に塗布した際に発泡するのは、過酸化水素が分解して酸素が発生するためである。これは微生物分析に応用されており、一般的に通性嫌気性細菌はカタラーゼを持つが、偏性嫌気性細菌は持たないことから、細菌の種類を判別するのに用いられる。また、カタラーゼは熱により変性することから、食品に混入した生物系の異物 (毛髪や昆虫など)が加熱殺菌工程の前後どちらで混入したかを判別する苦情対応にも用いられる。この場合、殺菌前に混入した物ではカタラーゼが失活するため泡が生じないことで判別する[15]。
また、洗浄・すすぎ・消毒・保存が1液で可能なコンタクトレンズの洗浄剤としても使用されている。中和剤として白金を使用するものが主流である。
生産
[編集]
過酸化水素(100 %相当)の2016年度日本国内生産量は 17万5673 t、工業消費量は 1万5747 t である[16]。今日では、一般的にアントラキノン法とよばれるアントラセン誘導体の自動酸化を利用して生産が行われている[17]。2-エチルアントラヒドロキノンもしくは2-アミルアントラヒドロキノンを溶媒に溶解し、空気中の酸素と混合するとアントラヒドロキノンが酸化されてアントラキノンと過酸化水素が生じる。ここからイオン交換水を用いて抽出し、アントラキノンと過酸化水素を分離する。分離後、わずかに混入している有機溶媒を除去し、さらに減圧蒸留することにより高濃度(30〜60 %)のものを得る。副生成物であるアントラキノンをニッケルまたはパラジウム触媒を用いてアントラヒドロキノンに還元して再利用する。アントラヒドロキノンの酸化の際に側鎖が酸化されたり、還元の際に芳香環が還元されてしまうことがあり、それぞれ適切な再生処理が必要である。本法ではアントラキノンをいかに効率よく循環・再生使用できるかが重要となる。
硫酸または硫酸水素アンモニウムの水溶液を電気分解して生じるペルオキソ二硫酸 (H2(SO4)2)2− を加水分解することによる生産法も行われていたが、電力消費などの理由から現在ではあまり行われていない。
2005年現在、工業的な利用量が増え続けており、アントラキノン法に代わる安価な製造法、精製法の研究開発が各所で進められている。実験室レベルの研究については、合成研究の項で述べる。
合成研究
[編集]工業的にはアントラキノン法がよく用いられる。しかし、アントラキノン法は、多段プロセスであること、有機溶媒を必要とすること、副反応を起こしたアントラキノンの再生が必要であること、など多数の問題があり、過酸化水素が高価になる原因となっている。そのため、新しい過酸化水素合成法の開発が切望されている。
他の合成法にパラジウム触媒を用いた合成法と燃料電池反応法がある。
パラジウム触媒を用いた合成法
[編集]Pd(-Au)/CまたはPd(-Au)/SiO2触媒を用いてハロゲン化物イオン存在下、酸性条件で酸素と水素を直接反応させる。古くは、徳山曹達(現・トクヤマ)がPd/SiO2触媒を用いて、高圧の酸素と水素を反応させると過酸化水素が高濃度で蓄積できることを特許取得している[18]。またデュポンも同様にPd触媒を用いた合成法を特許取得している[19]。最近では、石原らはPd-Auコロイド触媒を適切に調製することにより、ほぼ100 %の選択性で過酸化水素が生成することを報告している[20]。酸素0.5気圧、水素0.5気圧の混合ガスを用いて、2時間反応させたところ0.4 %の過酸化水素水が生成したとしている。本触媒系一般の問題点として、酸素と水素を直接混合するため爆発の危険性があること、過酸化水素を高濃度で蓄積するためには加圧が必要であること (1気圧では最高で1 %〜2 %)、生成する過酸化水素水には酸や塩が含まれることが挙げられる。
特に爆発の危険性の問題は重大であり、この危険性を回避するため、反応速度を犠牲にして水素と酸素の混合比を爆発範囲から外す方法のほかに、酸素と水素をパラジウム薄膜で隔てた合成法がChoudharyらにより提案されているが、パラジウムが水素透過能を示すのは通常遥かに高温であり、単に膜に穴が開いていることが疑われることに加え、過酸化水素生成速度が極めて遅いなどの難点がある[21]。
燃料電池反応法
[編集]酸素-水素燃料電池では通常は発電を目的とし、酸素を水にまで還元させるが、適切な触媒を選択することにより酸素を過酸化水素に選択的に還元する方法が提案されている[22]。燃料電池反応法では酸素と水素は電解質に隔てられているため爆発の危険性が無いことが利点して挙げられる。まず酸水溶液中での過酸化水素の合成[23] および塩基性での過酸化水素合成[24][25] が報告された。特に塩基性では高効率で過酸化水素が生成したと報告されているが、これらの反応系ではパラジウム系と同様に生成する過酸化水素水に電解質が含まれるという難点を持つ。しかし、最近ナフィオン膜を用いた電解質を含まない過酸化水素水の直接合成法が提案された[26]。1気圧の条件であるにもかかわらず、コバルト触媒の回転数 (ターンオーバー数)は8時間で40万に達し、生成する過酸化水素濃度は14 %と非常に高い。本反応系の問題点として、効率が約40 %(残りは水)と十分ではないことが挙げられる。
光電気化学法
[編集]光触媒を使用した光電気化学法による過酸化水素の合成法が研究されている[27][28]。
事故
[編集]- 1980年3月18日にソビエト連邦のプレセツク宇宙基地で、ターボポンプ駆動用の過酸化水素を充填中のボストーク-2Mロケットが爆発事故を起こし、48人が死亡した。原因はステンレス製フィルターをはんだ付けする際に純粋な錫ではなく鉛を含有する電子部品用のはんだを使用した事だった。鉛自体には過酸化水素を分解する触媒能はないが、鉛の酸化物は強力な触媒として作用する[29] ため過酸化水素の分解が急激に進んで爆発に至ったのである。
- 1999年10月29日には首都高速2号目黒線を走行中のタンクローリーが爆発し、積み荷の過酸化水素水溶液が飛散した。飛散した過酸化水素水溶液により、一般道路の歩行者が目の痛みと皮膚のただれを訴えるなどした[30]。このタンクローリーは普段は塩化銅を含む廃液の運搬に使用されており、残留していた金属成分により過酸化水素の分解が進み爆発した[31]。このように過酸化水素は遷移金属により容易に分解されるので、注意が必要である。
- 2000年8月12日にバレンツ海で原子力潜水艦クルスクに搭載されていた魚雷に溶接不備があり、ここから推進剤である過酸化水素が漏れて爆発した。不運にもこの爆発で魚雷の弾頭が誘爆し、魚雷発射管室から浸水してクルスクは沈没した[32][33][34]。
- 2008年(平成20年)3月3日時点で日本海沿岸地域に漂着が確認された、約4万個に及ぶポリタンクの多くから塩酸、過酸化水素水、酢酸、硝酸などが検出された[35]。このため環境省は海岸に漂着した廃ポリタンクに安易に触れないよう、注意を呼びかけた[35]。また、このうち約1万6000個にはハングルが見られたため、外務省は発生源の可能性がある韓国政府および韓国の担当行政機関に対し、外交ルートを通し公式に情報提供を行い、実態把握と原因究明、及び漂着ごみ削減のための更なる努力を要請した[35]。
生体内での過酸化水素
[編集]生体内での消去反応
[編集]
生体ではエネルギー代謝の際、細胞内に過酸化水素が発生する。過酸化水素は活性酸素の一種であり、脂肪酸、生体膜、DNA等を酸化損傷するため有害で、生体防御のため速やかに除去しなければならない。
カタラーゼ (catalase) は、代謝の過程で発生する過酸化水素を不均化して酸素と水に変える反応を触媒する酵素である。毎秒当たりの代謝回転数は全酵素のなかでも最も高く、4000万に達する[36]。ヒトの場合、カタラーゼは4つのサブユニットで構成されており、各サブユニットは526のアミノ酸から成る[37]。分子量は約24万で、ヘムとマンガンを補因子として用いる。
グルタチオン-アスコルビン酸回路は、過酸化水素を解毒化する代謝経路である。グルタチオン-アスコルビン酸回路には、アスコルビン酸、グルタチオン、NADPHおよび代謝に関連する酵素等の抗酸化物質が含まれている[38]。
この経路の最初のステップでは、過酸化水素はアスコルビン酸を電子供与体として利用してアスコルビン酸ペルオキシダーゼ (APX) によって水に還元される。酸化されたアスコルビン酸(モノデヒドロアスコルビン酸〈MDA〉)は、モノデヒドロアスコルビン酸レダクターゼ (NADH)(MDAR)によってアスコルビン酸 (ASC) に再生される[39]。しかし、モノデヒドロアスコルビン酸は反応性が高く、速やかに還元されない場合にはアスコルビン酸とデヒドロアスコルビン酸 (DHA) に不均化する。デヒドロアスコルビン酸は、還元型グルタチオン (GSH) を消費してデヒドロアスコルビン酸レダクターゼによってアスコルビン酸に還元され、酸化型グルタチオン (GSSG)(グルタチオンジスルフィド)を生成する。最後に、酸化型グルタチオンは、NADPHを電子供与体として利用してグルタチオンレダクターゼ (GR) によって還元される。こうしてアスコルビン酸とグルタチオンが消費されることはない。電子は実質的にNADPHからH2O2に流れることとなる。デヒドロアスコルビン酸の還元は、非酵素的または例えばグルタチオンS -トランスフェラーゼオメガ1やグルタレドキシンなどのようにデヒドロアスコルビン酸還元酵素 (DHAR) 活性を有したタンパク質によって触媒される[40][41]。
植物では、グルタチオン-アスコルビン酸回路は、細胞質、ミトコンドリア、色素体およびペルオキシソームで機能する[42][43]。グルタチオン、アスコルビン酸およびNADPHは、植物細胞に高濃度で存在しているので、グルタチオン-アスコルビン酸回路が過酸化水素の解毒に重要な役割を担っていることが想定される。それにもかかわらず、チオレドキシンまたはグルタレドキシンを還元基質として利用したペルオキシレドキシンやグルタチオンペルオキシダーゼを含む他の酵素(ペルオキシダーゼ)もまた、植物での過酸化水素の解毒に貢献している[44]。
ミトコンドリアの電子伝達系では、スーパーオキシドアニオン (O2-) などの活性酸素種が常に発生している。活性酸素は生体分子を破壊し有害であるため、防御機構が存在する。スーパーオキシドアニオンは、まずスーパーオキシドディスムターゼ (SOD) によって過酸化水素に変換され、ペルオキシダーゼによって無害な水に分解される[45][46][信頼性要検証]。
グルタチオンペルオキシダーゼはセレノシステインを含む酵素である。グルタチオンを電子供与体として用い、過酸化水素だけでなく有機過酸化物にも作用し、酸化ストレスから生体を守っている[47][48]。
白血球等での生成反応
[編集]白血球(好中球)は、体内に細菌が侵入してくると捕獲(貪食)し、白血球はNAD(P)Hオキシダーゼを使ってNADH(NADPH)とH+と酸素を反応させて、過酸化水素を生成し、貪食されてもまだ増殖しようとする細菌を殺菌し感染から守る生体防御メカニズムを有する[49][信頼性要検証]。
H2O2捕捉剤
[編集]構造
[編集]過酸化水素(H2O2)は、ねじれたC2対称性を持つ非平面分子であることが、1950年にPaul-Antoine Giguèreによって赤外線分光法を用いて初めて示された。O-O結合は単結合であるが、386 cm-1 (4.62 kJ/mol) という比較的高い回転障壁(エタンの回転障壁は1040 cm-1 (12.4 kJ/mol))を持っており、回転を抑制している。 この障壁は、隣接する酸素原子のローンペア間の反発と、2つのO-H結合の間の双極子効果によるものであると提唱されている。
2つのO-H結合の間に約100°の二面角があるため、分子はキラルである。これは、掌性を示す最も小さく、最も単純な分子である。片方ではなく、もう片方のエナンチオ特異的な相互作用によって、リボ核酸の一方のエナンチオマー形態が増幅され、RNAの世界でホモキラリティの起源となった可能性が提唱されている。
H2O2の構造は、気体と結晶とで大きく異なる。この違いは、気体状態では存在しない水素結合の効果に起因する。H2O2結晶は正方晶の空間群P4121をとる。
その他
[編集]- ミイデラゴミムシは体内に過酸化水素とヒドロキノンを貯めておき、これらを反応させて敵に対し蒸気とベンゾキノンから成る100℃以上の気体を爆発的に噴射する。
- 第二次世界大戦末期、日本はロケット戦闘機「秋水」の燃料用として過酸化水素の大量生産に乗り出した。電解装置の電極にはプラチナが用いられ、終戦まで1900 kgものプラチナが消費されたとされている[51]。
脚注
[編集]- ^ a b c 厚生労働省モデルSDS
- ^ a b 過酸化水素35 %水溶液 MSDS (PDF)
- ^ 曾根興三、「過酸化水素」、世界大百科事典、第二版CD-ROM版、平凡社、1998年
- ^ “安全データシート”. 2020年4月16日閲覧。
- ^ 液体モル濃度の求め方-富士フイルム和光純薬株式会社
- ^ 佐藤一彦「過酸化水素水を用いる環境調和型酸化反応」『有機合成化学協会誌』第60巻第10号、有機合成化学協会、2002年、974-982頁、doi:10.5059/yukigoseikyokaishi.60.974。
- ^ 住友化学の新しいε-カプロラクタム製造技術 (PDF) 住友化学
- ^ 1980年11月13日にタホ湖で試験走行中にフロートが波の衝撃に耐えられず破損して水面に叩きつけられ、ドライバーのリー・テイラーは死亡したGoing For Broke At 300 MPH - ウェイバックマシン。
- ^ フランス人: ロケット自転車を使って時速333キロの速度世界記録を樹立[リンク切れ]、businessnewsline、2014年11月11日、同年11月12日閲覧
- ^ 厚生労働省 「過酸化水素の規格基準改正について」(平成28年10月27日付生食発1027第1号)
- ^ 国民生活センター「物質名が表示されない食品添加物がある?」
- ^ 厚生労働省「食品添加物の表示について」
- ^ 国立医薬品食品衛生研究所「食品添加物含有量データベース」
- ^ “ポリリン酸を用いたホワイトニングの特徴 : Q&A 歯科一般 : Dental Diamond[デンタルダイヤモンド]”. www.dental-diamond.jp. 2021年1月17日閲覧。
- ^ 河岸宏和 (2008), 図解入門ビジネス 最新 食品工場の衛生と危機管理がよ〜くわかる本, 秀和システム, p. 58, ISBN 978-4-7980-2007-5
- ^ 経済産業省生産動態統計年報 化学工業統計編
- ^ 浜口高嘉、『過酸化水素の製造と関連製品』 月刊ファインケミカル, 2006年3月 NAID 40007161259
- ^ Y. Izumi, JP Patent 昭51-4097.
- ^ L. W. Gosser, M. A. Paoli, US5135731, 1992.
- ^ Y. Nomura, T. Ishihara, Y. Hata, K. Kitawaki, H. Matsumoto, ChemSusChem, 2008, 1, 619-621.
- ^ V. R. Choudhary, A. G. Galward, S. D. Sansare, Angew. Chem. Int. Ed., 2001, 40, 1776-1777.
- ^ K. Otsuka and I. Yamanaka, "One step synthesis of hydrogen peroxide through fuel cell reaction." Electrochim. Acta, 1990, 35, 319-322. doi:10.1016/0013-4686(90)87004-L
- ^ I. Yamanaka, T. Onizawa, H. Suzuki, N. Hanaizumi, Chem. Lett., 2006, 35, 1330-1331.
- ^ E. Brillas, F. Alcaida, P. L. Cabot, Electrochim. Acta, 2002, 48, 331-340.
- ^ I. Yamanaka, T. Onizawa, S. Takenaka, K. Otsuka, Angew. Chem. Int. Ed., 2003, 42, 3653-3654.
- ^ I. Yamanaka, S. Tazawa, T. Murayama, R. Ichihashi, N. Hanaizumi, ChemSusChem, 2008, 1, 988-990.
- ^ 太陽光により水と酸素から過酸化水素を合成する革新的光触媒の開発
- ^ 光電極を用いた酸化剤と水素の効率的な製造方法を開発
- ^ Boris Yevseyevich Chertok (2006-06-01). Rockets and People: Creating a rocket industry. Government Printing Office. pp. 636-640. ASIN B019NDFEHI. ISBN 9780160766725.
- ^ 首都高速2号線におけるタンクローリー爆発事故概要 - 消防庁危険物規制課 平成11年(1999年)11月1日、2020年4月16日閲覧
- ^ TOPIC No.2-51 タンクローリー爆発(首都高)
- ^ Debra Rosenberg et al. "A Mystery In The Deep." Newsweek 136.9 (2000): 34. Academic Search Premier. Web. 7 December 2011.
- ^ Sviatov, George. "The Kursk's Loss Offers Lessons." U.S. Naval Institute Proceedings, 129.6 (2003): 71. Academic Search Premier. Web. 7 December 2011.
- ^ Marshall, Geoff (July 2008), “The Loss of the HMS Sidon”, In Depth (Submarines Association Australia) 28 (4), オリジナルの2011-02-16時点におけるアーカイブ。 2 September 2010閲覧。
- ^ a b c “日本海沿岸地域等への廃ポリタンクの大量漂着について(第3報)”. 環境省 (2008年3月5日). 2020年5月21日閲覧。
- ^ カラー図解 アメリカ版 大学生物学の教科書 第1巻 細胞生物学、David Sadavaほか、講談社、2010年、p.18.
- ^ A Hirono et al."A Novel Human Catalase Mutation (358 T6del) Causing Japanese-type Acatalasemia," Blood Cells, Molecules, and Diseases (1995) 21(23) Dec 15: 232-234, PMID 8673475
- ^ Noctor G, Foyer CH (Jun 1998). “ASCORBATE AND GLUTATHIONE: Keeping Active Oxygen Under Control”. Annu Rev Plant Physiol Plant Mol Biol 49: 249–279. doi:10.1146/annurev.arplant.49.1.249. PMID 15012235.
- ^ Wells WW, Xu DP (August 1994). “Dehydroascorbate reduction”. J. Bioenerg. Biomembr. 26 (4): 369–77. doi:10.1007/BF00762777. PMID 7844111.
- ^ Whitbread AK, Masoumi A, Tetlow N, Schmuck E, Coggan M, Board PG (2005). “Characterization of the omega class of glutathione transferases”. Meth. Enzymol. 401: 78–99. doi:10.1016/S0076-6879(05)01005-0. PMID 16399380.
- ^ Rouhier N, Gelhaye E, Jacquot JP (2002). “Exploring the active site of plant glutaredoxin by site-directed mutagenesis”. FEBS Lett 511 (1-3): 145–9. doi:10.1016/S0076-6879(05)01005-0. PMID 16399380.
- ^ Meyer A (Sep 2009). “The integration of glutathione homeostasis and redox signaling”. J Plant Physiol 165 (13): 1390–403. doi:10.1016/j.jplph.2007.10.015. PMID 18171593.
- ^ Jimenez A, Hernandez JA, Pastori G, del Rio LA, Sevilla F (Dec 1998). “Role of the ascorbate-glutathione cycle of mitochondria and peroxisomes in the senescence of pea leaves”. Plant Physiol 118 (4): 1327–35. doi:10.1104/pp.118.4.1327. PMC 34748. PMID 9847106.
- ^ Rouhier N, Lemaire SD, Jacquot JP (2008). “The role of glutathione in photosynthetic organisms: emerging functions for glutaredoxins and glutathionylation”. Annu Rev Plant Biol 59: 143–66. doi:10.1146/annurev.arplant.59.032607.092811. PMID 18444899.
- ^ 市川祐介、中島洋、渡辺芳人「高度好熱菌由来シトクロム c552 を利用した ペルオキシダーゼ不安定中間体の観測 (PDF) 」 第33回 生体分子科学討論会 2006年7月14日9:20〜9:40 のプログラム案内 [1]
- ^ Ichikawa, Yusuke; Nakajima, Hiroshi; Watanabe, Yoshihito (2006-10-06). “Characterization of Peroxide-Bound Heme Species Generated in the Reaction of Thermally Tolerant Cytochrome c552 with Hydrogen Peroxide”. ChemBioChem 7 (10): 1582–1589. doi:10.1002/cbic.200600135. ISSN 1439-4227.
- ^ 老化のメカニズム 2006/09/25
- ^ 玉利祐三 5. 必須微量元素の栄養と欠乏症 - ウェイバックマシン(2015年9月20日アーカイブ分)
- ^ 理大の栞16:活性酸素 -解説 役立つ情報をあなたのポケットに!
- ^ 大阪武雄、日本化学会『活性酸素』丸善、1999年、p.27頁。ISBN 4-621-04634-9。
- ^ 白金はロケット戦闘機「秋水」製造用に(昭和20年10月20日 朝日新聞)『昭和ニュース辞典第8巻 昭和17年/昭和20年』毎日コミュニケーションズ刊 1994年 148頁
関連項目
[編集]外部リンク
[編集]- 府食第96号 平成28年2月23日 (PDF) 厚労省
- Hydrogen peroxide (chemical compound) - ブリタニカ百科事典
- ブリタニカ国際大百科事典 小項目事典『過酸化水素』 - コトバンク
- 過酸化水素 (試薬) JISK8230:2016

