アダリムマブ
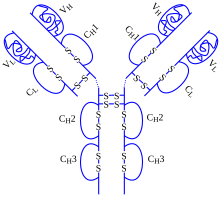 | |
| モノクローナル抗体 | |
|---|---|
| 種類 | 全長抗体 |
| 原料 | ヒト |
| 抗原 | TNF-α |
| 臨床データ | |
| 販売名 | ヒュミラ |
| Drugs.com | monograph |
| MedlinePlus | a603010 |
| 胎児危険度分類 | |
| 法的規制 | |
| 薬物動態データ | |
| 生物学的利用能 | 64% (皮下注), 0% (経口投与) |
| 半減期 | 10–20日 |
| データベースID | |
| CAS番号 |
331731-18-1 |
| ATCコード | L04AB04 (WHO) |
| DrugBank |
DB00051 |
| UNII |
FYS6T7F842 |
| KEGG |
D02597 |
| ChEMBL |
CHEMBL1201580 |
| 化学的データ | |
| 化学式 | C6428H9912N1694O1987S46 |
| 分子量 | 144190.3 g/mol |
アダリムマブ(Adalimumab:ADA)とは遺伝子組換えによって作られたヒト型抗ヒトTNF-αモノクローナル抗体製剤(医薬品)である。日本での販売名はヒュミラ(製造販売(輸入)元:アッヴィ合同会社、販売元:エーザイ、プロモーション提携:EAファーマ)。独BASF傘下の製薬会社であったKnoll AG(後に米アボット・ラボラトリーズが買収)が創製した。抗体成分である蛋白配列が完全ヒト由来であるため、先行のキメラ抗体製剤よりも理論的に生体適合性が高い(より過敏症を起こしにくい)とされる。剤型はプレフィルドシリンジ製剤及びペン型オートインジェクター。一定の条件を満たした患者においては自己投与も認められている。
解説
[編集]アダリムマブ等の免疫調節を作用機序とする生物学的製剤は従来のリウマチ治療薬に比べ全く異なる新しいアプローチとして高い治療効果を持つに至り、長年にわたり有効な治療法がなかった関節リウマチにおいて切り札的な治療法となった。しかし、一方でアダリムマブはヒトの免疫機構(細胞性免疫)の一部に関与するTNF-α(腫瘍壊死因子α)の生理活性を抑制する一種の免疫抑制剤であることから、投与中は特に細菌、真菌、ウイルスによる重篤な感染症(肺炎、結核、ウイルス性脳炎等)の発現に注意しながら使用することが重要である。また、アダリムマブ等の生物学的製剤は臨床使用(ヒトでの使用)が開始されてからまだ歴史が浅いため、今後、長期的な治療効果および安全性データの集積が待たれるという点で未知の要素を残している。
日本における適応症
[編集]製剤により適応症が異なっている。また疾患ごとに投与量、投与間隔も異なる。
- ヒュミラ皮下注20mgシリンジ0.2mL、ヒュミラ皮下注40mgシリンジ0.4mL、ヒュミラ皮下注40mgペン0.4mL
- 既存治療で効果不十分な下記疾患
- 多関節に活動性を有する若年性特発性関節炎
- 既存治療で効果不十分な下記疾患
- ヒュミラ皮下注40mgシリンジ0.4mL、ヒュミラ皮下注80mgシリンジ0.8mL、ヒュミラ皮下注40mgペン0.4mL、ヒュミラ皮下注80mgペン0.8mL
禁忌
[編集]重篤な感染症や活動性結核の患者、鬱血性心不全の患者、脱髄疾患 (多発性硬化症等) およびその既往歴のある患者等に禁忌とされている。
副作用
[編集]重大な副作用は、
- 重篤な感染症(敗血症(0.3%)、肺炎(2.8%)等)、結核(0.3%)、
- ループス様症候群(0.1%)、脱髄疾患(多発性硬化症、視神経炎、横断性脊髄炎、ギラン・バレー症候群等)、重篤なアレルギー反応、
- 重篤な血液障害(汎血球減少症、血小板減少症、白血球減少症、顆粒球減少症)、
- 間質性肺炎(0.7%)、劇症肝炎、肝機能障害、黄疸、肝不全
である。(頻度未記載は頻度不明)
国内臨床試験では82.9%、海外臨床試験では51.6%に副作用が発生した。主なものは上気道・鼻腔・咽頭感染症、注射部位の発赤・疼痛、頭痛等である。
作用機序
[編集]関節リウマチ:アダリムマブは関節リウマチにおいて過剰に産生されたTNF-αに特異的に結合し、TNF-αがTNF-α受容体に結合することによって生じる関節滑膜の炎症反応の抑制や関節破壊に関与する破骨細胞の形成およびその活性化の抑制により関節破壊の進展を防止する(関節破壊防止については海外データでのみ認められている)。
