コランニュレン
この項目「コランニュレン」は途中まで翻訳されたものです。(原文:en:corannulene00:30, 16 April 2011版) 翻訳作業に協力して下さる方を求めています。ノートページや履歴、翻訳のガイドラインも参照してください。要約欄への翻訳情報の記入をお忘れなく。(2011年4月) |
| コランニュレン | |
|---|---|

| |

| |
ジベンゾ[ghi,mno]フルオランテン | |
別称 [5]サーキュレン | |
| 識別情報 | |
| CAS登録番号 | 5821-51-2 |
| PubChem | 11831840 |
| ChemSpider | 10006487 |
| |
| |
| 特性 | |
| 化学式 | C20H10 |
| モル質量 | 250.29 g/mol |
| 外観 | ごく薄い黄色~黄緑色の結晶性粉末[1] |
| 融点 |
269℃[1] |
| 特記なき場合、データは常温 (25 °C)・常圧 (100 kPa) におけるものである。 | |
コランニュレン(コランヌレンとも、corannulene) はC20H10の化学式で表される多環芳香族炭化水素である[2]。 5つのベンゼン環がリング状に縮環した形状をしており、[5]サーキュレンとも呼ばれる 。この分子はジオデシックポリアレーンの一種であり、またバックミンスターフラーレンの部分構造と見ることができるため関心を集めている。お椀状の形をしており、バックミンスターフラーレンの愛称であるバッキーボール(buckyball)にちなんで時にバッキーボウル(buckybowl)と愛称される。コランニュレンはbowl-to-bowl反転をすることが知られており、その際のエネルギー障壁は-64℃で10.2kcal/mol(42.7kJ/mol)である[3]。
合成
[編集]コランニュレンの合成ルートはいくつか存在する。最初の合成は1966年に多段階有機合成によって達成され[4]、その後1991年に瞬間真空熱分解による合成がなされた[5]。この方法は一般的に溶液化学的合成よりも収率が低くなる傾向にあるが、より多くの誘導体を合成することができる。以下にフルオランテン誘導体からの求核置換-脱離反応による合成例[6]を示す。
ブロモ基を過剰のn-ブチルリチウムによって除去するとコランニュレンになる。
その後、Siegelらにより溶液化学的合成によるグラム単位、そしてキログラム単位での合成が可能となった[7]。
様々な官能基付加が試みられており、エチル基[3][8][9]、エーテル基[10]、スルフィド基[11]、白金置換基[12]、アリール基[13]、フェナレニル縮環構造[14]、インデノ環[15]などが付加したものが合成されている。
芳香族性
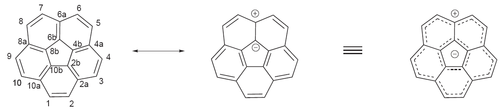
[編集]コランニュレンは芳香族性を示すが、最初に合成を達成したバースとロートンはこれを内外二つの環構造を考えることで説明した[4]。すなわち、コランニュレンは共鳴により分極して内側は6π電子系であるシクロペンタジエニルアニオン、外側は14π電子系である[15]アヌレニルカチオンと見るのである。コランニュレンという名称も彼らによる命名であり、このモデルに由来している(core + annulene)。なお、ロートンの夫人アン(Ann)の名が織り込まれているともいわれる[16]。
しかしながら、後に理論化学計算からこの予測の妥当性に疑問が示されている [17][18]。
関連項目
[編集]脚注
[編集]- ^ a b Corannulene(CAS番号:5821-51-2 製品コード:C2572)→MSDS(pdf)、東京化成工業
- ^ Scott, L. T.; Bronstein, H. E.; Preda, D. V.; Ansems, R. B. M.; Bratcher, M. S.; Hagen, S. (1999). "Geodesic polyarenes with exposed concave surfaces". Pure Appl. Chem. 71 (2): 209. doi:10.1351/pac199971020209
- ^ a b Scott, L. T.; Hashemi, M. M.; Bratcher, M. S. (1992). "Corannulene bowl-to-bowl inversion is rapid at room temperature". J. Am. Chem. Soc. 114 (5): 1920. doi:10.1021/ja00031a079
- ^ a b Barth, W. E.; Lawton, R. G. (1966). J. Am. Chem. Soc. 88 (2): 380.doi:10.1021/ja00954a049
- ^ Scott, L. T.; Hashemi, M. M.; Meyer, D. T.; Warren, H. B. (1991). "Corannulene. A convenient new synthesis". J. Am. Chem. Soc. 113 (18): 7082.doi:10.1021/ja00018a082
- ^ Sygula, A.; Rabideau, P. W. (2000). "A Practical, Large Scale Synthesis of the Corannulene System". J. Am. Chem. Soc. 122 (26): 6323.doi:10.1021/ja0011461
- ^ Anna M Butterfield, Buruno Gilomen, and Jay S. Siegel. (2012). "Kilogram-Scale Production of Corannulene". Org. Process. Res. Dev., Just Accepted. doi:10.1021/op200387s
- ^ Wu, Y.; Bandera, D.; Maag, R.; Linden, A.; Baldridge, K.; Siegel, J. (2008). "Multiethynyl corannulenes: synthesis, structure, and properties". J. Am. Chem. Soc. 130 (32): 10729–10739.doi:10.1021/ja802334n
- ^ Mack, J.; Vogel, P.; Jones, D.; Kaval, N.; Sutton, A. (2007). "The development of corannulene-based blue emitters". Org. Biomol. Chem. 5 (15): 2448–2452.doi:10.1039/b705621d
- ^ Gershoni-Poranne, R.; Pappo, D.; Solel, E.; Keinan, E. (2009). "Corannulene ethers via Ullmann condensation". Org. Lett. 11 (22): 5146–5149. doi:10.1021/ol902352k
- ^ Baldridge, K.; Hardcastle, K.; Seiders, T.; Siegel, J. (2010). "Synthesis, structure and properties of decakis(phenylthio)corannulene". Org. Biomol. Chem. 8 (1): 53–55.doi:10.1039/b919616a
- ^ Choi, H.; Kim, C.; Park, K. M.; Kim, J.; Kang, Y.; Ko, J. (2009). "Synthesis and structure of penta-platinum σ-bonded derivatives of corannulene". J. Org. Chem. 694 (22): 3529.doi:10.1016/j.jorganchem.2009.07.015
- ^ Pappo, D.; Mejuch, T.; Reany, O.; Solel, E.; Gurram, M.; Keinan, E. (2009). "Diverse Functionalization of Corannulene: Easy Access to Pentagonal Superstructure". Org. Lett. 11 (5): 1063.doi:10.1021/ol8028127
- ^ Nishida, S.; Morita, Y.; Ueda, A.; Kobayashi, T.; Fukui, K.; Ogasawara, K.; Sato, K.; Takui, T. et al. (2008). "Curve-structured phenalenyl chemistry: synthesis, electronic structure, and bowl-inversion barrier of a phenalenyl-fused corannulene anion". J. Am. Chem. Soc. 130 (45): 14954–14955.doi:10.1021/ja806708j
- ^ Steinberg, B.; Jackson, E.; Filatov, A.; Wakamiya, A.; Petrukhina, M.; Scott, L. (2009). "Aromatic pi-systems more curved than C(60). The complete family of all indenocorannulenes synthesized by iterative microwave-assisted intramolecular arylations". J. Am. Chem. Soc. 131 (30): 10537–10545.doi:10.1021/ja9031852
- ^ おもしろ命名法、有機って面白いよね!!
- ^ Sygula, A. (1995). "Structure and inversion barriers of corannulene, its dianion and tetraanion. An ab initio study". J. Mol. Struct.: THEOCHEM 333: 215–226.doi:10.1016/0166-1280(94)03961-J
- ^ Monaco, G.; Scott, L.; Zanasi, R. (2008). "Magnetic euripi in corannulene". J. Phys. Chem. A 112 (35): 8136–8147.doi:10.1021/jp8038779
外部リンク
[編集]- 亀の甲をつなげると - 有機化学美術館
- ナノの世界に朗報?!-コラニュレンのkg合成- - 化学者のつぶやき