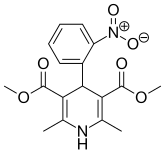
ニフェジピン
 | |
 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| 販売名 | Adalat, Procardia, others |
| Drugs.com | monograph |
| MedlinePlus | a684028 |
| 胎児危険度分類 |
|
| 薬物動態データ | |
| 生物学的利用能 | 45-56% |
| 血漿タンパク結合 | 92-98% |
| 代謝 | Gastrointestinal, Liver |
| 半減期 | 2 hours |
| 排泄 | Kidneys: >50%, Biliary: 5-15% |
| データベースID | |
| CAS番号 |
21829-25-4 |
| ATCコード | C08CA05 (WHO) |
| PubChem | CID: 4485 |
| IUPHAR/BPS | 2514 |
| DrugBank |
DB01115 |
| ChemSpider |
4330 |
| UNII |
I9ZF7L6G2L |
| KEGG |
D00437 |
| ChEBI |
CHEBI:7565 |
| ChEMBL |
CHEMBL193 |
| 化学的データ | |
| 化学式 | C17H18N2O6 |
| 分子量 | 346.335 g/mol |
| |
| 物理的データ | |
| 融点 | 173 °C (343 °F) |
ニフェジピン (Nifedipine) は狭心症、高血圧、レイノー現象、早産の際に用いられる血管拡張薬の一つである[1]。ジヒドロピリジン系のカルシウム拮抗薬に分類される[1]。プリンツメタル狭心症の治療に採用される。重症妊娠高血圧の治療にも使用できる[1]。早期陣痛に使用するとステロイドをより長時間使用でき、児の肺の状態を改善し、母体を高度医療施設に搬送する時間を稼ぐ事ができる。速放軟カプセル剤[2]、徐放錠[3]、複合錠[4]がある。商品名アダラート。開発コードBAY a1040。
一般的な副作用としては、立ちくらみ、頭痛、倦怠感、下肢腫脹、咳嗽、息切れがある。重篤な副作用として低血圧、心不全などが起こる[1]。妊婦を対象とした研究は充分にはされていない。授乳婦への投与は推奨されない[5]。
ニフェジピンは1966年にドイツで発見された[6]。米国では1981年に承認された[7][1]。日本では1976年に狭心症治療薬として発売され、1985年に高血圧治療薬として認可され、徐放・速放複合錠は1998年に発売された。
WHO必須医薬品モデル・リストに収載されている[8]。
効能・効果
[編集]承認されている効能・効果は、(本態性)高血圧症、腎性高血圧症、狭心症、異型狭心症である[2][3][4]。
高血圧
[編集]長期にわたる高血圧および狭心症に適応を持つ。高血圧の治療ガイドラインでは一般に利尿薬やACE阻害薬が好まれるが、55歳以上の患者ならびにアフリカ系アメリカ人の患者にはチアジド系利尿薬とカルシウム拮抗薬の併用が第一選択とされている[9]。
ニフェジピン舌下投与は以前は高血圧性緊急症の治療に用いられていた。モノアミン酸化酵素阻害薬を服用患者の症候的または実測値的高血圧クリーゼに多く処方されていた時期がある[10]が、危険性が認識される様になってからは使用されていない。ニフェジピン舌下投与は末梢血管を拡張させて血圧を低下させる。こうして低下した血圧は反射性頻脈や血管床での若干の盗血現象をきたす。脳虚血発作や脳梗塞、心筋梗塞、完全房室ブロック、死亡といったニフェジピン舌下投与の有害事象が多数、医学誌に投稿された。米国FDAは1995年に高血圧緊急症に対するニフェジピン舌下投与の有効性に関するあらゆるデータを検討し、安全性・有効性の両面の理由で舌下投与を避けるべきであると結論付けた[11][12]。例外として、脊髄損傷における自律神経反射障害に関連した高血圧症の治療については使用が了解されている[13]。
早期陣痛
[編集]ニフェジピンは子宮収縮抑制薬として頻繁に用いられる[要出典]。コクラン共同計画は硫酸マグネシウムやβ遮断薬(リトドリンなど)と同様に副作用が少ないと結論した[14]。アトシバンとの直接比較は実施されていない。
その他
[編集]レイノー病の治療にニフェジピンがしばしば使用される。2005年のメタアナリシスでは若干の使用利益(重篤な発作を33%減少し、1週間当りの発作回数を2.8〜5回減少させた)が認められたが、メタアナリシスの対象となった研究は総じてニフェジピンの用量が少量であったとされた[15]。
裂肛に対するニフェジピン坐薬は、硝酸塩の局所投与と同様に有効であることが示された[16]。
ニフェジピンは高山病である高地肺水腫の治療薬としても用いられる[17]。
そのほか、悪性腫瘍や破傷風を原因とする 痛みを伴う食道痙攣 の治療や、肺高血圧の患者の一部にも用いられる。
禁忌
[編集]ニフェジピンは、下記の患者には禁忌とされている[2][3][4]。
- 製剤成分に対し過敏症の既往歴のある患者
- 妊婦(妊娠20週未満)または妊娠している可能性のある婦人
- 心原性ショックの患者
- 急性心筋梗塞の患者(カプセル剤のみ)
副作用
[編集]添付文書に記載されている重大な副作用は、紅皮症(剥脱性皮膚炎)、無顆粒球症、血小板減少、ショック、意識障害、肝機能障害、黄疸である[2][3][4]。発現率はいずれも0.1%未満である。
ニフェジピンは速やかに血圧を低下させるので、患者は投与初期に眩暈や擬似発作を経験することが多い。反射性に頻脈が発生することがある。これらの副作用は徐放剤では少ない。より新しい徐放剤(Gastro-Intestinal Therapeutic System、GITS)を用いて、血圧に対する効果を検証するINSIGHT臨床試験[18]や狭心症に対するACTION臨床試験[19]が実施されている。
ニフェジピン徐放剤は空腹時に服用すべきであり、グレープフルーツやそのジュースはニフェジピンの血中濃度を上昇させるので特に避けるべきである。その機序はいくつか考えられており、その中にはCYP3A4の阻害(活性低下)がある[20]。
過量投与
[編集]多くの人々が事故または故意によるニフェジピン過量投与で毒性を経験している。毒性は経口投与でも非経口投与でも発生する。症状としては、無気力、徐脈、血糖低下、意識消失が知られている。入院患者の診断のため、または法医学での検死のために血中濃度を測定することができる。血中濃度は通常液体クロマトグラフィーまたはガスクロマトグラフィで測定される。測定可能範囲は通常、100〜1,000µg/Lである[21][22]。
作用機序
[編集]ニフェジピンはカルシウム拮抗剤であり、細胞膜上に存在する電位依存性カルシウムチャネルを遮断して、細胞外から血管平滑筋の細胞内へのCa2+の流入を減少させることにより降圧作用を示す。
開発の経緯
[編集]当初は鉱質コルチコイド受容体の阻害薬(抗鉱質コルチコイド薬)として発見された[23]。
ニフェジピンの臨床試験の多くは1970年台前半に実施された[24]。
ニフェジピンなどのカルシウム拮抗薬の使用量は、1995年の臨床試験でニフェジピンを服用した虚血性心疾患患者の死亡率が増加した事で激減した[25]。この臨床試験はメタアナリシスであり、主として短時間作用型のニフェジピン製剤(血圧を大きく変動させる)が多量(80mg/日以上)に用いられていた[26]。
剤形
[編集]いずれも経口投与する製剤であり、カプセル(5mg、10mg)、L錠(10mg、20mg)、CR錠(10mg、20mg、40mg)がある。
関連項目
[編集]出典
[編集]- ^ a b c d e “Nifedipine”. The American Society of Health-System Pharmacists. Dec 19, 2015閲覧。
- ^ a b c d “アダラートカプセル5mg/アダラートカプセル10mg 添付文書” (2016年10月). 2016年11月5日閲覧。
- ^ a b c d “アダラートL錠10mg/アダラートL錠20mg 添付文書” (2016年10月). 2016年11月5日閲覧。
- ^ a b c d “アダラートCR錠10mg/アダラートCR錠20mg/アダラートCR錠40mg 添付文書” (2016年10月). 2016年11月5日閲覧。
- ^ “Nifedipine Pregnancy and Breastfeeding Warnings”. 25 December 2015閲覧。
- ^ “アダラートの歴史”. バイエル. 2016年4月8日閲覧。
- ^ Corey, E.J. (2013). Drug discovery practices, processes, and perspectives. Hoboken, N.J.: John Wiley & Sons. p. 172. ISBN 9781118354469
- ^ “19th WHO Model List of Essential Medicines (April 2015)”. WHO (April 2015). May 10, 2015閲覧。
- ^ Hypertension: management of hypertension in adults in primary care. Clinical guideline CG34. National Institute for Health and Clinical Excellence (NICE), June 2006. Fulltext index. ISBN 1-86016-285-1.
- ^ “Nifedipine for MAOI Hypertension? Reversing a Previous Recommendation”. Biological Therapies in Psychiatry (March 1997). 22 Jan 2015閲覧。
- ^ Grossman E, Messerli FH, Grodzicki T, Kowey P (1996). “Should a moratorium be placed on sublingual nifedipine capsules given for hypertensive emergencies and pseudoemergencies?”. JAMA 276 (16): 1328–31. doi:10.1001/jama.276.16.1328. PMID 8861992.
- ^ Varon J, Marik PE (2003). “Clinical review: The management of hypertensive crises”. Critical care (London, England) 7 (5): 374–84. doi:10.1186/cc2351. PMC 270718. PMID 12974970.
- ^ Campagnolo, DI. “Autonomic Dysreflexia in Spinal Cord Injury”. eMedicine. 2011年7月14日閲覧。
- ^ King JF, Flenady VJ, Papatsonis DN, Dekker GA, Carbonne B (2003). Flenady, Vicki. ed. “Calcium channel blockers for inhibiting preterm labour”. Cochrane database of systematic reviews (Online) (1): CD002255. doi:10.1002/14651858.CD002255. PMID 12535434.
- ^ Thompson AE, Pope JE (2005). “Calcium channel blockers for primary Raynaud's phenomenon: a meta-analysis”. Rheumatology (Oxford, England) 44 (2): 145–50. doi:10.1093/rheumatology/keh390. PMID 15546967.
- ^ Ezri T, Susmallian S (2003). “Topical nifedipine vs. topical glyceryl trinitrate for treatment of chronic anal fissure”. Dis. Colon Rectum 46 (6): 805–8. doi:10.1007/s10350-004-6660-8. PMID 12794583.
- ^ Ali, Mir Omar and Qazi, Samia (2007年9月19日). “Pulmonary Edema, High-Altitude”. eMedicine. 2007年11月25日閲覧。
- ^ “Morbidity and mortality in patients randomised to double-blind treatment with a long-acting calcium-channel blocker or diuretic in the International Nifedipine GITS study: Intervention as a Goal in Hypertension Treatment (INSIGHT)”. Lancet 356 (9227): 366–72. (2000). doi:10.1016/S0140-6736(00)02527-7. PMID 10972368.
- ^ Poole-Wilson PA, Kirwan BA, Vokó Z, de Brouwer S, van Dalen FJ, Lubsen J (2006). “Safety of nifedipine GITS in stable angina: the ACTION trial”. Cardiovas Drugs Ther 20 (1): 45–54. doi:10.1007/s10557-006-6312-4. PMID 16552473.
- ^ “Grapefruit juice-nifedipine interaction: possible involvement of several mechanisms”. Journal Clinical Pharm Ther 30 (2): 153–8. (2005). doi:10.1111/j.1365-2710.2004.00618.x. PMID 15811168.
- ^ Nifediac package insert, TEVA Pharmaceuticals, Sellersville, Pennsylvania, August, 2009.
- ^ Baselt, Randall C. (2008). Disposition of Toxic Drugs and Chemicals in Man. Foster City, CA: Biomedical Publications. pp. 1108–1110. ISBN 0-9626523-7-7
- ^ Luther, James M. (2014). “Is there a new dawn for selective mineralocorticoid receptor antagonism?”. Current Opinion in Nephrology and Hypertension 23 (5): 456–461. doi:10.1097/MNH.0000000000000051. ISSN 1062-4821.
- ^ “[Pharmacology of 4-(2'-nitrophenyl)-2,6-dimethyl-1,4-dihydropyridine-3,5-dicarboxylic acid dimethyl ester (Nifedipine, BAY a 1040)]” (German). Arzneimittel-Forschung 22 (1): 1–14. (1972). PMID 4622472.
- ^ Furberg CD, Psaty BM, Meyer JV (1995). “Nifedipine. Dose-related increase in mortality in patients with coronary heart disease”. Circulation 92 (5): 1326–31. doi:10.1161/01.cir.92.5.1326. PMID 7648682.
- ^ Opie LH, Messerli FH (1995). “Nifedipine and mortality. Grave defects in the dossier”. Circulation 92 (5): 1068–73. doi:10.1161/01.cir.92.5.1068. PMID 7648646.
