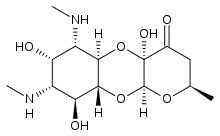
スペクチノマイシン
 | |
 | |
| IUPAC命名法による物質名 | |
|---|---|
| |
| 臨床データ | |
| Drugs.com | monograph |
| 胎児危険度分類 |
|
| 法的規制 |
|
| データベースID | |
| CAS番号 |
1695-77-8 |
| ATCコード | J01XX04 (WHO) |
| PubChem | CID: 15541 |
| DrugBank |
APRD01232 |
| ChemSpider |
14785 |
| UNII |
93AKI1U6QF |
| KEGG |
D08526 |
| ChEBI |
CHEBI:9215 |
| ChEMBL |
CHEMBL1167 |
| 別名 | (2R,4aR,5aR,6S,7S,8R,9S,9aR,10aS)-4a,7,9-trihydroxy-2-methyl-6,8-bis(methylamino)decahydro-4H-pyrano[2,3-b][1,4]benzodioxin-4-one |
| 化学的データ | |
| 化学式 | C14H24N2O7 |
| 分子量 | 332.35 g/mol |
| |
スペクチノマイシン(Spectinomycin)とは真正細菌のStreptomyces spectabilis によって産生されるアミノグリコシド系抗生物質であり、淋菌感染症の治療に用いられる[1][2]。塩酸塩がトロビシンとして商品化されている。臀部筋肉内注射で用いられる。
WHO必須医薬品モデル・リストに収載されている[3]。
スペクチノマイシンは1961年に発見された[4]。日本では1978年5月に承認された[5]:32。米国ではトロビシンは2001年に供給が中止された[6]。
作用機序
[編集]真正細菌のリボソーム30Sサブユニットに結合し、タンパク質合成を阻害する。
Pasteurella multocida の16SリボソームRNAにより耐性を持つものが存在する[7]。
効能・効果等
[編集]豚赤痢菌を選択的に培養するために血液寒天培地に添加されることがある。
スペクチノマイシン耐性遺伝子は、分子クローニングの目的で細菌の選択マーカーとして利用することができる。加えて、スペクチノマイシンは選択マーカー遺伝子SPCR を含む形質転換された植物細胞の選択剤として利用され得る[8]。
副作用
[編集]副作用として瘙痒感、悪寒、腹痛、紅斑が認められる。重大な副作用としてはショック(0.04%)がある[2]。
生合成
[編集]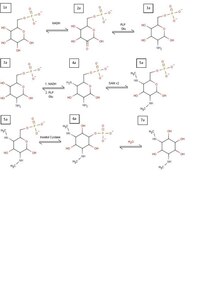
スペクチノマイシンの生合成は他のアミノグリコシドと同様に、イノシトール環の形成から始まるが、イノシトール環の形成過程が異なる。グルコース-6-リン酸(図中1a)がNADHで還元されて2位の炭素がケトンとなり(2a)、ケトンはピリドキサールリン酸(PLP)共存下でグルタミンからアミノ基を転移される(3a)。この過程は4位の炭素でも繰り返され、ジアミンを生成する(4a)。このジアミンはS-アデノシルメチオニン(SAM)2分子からメチル基を受け取り、2つの窒素がそれぞれモノメチル化される(5a)。メチル化される事で、イノシトールシクラーゼがグルコース環をイノシトール環に組み替える準備が完了する。その生成物(6a)はリン酸エステルを加水分解され、スペクチノマイシンのイノシトール骨格が完成する(7a)。
上記の反応が進行してる間、別の経路で同様の出発物質から残りの糖鎖部分が生成する。その経路ではグルコース-1-リン酸(1b)がTDP合成酵素でTDPグルコース(2b)となり、6位の炭素がヒドラターゼで脱水され(3b)、NADHで4位の炭素が酸化されてケトンとなり(4b)、PLPとグルタミンからアミノ基を受け取り(5b)、さらにデアミナーゼで変換されると共に、2分子のNADHで3位と4位の炭素が酸化されてケトンとなり、アミノグリコシド生成に必要な分子が完成する(6b)。
こうして生成した(7a)と(6b)が縮合してTDP基が離脱し、スペクチノマイシンが生成される[9]。
自然界での分布
[編集]アミノシクリトール系の抗生物質であり、アミノグリコシド系抗生物質と近縁関係にある。スペクチノマイシンは自然界ではシアノバクテリアや種々の植物にも存在する。主に植物の自己防御に関連して分泌される。
出典
[編集]- ^ “Spectinomycin Hydrochloride”. The American Society of Health-System Pharmacists. Sep 6, 2015閲覧。
- ^ a b “トロビシン筋注用2g 添付文書” (2016年5月). 2016年6月29日閲覧。
- ^ “WHO Model List of EssentialMedicines”. World Health Organization (October 2013). 22 April 2014閲覧。
- ^ Textbook of Drug Design and Discovery, Fourth Edition. CRC Press. (2009). p. 438. ISBN 9781439882405
- ^ “トロビシン筋注用2g インタビューフォーム” (PDF) (2010年10月). 2016年4月2日閲覧。
- ^ “From the Centers for Disease Control and Prevention. Update on spectinomycin availability in the United States”. JAMA 286 (11): 1308–9. (September 2001). PMID 11575327.
- ^ Kehrenberg C, Schwarz S (June 2007). “Mutations in 16S rRNA and ribosomal protein S5 associated with high-level spectinomycin resistance in Pasteurella multocida”. Antimicrob. Agents Chemother. 51 (6): 2244–6. doi:10.1128/AAC.00229-07. PMC 1891365. PMID 17371823.
- ^ “Spectinomycin Hydrochloride” (pdf). Toku-E (2010年10月10日). 2012年6月11日閲覧。
- ^ Dewick, Paul M. (4 Feb 2009). Medicinal Natural Products: A Biosynthetic Approach, 3rd Edition. Wiley Online Library: Wiley. pp. 485–508. ISBN 9780470741689 29 May 2014閲覧。
