超音波検査
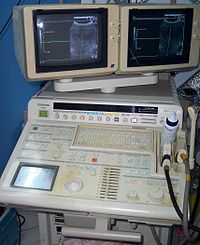
超音波検査(ちょうおんぱけんさ、英語: ultrasonography, US echo)とは、超音波を対象物に当ててその反響を映像化する画像検査法である。一般に「エコー検査」、略して「エコー」とも呼ばれることが多い[1]。超音波検査は非侵襲的な検査手法である他に、X線画像検査などとは違って超音波検査には被曝の心配がないため、放射線管理も不要なので装置さえ用意すれば病室でも行える上に、日を変えて検査を何回行っても問題ないこともあり医療分野で広く利用されている。また近年、金属材料などを対象として、レーザーを用いて超音波を励起・計測するレーザー超音波計測が行われる。肝臓、胆嚢、膵臓、腎臓、脾臓、心臓、甲状腺、乳腺 、下肢血管を主な検査対象とするが、医師の判断で、胃や腸、膀胱などの検査も行われる[1]。肝臓がんや乳がんなどでは、血流を見る目的で、造影剤を使用して超音波検査を行うこともある[2]。本稿では、主に医療用超音波検査について記述する。
原理
[編集]対象物に探触子(プローブ)を当てて超音波を発生させ、反射した超音波を受信し、画像データとして処理する。超音波を発生させると、ごく短い時間のうちに、その音は対象物の中を進んでいき、骨などの固い組織に当たると大部分は反射する [注釈 1] 。また、組織の境界のように性状が変わる場所でも一部が反射したり、散乱が起こる。その後、体表まで戻ってきた超音波を検知する。この時、超音波を発生させてから、その超音波が体表まで戻ってきた時間を計測することで、体表からの反射が起きた場所までの距離を知ることができる。なぜなら、音速をv、超音波の反射点までの距離をLとすると、組織中の音速を一定と仮定した場合 [注釈 2] 、体表まで超音波が戻ってくるのにかかる時間tは、
と表せるので、
と求まるからである。基本的には、これを利用して生体内部の様子を可視化する。
ただし、超音波が探触子から放射されると、超音波は減衰してゆくので、ある程度の強さの超音波を必要とする。しかしながら、超音波の強さを上げ過ぎると、超音波が減衰する時に熱を出すため、この熱によって生体に打撃を与える可能性がある。そして、約10 (W/cm)の強さだと、超音波のエネルギーそのものによって細胞そのものを破壊する [3] 。 したがって、使える超音波の強さには上限が存在する。なお、約0.1 (W/cm)程度の強さまでの超音波であれば、超音波による加熱作用も問題ないとされる [3] 。
また、血流のように動きのある物に対してはドップラー効果を利用して、動いている方向を調べることも行われる。これを利用して、例えば、心臓の拍出量を調べたり、血流の逆流が無いかを調べたりすることができる。
特徴
[編集]基本的に超音波は液体・固体がよく伝わり、気体は伝わりにくい。そのため、液状成分や軟体の描出に優れており、実質臓器の描出能が高く、肺・消化管の描出能は低い。また、骨は表面での反射が強く骨表面などの観察に留まる。
探触子の種類
[編集]
開発当初のエコー検査では、音波を一方向のみに発射するだけのものであったが、その後改良され、扇状に音波を発生することで、対象物の断面画像がリアルタイムに見られるようになっている。
- Linear型(リニア型)
- 体表へ接触させる超音波のビームを発射する部分は平面である。ここから、その平面に対して垂直方向のビームを、何本も発生させる。つまり、超音波ビームの発射点を、平面上において隈なく移動させる方法で走査している。よって、全ての超音波ビームは平行である。したがって、特にSector型と比べると、体表に近い部分では広範囲に超音波ビームを当てられる。このため、主に体表に近い部分に位置する組織の検査に用いられ、例えば、体表近くの血管や筋肉、乳腺や甲状腺などを見るのに向く。
- Sector型(セクタ型)
- 体表へ接触させる超音波のビームを発射する部分は、Linear型などと比べて狭く小さい。この接触部分の1点から超音波ビームを発射する。そして、超音波ビームは角度を変えて次々と放射される。つまり、超音波ビームを発射する角度を変える方法で走査している。よって、いずれの超音波ビームも平行ではない。したがって、体表に近い部分は狭い範囲にしか超音波ビームを当てられないのに対し、体表から遠い部分では広い範囲に超音波ビームを当てられる。また、Linear型とは違って、Sector型ならば超音波ビームが入ってゆく場所は狭くても問題がない。超音波は骨に当たると、そこで反射して体表に戻ってきてしまうものの、Sector型なら、肋骨の間から、その向こう側へと超音波ビームを放射することも容易である。このため、例えば肋骨で囲まれた胸腔内の臓器を標的とした超音波検査、例えば心臓超音波検査などに用いられる。なお、産婦人科で用いられる経膣超音波検査も、超音波ビームの発射部分、つまり、探触子はSector型のように小さくする必要が出てくる。
- Convex型(コンベックス型)
- 体表へ接触させる超音波のビームを発射する部分は、緩やかな凸面である。このため、Linear型と比べて、凹凸のある体表にも密着させやすい。しかも、接触面がさほど広くなくとも、体表から離れるにつれて超音波ビームが広がってゆくので、体表から遠い部分では広い範囲に超音波ビームを当てられる。このため、主に体表からの腹部超音波検査に用いられる。
画像の種類
[編集]
主に、以下の画像モードがある。
Aモード
[編集]受信したエコーを表現するための方法はいくつかあるが、A(amplitude:振幅)モードとB(brightness:輝度)モードが基本となっている。超音波は直進性に優れており、音響インピーダンスの異なった物質間の境界面で反射がおこり、受信するまでの時間を元に物質までの位置を計算することが出来る。 物質までの距離を横軸にとり、反射したエコーの振幅を縦軸にとったグラフがAモード像である。原理としては重要であるが、Aモードは実際の検査には、あまり用いられない。
Bモード
[編集]Aモードではエコーの振幅と位置を表示していたが、この振幅を点の明るさ(輝度)として表示したものがBモードである。1本の超音波ビームでは、一次元像しか得られないが、複数の超音波ビームを発生させると二次元像を作成することが出来る。単に超音波断層検査と言った場合にはBモードを指すことが多い。
Mモード
[編集]M(Motion:動き)モードとは、断面上のさらにある一直線上に注目し、そこでの音波反射の経時変化を画像化する検査である。心臓の弁や心筋の動きなど、動きのある部位を時系列で観察できるため、ドップラーエコーと同様心エコーでの有用性が高い。
カラードップラー
[編集]ドップラー効果によって、反射した音波の周波数が変化することを利用して、物体がプローブに近づいているのか遠ざかっているのかを判定し画像評価できる。
ドップラーには、特定位置の超音波ビームの周波数変化を流速に変換しグラフ化するドップラーモードと、Bモード画像上に指定した領域での流速変化を色で表現するカラードップラーモードがある。特に心エコーで、心臓の血流を評価する際に有用である。
カラードップラーでは、「赤方偏移」「青方偏移」がそれぞれ「遠ざかる」「近づく」場合のドップラーシフトに当たるが、医療用機器では逆に「近づく」「遠ざかる」を表示している。
パワードップラー
[編集]カラードップラーに比較して感度が高い。一方、フレームレートは落ち、分解能も落ちる。
ワイドバンドドップラー
[編集]Bモード並みの分解能とフレームレートを有する表示方法。 メーカーにより名称が異なる。
検査の種類
[編集]
超音波が伝わりやすいように、体の表面に検査用のゼリーを塗り、超音波を出す器械であるプローブをあてて検査を行う。食事をすると臓器が見えなくなるため飲食は禁止[1]。
主に以下のような検査の種類がある。
腹部超音波検査
[編集]体表よりアプローチし、肝臓・胆嚢・膵臓・脾臓・腎臓・子宮・卵巣・前立腺等の腹部の実質臓器や妊娠中の胎児の評価を行う。また、胃・大腸・虫垂等の描写にも用いられる。ただ、子宮・卵巣・前立腺等は体表腹部超音波検査よりも経膣・経肛門超音波検査からの描出の方が優れている。
心臓超音波検査
[編集]体表よりアプローチし、心臓・大血管の評価を行う。心腔内に関しては体表心臓超音波検査よりも経食道心臓超音波検査からの描出の方が優れている。
頸部超音波検査
[編集]体表よりアプローチし、頚部の甲状腺・副甲状腺・頸動脈・頸静脈の評価を行う。
乳房超音波検査
[編集]体表よりアプローチし、乳房の評価を行う。
血管超音波検査
[編集]体表よりアプローチし、腹腔内の大動脈・大静脈や上肢・下肢の動脈・静脈の評価を行う。
経膣超音波検査
[編集]運動器超音波検査
[編集]体表よりアプローチして「筋」「腱」などの形態診断と機能診断を行う。
超音波内視鏡検査
[編集]軟性管を用いて上部消化管や気管支の腔内よりアプローチし、管壁や周囲臓器の評価を行う。
その他の超音波検査
[編集]- FAST(Focused Assessment with Sonography for Trauma)
- 外傷患者の場合、致死的な臓器損傷の有無を即座に評価するための迅速超音波検査方法の名称。これは心嚢、左右肋間、モリソン窩、ダグラス窩、脾臓周囲の6か所をすばやく超音波検査施行し、腹腔内出血がないことを確認することである。出血所見により点数化し開腹手術の必要性を評価できる。
超音波装置を用いた治療
[編集]超音波装置を用いた治療として集束超音波とドラッグデリバリーシステム(DDS)に関して述べる。
集束超音波
[編集]強力集束超音波(High-Intensity Focused Ultrasound、HIFU)装置は標的部位に体外からピンポイントに超音波のエネルギーを集束できる装置であり前立腺癌、子宮筋腫、乳癌に対する低侵襲な治療法として利用されている[4]。これは強力超音波を癌に集中させることで焦点部分の温度を80度近くに熱することで癌細胞を凝固させる治療法である。本態性振戦ではMRIガイド下で経頭蓋的に脳内の視床腹中間核(Vim核)にHIFUを照射し凝固させる治療法が2019年より保険診療で可能となっている。超音波には照射部位を振動させたりする機械的作用と加熱などを引き起こす熱的作用がある。これらは超音波の周波数や強度により変化するものの、照射強度を高くしていくと機械的作用や熱的作用が増大していく。この機械的作用と熱的作用を利用して、HIFUで特定の部位を凝固させることが可能となる。
血液脳関門を通過するDDS
[編集]集束超音波の超音波照射エネルギーを徐々に下げていくと熱的作用が低下して機械的作用のみを利用することができる。この機会的作用による組織の振動は、組織内の毛細血管の密着結合を緩めることで血管透過性の亢進を導く。そのため集束超音波を用いて血液脳関門の透過性を亢進させ、治療薬を脳へ送達させる方法が考えられた。超音波照射のみで血管透過性を亢進させるためには超音波照射強度が高くなり組織障害のリスクが高まる[5]。事実、1990年の報告では血液脳関門の透過性を十分に高めるには頭蓋骨切除が必要であった[6]。超音波造影剤として利用されるマイクロバブルを併用すると比較的低い超音波強度で超音波の機械的作用を増強させることができる[7]。
マイクロバブルに超音波を照射すると振動(オシレーション)と圧壊(キャビテーション)が誘導される。マイクロバブルの振動と圧壊は細胞膜に作用し一過性の小孔を形成し、細胞外の物質が細胞内に取り込まれることが知られている。この作用をソノポレーションという。マイクロバブルを血管内投与し体外から超音波照射すると組織の血管内でマイクロバブルの振動や圧壊が誘導され、周囲の血管内皮細胞間の密着結合に作用して血管透過性を変化させることができるのではないかと考えられている[8][9] [10][11]。血液脳関門の透過性の亢進の持続時間は数時間で可逆的と考えられている[12]。代表的な研究として下記のようなものが挙げられる。集束超音波を血液脳関門に作用させ、乳癌治療薬の抗体医薬であるハーセプチンを脳内に移行させたという研究が知られている[13]。脳腫瘍の患者に集束超音波とマイクロバブルを用いて抗癌剤のドキソルビシンリポソームやテモゾロミドを脳腫瘍に送達させた報告がある[14] 。一方で集束超音波とマイクロバブルの併用は無菌性炎症を起こすという報告もあり副作用が懸念される[15]。
細胞膜を通過するDDS
[編集]治療用超音波とマイクロバブルを併用して細胞外の薬物や遺伝子を細胞内に導入させることができる[16][17]。
医療以外での超音波検査
[編集]対象物を破壊せずに、構造内部の評価が行える非破壊検査として、広く利用されている。またその検査方法において、超音波探傷試験とSAT試験の2つに大別される。
超音波探傷試験
[編集]英語: Ultrasonic Testing, UT とは、対象に直接探触子を当て評価を行う方法。鉄鋼構造物、電力、化学プラントなどにおいて構造物内部の欠陥や減肉調査を目的に使用される。製作時と経年変化をチェックする場合があり、たとえば建設物の欠陥や老朽化を測定したり、材料や部品の内部検査を行ったりする目的で、超音波検査が実用化されている。日本では社団法人破壊検査協会が、認定技術者の資格を発効している。鉄骨に関しては、通称「全鋼連」の資格が求められることが多い。
SAT試験
[編集]英語: Scanning Acoustic Tomograph, SAT とは、水などを媒体として対象を映像化する方法。探触子から対象へ水を媒体として超音波を発振し、その反射もしくは透過の強弱にて内部構造を映像化する。金属鋼材の接合部、半導体パッケージ、ウェハーなどの検査に使用されている[18][19]。
トピックス
[編集]- リピッドバブル
帝京大学の丸山らのグループは血中安定性や滞留性に優れたポリエチレングリコール(PEG)修飾リポソームに眼科領域で使用されている眼内長期滞留ガス(パーフルオロプロパン)を封入したバブル製剤、リピッドバブルを開発した[20][21]。リピッドバブルはもともとソノポレーションによる遺伝子・核酸導入ツールとしての有効性が報告されている。丸山らはリピッドバブルと強力集束超音波の併用で静脈投与されたエバンスブルーが脳内に蓄積することが報告した[22]。これは分子量67000程度の物質が血液脳関門を通過することを意味する。この血液脳関門の透過させる効果は一過性であった。蛍光標識したデキストランを用いると2000kDaの分子まで透過可能である。脳へのさらなる導入効率化を目指し、LRP1に対する高い親和性を有するペプチド配列であるAngiopep-2ペプチド[23]をリピッドバブル表面修飾ペプチドとして用いる試みも行われている[24]。
関連項目
[編集]注釈
[編集]- ^ ただし骨の囲まれた部分への体表からの超音波検査が不可能というわけではない。例えば、経頭蓋超音波検査と言って、頭皮の上から探触子を当てて、脳の様子を探る超音波検査も存在する。Transcranial Dopplerなど、幾つか種類がある。
- ^ 参考までに、ヒトの組織を伝わる音速は組織によって異なるものの、だいたい水中を伝わる音速に近く、おおよそ1500 (m/秒)前後である部分が多い。音速が大きく異なる場所は、骨と気体が溜まっている場所である。なお、音速は、骨では速く、気体が溜まっている部分では遅い。
出典
[編集]- ^ a b c “超音波(エコー)検査”. 日本赤十字社愛知医療センター名古屋第一病院. 2024年3月19日閲覧。
- ^ “がんの検査について 超音波(エコー)検査とは”. がん情報サービス. 2024年3月19日閲覧。
- ^ a b ME技術教育委員会 監修 『MEの基礎知識と安全管理(改訂第4版)』 p.60 南江堂 2002年4月20日発行 ISBN 4-524-22408-4
- ^ 鈴木亮, 小俣大樹, ウンガ・ヨハン ほか, 「超音波とマイクロバブルによる血管透過性亢進に基づくEPR効果促進への期待」『Drug Delivery System』 33巻 2号 2018年 p.115-122, doi:10.2745/dds.33.115
- ^ Ultrasonics. 2008 Aug;48(4):279-96. PMID 18511095
- ^ Adv Exp Med Biol. 1990;267:369-81. PMID 2088054
- ^ Radiology. 2001 Sep;220(3):640-6. PMID 11526261
- ^ J Control Release. 2015 Dec 10;219:61-75. PMID 26362698
- ^ Drug Discov Today Technol. 2016 Jun;20:41-48. PMID 27986222
- ^ F1000Res. 2016 Mar 10;5. pii: F1000 Faculty Rev-313. PMID 26998242
- ^ Front Pharmacol. 2019 Feb 7;10:86. PMID 30792657
- ^ ACS Chem Neurosci. 2013 Apr 17;4(4):519-26. PMID 23379618
- ^ Proc Natl Acad Sci U S A. 2006 Aug 1;103(31):11719-23. PMID 16868082
- ^ Sci Rep. 2019 Jan 23;9(1):321. PMID 30674905
- ^ Proc Natl Acad Sci U S A. 2017 Jan 3;114(1). PMID 27994152
- ^ J Control Release. 2011 Jan 5;149(1):36-41. PMID 20470839
- ^ 髙橋葉子, 丸山一雄, 根岸洋一, 「リピッドバブルと超音波によるセラノスティクスと遺伝子・核酸デリバリー」『Drug Delivery System』 34巻 2号 2019年 p.116-123, doi:10.2745/dds.34.116
- ^ 超音波映像装置・検査装置
- ^ (PDF) 超音波映像装置
- ^ J Control Release. 2007 Jan 22;117(1):130-6. PMID 17113176
- ^ J Control Release. 2008 Dec 8;132(2):124-30. PMID 18804499
- ^ Pharmaceutics. 2015 Sep 21;7(3):344-62. PMID 26402694
- ^ J Neurochem. 2008 Aug;106(4):1534-44. PMID 18489712
- ^ Biol Pharm Bull. 2016;39(6):977-83. PMID 27251499
外部リンク
[編集]- 超音波検査の原理 : Dr.SONOの公開講座「超音波の基礎」
- 学会 : 日本超音波医学会
- 学会 : 日本超音波検査学会


