メモリーT細胞
メモリーT細胞(めもりーてぃーさいぼう、英: memory T cell)は、T細胞の亜集団で、メモリーB細胞と同じ機能を持つ可能性がある。その系統は不明である。
機能
[編集]ウイルスや他の微生物分子に特異的な、抗原特異的メモリーT細胞は、TCMおよびTEMの両方の亜集団が発見されている。現在、これに関するほとんどの情報は、細胞傷害性T細胞(CD8陽性)亜集団の観察に基づいており、ヘルパーT細胞(CD4陽性)と細胞傷害性T細胞の両方に同様の集団が存在していると考えられている。メモリー細胞の主な機能は、関連する病原体を体内に再導入することによってメモリー細胞が再活性化された後の免疫応答の増強である。この分野は集中的に研究されており、まだ情報が得られていない場合もあることに注意が必要である。
- TCM : TCM細胞は、幹細胞と共通していくつかの特徴を持っているが、最も重要なのは自己複製能力であり、主に重要な転写因子であるSTAT5のリン酸化が高いレベルで行われていることである。マウスを用いた実験では、TCMは、TEM細胞と比較して、ウイルス[1]、細菌、がん細胞[2]に対してより強力な免疫力を発揮することが証明された。
- TEM : TEM細胞および TEMRA細胞は、主にCD8変異体として活動しており、主に病原体に対する細胞傷害作用を担っている[3]。
- TRM : TRM細胞は、組織内、またはさらに重要なのはバリア組織(上皮など)に長時間存在しており、バリア障害への迅速な対応と、関連する病原体への対応に不可欠である。TRMが病原体を制限するために使用される機構の1つは、グランザイムBの分泌である[4][5]。
- TSCM : これらのリンパ細胞は、TCM細胞と同様に自己複製することができ、TCMとTEMの両方の亜集団を生成することもできる。この集団がヒトに存在するかどうかは現在調査中である[6]。
- TVM : 現在のところ、TVM細胞で明らかに見られる機能は、さまざまなサイトカインの産生だけであるが[7][8]、望ましくない免疫状態を抑制するための影響力と、自己免疫疾患の治療への利用が推測されている[9]。
恒常性維持
[編集]特定のT細胞受容体を発現するメモリーT細胞のクローンは、私たちの体内で何十年も持続することができる。メモリーT細胞はナイーブT細胞よりも半減期が短いため、この維持プロセスには古い細胞の継続的な複製と交換が関与していると考えられる[3]。現在のところ、メモリーT細胞の背後にある機構は完全には解明されていなfい。T細胞受容体を介した活性化がその役割を果たしている可能性がある。メモリーT細胞は、時に新規抗原に反応することがあり、これは潜在的にT細胞受容体結合標的の固有の多様性と幅の広さに起因していることがわかっている。これらのT細胞は、環境抗原や、私たちの体内に常在する抗原(腸内細菌のようなもの)と交差反応して増殖する可能性がある。これらのイベントは、メモリーT細胞集団の維持に役立つ。粘膜組織では抗原密度が高いため、この交差反応メカニズムはメモリーT細胞にとって重要であると考えられる。血液、骨髄、リンパ系組織、脾臓に存在している場合は、恒常性サイトカイン(IL-17とIL-15を含む)または主要組織適合遺伝子複合体II(MHCII)シグナル伝達がより重要である可能性がある。
ライフタイムの概要
[編集]メモリーT細胞は、ヒトのさまざまなライフステージでさまざまな変化を遂げ、さまざまな役割を果たしている。出生時および幼児期には、末梢血中のT細胞は主にナイーブT細胞である[10]。抗原に頻繁に暴露されることにより、メモリーT細胞の集団が蓄積されてゆく。これは、生まれてから20~25歳頃まで続くメモリー生成期であり、私たちの免疫系が最も多くの新しい抗原に遭遇する時期である[3]。次に来るメモリー恒常性維持期では、メモリーT細胞の数は横ばい状態になり、恒常性維持によって安定化する。この段階では、新しい抗原にほとんど遭遇しないため、免疫応答は恒常性維持にシフトする。この段階では、腫瘍の監視も重要になる。人生の後期になると、65~70歳頃に免疫老化段階が到来し、免疫調節不全、T細胞機能の低下、および病原体に対する感受性の増加が見られる。
系統論議
[編集]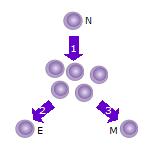
1. ナイーブT細胞(N)が抗原に遭遇すると活性化され、多くのクローンや娘細胞に増殖(分裂)し始める。
2. 一部のT細胞クローンは、その細胞の機能を果たすエフェクターT細胞(E)に分化する(例えば、ヘルパーT細胞の場合はサイトカインを産生し、細胞傷害性T細胞の場合は細胞死を引き起こす)。
3. 一部の細胞は、メモリーT細胞(M)を形成し、同じ抗原に再遭遇して再活性化するまで、宿主の中で不活性状態で長期間生存する。
2020年4月現在、エフェクターT細胞とメモリーT細胞の系統関係は不明である[11][12][13]。2つの競合するモデルが存在する。1つはオン-オフ-オンモデルと呼ばれるものである。ナイーブT細胞が、抗原に結合するT細胞受容体(TCR)とその下流のシグナル伝達経路によって活性化されると、活発に増殖し、エフェクター細胞の大規模なクローンを形成する。エフェクター細胞は、サイトカイン分泌などのエフェクター活動を活発に行う。抗原クリアランス後、これらのエフェクター細胞の一部は、ランダムに決定された方法で、またはその優れた特異性に基づいて選択されて、メモリーT細胞を形成する。これらの細胞は、活性化エフェクターとしての役割から、よりナイーブなT細胞に近い状態に逆戻りし、次の抗原曝露時に再び「オン」になる。このモデルでは、エフェクターT細胞がメモリーT細胞に移行して生存し、増殖する能力を保持できることを予測している。また、特定の遺伝子発現プロファイルが、ナイーブ期、エフェクター期、メモリー期の段階でオン-オフ-オンのパターンに従うと予測している。このモデルを支持する証拠として、インターロイキン-7受容体アルファ(IL-7Rα)、Bcl-2、CD26Lなど、オン-オフ-オンの発現パターンに従う生存とホーミングに関連する遺伝子の発見が挙げられる。

このモデルでは、メモリーT細胞はエフェクターT細胞を生成するが、その逆ではない。
もう一つのモデルは、発達分化モデルである[12]。このモデルでは、高度に活性化されたナイーブT細胞が産生するエフェクター細胞はすべて、抗原クリアランス後にアポトーシスを受けると主張している[11]。メモリーT細胞は、活性化されたナイーブT細胞によって産生されるが、エフェクター段階には全稼働で入ることはない。メモリーT細胞の子孫は、拡大するエフェクターT細胞ほど抗原に特異的ではないため、完全には活性化されない。細胞分裂の履歴を調べた研究では、エフェクターT細胞ではメモリーT細胞に比べてテロメアの長さとテロメラーゼの活性が低下していることがわかった。これはメモリーT細胞がエフェクターT細胞ほど多くの細胞分裂を起こさなかったことを示唆しており、オン-オフ-オンモデルとは矛盾している。HIV感染のように、T細胞の反復的または慢性的な抗原刺激は、エフェクター機能を上昇させるが、メモリー力は低下することが示唆された。また、大量に増殖したT細胞は短命のエフェクター細胞を生成しやすく、一方、最小限に増殖したT細胞はより長寿命の細胞を形成することが明らかになった。
エピジェネティック修飾
[編集]エピジェネティック修飾(英: epigenetic modification)は、ナイーブT細胞からの変化に関与している。たとえば、CD4+メモリーT細胞では、陽性ヒストン修飾は、IFNγ、IL4、IL17Aなどの二次免疫応答中にアップレギュレート(上方制御)される重要なサイトカイン遺伝子をマークしている。これらの修飾のいくつかは、抗原クリアランス後も持続し、抗原との再遭遇時により迅速な活性化を可能にするエピジェネティックメモリーを確立する。CD8+メモリーT細胞では、IFNγのような特定のエフェクター遺伝子は発現しないが、活性化時に迅速に発現するように転写されている。さらに、特定の遺伝子の発現の増強は、メモリーT細胞の子孫に対する初期TCRシグナル伝達の強度にも依存しており、これは遺伝子発現レベルを直接変化させる調節エレメントの活性化と相関している。
亜集団
[編集]歴史的に、メモリーT細胞は、エフェクター(TEM)またはセントラルメモリー(TCM)のいずれかの亜型に属すると考えられており、それぞれが独自の細胞表面マーカーの集まりを持っている(下記参照)[14]。その後、組織常在型メモリーT細胞(TRM)、幹メモリーT細胞(TSCM)、バーチャルメモリーT細胞(TVM)など、メモリーT細胞の多数の追加亜型が発見された。すべてのメモリーT細胞の亜型に共通しているのは、寿命が長く、抗原に再曝露するとすぐに大量のエフェクターT細胞に拡大できるということである。この機構により、これらの細胞は、以前に遭遇した病原体に対する「記憶」を免疫系に提供する。メモリーT細胞はCD4+またはCD8+のいずれかであり、通常はCD45ROを発現し、同時にCD45RAを欠いている[15]。
メモリーT細胞の亜型
[編集]- セントラルメモリーT細胞(TCM、Central memory T cells)は、CD45RO、C-Cケモカイン受容体タイプ7(CCR7)、およびL-セレクチン(CD62L)を発現する。セントラルメモリーT細胞はまたCD44を中等度から高度で発現する。このメモリー亜集団は、一般的にリンパ節と末梢循環で見られる。
- エフェクターメモリーT細胞(TEM、Effector memory T cells)はCD45ROを発現するが、CCR7およびL-セレクチンの発現を欠いている。また、CD44の発現は中等度から高度である。これらのメモリーT細胞は、リンパ節ホーミング受容体を欠いているため、末梢循環や組織に見られる[16]。TEMRAは、ナイーブT細胞に通常見られるマーカーであるCD45RAを再発現する最終分化型エフェクターメモリー細胞(Terminally differentiated effector memory cells)の略である[17]。
- 組織常在型メモリーT細胞(TRM、Tissue resident memory T cells)は、再循環することなく組織(皮膚、肺、消化管など)を占有する。TRMと関連しているいくつかの細胞表面マーカーは、CD69およびインテグリンαeβ7(CD103)である[5]。ただし、異なる組織で見られるTRM細胞は、異なる細胞表面マーカーを発現していることに注目に値する。CD103+ TRM細胞は上皮や神経組織に限定的に局在しているのに対し、マウスの唾液腺、膵臓、および女性生殖管に局在するTRM細胞はCD69もCD103も発現していない[18]。TRM細胞は、病原体に対する防御免疫において主要な役割を果たしていると考えられている[5][19]。研究ではまた、TRM細胞には保護と調節の二重の役割があることも示唆している[10]。TEM細胞と比較して、TRM細胞は防御免疫関連サイトカインを高レベルで分泌し、増殖マーカーKi67の発現量が低い。これらの特徴は、TRM細胞の長期的な維持と、抗原侵入に対する迅速な応答と不必要な組織損傷の回避との間で、バランスを保つのに役立つのではないかと提案された。機能不全のTRM細胞は、乾癬、関節リウマチ、炎症性腸疾患などの自己免疫疾患に関与している。TRM細胞に特異的なのは脂質代謝に関わる遺伝子であり、他のタイプのT細胞に比べて約20~30倍の活性があり、高い活性を持っている[19]。
- バーチャルメモリーT細胞(TVM、Virtual memory T cell)は、強力なクローン増殖イベントの後に発生しないという点で、他のメモリー亜集団とは異なる。したがって、この集団は全体として末梢循環内に豊富に存在するが、個々のバーチャルメモリーT細胞クローンは比較的低い頻度で存在する。一説には、恒常性増殖がこのT細胞集団を生み出しているというものがある。最初に記述されたのはCD8バーチャルメモリーT細胞であったが[20]、現在ではCD4バーチャルメモリーT細胞も存在することが分かっている[21]。
メモリーT細胞の他の多くの亜集団が示唆されている。研究者らは、幹メモリー細胞(TSCM、Stem memory T cells)を研究してきた。ナイーブT細胞と同様に、TSCM細胞はCD45RO-、CCR7+、CD45RA+、CD62L+(L-セレクチン)、CD27+、CD28+、IL-7Rα+であるが、CD95、IL-2Rβ、CXCR3、LFA-1を多量に発現し、メモリー細胞に特有の多数の機能的属性を示す[6]。
参照項目
[編集]脚注
[編集]- ^ “Lineage relationship and protective immunity of memory CD8 T cell subsets”. Nature Immunology 4 (3): 225–34. (March 2003). doi:10.1038/ni889. PMID 12563257.
- ^ “Central memory self/tumor-reactive CD8+ T cells confer superior antitumor immunity compared with effector memory T cells”. Proceedings of the National Academy of Sciences of the United States of America 102 (27): 9571–6. (July 2005). Bibcode: 2005PNAS..102.9571K. doi:10.1073/pnas.0503726102. PMC 1172264. PMID 15980149.
- ^ a b c “Human memory T cells: generation, compartmentalization and homeostasis”. Nature Reviews. Immunology 14 (1): 24–35. (January 2014). doi:10.1038/nri3567. PMC 4032067. PMID 24336101.
- ^ “Memory T cells in nonlymphoid tissue that provide enhanced local immunity during infection with herpes simplex virus”. Nature Immunology 10 (5): 524–30. (May 2009). doi:10.1038/ni.1718. PMID 19305395.
- ^ a b c “Tissue-resident memory T cells”. Immunological Reviews 255 (1): 165–81. (September 2013). doi:10.1111/imr.12087. PMC 3748618. PMID 23947354.
- ^ a b “A human memory T cell subset with stem cell-like properties”. Nature Medicine 17 (10): 1290–7. (September 2011). doi:10.1038/nm.2446. PMC 3192229. PMID 21926977.
- ^ “+ T cells: where they come from and why we need them”. Nature Reviews. Immunology 17 (6): 391–400. (June 2017). doi:10.1038/nri.2017.34. PMC 5569888. PMID 28480897.
- ^ “Virtual memory CD8 T cells display unique functional properties”. Proceedings of the National Academy of Sciences of the United States of America 110 (33): 13498–503. (August 2013). Bibcode: 2013PNAS..11013498L. doi:10.1073/pnas.1307572110. PMC 3746847. PMID 23898211.
- ^ “Strong homeostatic TCR signals induce formation of self-tolerant virtual memory CD8 T cells”. The EMBO Journal 37 (14). (July 2018). doi:10.15252/embj.201798518. PMC 6043851. PMID 29752423.
- ^ a b “Human T Cell Development, Localization, and Function throughout Life”. Immunity 48 (2): 202–213. (February 2018). doi:10.1016/j.immuni.2018.01.007. PMC 5826622. PMID 29466753.
- ^ a b “Lineage relationship of effector and memory T cells”. Current Opinion in Immunology 25 (5): 556–63. (October 2013). doi:10.1016/j.coi.2013.09.003. PMC 3858177. PMID 24148236.
- ^ a b “+ T cell differentiation”. Nature Reviews. Immunology 18 (5): 340–356. (May 2018). doi:10.1038/nri.2017.146. PMC 6327307. PMID 29379213.
- ^ “T-cell memory differentiation: insights from transcriptional signatures and epigenetics”. Immunology 139 (3): 277–84. (July 2013). doi:10.1111/imm.12074. PMC 3701173. PMID 23347146.
- ^ “Two subsets of memory T lymphocytes with distinct homing potentials and effector functions”. Nature 401 (6754): 708–12. (October 1999). Bibcode: 1999Natur.401..708S. doi:10.1038/44385. PMID 10537110.
- ^ “Loss of CD45R and gain of UCHL1 reactivity is a feature of primed T cells”. Journal of Immunology 140 (7): 2171–8. (April 1988). PMID 2965180.
- ^ “Molecular signatures distinguish human central memory from effector memory CD8 T cell subsets”. Journal of Immunology 175 (9): 5895–903. (November 2005). doi:10.4049/jimmunol.175.9.5895. PMID 16237082.
- ^ “Multiparameter flow cytometric analysis of CD4 and CD8 T cell subsets in young and old people”. Immunity & Ageing 5 (6): 6. (July 2008). doi:10.1186/1742-4933-5-6. PMC 2515281. PMID 18657274.
- ^ “Quantifying Memory CD8 T Cells Reveals Regionalization of Immunosurveillance”. Cell 161 (4): 737–49. (May 2015). doi:10.1016/j.cell.2015.03.031. PMC 4426972. PMID 25957682.
- ^ a b “Study highlights possible Achilles' heel in key immune memory cells”. 2021年1月24日閲覧。
- ^ “Alternative memory in the CD8 T cell lineage”. Trends in Immunology 32 (2): 50–6. (February 2011). doi:10.1016/j.it.2010.12.004. PMC 3039080. PMID 21288770.
- ^ “+ virtual memory: Antigen-inexperienced T cells reside in the naïve, regulatory, and memory T cell compartments at similar frequencies, implications for autoimmunity”. Journal of Autoimmunity 77: 76–88. (February 2017). doi:10.1016/j.jaut.2016.11.001. PMC 6066671. PMID 27894837.
